Asignatura Anlisis Qumico Grado Bioqumica Curso acadmico 201112

Asignatura: Análisis Químico Grado: Bioquímica Curso académico: 2011/12 N. Campillo Seva 1

1. Generalidades 2. Curvas de valoración 2. 1. Factores que influyen en la forma de la curva de valoración 2. 2. Construcción de una curva de valoración 2. 3. Valoración de una mezcla 3. Detección del punto final 3. A. Vía instrumental 3. B. Mediante el empleo de indicadores químicos: 3. B. 1. Valoración por el método de Mohr 3. B. 2. Valoración por el método de Volhard 3. B. 3. Valoración por el método de Fajans N. Campillo Seva 2
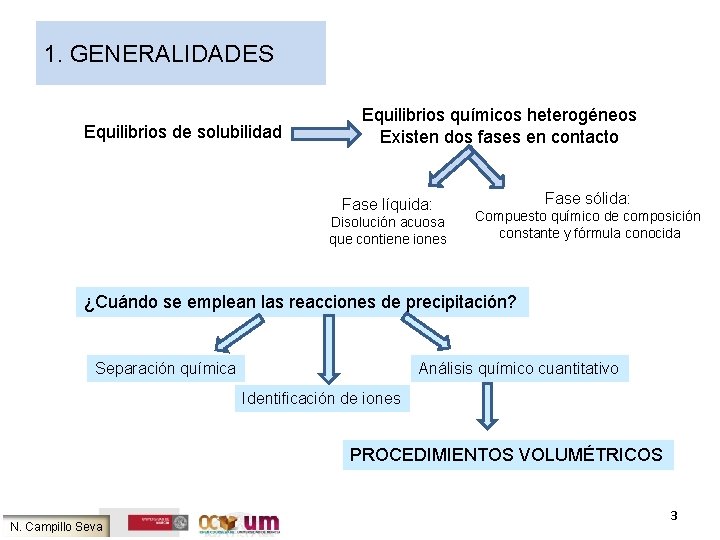
1. GENERALIDADES Equilibrios de solubilidad Equilibrios químicos heterogéneos Existen dos fases en contacto Fase líquida: Disolución acuosa que contiene iones Fase sólida: Compuesto químico de composición constante y fórmula conocida ¿Cuándo se emplean las reacciones de precipitación? Separación química Análisis químico cuantitativo Identificación de iones PROCEDIMIENTOS VOLUMÉTRICOS N. Campillo Seva 3
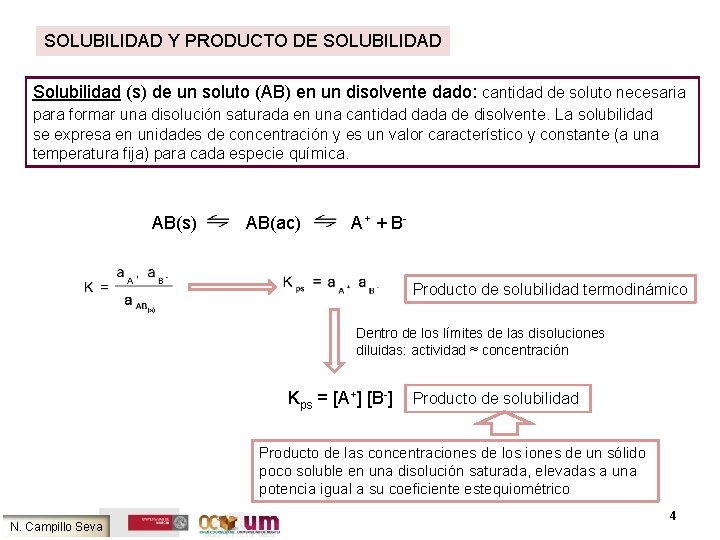
SOLUBILIDAD Y PRODUCTO DE SOLUBILIDAD Solubilidad (s) de un soluto (AB) en un disolvente dado: cantidad de soluto necesaria para formar una disolución saturada en una cantidad dada de disolvente. La solubilidad se expresa en unidades de concentración y es un valor característico y constante (a una temperatura fija) para cada especie química. AB(s) AB(ac) A + + B- Producto de solubilidad termodinámico Dentro de los límites de las disoluciones diluidas: actividad ≈ concentración Kps = [A+] [B-] Producto de solubilidad Producto de las concentraciones de los iones de un sólido poco soluble en una disolución saturada, elevadas a una potencia igual a su coeficiente estequiométrico N. Campillo Seva 4
![De forma general, Am. Bn(s) m. An+ + n. Bm- Kps = [An+]m [Bm-]n De forma general, Am. Bn(s) m. An+ + n. Bm- Kps = [An+]m [Bm-]n](http://slidetodoc.com/presentation_image/1e3447a53342ef0d7e451ef079bbbed3/image-5.jpg)
De forma general, Am. Bn(s) m. An+ + n. Bm- Kps = [An+]m [Bm-]n Condiciones de precipitación y disolución: [An+]m [Bm-]n > Kps Condición de precipitación. Disolución sobresaturada. [An+]m [Bm-]n = Kps Condición de equilibrio. Disolución saturada. [An+]m [Bm-]n < Kps Condición de disolución. Disolución insaturada. N. Campillo Seva 5

Factores que afectan a la solubilidad de los precipitados • Temperatura • Naturaleza del disolvente • Factores cristalográficos o morfológicos: tamaño de partícula, grado de hidratación, envejecimiento. • Presencia de electrolitos: – Electrolito inerte: Efecto salino – Electrolito no inerte: Efecto del ión común • Influencia de otros equilibrios iónicos N. Campillo Seva 6
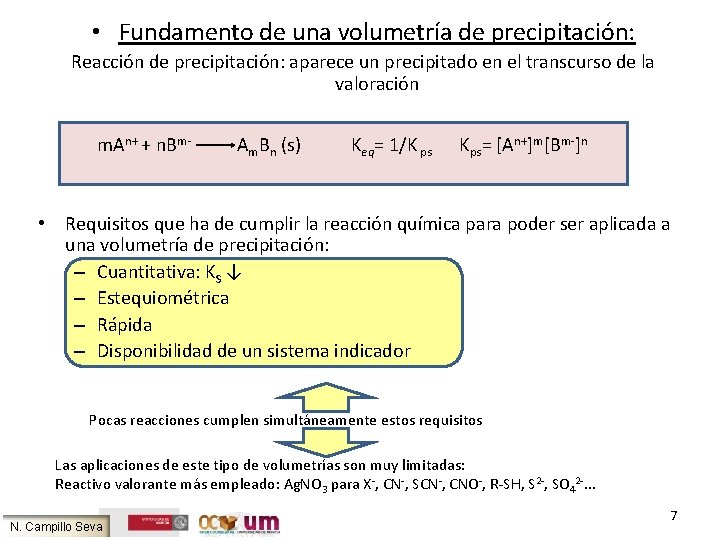
• Fundamento de una volumetría de precipitación: Reacción de precipitación: aparece un precipitado en el transcurso de la valoración m. An+ + n. Bm- Am. Bn (s) Keq= 1/K ps Kps= [An+]m[Bm-]n • Requisitos que ha de cumplir la reacción química para poder ser aplicada a una volumetría de precipitación: – Cuantitativa: KS ↓ – Estequiométrica – Rápida – Disponibilidad de un sistema indicador Pocas reacciones cumplen simultáneamente estos requisitos Las aplicaciones de este tipo de volumetrías son muy limitadas: Reactivo valorante más empleado: Ag. NO 3 para X-, CN-, SCN-, CNO-, R-SH, S 2 -, SO 42 -. . . N. Campillo Seva 7
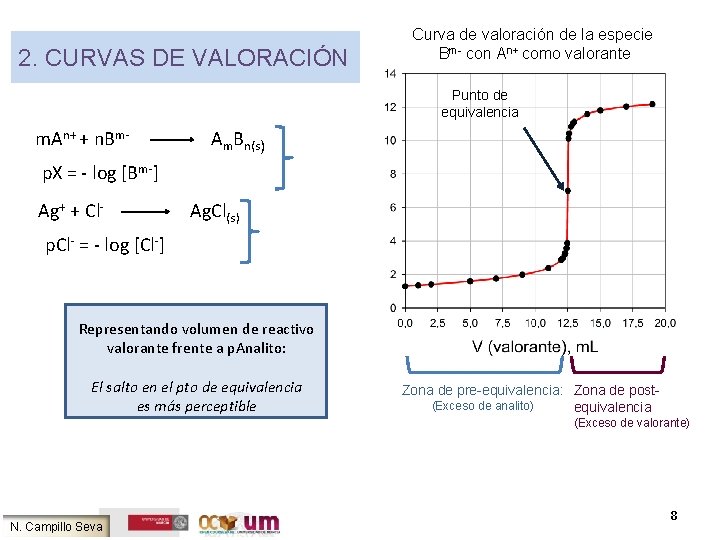
2. CURVAS DE VALORACIÓN Curva de valoración de la especie Bm- con An+ como valorante Punto de equivalencia m. An+ + n. Bm- Am. Bn(s) p. X = - log [Bm-] Ag+ + Cl- Ag. Cl(s) p. Cl- = - log [Cl-] Representando volumen de reactivo valorante frente a p. Analito: El salto en el pto de equivalencia es más perceptible Zona de pre-equivalencia: Zona de post(Exceso de analito) equivalencia (Exceso de valorante) N. Campillo Seva 8
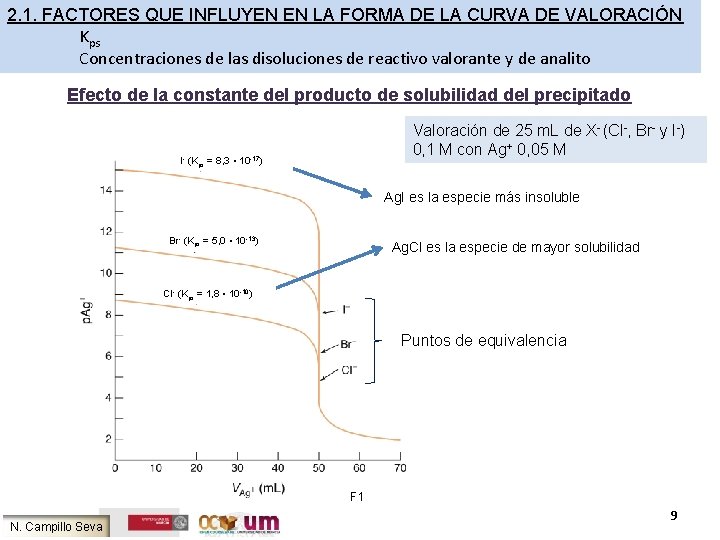
2. 1. FACTORES QUE INFLUYEN EN LA FORMA DE LA CURVA DE VALORACIÓN Kps Concentraciones de las disoluciones de reactivo valorante y de analito Efecto de la constante del producto de solubilidad del precipitado Valoración de 25 m. L de X- (Cl-, Br- y I-) 0, 1 M con Ag+ 0, 05 M I- (Kps = 8, 3 • 10 -17) Ag. I es la especie más insoluble Br- (Kps = 5, 0 • 10 -13) Ag. Cl es la especie de mayor solubilidad Cl- (Kps = 1, 8 • 10 -10) Puntos de equivalencia F 1 N. Campillo Seva 9
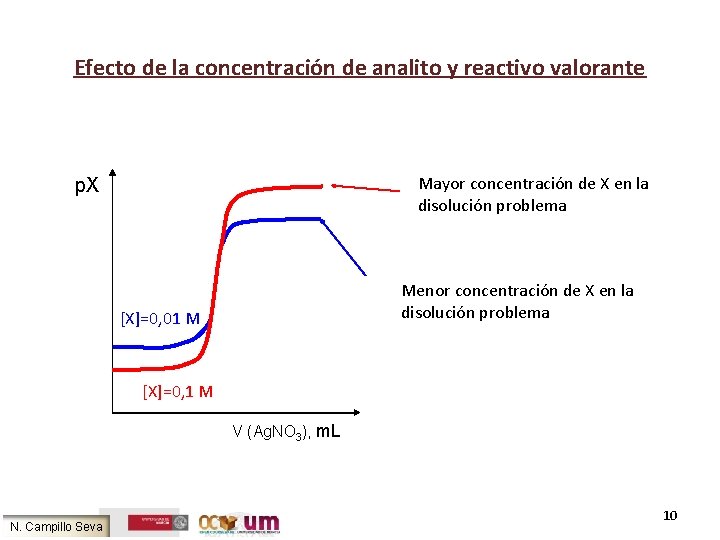
Efecto de la concentración de analito y reactivo valorante Mayor concentración de X en la disolución problema p. X Menor concentración de X en la disolución problema [X]=0, 01 M [X]=0, 1 M V (Ag. NO 3), m. L N. Campillo Seva 10
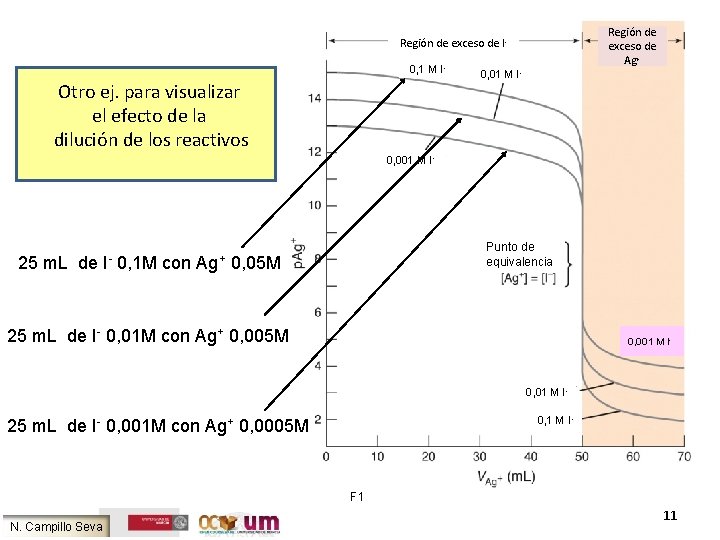
Región de exceso de Ag+ Región de exceso de I 0, 1 M I- Otro ej. para visualizar el efecto de la dilución de los reactivos 0, 01 M I- 0, 001 M I- 25 m. L de I- 0, 1 M con Ag+ Punto de equivalencia 0, 05 M 25 m. L de I- 0, 01 M con Ag+ 0, 005 M 0, 001 M I- 0, 01 M I 0, 1 M I- 25 m. L de I- 0, 001 M con Ag+ 0, 0005 M F 1 N. Campillo Seva 11

2. 2. Construcción de una curva de valoración Ejemplo: Valoración de 50 m. L de Na. Cl aproximadamente 0, 1 M con una disolución de Ag. NO 3 0, 1000 M 1. Reacción química de valoración: Ag+ + Cl- → Ag. Cl(s) Kps Ag. Cl = 1, 78 • 10 -10 2. Cálculo del volumen de valorante en el punto de equivalencia: 50 m. L 3. Establecimiento de los puntos donde calcularemos p. Cl: - Punto inicial: V(Ag. NO 3) = 0 - Antes del punto de equivalencia: Ej: V(Ag. NO 3)= 10 m. L V(Ag. NO 3)= 49, 99 m. L - Punto de equivalencia: V(Ag. NO 3 )= 50 m. L - Tras el punto de equivalencia: Ej: V(Ag. NO 3) = 50, 5 m. L V(Ag. NO 3) = 60 m. L N. Campillo Seva 12

● Punto inicial: Volumen de valorante agregado al medio de valoración igual a 0 p. Cl = 1, 0 ● Antes del punto de equivalencia: V(Ag. NO 3)= 10 m. L En este punto ya ha comenzado a precipitar el Ag. Cl de acuerdo con la reacción de valoración y la concentración total de cloruro se calcula según la ecuación: [Cl-] = [Cl-]sin valorar + [Cl-]por solubilidad del Ag. Cl siendo [Cl-]sin valorar >> [Cl-]por solubilidad del Ag. Cl [Cl-] = 0, 067 M N. Campillo Seva p. Cl = 1, 18 13
![● Antes del punto de equivalencia: V(Ag. NO 3)= 49, 99 m. L [Cl-] ● Antes del punto de equivalencia: V(Ag. NO 3)= 49, 99 m. L [Cl-]](http://slidetodoc.com/presentation_image/1e3447a53342ef0d7e451ef079bbbed3/image-14.jpg)
● Antes del punto de equivalencia: V(Ag. NO 3)= 49, 99 m. L [Cl-] = 1, 92 • 10 -5 M Si despreciamos 2º término de la ecuación: Valor correcto p. Cl = 4, 72 Valor incorrecto [Cl-] = 1, 0 • 10 -5 M p. Cl = 5, 0 Para volúmenes muy cercanos al del punto de equivalencia, la cantidad de Cl- presente en la disolución, como consecuencia de la solubilidad del precipitado , puede ser apreciable respecto de la queda de Cl- sin valorar ● En el punto de equivalencia: V(Ag. NO 3)= 50 m. L Todo el Cl- ha sido precipitado como Ag. Cl, así que el Cl- que existe en disolución es producto de la disociación del Ag. Cl precipitado, gobernada por su Kps [Cl-] = [Ag+] = (Kps)1/2 = 1, 34 • 10 -5 N. Campillo Seva p. Cl = 4, 87 14
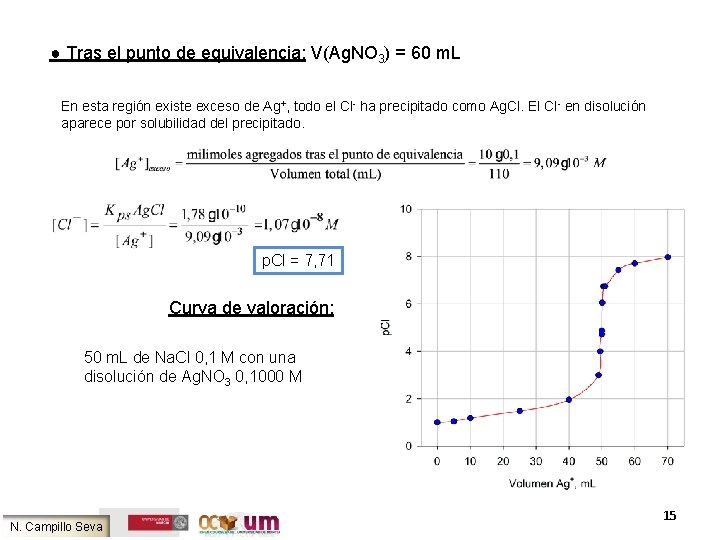
● Tras el punto de equivalencia: V(Ag. NO 3) = 60 m. L En esta región existe exceso de Ag+, todo el Cl- ha precipitado como Ag. Cl. El Cl- en disolución aparece por solubilidad del precipitado. p. Cl = 7, 71 Curva de valoración: 50 m. L de Na. Cl 0, 1 M con una disolución de Ag. NO 3 0, 1000 M N. Campillo Seva 15

Siguiendo con el mismo ejemplo: Valoración de 50 m. L de Na. Cl aproximadamente 0, 1 M con una disolución de Ag. NO 3 0, 1000 M Representación de p. Ag frente al volumen de Ag+ ● Punto inicial: Volumen de valorante agregado al medio de valoración igual a 0. No es posible calcular p. Ag ● Antes del punto de equivalencia: V(Ag. NO 3)= 10 m. L p. Ag = 8, 57 ● En el punto de equivalencia: V(Ag. NO 3)= 50 m. L [Cl-] = [Ag+] = (Kps)1/2 = 1, 34 • 10 -5 M N. Campillo Seva p. Ag = p. Cl = 4, 87 16
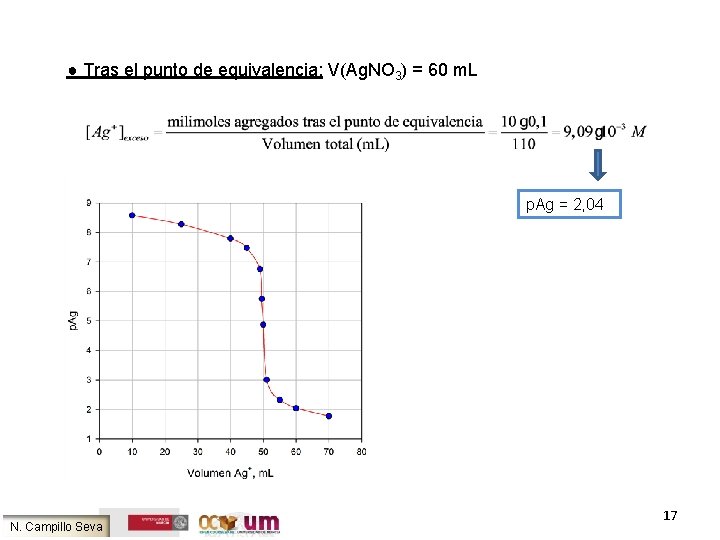
● Tras el punto de equivalencia: V(Ag. NO 3) = 60 m. L p. Ag = 2, 04 N. Campillo Seva 17
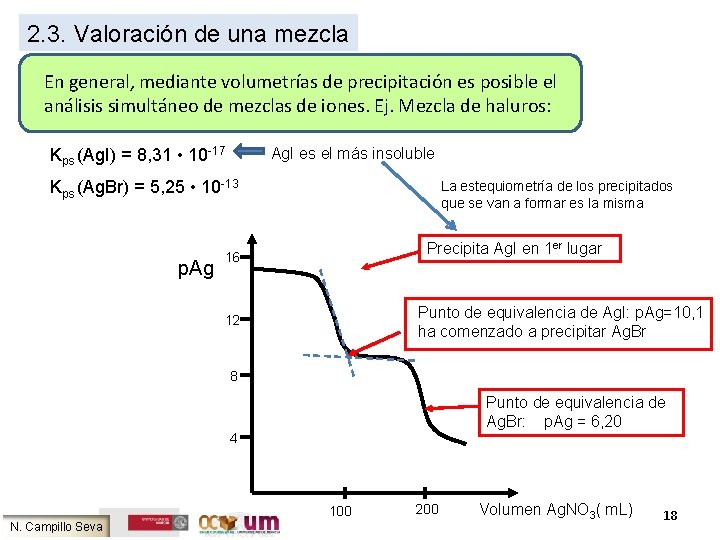
2. 3. Valoración de una mezcla En general, mediante volumetrías de precipitación es posible el análisis simultáneo de mezclas de iones. Ej. Mezcla de haluros: Ag. I es el más insoluble Kps (Ag. I) = 8, 31 • 10 -17 Kps (Ag. Br) = 5, 25 • 10 -13 p. Ag La estequiometría de los precipitados que se van a formar es la misma Precipita Ag. I en 1 er lugar 16 Punto de equivalencia de Ag. I: p. Ag=10, 1 ha comenzado a precipitar Ag. Br 12 8 Punto de equivalencia de Ag. Br: p. Ag = 6, 20 4 100 N. Campillo Seva 200 Volumen Ag. NO 3( m. L) 18
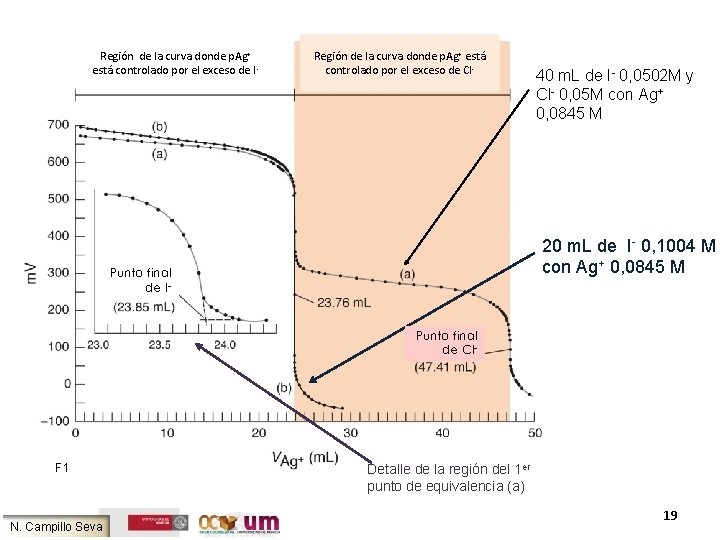
Región de la curva donde p. Ag+ está controlado por el exceso de I - Región de la curva donde p. Ag+ está controlado por el exceso de Cl - Fig. 7. 8 Harris 40 m. L de I- 0, 0502 M y Cl- 0, 05 M con Ag+ 0, 0845 M 20 m. L de I- 0, 1004 M con Ag+ 0, 0845 M Punto final de I- Punto final de Cl- F 1 N. Campillo Seva Detalle de la región del 1 er punto de equivalencia (a) 19

3. DETECCIÓN DEL PUNTO FINAL 3. A. Vía instrumental Ejemplo 1: Potenciometría Uso de Electrodos Selectivos de Iones (ESI): Al potenciómetro Entrada de aire Alambre de Ag Electrodo selectivo de Ag+ responde directamente a la concentración de Ag+ e indirectamente a la de Cl- E medido = cte + 0, 059 log [Ag+] E medido = cte + 0, 059 log KPS/[Cl-] Disolución acuosa saturada de KCl y Ag. Cl Pasta de Ag. Cl Ejemplo 2: Turbidimetría KCl sólido con Ag. Cl Contacto con la disolución externa Determinación de SO 42 empleando Ba 2+ como valorante F 1 Posibilidad de registrar la curva de valoración de forma automática N. Campillo Seva 20

3. B. Mediante el empleo de indicadores químicos - Por formación de un compuesto coloreado - Método de Mohr: Determinación de Cl- y Br- Método de Volhard: - Determinación directa de Ag+ - Determinación indirecta de haluros - Empleando indicadores de adsorción - Método de Fajans En cualquier caso la reacción volumétrica es una argentometría: Ag+ + X- N. Campillo Seva Ag. X(s) 21
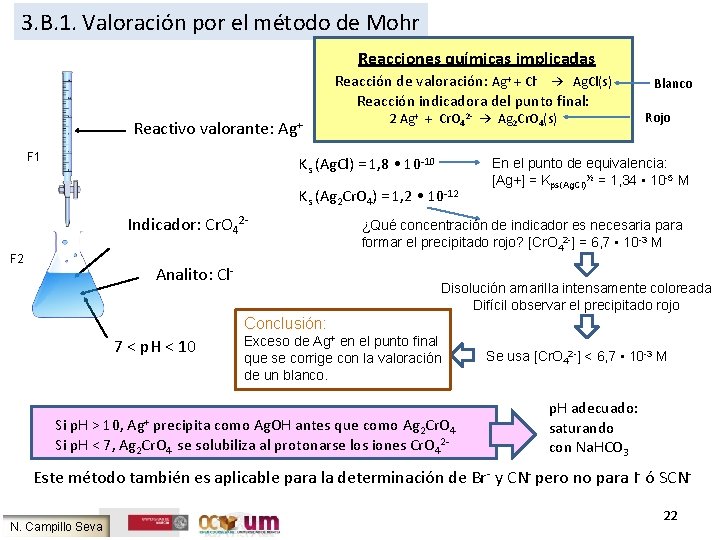
3. B. 1. Valoración por el método de Mohr Reacciones químicas implicadas Reacción de valoración: Ag+ + Cl- → Ag. Cl(s) Reacción indicadora del punto final: Reactivo valorante: F 1 Ag+ 2 Ag+ + Cr. O 42 - → Ag 2 Cr. O 4(s) Ks (Ag. Cl) = 1, 8 • 10 -10 Ks (Ag 2 Cr. O 4) = 1, 2 • 10 -12 Indicador: Cr. O 42 F 2 Analito: Cl- Blanco Rojo En el punto de equivalencia: [Ag+] = Kps(Ag. Cl)½ = 1, 34 • 10 -5 M ¿Qué concentración de indicador es necesaria para formar el precipitado rojo? [Cr. O 42 -] = 6, 7 • 10 -3 M Disolución amarilla intensamente coloreada Difícil observar el precipitado rojo Conclusión: 7 < p. H < 10 Ag+ Exceso de Ag+ en el punto final que se corrige con la valoración de un blanco. Si p. H > 10, precipita como Ag. OH antes que como Ag 2 Cr. O 4 Si p. H < 7, Ag 2 Cr. O 4 se solubiliza al protonarse los iones Cr. O 42 - Se usa [Cr. O 42 -] < 6, 7 • 10 -3 M p. H adecuado: saturando con Na. HCO 3 Este método también es aplicable para la determinación de Br- y CN- pero no para I- ó SCNN. Campillo Seva 22
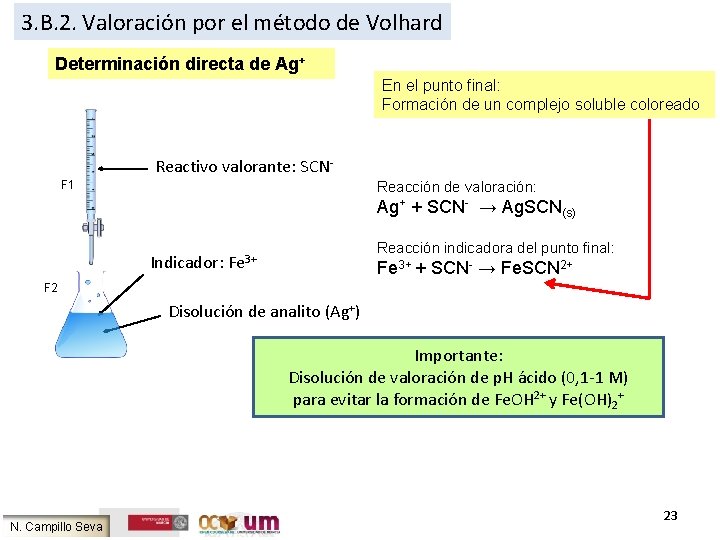
3. B. 2. Valoración por el método de Volhard Determinación directa de Ag+ En el punto final: Formación de un complejo soluble coloreado Reactivo valorante: SCNF 1 Reacción de valoración: Ag+ + SCN- → Ag. SCN(s) Reacción indicadora del punto final: Indicador: Fe 3+ + SCN- → Fe. SCN 2+ F 2 Disolución de analito (Ag+) Importante: Disolución de valoración de p. H ácido (0, 1 -1 M) para evitar la formación de Fe. OH 2+ y Fe(OH)2+ N. Campillo Seva 23
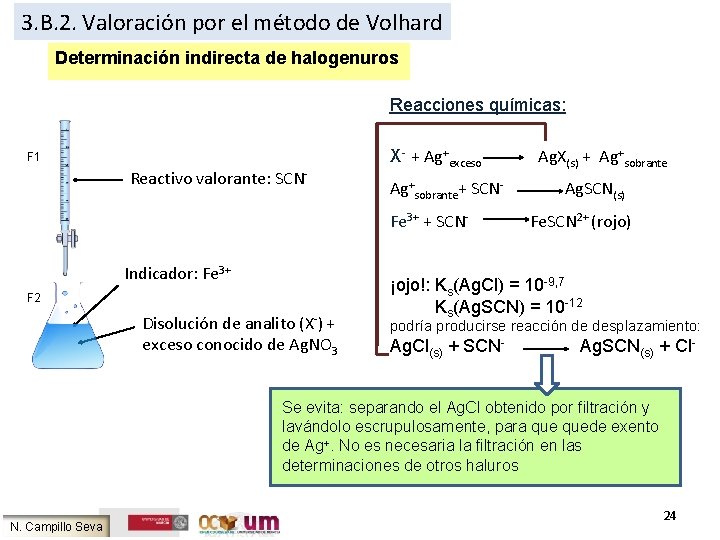
3. B. 2. Valoración por el método de Volhard Determinación indirecta de halogenuros Reacciones químicas: F 1 Reactivo valorante: SCN- X- + Ag+exceso Ag+sobrante+ SCNFe 3+ + SCN- Indicador: Fe 3+ F 2 Disolución de analito (X-) + exceso conocido de Ag. NO 3 Ag. X(s) + Ag+sobrante Ag. SCN(s) Fe. SCN 2+ (rojo) ¡ojo!: Ks(Ag. Cl) = 10 -9, 7 Ks(Ag. SCN) = 10 -12 podría producirse reacción de desplazamiento: Ag. Cl(s) + SCN- Ag. SCN(s) + Cl- Se evita: separando el Ag. Cl obtenido por filtración y lavándolo escrupulosamente, para quede exento de Ag+. No es necesaria la filtración en las determinaciones de otros haluros N. Campillo Seva 24
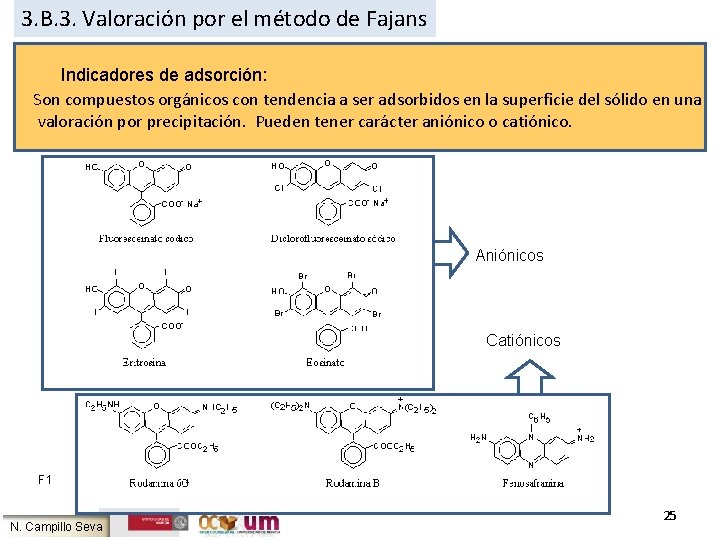
3. B. 3. Valoración por el método de Fajans Indicadores de adsorción: Son compuestos orgánicos con tendencia a ser adsorbidos en la superficie del sólido en una valoración por precipitación. Pueden tener carácter aniónico o catiónico. Aniónicos Catiónicos F 1 N. Campillo Seva 25
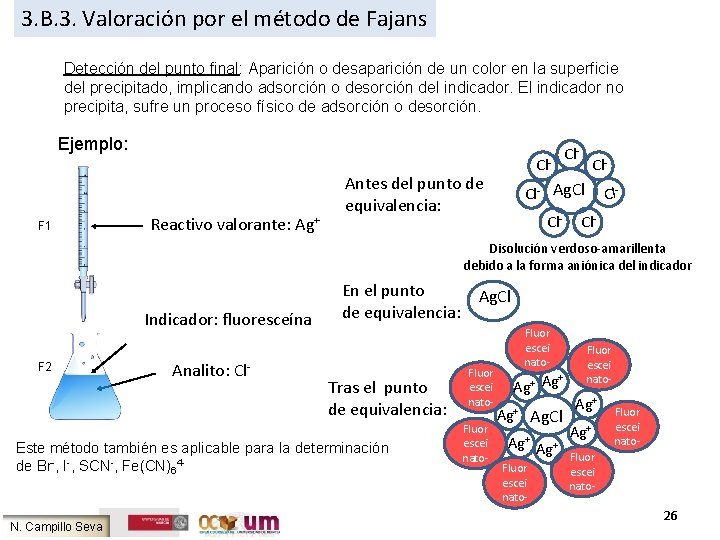
3. B. 3. Valoración por el método de Fajans Detección del punto final: Aparición o desaparición de un color en la superficie del precipitado, implicando adsorción o desorción del indicador. El indicador no precipita, sufre un proceso físico de adsorción o desorción. Ejemplo: F 1 Reactivo valorante: Ag+ Cl- Antes del punto de equivalencia: Cl- Cl- Ag. Cl Cl- Cl- Disolución verdoso-amarillenta debido a la forma aniónica del indicador Indicador: fluoresceína F 2 Analito: Cl- En el punto de equivalencia: Tras el punto de equivalencia: Este método también es aplicable para la determinación de Br-, I-, SCN-, Fe(CN)64 - N. Campillo Seva Ag. Cl Fluor escei nato- Fluor escei nato+ Ag Ag+ Ag. Cl Ag+ Ag+ Fluor escei nato- 26
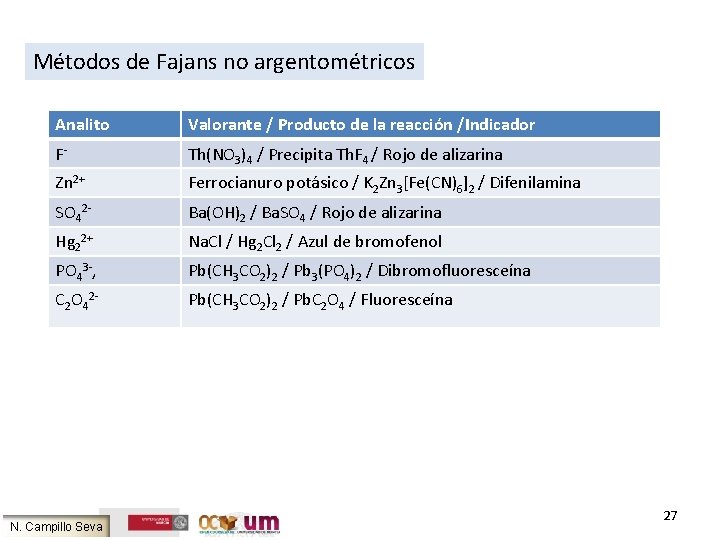
Métodos de Fajans no argentométricos Analito Valorante / Producto de la reacción /Indicador F- Th(NO 3)4 / Precipita Th. F 4 / Rojo de alizarina Zn 2+ Ferrocianuro potásico / K 2 Zn 3[Fe(CN)6]2 / Difenilamina SO 42 - Ba(OH)2 / Ba. SO 4 / Rojo de alizarina Hg 22+ Na. Cl / Hg 2 Cl 2 / Azul de bromofenol PO 43 -, Pb(CH 3 CO 2)2 / Pb 3(PO 4)2 / Dibromofluoresceína C 2 O 42 - Pb(CH 3 CO 2)2 / Pb. C 2 O 4 / Fluoresceína N. Campillo Seva 27

CRÉDITOS DE LAS ILUSTRACIONES – PICTURES COPYRIGHTS -Logo Portada OCW-UM. Autor: Universidad de Murcia. Dirección web: http: //ocw. um. es. -Página 4, flechas de equilibrio. Dirección web: http: //commons. wikimedia. org/wiki/Category: Arrows_for_chemical_reactions -Página 9, F 1. Fuente: “Quantitative Chemical Analysis”, Seventh Edition, © 2007 W. H. Freeman and Company. -Página 11, F 1. Fuente: “Quantitative Chemical Analysis”, Seventh Edition, © 2007 W. H. Freeman and Company. -Página 20, F 1. Fuente: “Quantitative Chemical Analysis”, Seventh Edition, © 2007 W. H. Freeman and Company. -Página 22, 23, 24 y 26, F 1. Autor: Mysid (original by Quantockgoblin. Dirección web: http: //commons. wikimedia. org/wiki/File: burette. svg -Página 22, 23, 24 y 26, F 2. Dirección web: http: //commons. wikimedia. org/wiki/File: Chemistry_flask_matthew_02. svg. -Página 25, F 1. Dirección web: http: //www. iq. uva. es/analitica/Auxiliar/aux 42. htm N. Campillo Seva 28
- Slides: 28