ASAM KARBOKSILAT Asam karboksilat adalah suatu senyawa organik


ASAM KARBOKSILAT Asam karboksilat adalah suatu senyawa organik yang mengandung gugus karboksil, -CO 2 H. Gugus karboksil mengandung sebuah gugus karbonil dan sebuah gugus hidroksil; antar-aksi dari kedua gugus ini mengakibatkan suatu kereaktivan kimia yang unik untuk asam karboksilat.

A. TATA NAMA Penamaan untuk asam karboksilat untuk empat karboksilat pertama menggunakan nama trivial yaitu asam format, asam asetat, asam propionat, dan asam butirat. Nama IUPAC dari suatu asam karboksilat alifatik diawali dengan kata asam dan akhiran –a dari alkana diganti –oat. Seperti halnya aldehida, karbon pada gugus karboksil selalu menempati posisi karbon nomor 1. Bila ada dua gugus karboksil maka penamaan dengan awalan asam dan akhiran –dioat.

Gugus karboksil (-CO 2 H) yang terikat pada suatu cincin maka penamaannya menggunakan awalan asam dan akhiran karboksilat. O C Asam siklopentanakarboksilat OH Gugus karboksil yang terikat pada cincin aromatik 6 karbon diberi nama sebagai asam benzoat, apabila ada substituen maka penomoran mengikuti posisi dari gugus karboksilnya. Bila substituen terletak pada karbon 2 dapat diberi nama dengan orto(dilambangkan o), substituen pada karbon 3 diberi nama meta (m), dan para (p) bila posisi pada karbon 4.
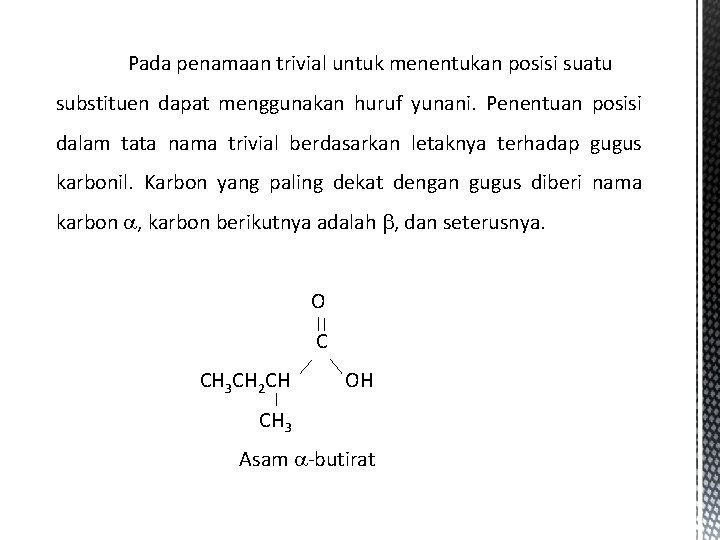
Pada penamaan trivial untuk menentukan posisi suatu substituen dapat menggunakan huruf yunani. Penentuan posisi dalam tata nama trivial berdasarkan letaknya terhadap gugus karbonil. Karbon yang paling dekat dengan gugus diberi nama karbon , karbon berikutnya adalah , dan seterusnya. O C CH 3 CH 2 CH OH CH 3 Asam -butirat

B. SIFAT ASAM KARBOKSILAT Sifat fisik asam karboksilat dipengaruhi oleh gugus karbonilnya. Asam karboksilat bersifat polar karena mempunyai dua gugus yang bersifat polar yaitu hidroksil (-OH) dan karbonil (C=O). Sifat fisik karboksilat juga ditentukan oleh gugus hidroksil. Karena adanya gugus hidroksil maka asam karboksilat dapat membentuk dimer (sepasang molekul yang saling berikatan) melalui ikatan hidrogen antar gugus polar dari dua gugus karboksil.

C. REAKSI ASAM KARBOKSILAT 1. Reaksi Asam Karboksilat dengan Basa Dibandingkan dengan asam mineral seperti HCl, asam karboksilat adalah asam lemah, namun bersifat lebih asam daripada alkohol atau fenol. Karena keasamannya ini reaksi asam karboksilat dapat bereaksi dengan basa. Reaksi suatu asam karboksilat dengan suatu basa akan menghasilkan garam. CH 3 CO 2 H asam asetat + Na+ OHnatrium asetat CH 3 CO 2 - Na+ + H 2 O
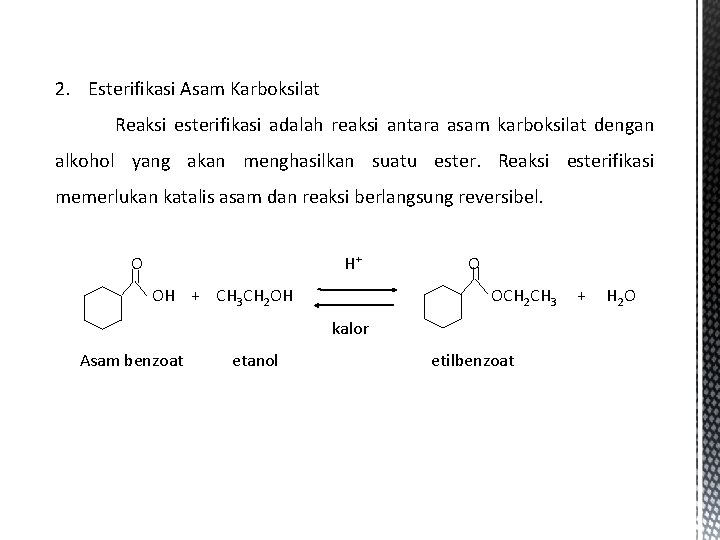
2. Esterifikasi Asam Karboksilat Reaksi esterifikasi adalah reaksi antara asam karboksilat dengan alkohol yang akan menghasilkan suatu ester. Reaksi esterifikasi memerlukan katalis asam dan reaksi berlangsung reversibel. O H+ OH + CH 3 CH 2 OH O OCH 2 CH 3 kalor Asam benzoat etanol etilbenzoat + H 2 O

3. Reduksi Asam Karboksilat Reduksi asam karboksilat dapat dilakukan dengan menggunakan hidrida logam seperti Li. Al. H 4 akan mereduksi gugus karboksil langsung menjadi gugus –CH 2 OH, reduksi ini juga akan mengubah gugus fungsional karbonil lain dalam molekul. CH 3 CO 2 H Asam asetat (1) Li. Al. H 4 (2) H 2 O, H- CH 3 CH 2 OH etanol

D. PEMBUATAN ASAM KARBOKSILAT Pembuatan asam karboksilat melalui jalur sintetik dapat dikelompokkan dalam tiga tipe reaksi yaitu (1) hidrolisis derivat asam karboksilat; (2) reaksi oksidasi; (3) reaksi grignard. Hidrolisis adalah reaksi yang melibatkan air dengan katalis asam atau basa. Oksidasi alkohol primer dan aldehida akan menghasilkan asam karboksilat. Selain oksidasi alkohol, asam karboksilat juga dapat diperoleh dari oksidasi alkena. Asam karboksilat dapat dibuat melalui jalur reaksi dengan reagensia grignard. Pada reaksi ini dibuat dari reaksi CO 2 dengan reagensia grignard, dalam air dan katalis asam.

E. DERIVAT ASAM KARBOKSILAT Derivat asam karboksilat adalah senyawa yang menghasilkan asam karboksilat bila direaksikan dengan air. Yang termasuk derivat asam karboksilat: 1. Ester 2. Halida asam karboksilat 3. Anhidrida karboksilat 4. Amida 5. Nitril

1. Ester Berdasarkan susunannya, ester terbagi atas tiga golongan, yaitu sari buah-buahan, lemak atau minyak, dan lilin. 1. Sari buah-buahan, yaitu ester dari alkohol suku rendah atau tengah. Ester ini mempunyai aroma yang sedap, banyak digunakan dalam pemberi aroma pada makanan dan parfum. 2. Lemak dan minyak, yaitu ester dari gliserol dan asam karboksilat suku tengah atau tinggi. 3. Lilin, yaitu ester dari alkohol suku tinggi dan asam karboksilat suku tinggi.

1. 1 Tata Nama Ester diberi nama dengan menyebutkan terlebih dahulu gugus alkil yang terikat pada oksigen ester dan diikuti dengan nama karboksilatnya. Contoh: HCOOCH 3 Metil metanoat (IUPAC) ; Metil formiat (Trivial) 1. 2 Sifat Fisik Ester bersuku rendah berwujud cair encer, ester bersuku tengah berwujud cair kental, ester bersuku tinggi berwujud padat. Ester tidak mampu membentuk ikatan hidrogen antar molekulnya sehingga titik didih dan titik leleh ester rendah dibandingkan asam karboksilat padanannya.
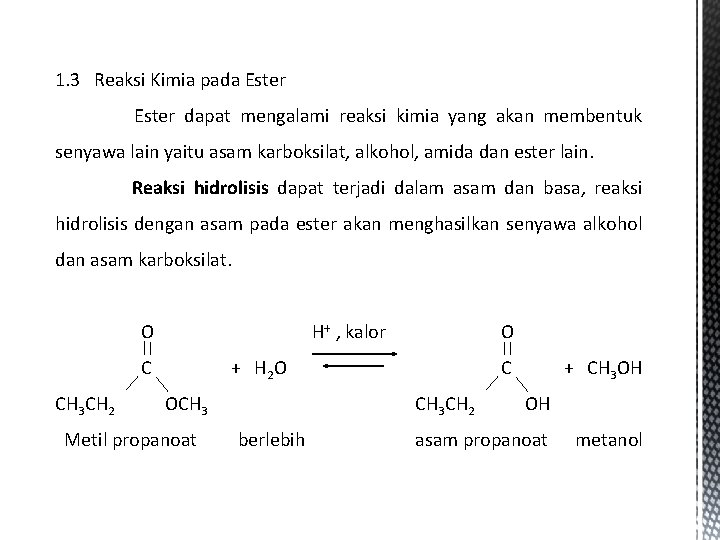
1. 3 Reaksi Kimia pada Ester dapat mengalami reaksi kimia yang akan membentuk senyawa lain yaitu asam karboksilat, alkohol, amida dan ester lain. Reaksi hidrolisis dapat terjadi dalam asam dan basa, reaksi hidrolisis dengan asam pada ester akan menghasilkan senyawa alkohol dan asam karboksilat. O H+ , kalor C CH 3 CH 2 O + H 2 O OCH 3 Metil propanoat C CH 3 CH 2 berlebih + CH 3 OH OH asam propanoat metanol

Transesterifikasi, merupakan reaksi pertukaran bagian alkohol dari suatu ester, reaksi ini dapat terjadi dalam asam dan basa yang bersifat riversible. O CH 2=HC H+ OCH 3 + CH 3 CH 2 OH O CH 2= CH OCH 2 CH 3 + CH 3 OH Reaksi dengan reagensia grignard, reaksi ester dengan reagensia grignard akan menghasilkan alkohol tersier dengan dua gugus alkil yang identik. Dapat juga menghasilkan alkohol sekunder apabila digunakan suatu ester format (HCOOR). O CH 3 CH 2 2 CH 3 Mg. Br OCH 2 CH 3 H 2 O, H+ OH CH 3 CH 2 – CH 3 alkohol tersier

1. 4 Pembuatan Ester Pembuatan ester dapat dilakukan dengan reaksi esterifikasi yaitu reaksi yang melibatkan asam karboksilat dan alkohol. 2. Halida Asam Halida asam adalah derivat asam karboksilat yang paling reaktif diantara semua derivat asam karboksilat. 2. 1 Tata Nama Halida Asam Penamaan pada halida asam berdasarkan pada asam karboksilat induknya dengan akhiran asam –at diubah menjadi –il diikuti nama halida.
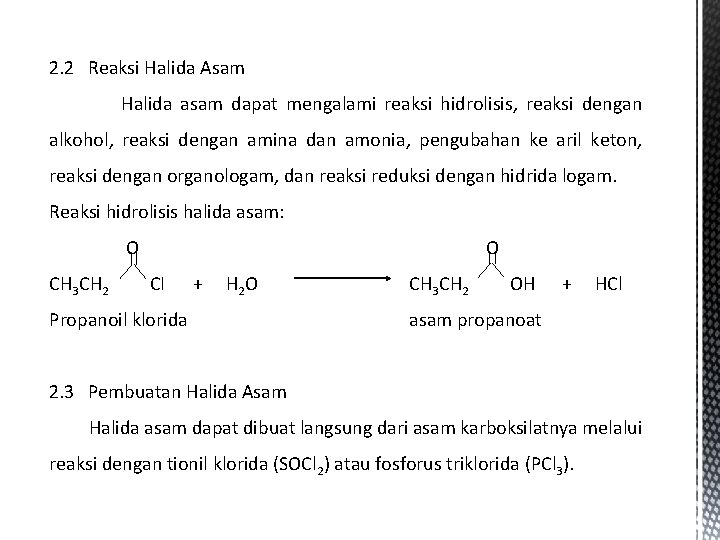
2. 2 Reaksi Halida Asam Halida asam dapat mengalami reaksi hidrolisis, reaksi dengan alkohol, reaksi dengan amina dan amonia, pengubahan ke aril keton, reaksi dengan organologam, dan reaksi reduksi dengan hidrida logam. Reaksi hidrolisis halida asam: O CH 3 CH 2 O CI + H 2 O Propanoil klorida CH 3 CH 2 OH + HCl asam propanoat 2. 3 Pembuatan Halida Asam Halida asam dapat dibuat langsung dari asam karboksilatnya melalui reaksi dengan tionil klorida (SOCl 2) atau fosforus triklorida (PCl 3).

3. Anhidrida Asam Anhidrida asam karboksilat jarang ditemukan di alam. Salah satu contoh senyawanya di alam adalah anhidrida siklik yang terdapat dalam lalat spanyol yaitu kantaridin. Struktur dari anhidrida asam karboksilat merupakan penggabungan dari dua molekul asam karboksilat dengan menghilangkan satu molekul air. 3. 1 Tata Nama Anhidrida Penamaan untuk anhidrida diawali dengan kata anhidrida diikuti dengan nama karboksilnya, bila gugus aslinya sama maka penamaan dengan menggunakan nama asam karboksilat induknya. Tetapi bila gugus aslinya berbeda penamaan menggunakan nama asam-asamnya.

3. 2 Reaksi Anhidrida dapat mengalami hidrolisis, reaksi dengan alkohol dan fenol, dan reaksi dengan amonia dan amina. Hidrolisis anhidrida akan menghasilkan senyawa asam karboksilat. Reaksi dengan alkohol akan menghasilkan ester, dan reaksi dengan amina akan menghasilkan amida. O O CH 3 - C -O-C-CH 2 CH 3 + H 2 O Anhidrida etanoat propanoat O O CH 3 - C -OH + CH 3 CH 2 - C –OH asam etanoat asam propanoat

3. 3 Pembuatan Anhidrida asam dibuat dari derivat asam karboksilat yang lebih reaktif dengan suatu ion karboksilat. 4. Amida merupakan derivat asam karboksilat yang paling tidak reaktif. Amida banyak ditemukan di alam terutama sebagai protein yaitu suatu poliamida. 4. 1 Tata Nama Amida Penamaan amida berdasarkan nama asam karboksilatnya dimana imbuhan asam –oat digantikan dengan amida. Bila pada Nitrogen mengikat gugus alkil lain maka penamaannya menggunakan nama N-alkil.

4. 2 Reaksi Amida dapat mengalami reaksi hidrolisis dan reaksi reduksi dengan hidrida logam. Reaksi hidrolisis amida akan menghasilkan asam karboksilat dan amonia. Sedangkan amida yang direduksi dengan anhidrida logam akan membentuk senyawa amina. O CH 3 CH 2 – C – NH 2 + H 2 O Propanamida H+ / OH- O CH 3 CH 2 – C – OH + NH 3 asam propanoat 4. 3 Pembuatan Amida dapat dibuat dari turunan asam karboksilat dengan amoniak.

SOAL 1. Suatu sifat yang bukan merupakan sifat fisis dari asam karboksilat berbobot-molekul rendah ialah baunya. a. Bau mentega tengik sebagian ditimbulkan oleh jenis asam karboksilat apa? b. keringat kambing mengandung asam karboksilat apa? c. Bau lemak tengik ditimbulkan oleh asam apa? 2. Sebutkan perbedaan antara fenol dan asam karboksilat dalam kereaktifannya terhadap Na. OH dan Na. HCO 3 ? 3. Sebutkan 4 jenis turunan pertama dari asam karboksilat ?
- Slides: 22