ASAM BASA Oleh RYANTO BUDIONO Ada 3 teori

ASAM – BASA Oleh : RYANTO BUDIONO

Ada 3 teori Asam Basa, yaitu : 1. Teori Arrhenius (1884) Asam adalah yang dapat memberikan ion H+ dalam larutan air, sedangkan Basa adalah yang memberikan ion OH- dalam larutan air.

Teori ini banyak kekurangan, antara lain : n pelarut yang digunakan adalah air n ada beberapa zat yang bersifat asam atau basa tidak mengandung H+ atau OHn misal : Na 2 CO 3, NH 3, Na. HCO 3, … dll n Natrium Karbonat dapat menetralkan asam tanpa melepaskan OH-. n Na 2 CO 3 + 2 HCl 2 Na. Cl + H 2 O + CO 2

Teori Bronsted – Lowry (1923) Asam : zat yang dapat memberikan proton, dan Basa : zat yang menerima proton. Menurut teori ini, tidak ada zat yang dapat bertindak sebagai asam jika tdk terdapat basa yang dapat menerima proton.

Asam dan basa yang saling berkaitan dalam pertukaran proton disebut : pasangan asam – basa konyugasi Reaksi : Asam 1 basa konyugasi 1 + H+ Basa 2 + H+ asam konyugasi 2 ------------------ (+) Asam 1 + basa 2 basa konyugasi 1 + asam konyugasi 2
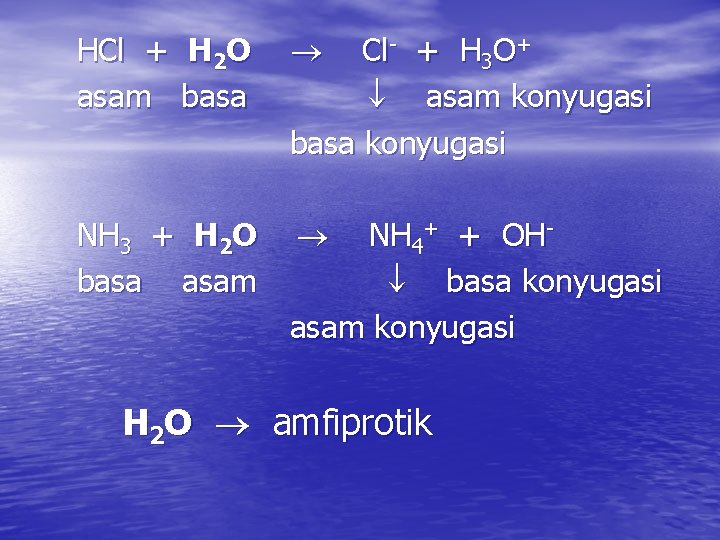
HCl + H 2 O asam basa Cl- + H 3 O+ asam konyugasi basa konyugasi NH 3 + H 2 O basa asam NH 4+ + OH basa konyugasi asam konyugasi H 2 O amfiprotik

INGAT : Reaksi asam – basa Bronsted – Lowry dapat berlangsung dlm berbagai pelarut, dan dapat juga berlangsung dalam fase gas dimana tidak terdapat pelarut, misalnya : HCl (g) + NH 3 (g) NH 4+ + Cl-

Semakin kuat suatu asam, semakin lemah basa konyugasinya. Semakin kuat suatu basa, semakin lemah asam konyugasinya.

Teori GN Lewis (1923) Asam adalah setiap spesi yang mengandung atom yang dapat menerima pasangan elektron, sedangkan Basa adalah setiap spesi yang mengandung atom yang dapat memberikan pasangan elektron.

Contoh : Ag+ + 2 NH 3 Asam basa Ag(NH 3)2+ Seny. Kompleks Ikatan yang terjadi antara Ag dan NH 3 adalah kovalen koordinasi Al 3+ + 6 H 2 O Al(H 2 O)63+
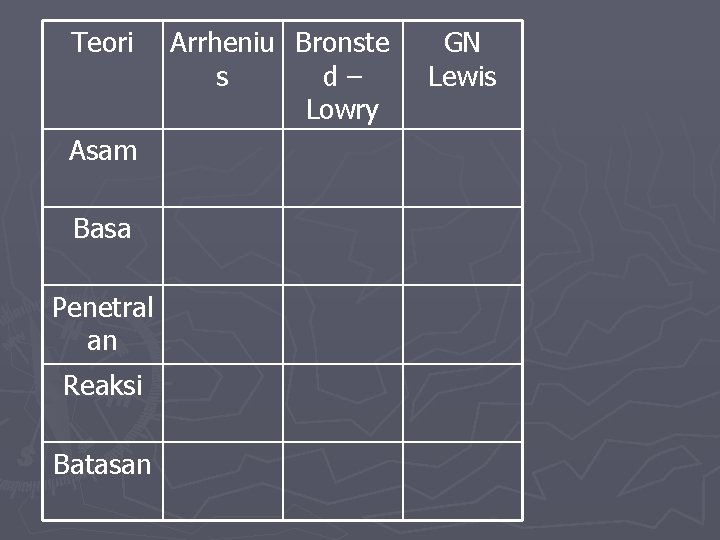
Teori Asam Basa Penetral an Reaksi Batasan Arrheniu Bronste s d– Lowry GN Lewis

DERAJAT IONISASI & TETAPAN IONISASI Asam lemah atau basa lemah dalam larutan tidak terurai sempurna menjadi ion. Jumlah fraksi molekul yang terurai dibandingkan dengan molekul mula – mula disebut derajat disosiasi dan dinyatakan dengan
![HA H+ + A - [H+][A-] Ka = ------[HA] Ka disebut : tetapan kesetimbangan HA H+ + A - [H+][A-] Ka = ------[HA] Ka disebut : tetapan kesetimbangan](http://slidetodoc.com/presentation_image_h/1abf8453bf3910f459ba636e804c3517/image-13.jpg)
HA H+ + A - [H+][A-] Ka = ------[HA] Ka disebut : tetapan kesetimbangan asam

HA H+ + Aa 0 0 Mula – mula Terurai Setimbang a – a a a Konsentrasi pada saat setimbang, HA = (a – a )/V molar, (H+) = (A-) = a /V molar
![[H+][A-] [a /V] a 2 Ka = -------------- = ------[HA] [(a – a )/V] [H+][A-] [a /V] a 2 Ka = -------------- = ------[HA] [(a – a )/V]](http://slidetodoc.com/presentation_image_h/1abf8453bf3910f459ba636e804c3517/image-15.jpg)
[H+][A-] [a /V] a 2 Ka = -------------- = ------[HA] [(a – a )/V] (1 – ). V Karena sangat kecil terhadap 1, maka (1 – ) dapat dianggap 1 _____ = Ka/C

KEKUATAN ASAM ATAU BASA DALAM LARUTAN Kekuatan suatu asam atau basa diten-tukan oleh kemampuan asam atau basa untuk menghasilkan ion H+ atau ion OH-. Kekuatan suatu asam bergantung juga pada pelarutnya. Makin kuat sifat kebasaan pelarut, makin mudah asam melepaskan proton.

Contoh : Asam asetat merupakan asam lemah dalam larutan air, tetapi bila amonia digunakan sebagai pelarut (basa-nya lebih kuat dari air), maka asam asetat merupakan asam kuat.

Kekuatan asam atau basa dapat dilihat dari Ka atau Kbnya. Semakin kecil harga Ka atau Kb, maka asam atau basa tersebut semakin lemah sifat asam atau basanya. Contoh : Asam kuat asam sangat lemah asam lemah HCl CH 3 COOH HCN H 2 SO 4 H 2 C 2 O 4 H 2 CO 3 HNO 3 H 3 PO 4 H 3 BO 3
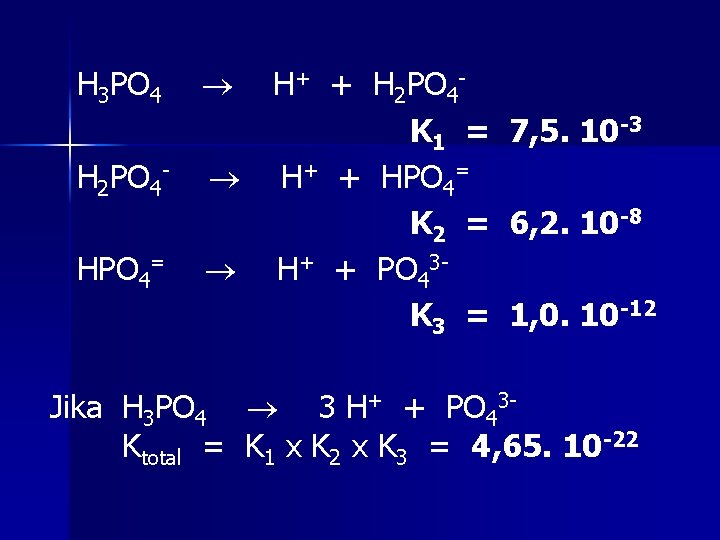
H 3 PO 4 H 2 PO 4 HPO 4= H+ + H 2 PO 4 K 1 = 7, 5. 10 -3 H+ + HPO 4= K 2 = 6, 2. 10 -8 H+ + PO 43 K 3 = 1, 0. 10 -12 Jika H 3 PO 4 3 H+ + PO 43 Ktotal = K 1 x K 2 x K 3 = 4, 65. 10 -22

H 3 PO 4 dapat menghasilkan lebih dari satu ion H+. Asam ini disebut asam poliprotik. Asam ini dapat me ngalami disosiasi secara bertahap dan setiap tahapnya dinyatakan dengan tetapan kesetimbangan, sedangkan K 1 K 2 K 3. Harga K 1, K 2, K 3 yang makin berkurang (semakin kecil), hal ini berarti pada setiap tahap pengionan lebih sedikit dibandingkan tahap berikutnya.

Biasanya konsentrasi ion H+ dan ion OH- dinyatakan dengan p. H atau p. OH berasal dari : p. H = – log H+ atau p. OH = – log OH-. p. OH + p. H = 14 (berasal dari p. Kw)
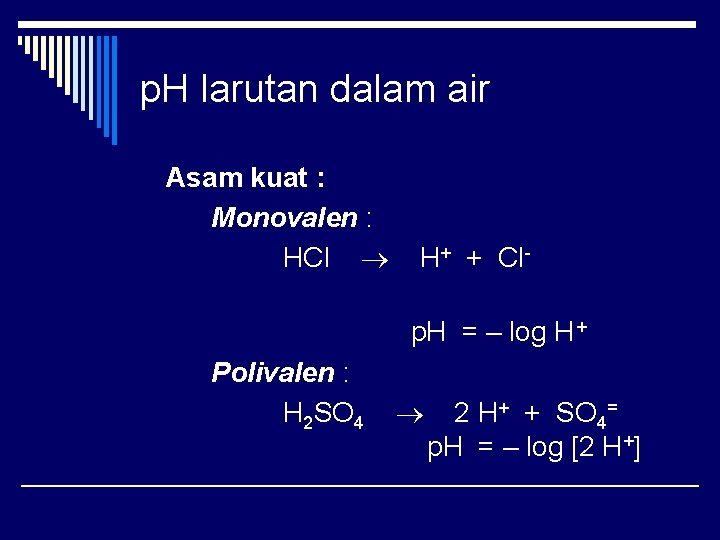
p. H larutan dalam air Asam kuat : Monovalen : HCl H+ + Clp. H = – log H + Polivalen : H 2 SO 4 2 H+ + SO 4= p. H = – log [2 H+]
![Jika konsentrasi ion H+ 10 -7 M, maka rumus yang digunakan adalah : [H+]2 Jika konsentrasi ion H+ 10 -7 M, maka rumus yang digunakan adalah : [H+]2](http://slidetodoc.com/presentation_image_h/1abf8453bf3910f459ba636e804c3517/image-23.jpg)
Jika konsentrasi ion H+ 10 -7 M, maka rumus yang digunakan adalah : [H+]2 – Ca. [H+] – Kw = 0 CONTOH : Hitung p. H dari larutan : a). HCl 0, 1 M b). H 2 SO 4 0, 05 M c). HCl 10 -8 M

Asam lemah : Monovalen : H Ast Polivalen : H 2 C 2 O 4 H+ p. H = + Ast½ (p. Ka + p. C) H+ + HC 2 O 4 p. H = ½ (p. K 1 + p. C)

Garam Dapat berasal dari : Asam kuat dan basa kuat : p. H = 7 Asam kuat dan basa lemah : p. H = ½ (p. Kw – p. Kb + p. C) Asam lemah dan basa kuat : p. H = ½ (p. Kw + p. Ka – p. C)

Asam lemah dan basa lemah : p. H = ½ (p. Kw + p. Ka – p. Kb) Garam yang berasal dari Asam Lemah & Basa Lemah yang ekivalen : p. H tidak bergantung pada konsentrasi garamnya Jika Ka = Kb, maka p. H larutannya = 7

CONTOH : Hitung p. H dari larutan : a). CH 3 COONa 0, 1 M (p. Ka = 4, 74) b). NH 4 Cl 0, 1 M (p. Kb = 4, 74) c). CH 3 COONH 4 0, 1 M (p. Ka = 4, 74, p. Kb = 4, 74)

Garam asam : Garam asam adalah garam yang masih mengandung sisa asam. Misal : Na. HCO 3, Na 2 HPO 4, Na. H 2 PO 4, … dll. p. Hnya dapat dihitung dengan persamaan = ½ (p. Kn + p. K(n – 1))

Contoh : Hitung p. H dari larutan : a). Na. HCO 3 0, 1 M (p. K 1 = 6, 37; p. K 2 = 10, 25) b). Na. H 2 PO 4 0, 1 M (p. K 1 = 2, 1; p. K 2 = 7, 2; p. K 3 = 12, 3) c). Na 2 HPO 4 0, 1 M

Buffer Pada umumnya terdiri dari atas : campuran asam lemah dan garamnya atau basa lemah dan garamnya, misal : campuran antara : asam asetat – Natrium asetat atau NH 3 – NH 4 Cl

Larutan buffer : n Mempunyai p. H tertentu n p. Hnya tidak berubah jika diencerkan. (yang berubah adalah : kapasitas buffernya) n p. Hnya relatif tidak berubah, jika ditambah sedikit asam atau basa.
![Untuk buffer asam lemah HA dan garamnya MA : [G] p. H = p. Untuk buffer asam lemah HA dan garamnya MA : [G] p. H = p.](http://slidetodoc.com/presentation_image_h/1abf8453bf3910f459ba636e804c3517/image-32.jpg)
Untuk buffer asam lemah HA dan garamnya MA : [G] p. H = p. Ka + log ----[A] Untuk buffer basa lemah MOH dan garamnya MA : [MA] p. H = p. Kb + log -------[MOH]

Kapasitas buffer Atau indeks buffer yaitu : suatu ukuran kemampuan buffer untuk mempertahankan p. H-nya yang konstan, jika ditambahkan asam kuat atau basa kuat.

Kapasitas buffer ( ), didefinisikan dengan persamaan : d. CB d. CA = -------dp. H d. CB / d. CA jumlah mol basa kuat atau asam kuat yang ditambahkan dp. H perubahan p. H

Atau : ( CHA. CA ) = 2, 303 x --------( CHA + CA ) CA CHA Kapasitas Buffer Konsentrasi Garam Konsentrasi Asam Lemah

Larutan buffer dapat dibuat dengan jalan : n Mencampurkan asam lemah dengan basa konyugasinya atau basa lemah dengan asam konyugasinya. n Mencampur asam lemah berlebih dengan jumlah terbatas basa kuat. n Mencampur basa lemah berlebih dengan jumlah terbatas asam kuat.

Buffer dalam darah. Ada beberapa buffer dalam darah yg mempertahankan p. H darah yaitu : pada p. H sekitar 7, 4; misalnya buffer H 2 CO 3/HCO 3 -, H 2 PO 4 -/HPO 4=, HHb. O 2/Hb. O 2 -, … dll

CONTOH : Hitung p. H dan kapasitas buffer suatu larutan yang diperoleh dengan men-campurkan : 112 ml H 3 PO 4 0, 1325 M dan 136 ml Na 2 HPO 4 0, 1450 M !
- Slides: 38