ASAM BASA dan GARAM BASA ASAM AS AM

ASAM, BASA dan GARAM :

BASA ASAM AS AM

TEORI ASAM BASA Secara Umum : Cairan berasa asam dan Asam dapat memerahkan kertas lakmus biru Basa Cairan berasa pahit dan dapat membirukan kertas lakmus merah Garam Cairan yang berasa asin
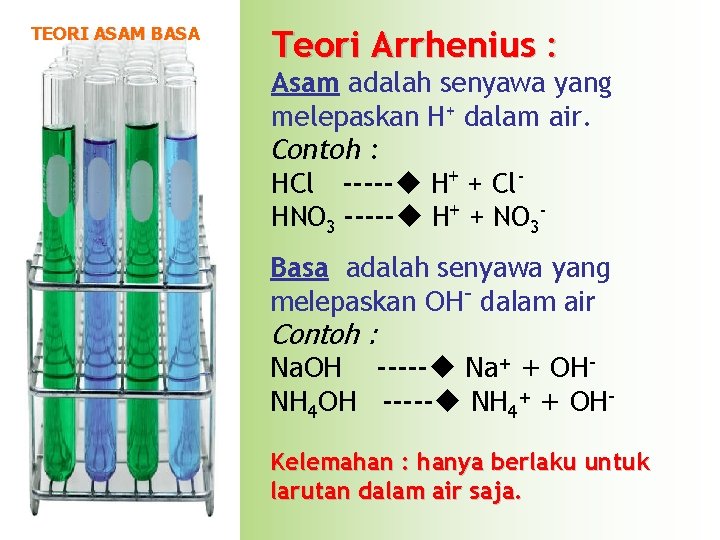
TEORI ASAM BASA Teori Arrhenius : Asam adalah senyawa yang melepaskan H+ dalam air. Contoh : HCl ----- H+ + Cl. HNO 3 ----- H+ + NO 3 Basa adalah senyawa yang melepaskan OH- dalam air Contoh : Na. OH ----- Na+ + OHNH 4 OH ----- NH 4+ + OHKelemahan : hanya berlaku untuk larutan dalam air saja.
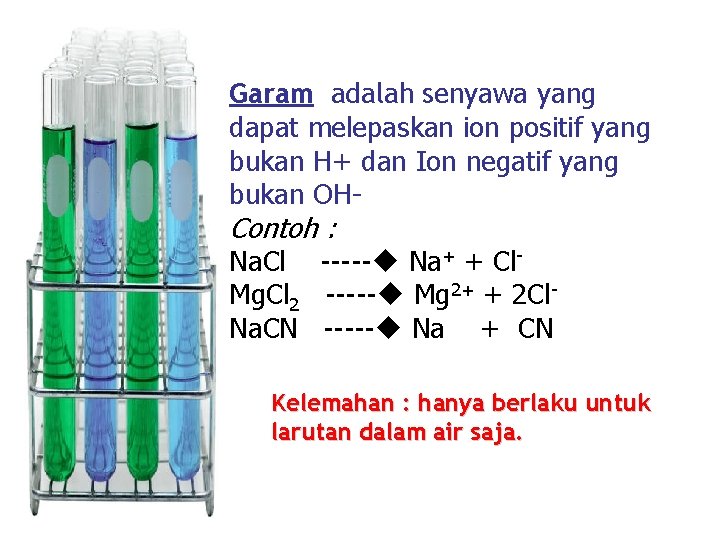
Garam adalah senyawa yang dapat melepaskan ion positif yang bukan H+ dan Ion negatif yang bukan OH- Contoh : Na. Cl ----- Na+ + Cl. Mg. Cl 2 ----- Mg 2+ + 2 Cl. Na. CN ----- Na + CN Kelemahan : hanya berlaku untuk larutan dalam air saja.
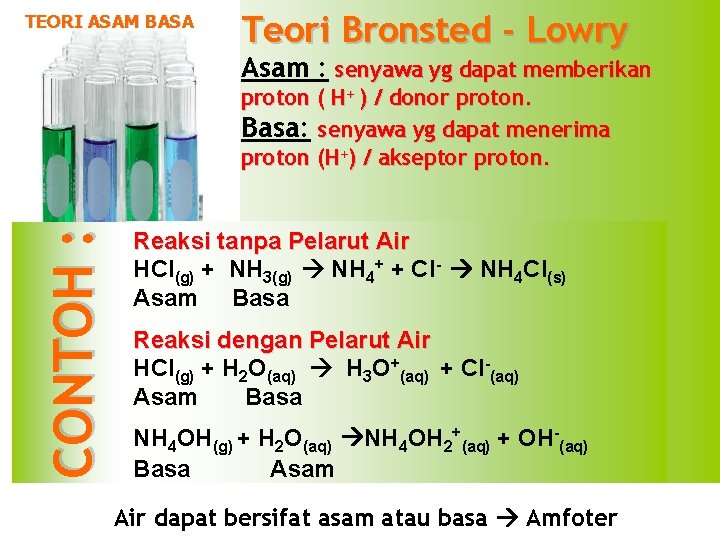
TEORI ASAM BASA Teori Bronsted - Lowry Asam : senyawa yg dapat memberikan CONTOH : proton ( H+ ) / donor proton. Basa: senyawa yg dapat menerima proton (H+) / akseptor proton. Reaksi tanpa Pelarut Air HCl(g) + NH 3(g) NH 4+ + Cl- NH 4 Cl(s) Asam Basa Reaksi dengan Pelarut Air HCl(g) + H 2 O(aq) H 3 O+(aq) + Cl-(aq) Asam Basa NH 4 OH(g) + H 2 O(aq) NH 4 OH 2+(aq) + OH-(aq) Basa Asam Air dapat bersifat asam atau basa Amfoter

TEORI ASAM BASA Pasangan Asam Basa Konjugasi HCl + H 2 O Asam 1 Basa 1 H 3 O+ + Cl- Asam 2 Basa 2 Konjugasi Pasangan asam basa konjugasi : pasangan asam 1 – basa 2 dan basa 1 – asam 2 HCl – Cl- dan H 2 O – H 3 O+ Asam konjugasi : Asam yg terbentuk dari basa yang menerima Proton H 3 O+ Basa konjugasi : Basa yg terbentuk dari asam yang melepaskan Proton Cl-

TEORI ASAM BASA Jelaskan untuk reaksi : NH 3 + H 2 O NH 4+ + OH- a. Pasangan asam basa konjugasi b. Asam konjugasi c. Basa konjugasi
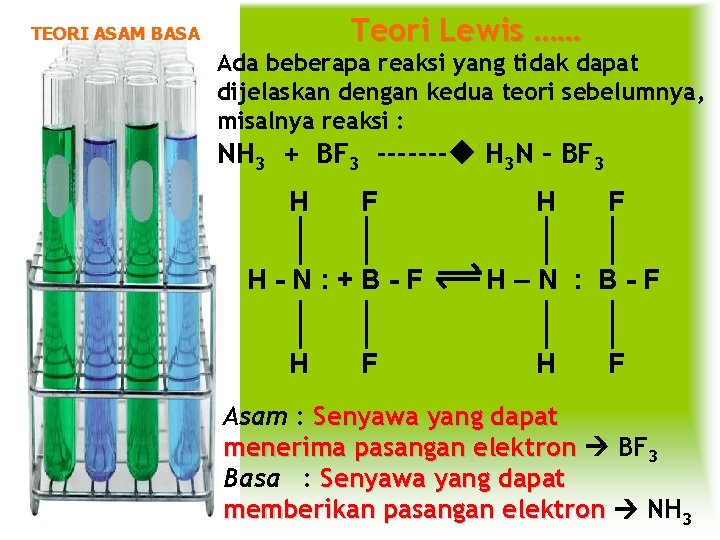
Teori Lewis …… TEORI ASAM BASA Ada beberapa reaksi yang tidak dapat dijelaskan dengan kedua teori sebelumnya, misalnya reaksi : NH 3 + BF 3 ------- H 3 N – BF 3 H F H-N: +B-F H F H–N : B-F H F Asam : Senyawa yang dapat menerima pasangan elektron BF 3 Basa : Senyawa yang dapat memberikan pasangan elektron NH 3

GARAM Adalah senyawa yang terbentuk dari reaksi asam dan basa contoh garam dapur ( Na. Cl ) dapat diperoleh dgn cara : ˜ mengendapkan air laut (penguapan atau kristalisasi ) ˜ mereaksikan asam dan basa (netralisasi) HCl + Na. OH Na. Cl + H 2 O

IDENTIFIKASI ASAM, BASA DAN GARAM Sifat larutan dapat ditunjukan dengan indikator asam-basa. yaitu : zat-zat warna yang menghasilkan warna berbeda dlm larutan asam dan basa. antara lain : kertas lakmus larutan indikator / larutan alami

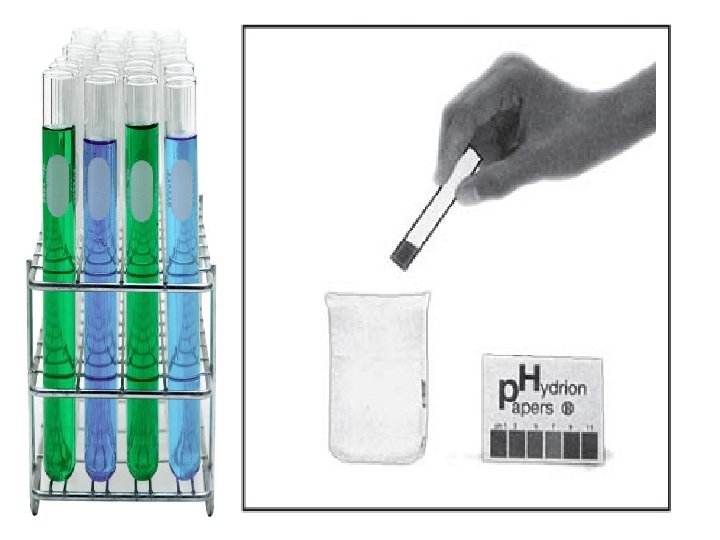
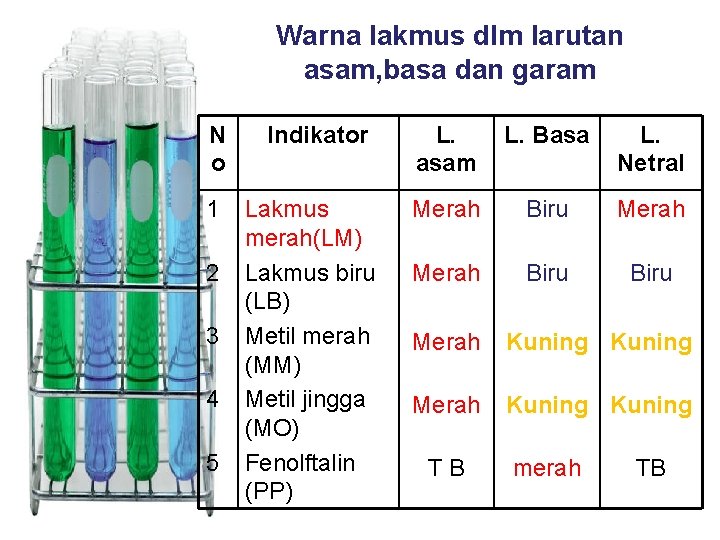
Warna lakmus dlm larutan asam, basa dan garam N o 1 2 3 4 5 Indikator L. asam L. Basa L. Netral Lakmus merah(LM) Lakmus biru (LB) Metil merah (MM) Metil jingga (MO) Fenolftalin (PP) Merah Biru Merah Kuning TB merah TB

Beberapa keuntungan lakmus sebagai indikator asam-basa 1. Dapat berubah warna dengan cepat saat bereaksi dengan asam maupun basa 2. Sukar bereaksi dengan oksigen dalam udara, sehingga dapat tahan lama 3. Mudah diserap oleh kertas. Selain indikator buatan, bisa dipakai juga indikator alami. Misalnya : bunga sepatu, kunyit, kulit manggis, kubis ungu

Penentuan Skala Keasaman dan Kebasaan Perubahan Warna Indikator Universal Larutan p. H ≤ 3 4 5 6 7 8 9 ≥ 10 Warna indikator Universal Merah jingga Jingga Kuning Hijau kekuningan Biru kehijauan Biru ungu

TATA NAMA ASAM • Rumus asam terdiri atas : a. atom hidrogen (di depan, dapat dianggap sebagaiion H+) b. suatu anion yang disebut sisa asam. • . Akan tetapi, perlu diingat bahwa asam adalah senyawa kovalen, bukan senyawa ion. Nama anion sisaasam sama dengan asam yang bersangkutan tanpa kata asam.

Contoh: H 3 PO 4 ��→ 3 H+ + PO 43– ↓ ↓ ion asam anion sisa asam (fosfat) • Nama asam tersebut adalah asam fosfat.

TATA NAMA BASA • Nama senyawa basa sama dengan nama kationnya yang diikuti kata hidroksida. • Contoh: Na. OH ��→ Na+ + OH– ↓ ↓ natrium hidroksida

TATA NAMA GARAM • Garam adalah senyawa ion yang terdiri dari kation basa dan anion sisa asam. • Rumus dan pemberian nama senyawa garam sama dengan senyawa ion
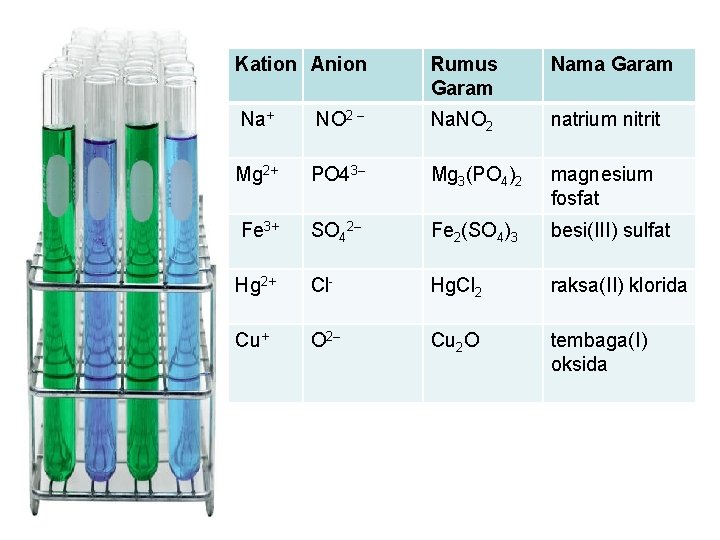
Kation Anion Rumus Garam Nama Garam Na+ NO 2 – Na. NO 2 natrium nitrit Mg 2+ PO 43– Mg 3(PO 4)2 magnesium fosfat Fe 3+ SO 42– Fe 2(SO 4)3 besi(III) sulfat Hg 2+ Cl- Hg. Cl 2 raksa(II) klorida Cu+ O 2– Cu 2 O tembaga(I) oksida
![KESETIMBANGAN ASAM DAN BASA Kesetimbangan Asam Monoprotik : H+ + A - HA [H+] KESETIMBANGAN ASAM DAN BASA Kesetimbangan Asam Monoprotik : H+ + A - HA [H+]](http://slidetodoc.com/presentation_image_h2/b0b7c41208ee00d1572bd394050165d7/image-22.jpg)
KESETIMBANGAN ASAM DAN BASA Kesetimbangan Asam Monoprotik : H+ + A - HA [H+] [A-] Ka = [HA] Asam diprotik : H 2 A Ka = Konstanta kesetimbangan asam H+ + A [H+] [A-] Ka = [H 2 A]
![KESETIMBANGAN ASAM DAN BASA HA- H+ + A 2[H+] [A 2 -] Ka 2 KESETIMBANGAN ASAM DAN BASA HA- H+ + A 2[H+] [A 2 -] Ka 2](http://slidetodoc.com/presentation_image_h2/b0b7c41208ee00d1572bd394050165d7/image-23.jpg)
KESETIMBANGAN ASAM DAN BASA HA- H+ + A 2[H+] [A 2 -] Ka 2 = Ka 1 x Ka 2 = ? ? ? [HA-] Konstanta kesetimbangan Asam pada 250 C Nama Rumus Ka Asam Klorida Asam Nitrat Asam Sulfat HCl HNO 3 H 2 SO 4 Asam Florida Asam Nitrit Asam Sulfita HF HNO 2 H 2 S 1, 0 x 107 sifat asam 1, 0 x 109 (Ka 1) 1, 2 x 10 -2 (Ka 2) 6, 6 x 10 -4 5, 1 x 10 -4 1, 1 x 10 -7 (Ka 1) 1, 0 x 10 -14 (Ka 2) Nilai Ka : Ka > 10 : Asam kuat Ka < 10 : Asam lemah
![Kesetimbangan Basa KESETIMBANGAN ASAM DAN BASA Basa Monohidroksi : B+ + OH- BOH [B+] Kesetimbangan Basa KESETIMBANGAN ASAM DAN BASA Basa Monohidroksi : B+ + OH- BOH [B+]](http://slidetodoc.com/presentation_image_h2/b0b7c41208ee00d1572bd394050165d7/image-24.jpg)
Kesetimbangan Basa KESETIMBANGAN ASAM DAN BASA Basa Monohidroksi : B+ + OH- BOH [B+] [OH-] Kb = Konstanta kesetimbangan basa Kb = [BOH] Basa dihidroksi : B(OH)2 B 2+ + 2(OH)[B 2+] [OH-]2 Kb = B[OH]2
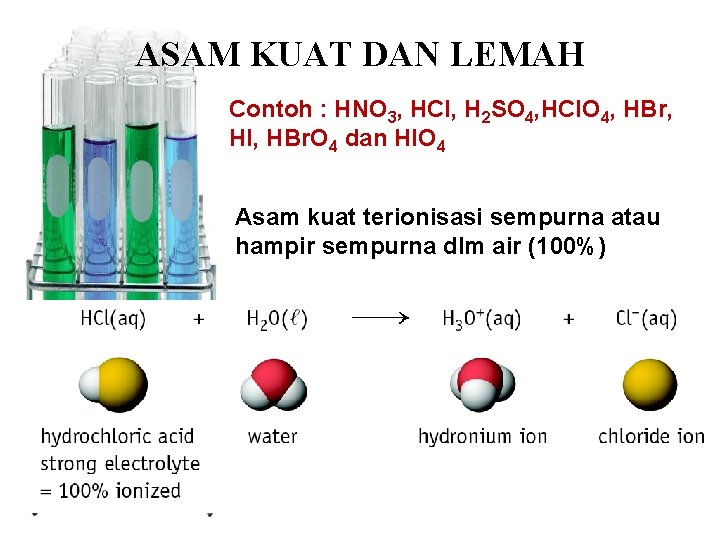
ASAM KUAT DAN LEMAH Contoh : HNO 3, HCl, H 2 SO 4, HCl. O 4, HBr, HI, HBr. O 4 dan HIO 4 Asam kuat terionisasi sempurna atau hampir sempurna dlm air (100%)
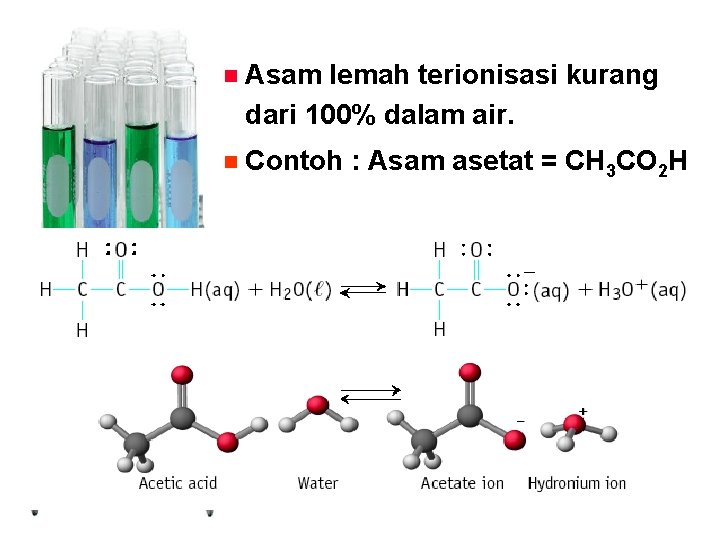
n Asam lemah terionisasi kurang dari 100% dalam air. n Contoh : Asam asetat = CH 3 CO 2 H

• • ASAMKUATHASILKANBASA TERKONJUGASIYANGLEMAH • • ASAMLEMAHHASILKANBASA TERKONJUGASIYANGKUAT • • ASAMKUAT: : HH 2 SO HCl, HNO 3 3 2 SO 4, 4, HCl, DANHCl. O 4 4 • • ASAMLEMAH: : HH 3 PO HNO 2, 2, HOCl, 3 PO 4, 4, HNO ASAM HOCl, ORGANIK ASAM ORGANIK

KEKUATAN ASAM DAN BASA • NAMA ASAM HCl. O 4 HCl H 2 SO 4 HNO 3 H 3 O+ H 2 SO 3 H 2 SO 4 H 3 PO 4 HF HC 2 H 3 O 2 H 2 CO 3 H 2 S KEKUATAN MENURUN BASA KONJUGAT Cl. O 4 Cl HSO 4 NO 3 H 2 O HSO 3 SO 42 H 2 PO 4 FC 2 H 3 02 HCO 3 HS- KEKUATAN MENINGKAT

Lanjutan : KEKUATAN ASAM DAN BASA Nama Asam HSO 4 HCN NH 4+ HCO 3 HSH 2 O NH 3 OH- Basa Konjugat SO 32 CNNH 3 CO 32 S 2 OHNH 2 O 2 -
![• [H+] = [OH-] • [H+] > [OH-] • [H+] < [OH-] NEUTRAL • [H+] = [OH-] • [H+] > [OH-] • [H+] < [OH-] NEUTRAL](http://slidetodoc.com/presentation_image_h2/b0b7c41208ee00d1572bd394050165d7/image-30.jpg)
• [H+] = [OH-] • [H+] > [OH-] • [H+] < [OH-] NEUTRAL ACIDIC BASIC • SKALA p. H = - log [H+] p. OH = - log [OH-] p. H + p. OH = 14 Kw = [H+] [OH-] Contoh : p. H Coca Cola = 3, 12 Berapa [H 3 O+] Jawab : p. H = -log [H 3 O+] = - p. H [H 3 O+] = 10 -p. H (antilog) = 10 -3, 12 = 7, 6 x 10 -4
![1. Diketahui p. H darah manusia 7, 41 Berapa p. OH, [H+], [OH-] ? 1. Diketahui p. H darah manusia 7, 41 Berapa p. OH, [H+], [OH-] ?](http://slidetodoc.com/presentation_image_h2/b0b7c41208ee00d1572bd394050165d7/image-31.jpg)
1. Diketahui p. H darah manusia 7, 41 Berapa p. OH, [H+], [OH-] ? p. OH : p. H + p. OH = 14 7, 41 + p. OH = 14 p. OH = 6, 59 [H+] : p. H = - log [H+] 7, 41 = - log [H+] 10 -7, 41 = [H+]= 3, 89 x 10 -8 M [OH-] : p. OH = - log [OH-] 6, 59 = - log [OH-] 10 -6, 59 = [OH-] = 2, 57 x 10 -7 M Berapa p. H pada 0, 1 M HNO 3 p. H = - log [H+] = - log 0, 1 = 1
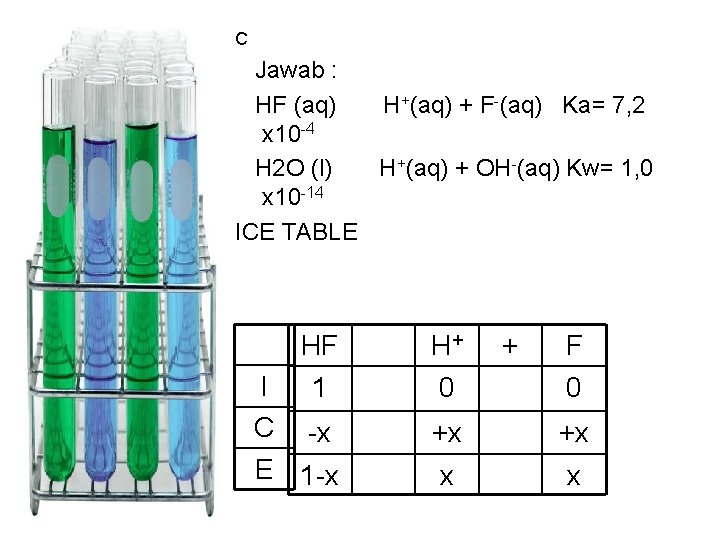
C Jawab : HF (aq) H+(aq) + F-(aq) Ka= 7, 2 x 10 -4 H 2 O (l) H+(aq) + OH-(aq) Kw= 1, 0 x 10 -14 ICE TABLE HF H+ + F I 1 C -x E 1 -x 0 0 +x +x x x
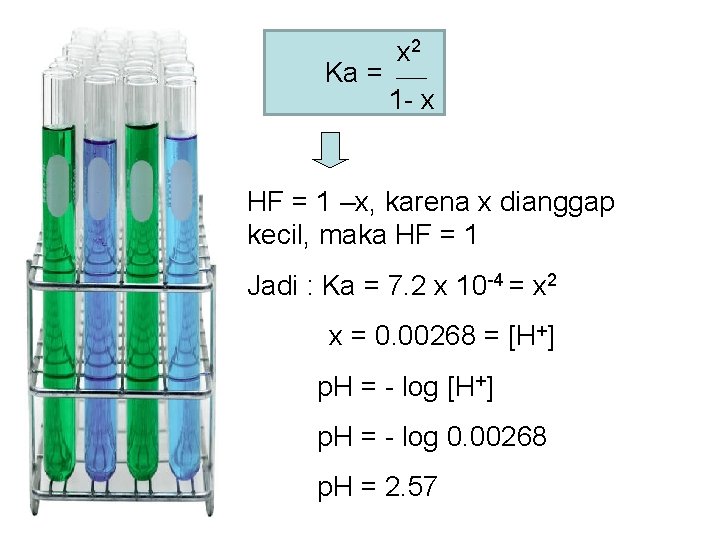
Ka = x 2 1 - x HF = 1 –x, karena x dianggap kecil, maka HF = 1 Jadi : Ka = 7. 2 x 10 -4 = x 2 x = 0. 00268 = [H+] p. H = - log 0. 00268 p. H = 2. 57

KESETIMBANGAN ASAM DAN BASA TUGAS Carilah 20 jenis asam dan basa, beserta rumus molekul dan nilai konstanta kesetimbangannya, serta klasifikasikan berdasarkan kekuatan sifat asamnya.
- Slides: 34