Aromatik Bileikler 1 Philosophical Transactions the worlds first

Aromatik Bileşikler 1

Philosophical Transactions − the world's first science journal In 1662, the newly formed 'Royal Society of London for Improving Natural Knowledge' was granted a charter to publish by King Charles II and on 6 March 1665, the first issue of Philosophical Transactions was published under the visionary editorship of Henry Oldenburg, who was also the Secretary of the Society. The first volumes of what was the world's first scientific journal were very different from today's journal, but in essence it served the same function; namely to inform the Fellows of the Society and other interested readers of the latest scientific discoveries. As such, Philosophical Transactions established the important principles of scientific priority and peer review, which have become the central foundations of scientific journals ever since. In 1886, the breadth and scope of scientific discovery had increased to such an extent that it became necessary to divide the journal into two, Philosophical Transactions A and B, covering the physical sciences and the life sciences respectively. http: //rstl. royalsocietypublishing. org/

https: //royalsocietypublishing. org/doi/pdf/10. 1098/rstl. 1825. 0022

Michael Faraday 1791 – 1867 Michael Faraday‘ın izole ettiği bileşik “Bi-carburet of hydrogen”. http: //www. rigb. org/our-history/iconic-objects-list/faradaybenzene

Faraday’ın saf olarak elde ettiği bileşik için belirlediği basit formül ve molekül formülü Basit formül = C 2 H Molekül formülü= C 6 H 3 Molekül Ağırlığı= 39

Eilhard Mitscherlich 1794 - 1863 1834 Yılında benzoik asit bileşiğinin ısıtılmasıyla Faraday’ın “Bi-carburet of hydrogen” olarak isimlendirdiği bileşiği sentezliyor. Bileşiğin Basit formülünün CH ve Molekül formülünün C 6 H 6 ve Molekül Ağırlığının 79 olduğunu belirliyor. Bileşiği “benzin” olarak isimlendiriyor. Günümüzde bu bileşik benzen olarak isimlendiriliyor.

Friedrich August Kekule von Stradoniz 1829 -1 896 1866 Yılında Friedrich August Kekule, benzen bileşiğinin üç adet ikili bağ içeren halkalı bir yapıda olduğunu ileri sürüyor.
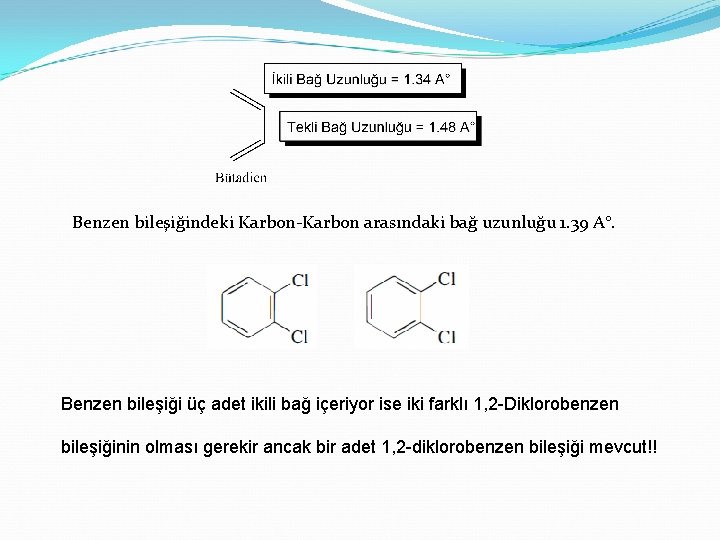
Benzen bileşiğindeki Karbon-Karbon arasındaki bağ uzunluğu 1. 39 A°. Benzen bileşiği üç adet ikili bağ içeriyor ise iki farklı 1, 2 -Diklorobenzen bileşiğinin olması gerekir ancak bir adet 1, 2 -diklorobenzen bileşiği mevcut!!
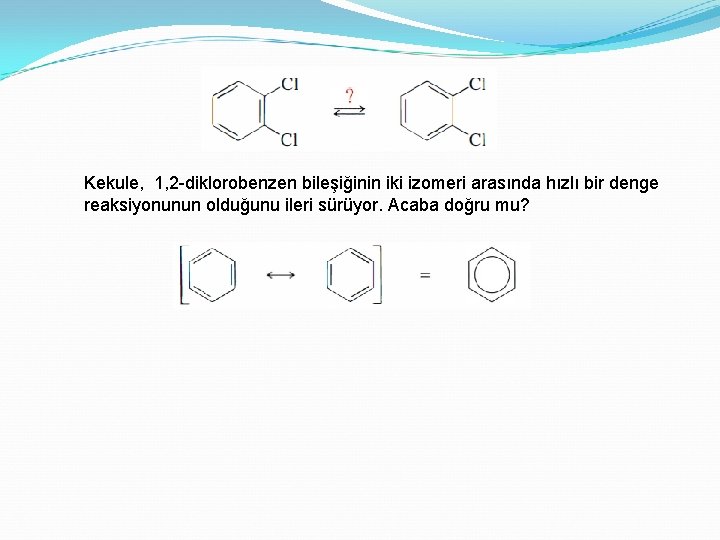
Kekule, 1, 2 -diklorobenzen bileşiğinin iki izomeri arasında hızlı bir denge reaksiyonunun olduğunu ileri sürüyor. Acaba doğru mu?
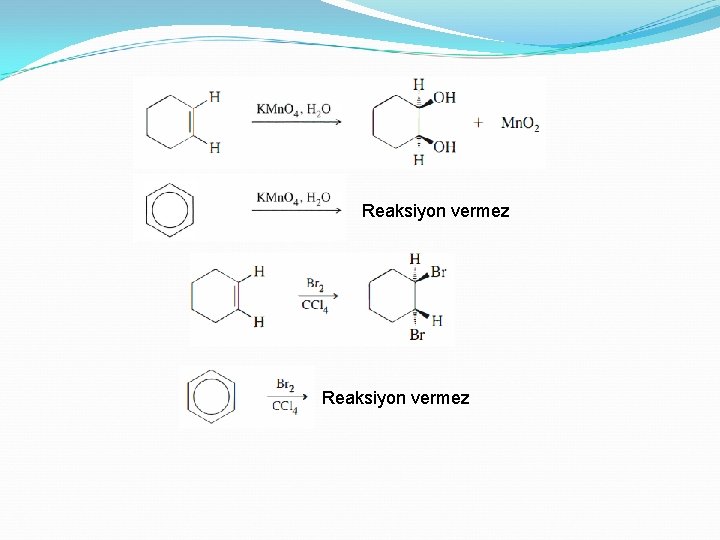
Reaksiyon vermez
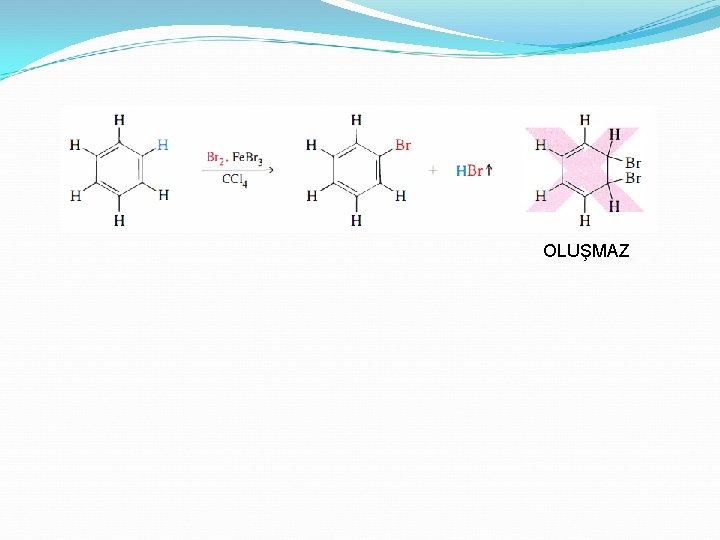
OLUŞMAZ

Richard Willstätter 1872 -1942 Siklooktatetraen 1900 Yılından önce kimyacılar, aromatikliği sağlayan yapı özelliklerinden birisinin halkalı bileşiklerin birbirini izleyen birli ve ikili bağlara (konjuge çifte bağlara) sahip olması gerektiğini kabul etmişlerdi. O yıllarda sadece benzen ve benzen türevleri (yani altı üyeli halkalı bileşikler) bilinen aromatik bileşikler olduğu için kimyacılar başka örnekleri sentezlemeyi düşündüler. 1911 Yılında Richard Willstätter, sekiz karbondan oluşan ve konjuge çifte bağ içeren halkalı bir bileşik olan siklooktatetraen’i sentezlemeyi başardı.
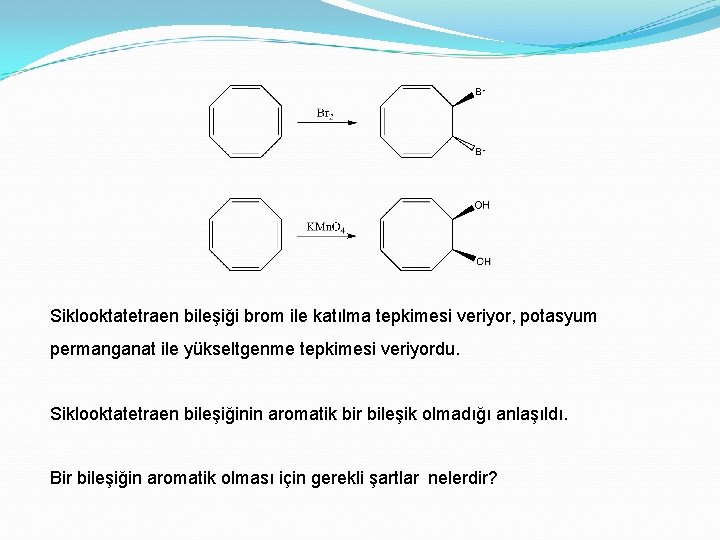
Siklooktatetraen bileşiği brom ile katılma tepkimesi veriyor, potasyum permanganat ile yükseltgenme tepkimesi veriyordu. Siklooktatetraen bileşiğinin aromatik bir bileşik olmadığı anlaşıldı. Bir bileşiğin aromatik olması için gerekli şartlar nelerdir?

Benzenin Yapısıyla İlgili Modern Teoriler Kuantum mekaniğinin gelişimine kadar (1920’li yıllar) benzen bileşiğinin olağan dışı davranışı ve kararlılığı anlaşılamamıştır. Kuantum mekaniği, moleküllerdeki bağların açıklanmasını iki yolla yapar; 1) Rezonans teorisi 2) Moleküler orbital teorisi

1) Benzen’in yapısının rezonans teorisi ile açıklanması Rezonans teorisi, bir molekül için sadece π veya n elektronlarının konumlarının farklı olduğu iki veya daha fazla Lewis yapısı yazılabildiğinde, bu yapıların hiçbirisinin bileşiğin kimyasal ve fiziksel özellikleri ile tam bir uyum içerisinde olmadığı esasına dayanır. Benzen bileşiğinin yapısı Kekule’nin önerdiği gibi dengedeki iki farklı molekülü temsil etmezler. Yazılan mezomer limit formülleri molekülün gerçek yapıları değildir, en yakın yapılardır, fakat gerçek molekül tüm mezomer limit formüllerinin bir melezidir.

Spektroskopik ölçümler, benzen molekülünün düzlemsel ve bütün karbon bağlarının eşit uzunlukta olduğunu göstermiştir. Melez yapı, düzgün altıgen içine bir daire çizilerek gösterilir ve bu gösteriş biçimi günümüzde en çok kullanılan formüldür. Elektronların gözönüne alınması gereken durumlarda Kekule yapılarından herhangi birini kullanabiliriz. Benzen formülündeki daire, altı elektronun benzen halkasındaki altı karbon atomu üzerinde dağıldığını gösterir. Diğer aromatik sistemlerde ise daire, altıdan farklı sayıdaki elektronun halkada dağıldığını gösterebilir.
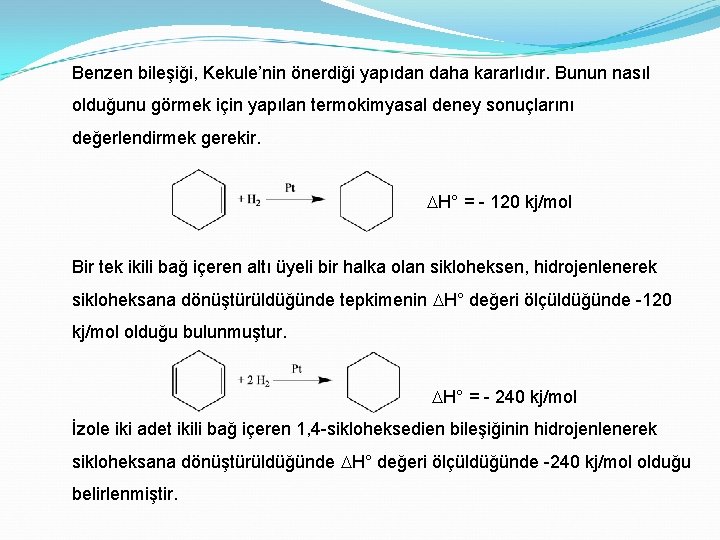
Benzen bileşiği, Kekule’nin önerdiği yapıdan daha kararlıdır. Bunun nasıl olduğunu görmek için yapılan termokimyasal deney sonuçlarını değerlendirmek gerekir. DH° = - 120 kj/mol Bir tek ikili bağ içeren altı üyeli bir halka olan sikloheksen, hidrojenlenerek sikloheksana dönüştürüldüğünde tepkimenin DH° değeri ölçüldüğünde -120 kj/mol olduğu bulunmuştur. DH° = - 240 kj/mol İzole iki adet ikili bağ içeren 1, 4 -sikloheksedien bileşiğinin hidrojenlenerek sikloheksana dönüştürüldüğünde DH° değeri ölçüldüğünde -240 kj/mol olduğu belirlenmiştir.
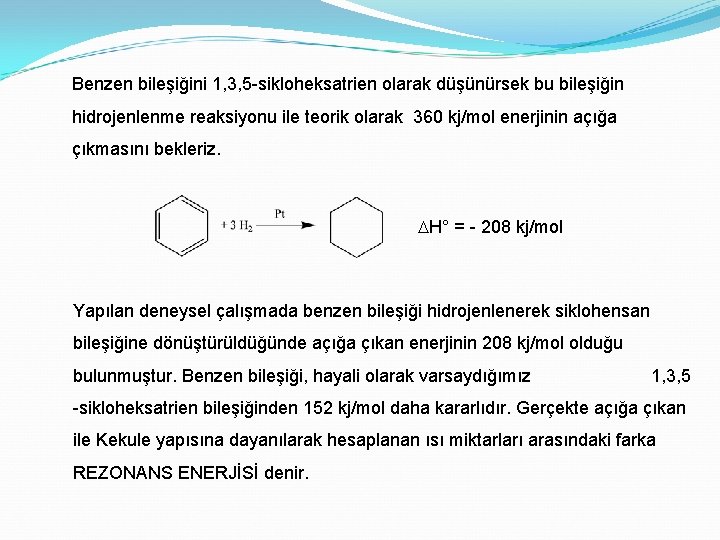
Benzen bileşiğini 1, 3, 5 -sikloheksatrien olarak düşünürsek bu bileşiğin hidrojenlenme reaksiyonu ile teorik olarak 360 kj/mol enerjinin açığa çıkmasını bekleriz. DH° = - 208 kj/mol Yapılan deneysel çalışmada benzen bileşiği hidrojenlenerek siklohensan bileşiğine dönüştürüldüğünde açığa çıkan enerjinin 208 kj/mol olduğu bulunmuştur. Benzen bileşiği, hayali olarak varsaydığımız 1, 3, 5 -sikloheksatrien bileşiğinden 152 kj/mol daha kararlıdır. Gerçekte açığa çıkan ile Kekule yapısına dayanılarak hesaplanan ısı miktarları arasındaki farka REZONANS ENERJİSİ denir.

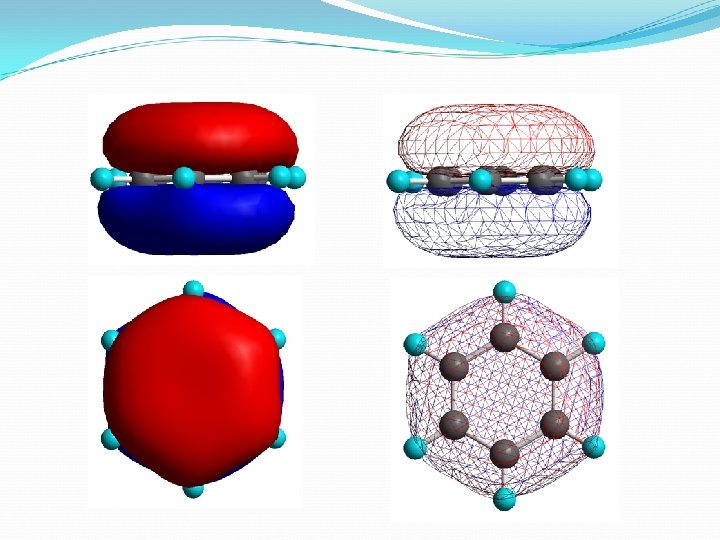
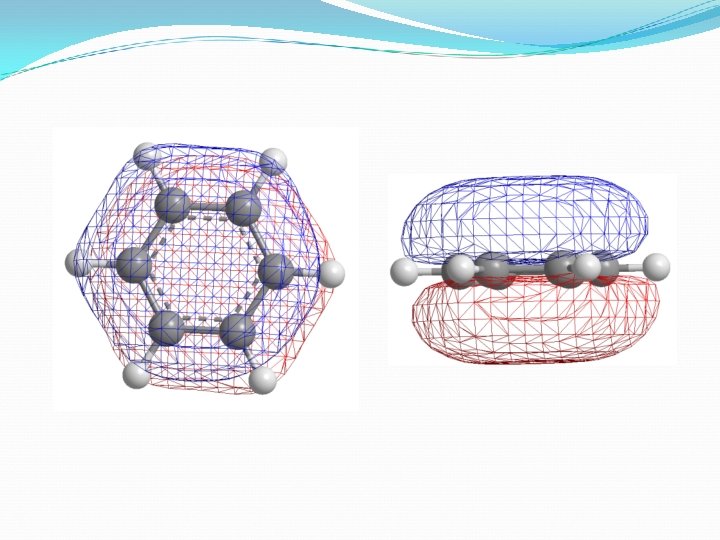
2) Benzen’in yapısının moleküler orbital teorisi ile açıklanması Benzen halkasındaki karbon atomlarının bağ açılarının 120° olması, karbon atomlarının sp 2 melezleşmiş olduğunu belirtir. Karbon karbon bağ uzunluklarının tamamı 1, 39 A°’dır ve molekül altı üyeli düzlemsel bir halka yapısına sahiptir. Moleküler orbital teorisine göre her bir karbon atomundaki altı p orbitali, altı π moleküler orbitali oluşturmak üzere birleşir. Benzen bileşiğinde bütün bağ yapıcı π moleküler orbitallerinin dolu olduğu, bağ karşıtı moleküler orbitallerde elektron bulunmadığı görülür. Benzen bileşiğindeki altı adet dağılmış π elektronlarının molekül kararlılığından sorumludur.

ANULENLER Anulen adı, halkada birer atlayarak birli ve ikili bağlar taşıyan tek halkalı bileşiklerin genel adıdır. Annulenlerde halka büyüklüğü köşeli parantez içindeki bir sayıyla belirtilir.

Erich Huckel 1896 -1980 Hückel Kuralı, her atomunda bir p orbitali bulunan (4 n+2) sayıda (n= 0, 1, 2, 3, …) π elektronuna sahip düzlemsel yapıdaki tek halkalı bileşikler aromatiktir. Bir başka ifadeyle 2, 6, 10, 14, …. vb. sayıda π elektronuna sahip düzlemsel yapıdaki tek halkalı bileşikler aromatiktir.

Benzen molekülünde bulunan her bir karbon atomu sp 2 hibritleşmesine uğramıştır. Yani her bir karbon atomunda birer adet hibritleşmeye uğramamış p orbitali bulunmaktadır. Benzen molekülü 6 adet π elektronuna sahiptir; Hückel Kuralına uyar (4 n+2=6, n=1, n tam sayı). Benzen molekülü düzlemsel yapıdadır. Benzen bileşiği aromatik bir bileşiktir

1, 3 -Sikloheksadien bileşiği aromatik midir? 1, 3 -Sikloheksadien bileşiğinde 1, 2, 3, 4 nolu karbon atomları sp 2 hibritleşmesine uğramıştır ve bu karbon atomunlarında birer adet hibritleşmeye uğramamış p orbitali bulunmaktadır. 5 ve 6 Numaralı karbon atomları ise sp 3 hibritleşmesine uğramışlardır. 5 ve 6 nolu karbon atomlarında p orbitali YOKTUR. Bileşikte 4 adet π elektronuna sahiptir; Hückel Kuralına göre değerlendirildiğinde 4 n+2=4, n=0. 5, n tam sayı değil. Hückel kuralına UYMAZ. Bileşik düzlemsel DEĞİLDİR. AROMATİK DEĞİL.
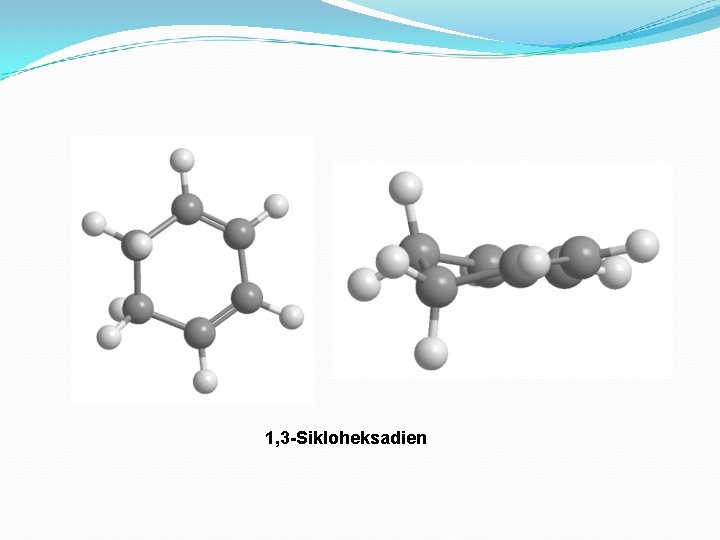
1, 3 -Sikloheksadien

Siklooktatetraen bileşiği aromatik midir? Moleküldeki tüm karbonlar sp 2 hibritleşmesine uğramıştır ve bu karbon atomunlarında birer adet hibritleşmeye uğramamış p orbitali bulunmaktadır. Bileşikte 8 adet π elektronuna sahiptir; Hückel Kuralına göre değerlendirildiğinde 4 n+2=8, n=1. 5, n tam sayı değil. Hückel kuralına UYMAZ. Bileşik düzlemsel DEĞİLDİR. AROMATİK DEĞİL.
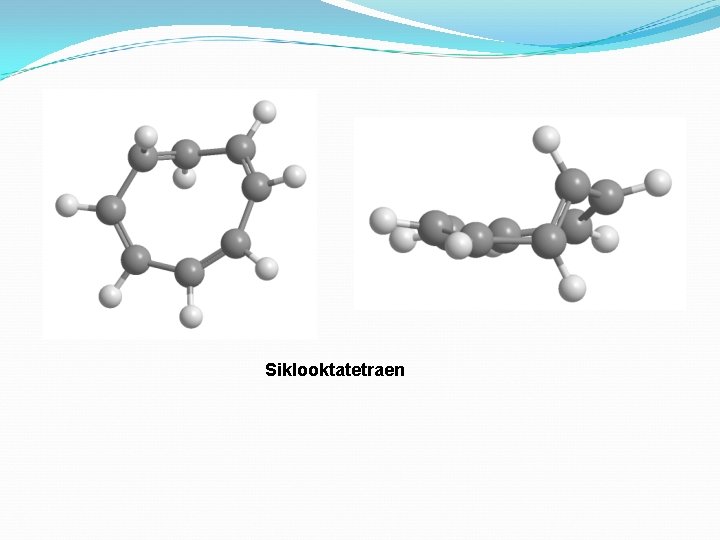
Siklooktatetraen
![Aşağıda isimleri yazılı olan annulen’lerin hangileri aromatiktir? [6] Anulen [8] Anulen [10] Anulen [12] Aşağıda isimleri yazılı olan annulen’lerin hangileri aromatiktir? [6] Anulen [8] Anulen [10] Anulen [12]](http://slidetodoc.com/presentation_image_h/25af74f261e25589d7687761bc87a4ef/image-29.jpg)
Aşağıda isimleri yazılı olan annulen’lerin hangileri aromatiktir? [6] Anulen [8] Anulen [10] Anulen [12] Anulen [14] Anulen [16] Anulen [18] Anulen Not = [6] Anulen [14] Anulen ve [18] Anulen bileşikleri düzlemseldir.
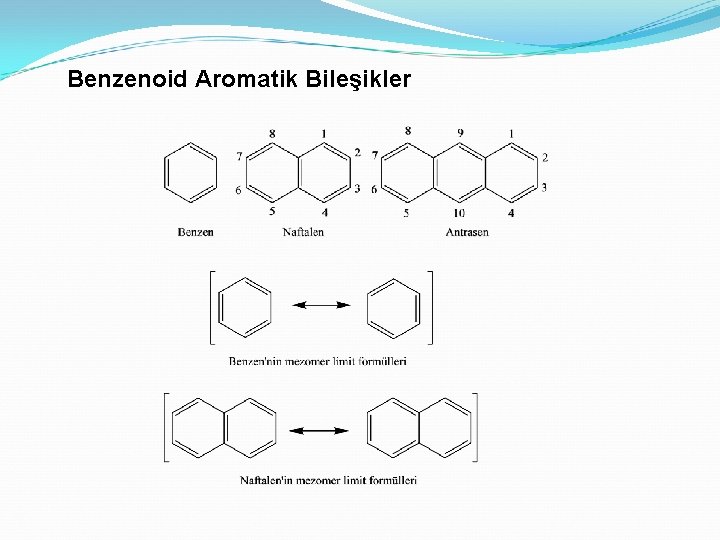
Benzenoid Aromatik Bileşikler
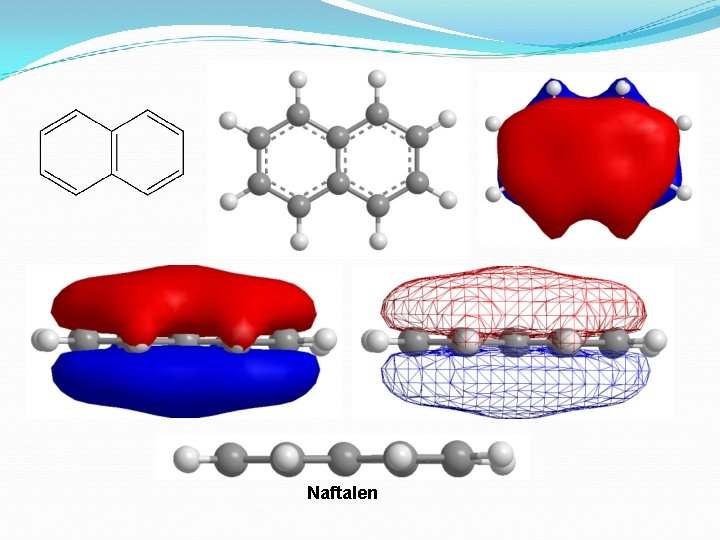
Naftalen
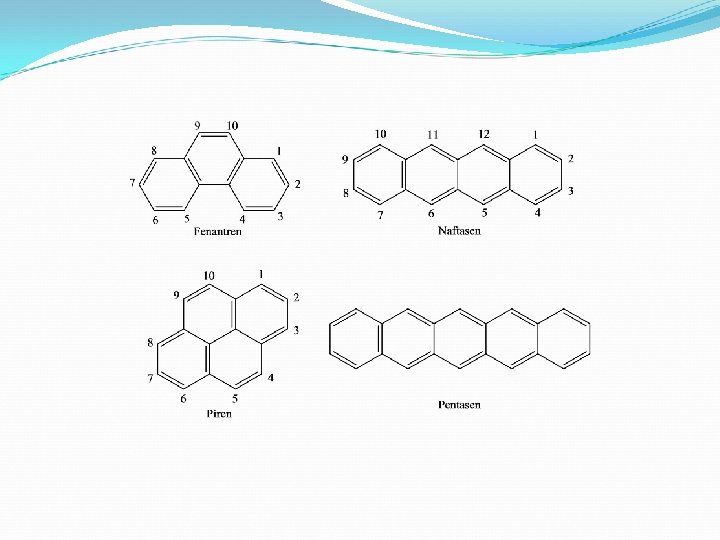

Aromatik iyonlar Siklopentadien bileşiği 4 adet π elektronu olduğu için Huckel kuralına uymaz. sp 3 Hibritleşmesi yapmış bir karbon atumu içerdiği için π elektronları halkayı oluşturan tüm karbon atomlarına dağılamaz. Sonuç olarak siklopentadien bileşiği aromatik değildir. Siklopentadienil anyonu ise 6 adet π elektronu taşır ve Hückel kuralına uyar. Tüm karbon atomları sp 2 hibritleşmesine uğramıştır. Siklopentadienil anyonu aromatik bir bileşiktir.

Aromatik iyonlar Sikloheptatrien bileşiği 6 adet π elektronu olduğu için Huckel kuralına uyar ancak halkayı oluşturan karbon atomlarından birisi sp 3 hibritleşmesi yaptığı için π elektronları halkayı oluşturan tüm karbon atomlarına dağılamaz. Sikloheptatrien bileşiği aromatik değildir. Sikloheptatrien katyonu 6 adet π elektronu taşır ve Hückel kuralına uyar. Tüm karbon atomları sp 2 hibritleşmesine uğramıştır. Sikloheptatrienil katyonu aromatik bir bileşiktir.
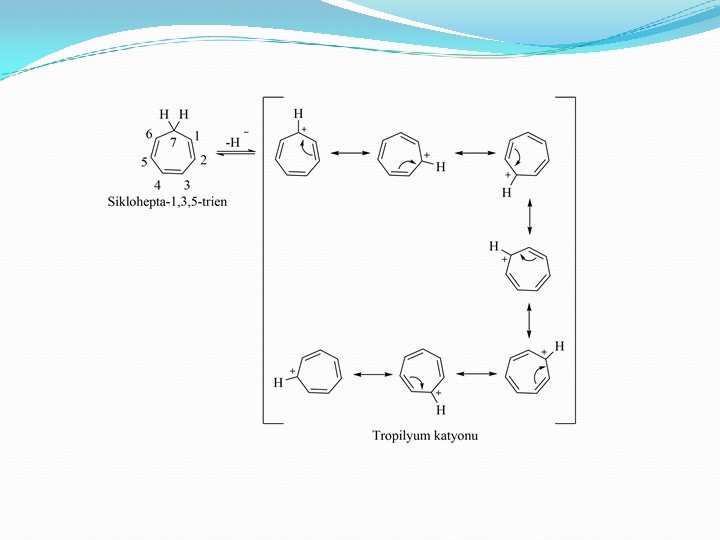

Heterohalkalı Aromatik Bileşikler Halkalı bir organik bileşikte, halkayı oluşturan atomlardan bir ya da birden fazlası karbon dışında bir element ise bu bileşiklere heterohalkalı bileşikler denir. Heterohalkalı bileşiklerde halkada azot, oksijen veya kükürt bulunan bileşikler çok yaygındır.

Piridin 6 üyeli halkalı bir bileşiktir. Benzen bileşiğindeki karbon atomundan birisinin yerine azot atomu bulunmaktadır. Azot atomu da halkayı oluşturan diğer karbon atomları gibi sp 2 hibritleşmesine uğramıştır. Piridin’de azot atomu üzerindeki ortaklanmamış elektron çifti halka ile aynı düzlemde bulunduğu için halkadaki diğer p orbitalleri ile örtüşmez ve Hückel Kuralı’nda bu iki elektron dahil edilmez. Piridin heteroaromatik bir bileşiktir.

Pirol 5 üyeli halkalı bir bileşiktir. Azot atomu da halkayı oluşturan diğer karbon atomları gibi sp 2 hibritleşmesine uğramıştır. Piridin’den farklı olarak Pirol bileşiğinde azot atomu üzerindeki ortaklanmamış elektron çifti π sisteminin bir parçasıdır, iki elekatronun da katkısıyla aromatik altı elektronlu yapıya ulaşılır.

Furan ve Tiyofen 5 üyeli halkalı aromatik bileşiklerdir. Oksijen ve kükürt atomlarındaki sp 2 hibrit orbitallerindeki iki elektron halka ile aynı düzlemde bulunduğu için π sisteminin bir parçası değildir. O ve S atomlarının p orbitalinde bulunan iki elektron ise halkadaki π sisteminin bir parçasıdır.
Fullerenler

Fullerenler 1980’li yıllara kadar elementel karbonun iki allotropik şekli, elmas ve grafit biliniyordu. Elmas Grafit 1985 Yılında bilim adamları uzaydaki kımızı yıldızlardan gelen karbon bileşikleri üzerinde araştırmalar yaptılar ve daha sonra bu bileşikleri laboratuvarda sentezlemek için grafiti yüksek enerjili lazer ışınlarına maruz bıraktılar.

Gerçekleştirilen deney sonuçlarının değerlendirildiğinde sentezlenmesi amaçlanan bileşikler dışında molekül ağırlığı 720 ve 840 olan iki bileşiğin bulunduğunu tespit edildi. Çalışmayı yapan bilim insanları Molekül ağırlığı 720 olan bileşiğin kapalı formülünün C 60 olduğu belirledi ve bu bileşik için bir yapı formülü önerdiler. Beş yıl sonra geliştirilen analiz yöntemleri ile önerilen kimyasal yapının doğru olduğu kanıtlandı. Fuleren bileşiğinin yapısı

Richard Buckminster Fuller 1895 -1983 Richard Buckminster Fuller mimarlıkta bir mekanı en az gereçle örtmeyi sağlayan ‘jeodozik kubbe’ yapısını geliştiren mühendis, mimar, felsefeci, mucit. https: //www. wired. com/2016/03/buckminster-fuller-brilliant-crank-lot-teachsilicon-valley/

Kapalı formülü C 60 olan ve açık kimyasal formülü aletsel analiz yöntemleri kullanılarak belirlenen bileşiğe, ‘jeodozik kubbe’ yapılarını geliştirirken benzer şekiller kullanan Richard Buckminster Fuller’in anısına ‘buchminster fulleren’ adı verilmiştir. Günümüzde bu bileşik ‘bucky topları’ olarak adlandırılmaktadır. Fuleren bileşiğindeki tüm karbon atomları sp 2 hibritleşmesine uğramıştır. Her bir karbon atomu üç karbon atomu ile bağ yapmakta, tüm karbon atomlarındaki p orbitalleri, benzen molekülündekine benzer şekilde molekül yüzeyine dik olacak şekilde π bulutu oluşturmaktadır. Günümüzde kapalı formülü C 60 , C 76 , C 84 vb fuleren türevi bileşikler bilinmektedir.

Kaynaklar 1. Organik Kimya, Craig Fryhle, Graham Solomons, 7. Basımdan Çeviri, Literatür Yayıncılık, 2003. 2. Organic Chemistry, L. G. Wade (6 th Edition) Prentice Hall, 2005.
- Slides: 45