APRENDIZAJE ESPERADO Diferenciar istopos de isbaros ISTOPOS Dalton

APRENDIZAJE ESPERADO • Diferenciar isótopos de isóbaros

ISÓTOPOS • Dalton estaba equivocado acerca de que todos los elementos del mismo tipo son idénticos. Los átomos de un mismo elemento pueden tener diferente número de neutrones. Por lo tanto, diferente número de masa. • Estos se denominan isótopos

ISÓTOPOS • Frederick Soddy (1877 -1956) propuso la idea de los isótopos en 1912 Los isótopos son átomos del mismo elemento con diferentes masas, debido al diferente número de neutrones. Soddy ganó el Premio Nobel de Química en 1921 por su trabajo con isótopos y materiales radiactivos
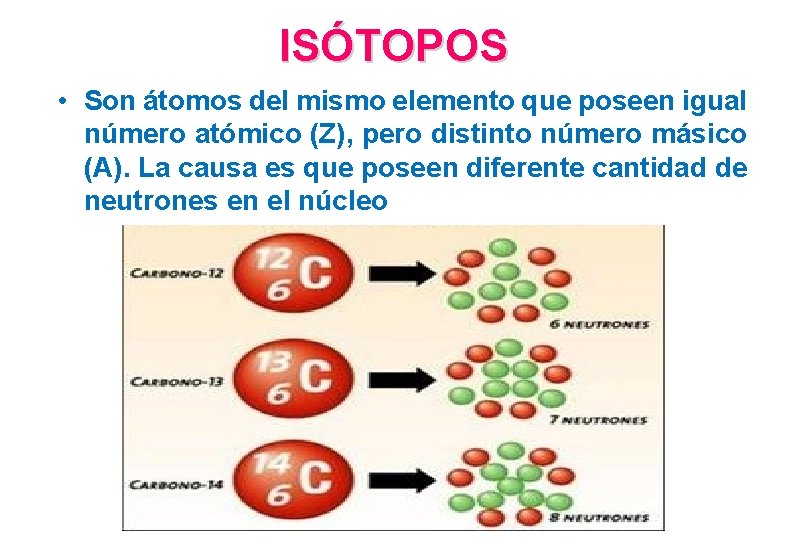
ISÓTOPOS • Son átomos del mismo elemento que poseen igual número atómico (Z), pero distinto número másico (A). La causa es que poseen diferente cantidad de neutrones en el núcleo

Nombrando Isótopos • Se puede poner el número másico después del nombre del elemento: Carbono-12 Carbono-14 Uranio-235
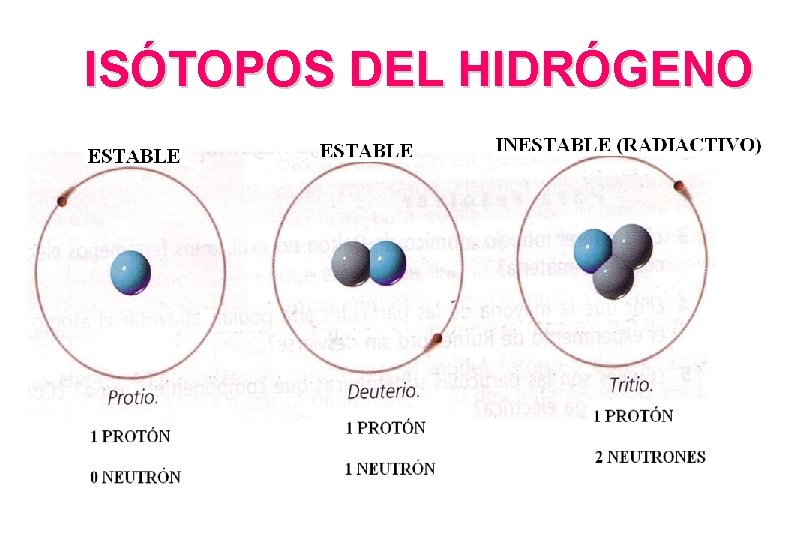
ISÓTOPOS DEL HIDRÓGENO
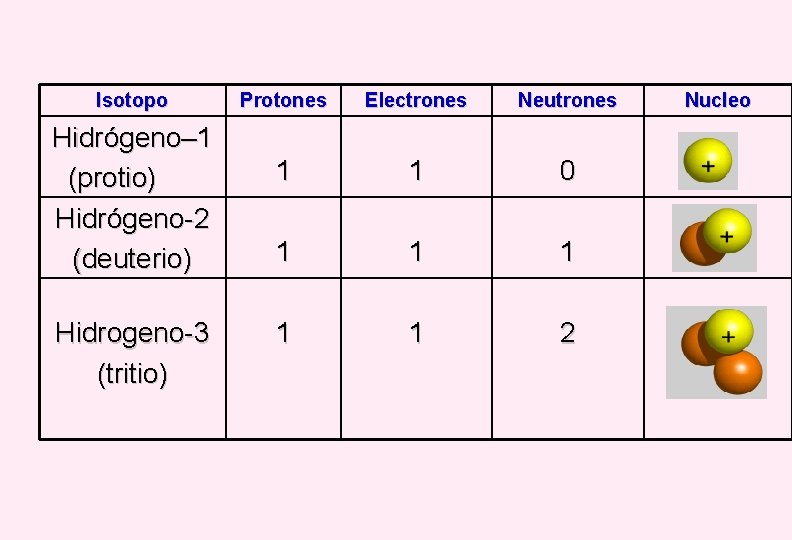
Isotopo Hidrógeno– 1 (protio) Hidrógeno-2 (deuterio) Hidrogeno-3 (tritio) Protones Electrones Neutrones 1 1 0 1 1 1 2 Nucleo
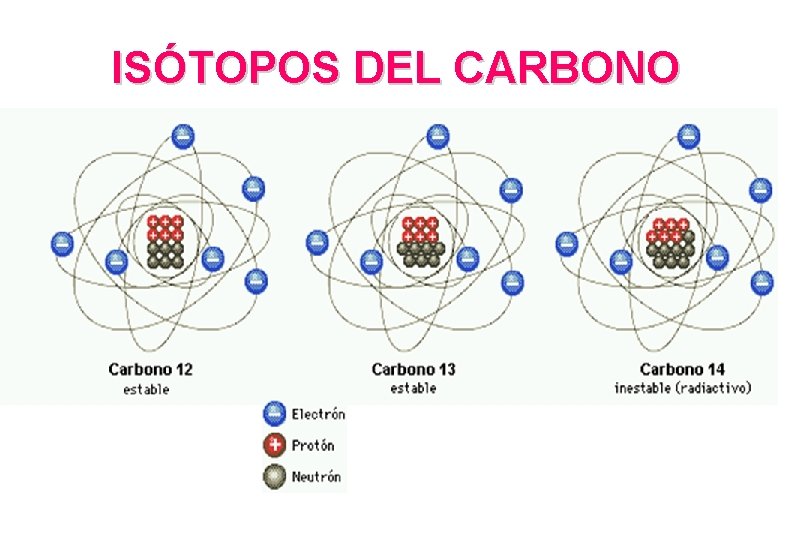
ISÓTOPOS DEL CARBONO

Se establece en átomos de un mismo elemento. EJEMPLO

NÚMERO MÁSICO EN LA TABLA PERIÓDICA • ¿Cuál es la masa de un átomo de oxígeno? Depende, porque hay diferentes tipos de átomos de oxígeno (isótopos). En la tabla periódica aparece la masa atómica promedio. Esto se basa en la abundancia (porcentaje) de cada variedad de ese elemento en la naturaleza. • No utilizamos gramos de esta masa porque los números serían demasiado pequeños

MIDIENDO LA MASA ATÓMICA • En lugar de gramos, la unidad que utilizamos es la unidad de masa atómica (uma) Se define como un doceavo de la masa de un átomo de carbono-12. • Carbono-12 elegido por su pureza isotópica. Cada isótopo tiene su propia masa atómica, por lo que se determina el promedio de abundancia por ciento

PROMEDIO DE MASA ATÓMICA • Para calcular el promedio Multiplique la masa atómica de cada isótopo por su abundancia (expresado con un decimal), luego sume los resultados. Si no se dice lo contrario, la masa del isótopo se expresa en unidades de masa atómica (uma)

MASA ATÓMICA La masa atómica es el promedio, de la masa de todos los ísótopos naturales del elemento. Isotopo Simbolo Carbono-12 12 C Carbono-13 13 C Carbono-14 14 C Composición del núcleo 6 protones 6 neutrones 6 protones 7 neutrones 6 protones 8 neutrones Carbon = 12. 011 % en la naturaleza 98. 89% 1. 11% <0. 01%

- Page 117 Question Knowns and Unknown Solution Answer

ISOBAROS • Son átomos diferentes (distintos elementos), por lo cual tienen distinto Z, pero igual número másico (A).

ISÓTONOS • Son átomos que presentan distinto número másico, distinto número atómico, pero tienen igual número de neutrones. Ejemplos:

Ejercicios: 1_ Un átomo posee 19 protones, 20 neutrones y 19 electrones. ¿Cuál de los siguientes átomos es su isótono? A) B) C) D) E) C Aplicación

2_ Identifique cuál (es) de las siguientes parejas son Isóbaros, Isótopos o Isótonos: Isótopos Isóbaros

Isótopos Isótonos Isóbaros Isótopos

RESUMEN • Isótopos: Átomos que presentan igual número atómico, pero distinto número másico. Se establece en átomos de un mismo elemento. • Isóbaros: Átomos de distinto elementos que presentan igual número másico y distinto número atómico. • Isótonos: Son átomos que presentan distinto número másico, distinto número atómico, pero tienen igual número de neutrones
- Slides: 21