Application de la raction de Michael des bnaminoesters

Application de la réaction de Michael à des b-énaminoesters Sous la Direction du Pr. Christian Cavé et du Dr Sandrine Delarue. Cochin Laboratoire de Synthèse Organique et de Pharmacochimie UMR CNRS 8076 Bio. CIS Faculté de Pharmacie de Châtenay-Malabry 5, rue J-B. Clément 92296 Châtenay-Malabry Cedex 1

PLAN I- Introduction 1 - Présentation du laboratoire d’accueil 2 - Objectif du stage II- Réaction de Michael 1 - Synthèse du b-énaminoester 2 - Réaction de Michael – Mécanisme 3 - Mode opératoire III- Appareillage utilisé 1 - Spectromètre RMN 2 - Autres appareils utilisés IV- Résultats et analyse V- Conclusion et perspectives 2
I-Introduction 1 - Présentation du laboratoire Laboratoire de Synthèse Organique et de Pharmacochimie Thèmes de recherche : Ø Synthèse d’analogues de glutamate. Ø Synthèse de peroxydes potentiellement antipaludiques. 3
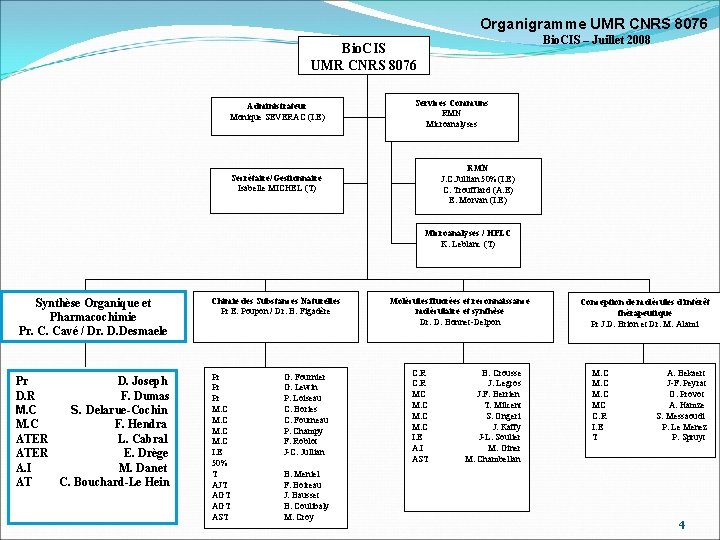
Organigramme UMR CNRS 8076 Bio. CIS – Juillet 2008 Bio. CIS UMR CNRS 8076 Administrateur Monique SEVERAC (I. E) Services Communs RMN Microanalyses RMN J. C. Jullian 50%(I. E) C. Troufflard (A. E) E. Morvan (I. E) Secrétaire/Gestionnaire Isabelle MICHEL (T) Microanalyses / HPLC K. Leblanc (T) Synthèse Organique et Pharmacochimie Pr. C. Cavé / Dr. D. Desmaele Pr D. Joseph D. R F. Dumas M. C S. Delarue-Cochin M. C F. Hendra ATER L. Cabral ATER E. Drège A. I M. Danet AT C. Bouchard-Le Hein Chimie des Substances Naturelles Pr E. Poupon / Dr. B. Figadère Pr Pr Pr M. C I. E 50% T AJT AGT AST G. Fournier G. Lewin P. Loiseau C. Bories C. Fourneau P. Champy F. Roblot J-C. Jullian B. Meniel F. Boireau J. Bausset B. Coulibaly M. Croy Molécules fluorées et reconnaissance moléculaire et synthèse Dr. D. Bonnet-Delpon C. R MC M. C I. E A. I AST B. Crousse J. Legros J. F. Berrien T. Milcent S. Ongeri J. Kaffy J-L. Soulier M. Giner M. Chambellan Conception de molécules d'intérêt thérapeutique Pr J. D. Brion et Dr. M. Alami M. C MC C. R I. E T A. Bekaert J-F. Peyrat O. Provot A. Hamze S. Messaoudi P. Le Menez P. Spruyt 4
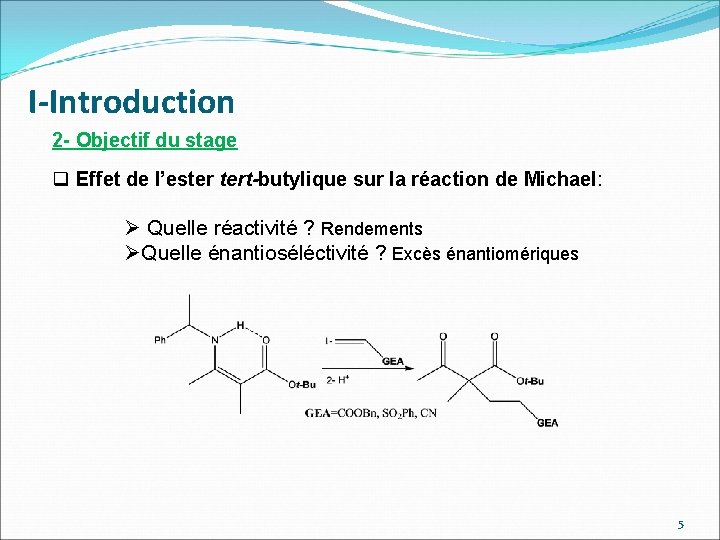
I-Introduction 2 - Objectif du stage q Effet de l’ester tert-butylique sur la réaction de Michael: Ø Quelle réactivité ? Rendements ØQuelle énantioséléctivité ? Excès énantiomériques 5

II-Réaction de Michael 2 - Synthèse du b-énaminoester q Deux conditions différentes : Deux produits différents : Rdt = 20% Rdt = 81% 6

II-Réaction de Michael 2 - Réaction de Michael - mécanisme Rdt = 48% 7
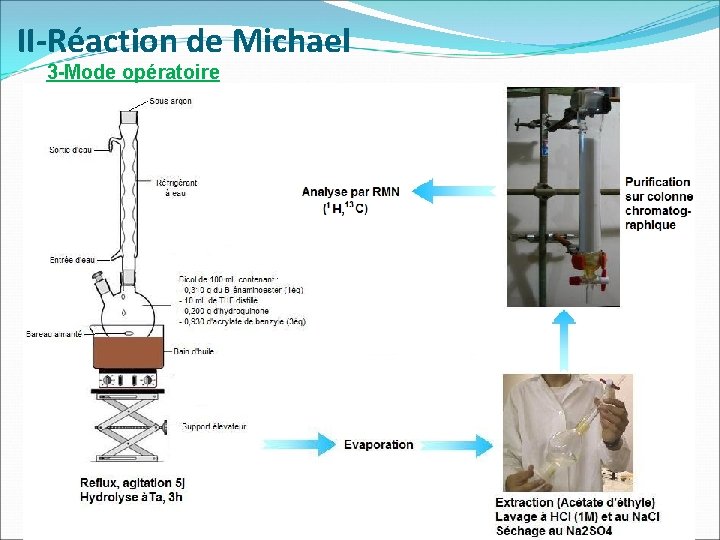
II-Réaction de Michael 3 -Mode opératoire 8

III-Appareillage utilisé 1 -Spectromètre Moment magnétique de spin non nul B 0 Deux niveaux d’énergies possibles RMN Modification du moment magnétique nucléaire Fréquence de résonance n 0=g. B 0/2 p 9

III-Appareillage utilisé 1 -Spectromètre Déplacement chimique : d =( n – n. TMS ). 106 / n 0 ü Référence : Pic du solvant CDCl 3 ü Solvant : Chloroforme deutéré CDCl 3 ü RMN du 1 H la plus utilisée (spin non nul) ü Autres RMN : 13 C, 31 P ü Très cher (de 300 K€ à 10 M€ ) 2 - Autres appareils Spectrophotomètre IR Polarimètre 10
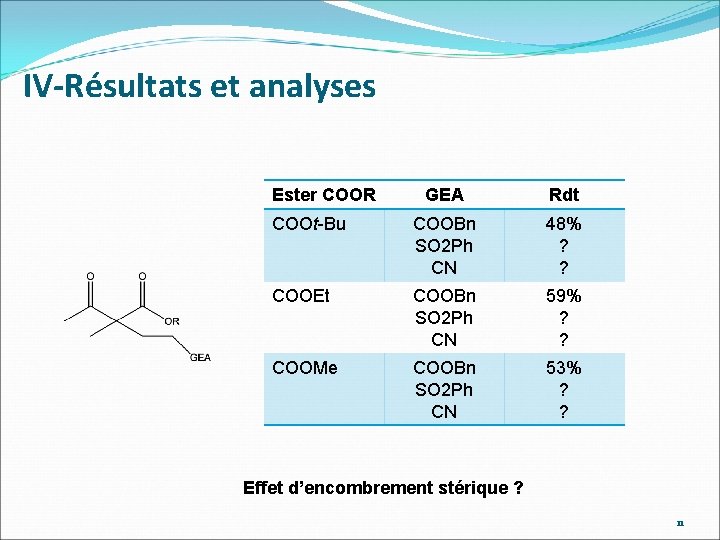
IV-Résultats et analyses Ester COOR GEA Rdt COOt-Bu COOBn SO 2 Ph CN 48% ? ? COOEt COOBn SO 2 Ph CN 59% ? ? COOMe COOBn SO 2 Ph CN 53% ? ? Effet d’encombrement stérique ? 11

V-Conclusion et Perspectives Projet: § Application de la réaction de Michael à des b-énaminoesters. Mon travail: § § Préparation de 2 -méthylacétoacétate de tert-butyle. Synthèse de b-énaminoesters. Synthèse du composé final issu de la réaction de Michael. Une étude en phase solide a été initiée. Perspectives: § Synthèse de ce composé en version chirale. § Poursuivre les synthèses en phase solide (les mêmes qu’en phase soluble). 12

Merci de votre attention 13
- Slides: 13