Aplicaciones de la espectrometra de absorcin molecular ultravioletavisible

Aplicaciones de la espectrometría de absorción molecular ultravioleta/visible Cap. 14

• La absorción de la radiación UV/VIS por una molécula puede considerarse en dos etapas: 1. excitación electrónica 2. relajación - El calor desarrollado no es detectable. - Vida media de la especie excitada M* es de 10 -8 a 10 -9 segundos.

• La relajación también puede ocurrir por: - descomposición de M* en dos especies nuevas (reacción fotoquímica) - reemisión de fluorescenciaa o fosforescenciab (recordar que a dura menos tiempo que b)

• La absorción de radiación UV/VIS resulta de la excitación de los electrones de enlace; los picos de absorción pueden relacionarse con los tipos de enlace (identificación de grupos funcionales en una molécula). • Sin embargo, la aplicación más importante es la determinación cuantitativa de compuestos que contienen grupos absorbentes.

Reconocemos tres tipos de transiciones electrónicas: 1. Las que incluyen electrones π, σ y n. 2. Las que incluyen electrones d y f. 3. Las de los electrones de transferencia de carga.

Las especies absorbentes son: • Iones y moléculas orgánicas así como algunos aniones inorgánicos. • TODOS los compuestos orgánicos son capaces de absorber radiación porque todos contienen electrones de valencia (π, σ o n) que pueden ser excitados a niveles de energía superiores.

Tipos de electrones absorbentes • Aquellos que participan directamente en la formación del enlace entre átomos. • Electrones no enlazantes o electrones que no participan en ningún enlace que están en gran parte localizados alrededor de átomos como oxígeno, halógenos, azufre o nitrógeno.
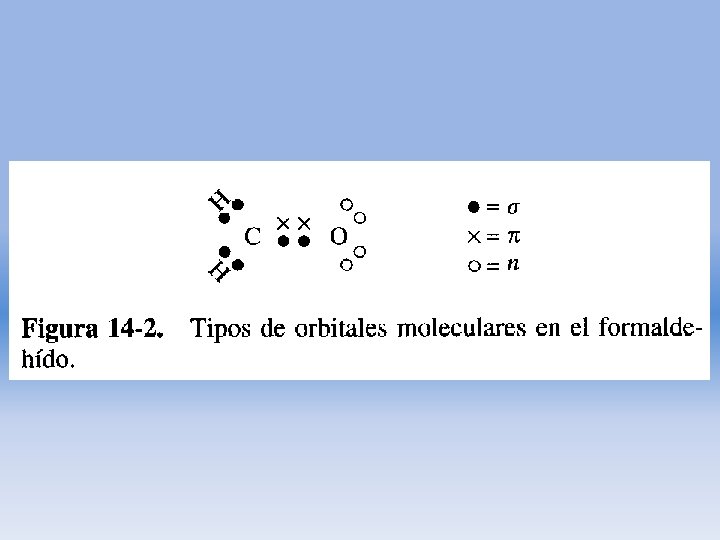
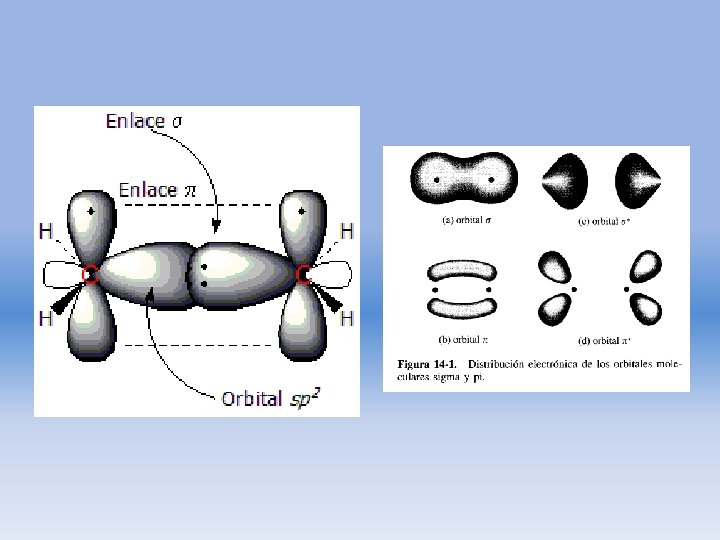
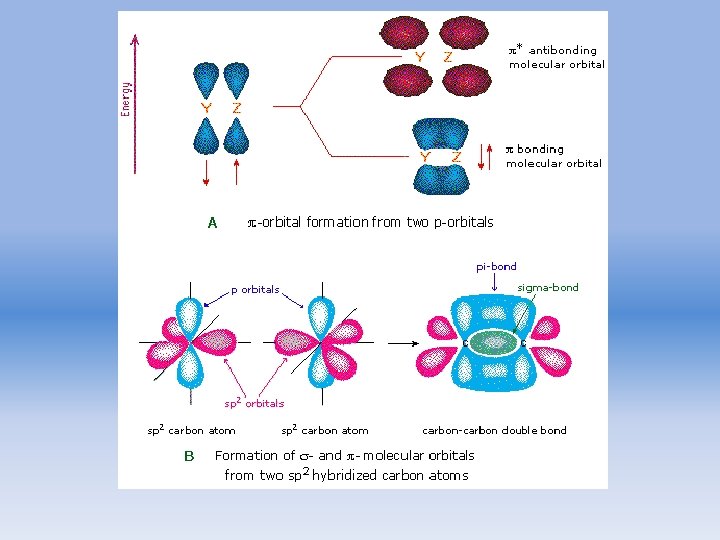
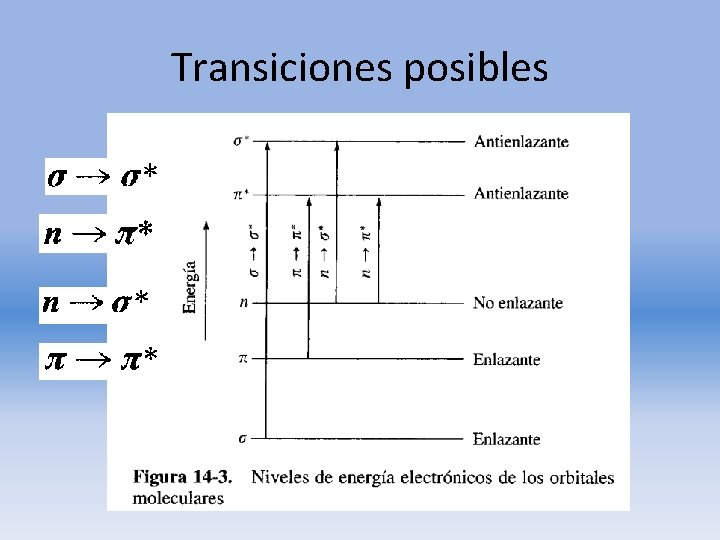
Transiciones posibles
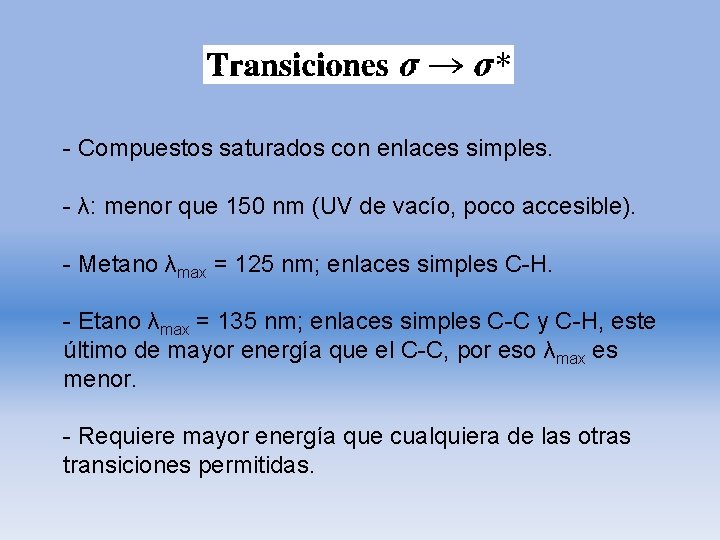
- Compuestos saturados con enlaces simples. - λ: menor que 150 nm (UV de vacío, poco accesible). - Metano λmax = 125 nm; enlaces simples C-H. - Etano λmax = 135 nm; enlaces simples C-C y C-H, este último de mayor energía que el C-C, por eso λmax es menor. - Requiere mayor energía que cualquiera de las otras transiciones permitidas.

- Compuestos saturados con pares de electrones compartidos. - λ: entre 150 a 250 nm. - ε: es baja a intermedia, 100 a 3000 L cm-1 mol-1 - En presencia de solventes polares λmax se desplaza a λ más cortas. - En pocos grupos funcionales se detecta con facilidad.
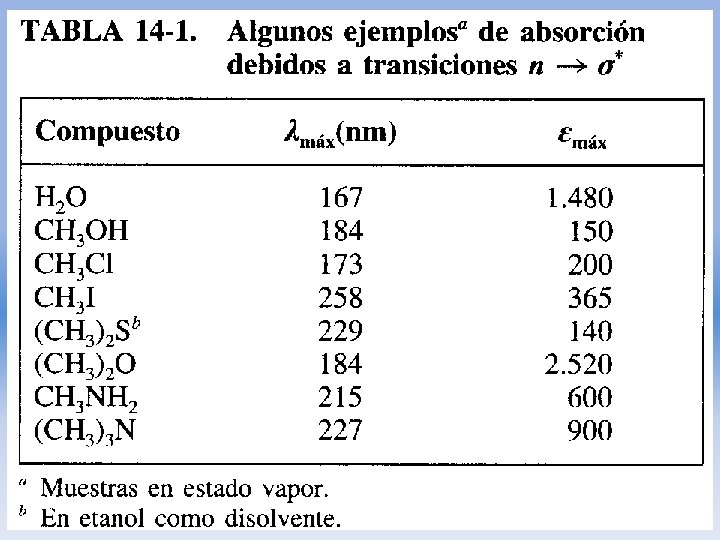

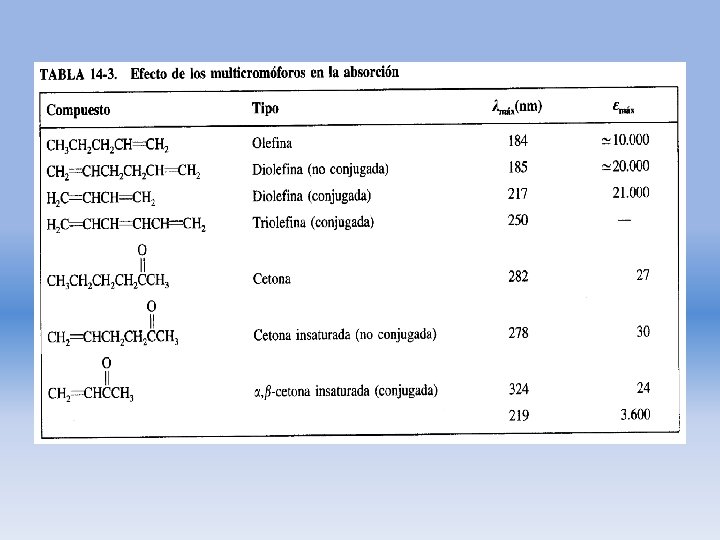
• Ambas requieren la presenci a de grupos funcionales no saturados que aportan los electrones π. • Producen picos de absorción dentro de una región espectral experimentalmente accesible. • A estos centros absorbentes no saturados se aplica el término cromóforos.

- Compuestos no saturados con pares de electrones no compartidos. - λ: entre 200 a 700 nm. - ε: es baja, 10 a 100 L cm-1 mol-1 - Al aumentar la polaridad del solvente λmax se desplaza a λ más cortas (desplazamiento hipsocrómico o hacia el azul). - En muchos grupos funcionales se detecta con facilidad.

- Compuestos no saturados. - λ: entre 200 a 700 nm. - ε: es media a alta, 1000 a 10000 L cm-1 mol-1 - Al aumentar la polaridad del solvente λmax se desplaza a λ más largas (desplazamiento batocrómico o hacia el rojo). - En muchos grupos funcionales se detecta con facilidad.
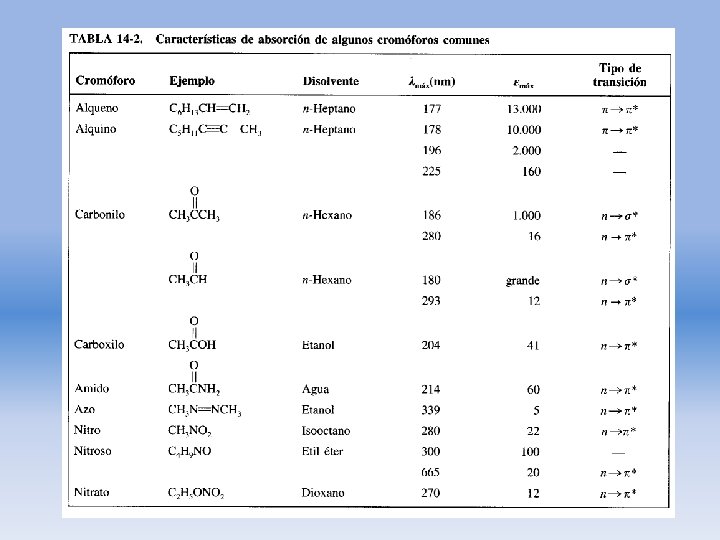

Efecto de la conjugación de cromóforos • La absorción de los multicromóforos en una molécula orgánica es aproximadamente aditiva, siempre que estén separados por más de u enlace sencillo. • Si los cromóforos estan conjugados las propiedades espectrales cambian, λmax se desplaza a λ más largas (desplazamiento batocrómico o hacia el rojo).

Absorción por sistemas aromáticos • Los espectros UV de los aromáticos se caracterizan por tres grupos de bandas debidas a transciones. • Ej: benceno, • λmax = 184 nm, ε =60, 000; Banda E 2 λdébil = 204 nm, ε =7, 000; Banda B λ+débil = 256 nm, ε =200. • Se ven muy afectadas por la sustitución del anillo y por los disolventes.
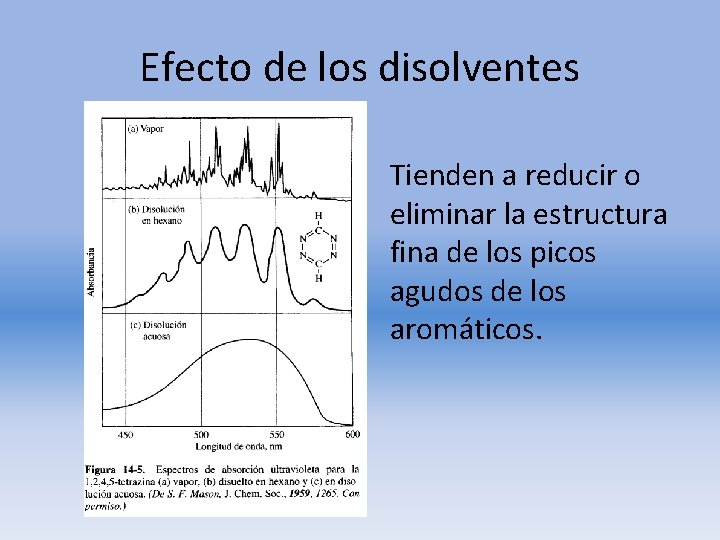
Efecto de los disolventes Tienden a reducir o eliminar la estructura fina de los picos agudos de los aromáticos.

Efecto de los sustituyentes • Auxocromo: grupo funcional que no absorbe en la región UV pero que tiene el efecto de desplazar los picos del cromóforo hacia longitudes de onda más largas, e incrementar sus intensidades. • Tienen al menos un par de electrones n capaces de interaccionar con los electrones π del anillo.
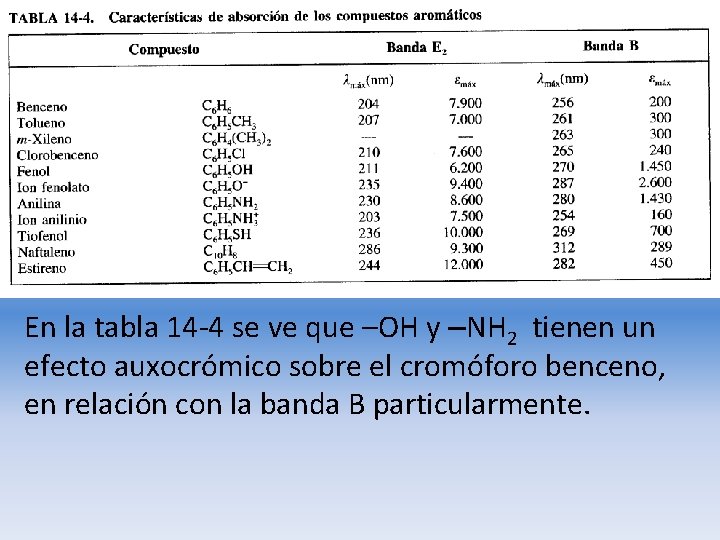
En la tabla 14 -4 se ve que –OH y –NH 2 tienen un efecto auxocrómico sobre el cromóforo benceno, en relación con la banda B particularmente.

Absorción por aniones inorgánicos • Presentan picos de absorción UV que son consecuencia de transiciones. • Ejemplos: - Nitrato 313 nm - Carbonato 217 nm - Nitrito 360 y 280 nm - Azida 230 nm - Tritiocarbonato: 500 nm

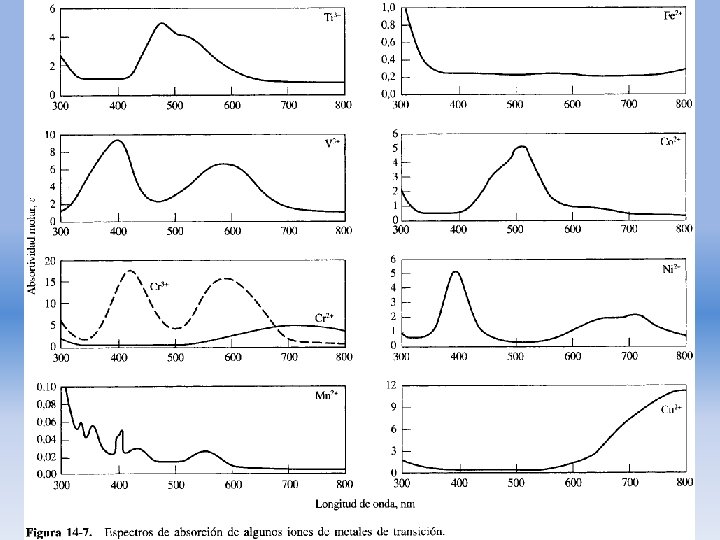
Absorción por los elementos de la 1 era. y 2 da. serie de los metales de transición • Los iones y complejos de los 18 elementos de 1 era. serie de los metales de transición tienden a absorber radiación VIS en uno o en todos sus estados de oxidación. • Transiciones de electrones entre los distintos niveles de energía de los orbitales d (3 d en la 1 era. serie y 4 d en la 2 da).

• Las bandas de absorción son anchas, influenciadas por los factores químicos del entorno. • Ejemplo: Ión cobre II acuoso es azul pálido; ión cobre II con amoníaco forma un complejo azul oscuro.

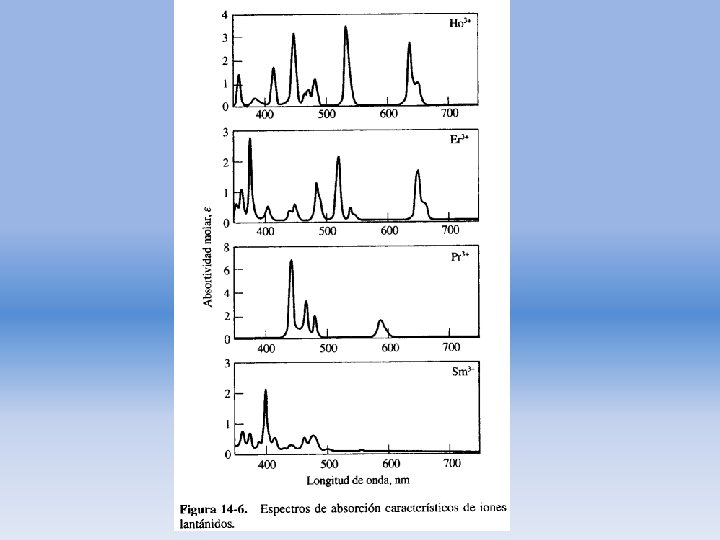
Absorción por iones lantánidos y actínidos • Absorben en la región UV/VIS. • Transiciones de electrones entre los distintos niveles de energía de los orbitales f (4 f en los lantánidos y 5 f en los actínidos).

• Espectros formados por picos de absorción característicos, bien definidos y estrechos, muy poco afectados por los factores químicos del entorno, o por el tipo de ligando asociado con el ión metálico. • Difieren de la mayoría de los espectros de los absorbentes inorgánicos y orgánicos.

http: //chrom. tutms. tut. ac. jp/JINNO/DRUGDATA/35 diazepam. html#UV http: //webbook. nist. gov/chemistry/
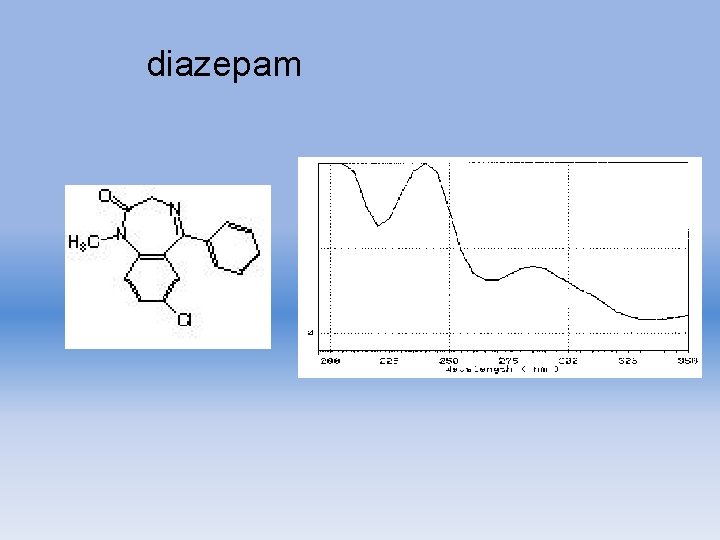
diazepam

Resultados de análisis por HPLC Tiempo de retención: 12. 33 min · Longitud de onda óptima: 240 nm · Sensibilidad : 5. 63 ng · Absorbancia / 100 ng : 0. 3851 abs. sec Aparato y condiciones de análisis Fase móvil: (10 m. M HCl. O 4 + 10 m. M Na. Cl. O 470%) + (CH 3 CN 30%) Velocidad de flujo: 1. 0 m. L/min. Columna : Fine. SIL C 18 T (25 cm x 4. 0 mm i. d. ) (monomeric. ODS, particle size 5 x 10 -6 m ) (Jasco). Longitud de onda : 210 -350 nm. Temperatura de columna: 50 c 880 PU LC pump (Jasco, Hachioji, Japan) System controller 801 -SC Gradient device 880 -02 Detector MULTI-320 Sistema de procesamiento de datos: DPL 320/98(Jasco, Hachioji, Japan) (Tiempo Acumulación 0. 8 sec. ) Propiedades Físicas Fórmula Molecular : C 16 H 13 Cl. N 2 O Peso Molecular : 284. 75 Nombre químico: 7 -chloro-1, 3 -dihydro 1 -methyl-5 -phenyl-2 H-1, 4 benzodiazepin-2 -one Propiedades : White, Light yellow crystalline powder. Non smell. Taste is slightly bitter. Punto de fusión: 130 -134 c log P : 2. 80 ( Experimentally determined value ) 3. 18 ( Calculated value ) Constante de ionización p. Ka : 3. 3 Solubilidad Chloroform : easily soluble acetic anhydride, Ethanol : partially soluble Ether : hardly soluble Water : almost insoluble Administración oral / 1 day : 30 -60 mg Clasificación Actividad de la Droga: Tranquilizer Diazepam
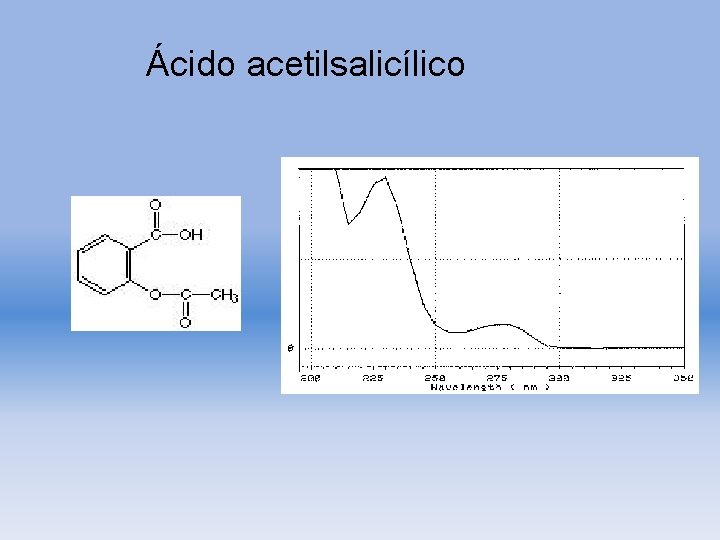
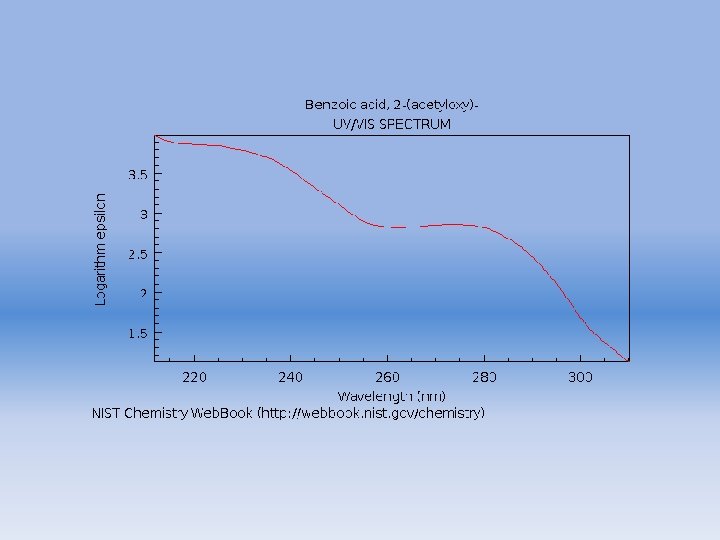
Ácido acetilsalicílico

Resultados de análisis por HPLC · · Tiempo de retención: 4. 14 min Longitud de onda óptima: 230 nm Sensibilidad : 4. 59 ng Absorbancia / 100 ng : 0. 1853 abs. sec Aparato y condiciones de análisis Fase móvil: (10 m. M HCl. O 4 + 10 m. M Na. Cl. O 470%) + (CH 3 CN 30%) Velocidad de flujo: 1. 0 m. L/min. Columna : Fine. SIL C 18 T (25 cm x 4. 0 mm i. d. ) (monomeric. ODS, particle size 5 x 10 -6 m ) (Jasco). Longitud de onda : 210 -350 nm. Temperatura de columna: 50 c 880 PU LC pump (Jasco, Hachioji, Japan) System controller 801 -SC Gradient device 880 -02 Detector MULTI-320 Sistema de procesamiento de datos. DPL 320/98(Jasco, Hachioji, Japan) (Tiempo Acumulación 0. 8 sec. ) Propiedades Físicas Fórmula Molecular : C 9 H 8 O 4 Peso Molecular : 180. 16 log P : 1. 19 ( Experimentally determined value ) 1. 10 ( Calculated value ) Constante de ionización p. Ka : 3. 5 Administración oral / 1 day : 5001000 mg Clasificación Actividad de la Droga: Analgesic; antipyretic Ácido acetilsalicílico
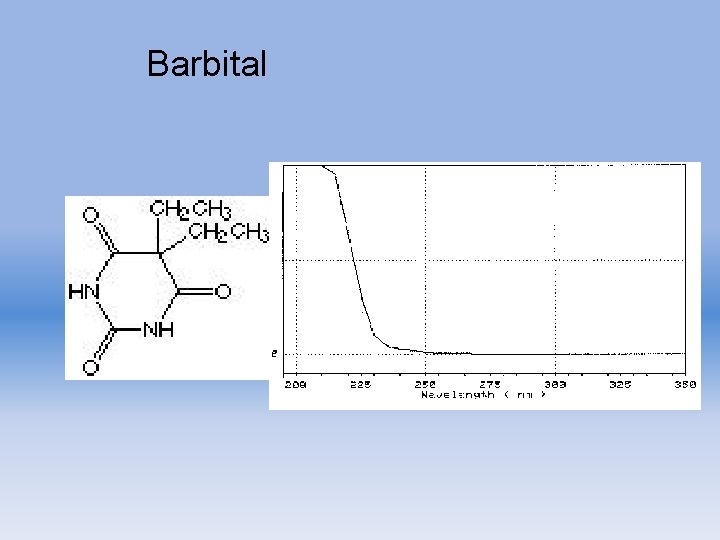
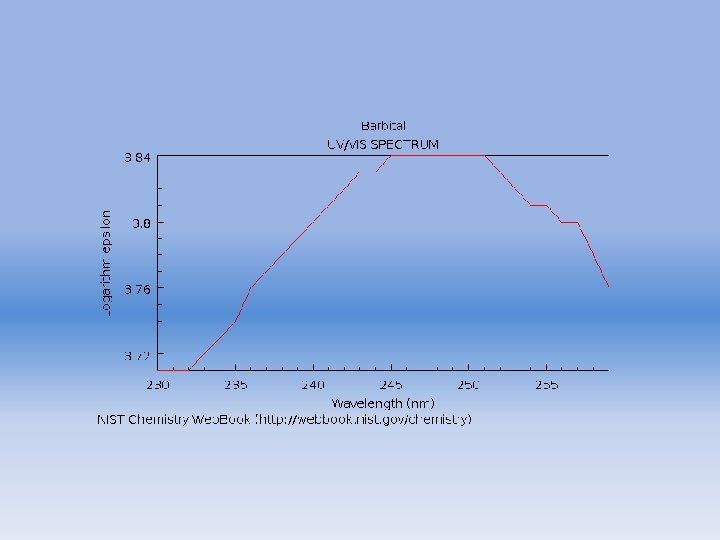
Barbital

Resultados de análisis por HPLC · · Tiempo de retención: 3. 00 min Longitud de onda óptima: 210 nm Sensibilidad : 3. 95 ng Absorbancia / 100 ng : 0. 1833 abs. sec Aparato y condiciones de análisis Fase móvil: (10 m. M HCl. O 4 + 10 m. M Na. Cl. O 470%) + (CH 3 CN 30%) Velocidad de flujo: 1. 0 m. L/min. Columna : Fine. SIL C 18 T (25 cm x 4. 0 mm i. d. ) (monomeric. ODS, particle size 5 x 10 -6 m ) (Jasco). Longitud de onda : 210 -350 nm. Temperatura de columna: 50 c 880 PU LC pump (Jasco, Hachioji, Japan) System controller 801 -SC Gradient device 880 -02 Detector MULTI-320 Sistema de procesamiento de datos. DPL 320/98(Jasco, Hachioji, Japan) (Tiempo Acumulación 0. 8 sec. ) Propiedades Físicas Fórmula Molecular : C 8 H 12 N 2 O 3 Peso Molecular : 184. 20 Nombre químico: 5, 5 -diethyl barbituric acid Propiedades : colourless or white crystalline powder. Non smell. Taste is slightly bitter. Punto de fusión: 189 -192 c p. H : 5. 0 -6. 0 log P : 0. 65 ( Experimentally determined value ) 0. 65 ( Calculated value ) Constante de ionización p. Ka : 7. 97 Solubilidad Acetone, Ethanol : soluble Water, Chloroform, Ether : hardly soluble Administración oral / 1 day : 300 mg Clasificación Actividad de la Droga: Hypnotic Barbital
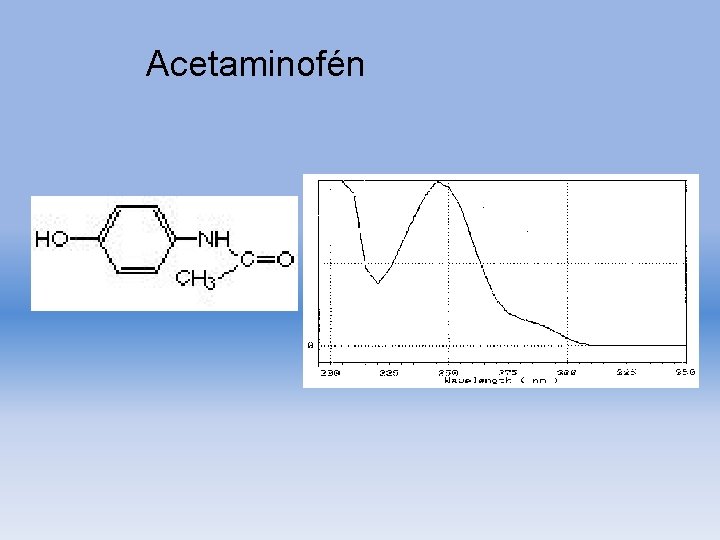
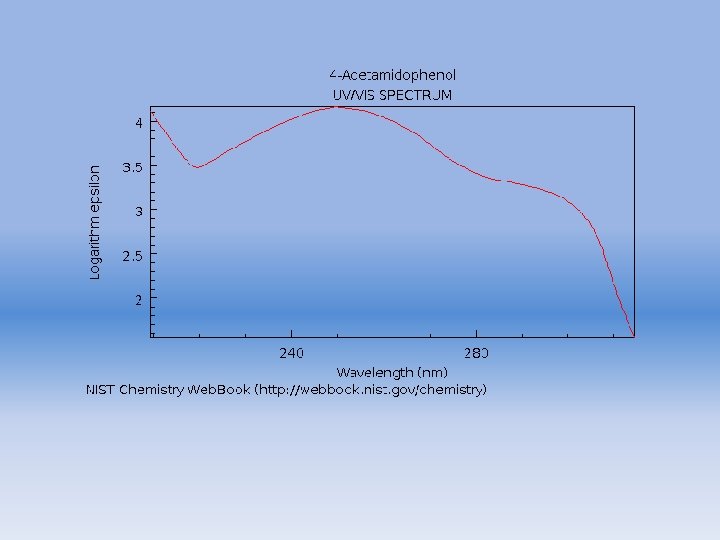
Acetaminofén

Resultados de análisis por HPLC · · Tiempo de retención: 2. 41 min Longitud de onda óptima: 245 nm Sensibilidad : 2. 81 ng Absorbancia / 100 ng : 0. 3225 abs. sec Aparato y condiciones de análisis Fase móvil: (10 m. M HCl. O 4 + 10 m. M Na. Cl. O 470%) + (CH 3 CN 30%) Velocidad de flujo: 1. 0 m. L/min. Columna: Fine. SIL C 18 T (25 cm x 4. 0 mm i. d. ) (monomeric. ODS, particle size 5 x 10 -6 m ) (Jasco). Longitud de onda: 210 -350 nm. Temperatura de columna: 50 c 880 PU LC pump (Jasco, Hachioji, Japan) System controller 801 -SC Gradient device 880 -02 Detector MULTI-320 Sistema de procesamiento de datos. DPL 320/98(Jasco, Hachioji, Japan) (Tiempo Acumulación 0. 8 sec. ) Propiedades Físicas Fórmula Molecular : C 8 H 9 NO 2 Peso Molecular : 151. 17 Nombre químico: N-(4 hydroxyphenyl)acetamide Propiedades : White crystal or Crystalline powder. Non smell. Taste is slightly bitter. Punto de fusión: 169 -172 c log P : 0. 51 ( Experimentally determined value ) 0. 49 ( Calculated value ) Constante de ionización� @p. Ka : 9. 71 Solubilidad aceton : easily soluble ether, benzene : hardly soluble Saturated solution : slight acidity Administración oral / 1 day : 300 -500 mg Clasificación Actividad de la Droga: Analgesic; antipyretic Acetaminofén

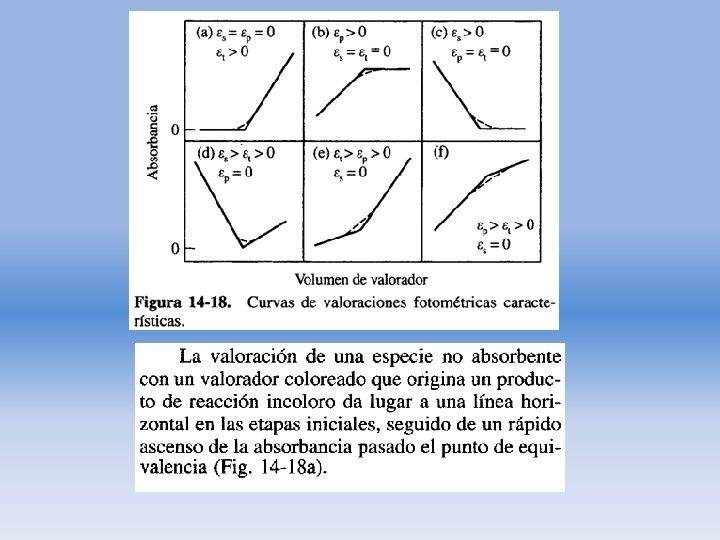
Titulaciones fotométricas
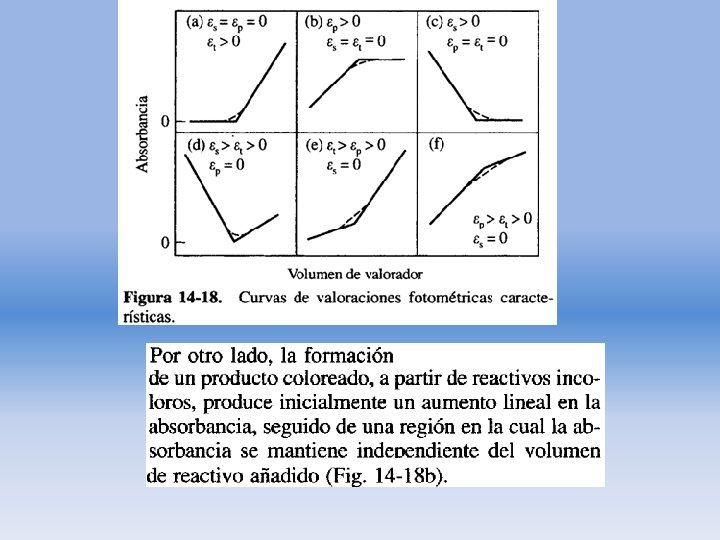
- Slides: 46