Antiinfekn imunita Jitka Ochotn Vztah mezi hostitelem a































- Slides: 37

Antiinfekční imunita Jitka Ochotná

Vztah mezi hostitelem a mikroorganismem q mikroorganismy - komensální - potencionální patogeny - patogenní mikroorganismy q Mikroorganismy mohou poškozovat organismus přímými mechanismy (toxiny, cytopatický efekt) nebo nepřímými, kdy iniciují poškozující imunitní reakce. q Při obraně proti různým mikroorganismům se, i přes převažující typ určité imunitní reakce, na jejich eliminaci podílejí všechny složky nespecifické imunity.

Využití receptorů na buňkách hostitele jako vstupních bran infekce § CD 4 - HIV, herpesvirus 7 § CD 21 (CR 2) - EBV § CD 71 - virus hepatitidy B § CD 81 - virus hepatitidy C § 1 integriny - Yersinia, patogenní E. coli § 3 integriny - Borrelia

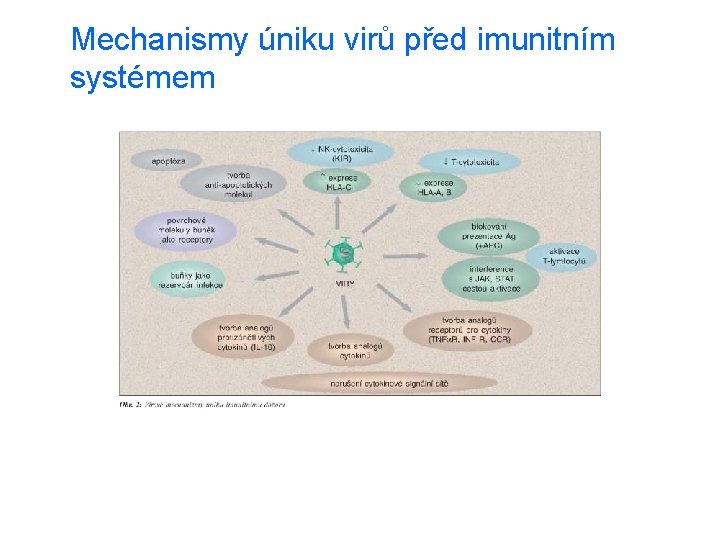
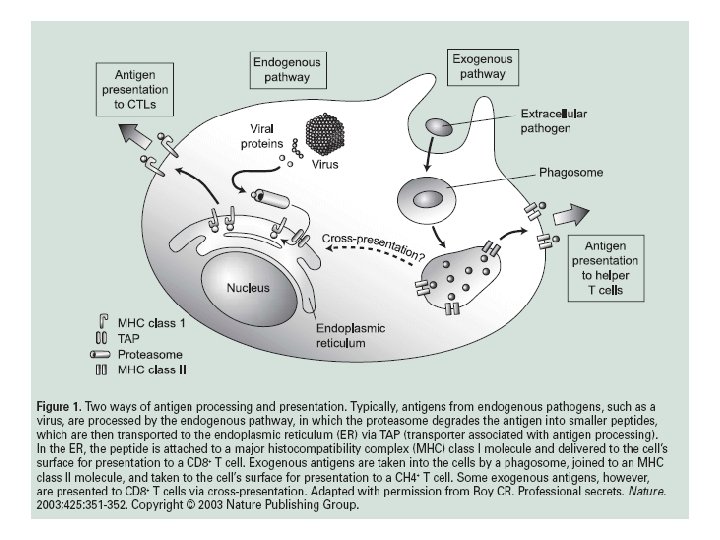
Mechanismy úniku mikroorganismů před obranným systémem q ukrytí do buněk; integrace do genomu a přetrvávání v latentní formě (herpetické viry, retroviry) q variabilita povrchových molekul (viry chřipky, HIV. . . ) q potlačení exprese MHC gp v napadené bb (adenoviry, herpetické viry) q potlačení prezentace Ag (blokování štěpení antigenu) q potlačení zánětlivé reakce produkcí virových analogů cytokinů nebo jejich inhibitorů q inhibice komplementu produkcí ochranných proteinů (herpesviry); sekrece proteáz, které inaktivují C 3 a a C 5 a; buněčná stěna chrání před membranolytickým účinkem komplementu

q štěpení blokujících s. Ig. A protilátek q využití cytokinů produkovaných hostitelem k vytvoření optimálního životního prostředí (TNF stimuluje replikaci HIV) q integrace molekul vlastních hostiteli do mikrobiální stěny (Borelia burgdorferi) q antigenní mimikry - povrchové struktury mikroorganismu napodobují strukturu hostitelských buněk q inhibice fagocytózy; inhibice fúze fagozómu s lysozómem; únik z fagozómu do cytoplasmy; inhibice tvorby kyselého p. H uvnitř fagolysozómu q produkce antagonistických peptidů (virus hepatitidy B, HIV)

Mechanismy úniku virů před imunitním systémem

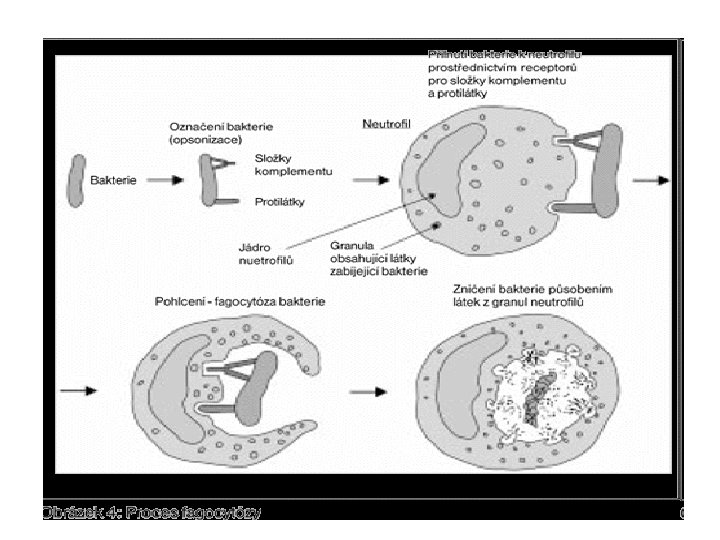
Obrana proti extracelulárním baktériím q gram-negativní, gram-pozitivní koky, bacily q k jejich eliminaci je nezbytná opsonizace (C 3 b, lektiny, protilátky. . . ) q neutrofilní granulocyty jsou do místa infekce lákány chemotakticky (C 5 a, C 3 a a chemotaktické produkty bakterií) q pohlcené bakterie jsou likvidovány mikrobicidními systémy (produkty NADP-H oxidázy, hydrolytické enzymy a baktericidní látky v lysozomech) q produkce prozánětlivých cytokinů fagocyty (IL-1, IL-6, TNF), které indukují zvýšení teploty, metabolickou odpověď organismu a syntézu proteinů akutní fáze

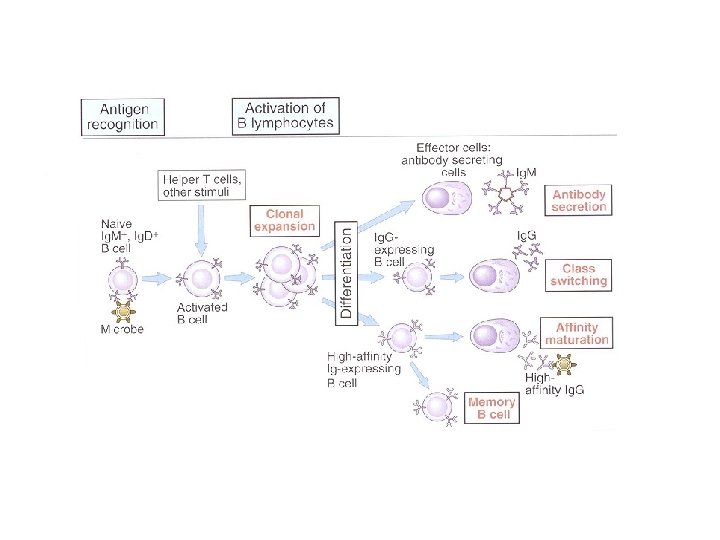
q v pozdějších fázích infekce jsou stimulovány antigenně specifické mechanismy q plazmatické buňky produkují nejprve Ig. M, po izotypovém přesmyku produkují Ig. G 1 nebo Ig. A (opsonizace) q s. Ig. A brání před infekcemi střevními a respiračními bakteriemi q bakterie s polysacharidovým pouzdrem mohou vyvolat T-independentní produkci protilátek Ig. M ( po navázání na bakterii aktivují klasickou cestu komplementu) q po infekci přetrvávají v Ig. G, Ig. A (protektivní účinek) a paměťové T a B lymfocyty



q v obraně proti bakteriálním toxinům se uplatňují neutralizační protilátky (Clostridium tetani a botulinum. . . ) q "nepřímé toxiny"- bakteriální lipopolysacharid (LPS) stimuluje velké množství monocytů k uvolnění TNF, který může vyvolat septický šok q infekcemi extracelulárními bakteriemi jsou ohroženi především jedinci s poruchami funkce fagocytů, komplementu a tvorby protilátek

Obrana proti intracelulárním bakteriím a plísním q intracelulární parazitismus je dán schopností mikroorganismů uniknout mikrobicidním mechanismům fagocytů q mykobakterie, některé kvasinky a plísně q makrofágy, které je pohltily produkují IL-12 → diferenciace TH 1, které produkují IFNg a membránový TNF→ aktivace makrofágů a indukce i. NOS q plazmatické buňky pod vlivem IFNg produkují Ig. G 2; imunokomplexy obsahující Ig. G 2 se váží na Fc receptory makrofágů a tím je stimulují q v obraně proti intacelulárním parazitům, kteří unikají z fagolysozómu se uplatňují TC lymfocyty q infekcemi intracelulárními mikroorganismy jsou ohroženi jedinci s některými poruchami funkcí fagocytů a s defekty T lymfocytů

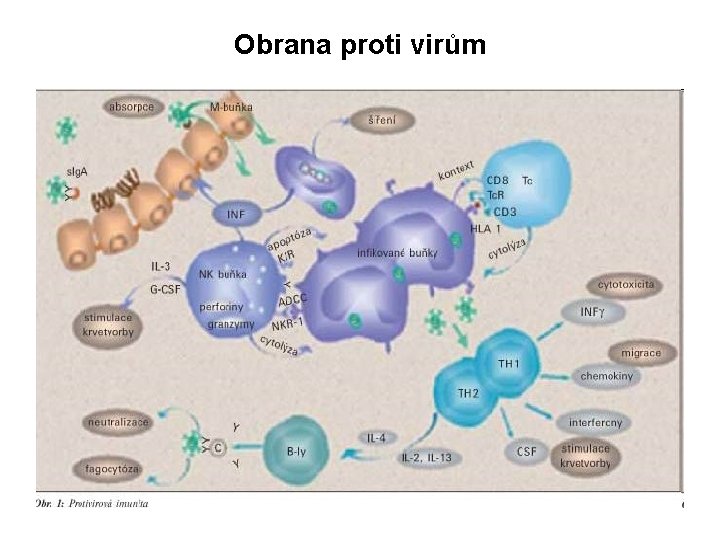
Obrana proti virům q interferony - v infikovaných bb. je indukována produkce IFNa a IFN (brání replikaci viru a v neinfikovaných bb. navozují tzv. antivirový stav); IFNg stimuluje přeměnu makrofágů v aktivované (i. NOS) q NK buňky - ADCC (Antibody-dependent cell-mediated cytotoxicity) = cytotoxická reakce závislá na protilátkách; rozpozná-li NK lymfocyt buňku opsonizovanou Ig. G pomocí svých stimulačních Fc receptorů CD 16 dojde k aktivaci cytotoxických mechanismů (degranulaci) q infikované makrofágy produkují IL-12 (silný aktivátor NK bb. )

Obrana proti virům


q efektorové TC lymfocyty v přímém kontaktu ničí infikované buňky a produkují cytokiny, které inhibují replikaci virů q v obraně proti cytopatickým virům se nejvíce uplatňují protilátky q s. Ig. A na sliznicích blokují adhezi virů (obrana proti respiračním virům a enterovirům) q neutralizační protilátky Ig. G nebo Ig. M aktivují klasickou cestu komplementu, který je schopný některé viry lyzovat q Ig. A a Ig. G vzniklé při virové infekci mají preventivní efekt při sekundární infekci

q některé viry se po infekci integrují do hostitelského genomu, kde perzistují po léta (varicella zoster, EBV, papilomaviry) q virovými infekcemi jsou ohroženi jedinci s imunodeficity T lymfocytů a s kombinovanými poruchami imunity q zvýšená náchylnost k herpetickým infekcím u jedinců s dysfunkcí NK bb.

Obrana proti protozoálním parazitům q obrana proti protozoálním parazitům je podobná jako u bakterií q extracelulární parazité - protilátky q intracelulární parazité - TH 1 lymfocyty a aktivované makrofágy

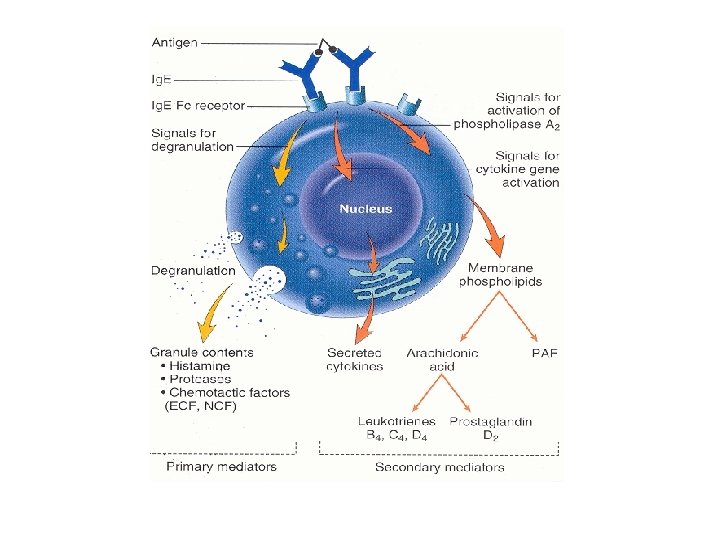
Obrana proti mnohobuněčným parazitům q kontakt mastocytů, bazofilů a eosinofilů s antigeny parazita q stimulace TH 2 pod vlivem IL-4 (mastocyty a další APC stimulované parazitem) q TH 2 stimulují B lymfocyty s BCR specifickým pro parazitární antigeny q pod vlivem IL-4 izotypový přesmyk v Ig. E


q Ig. E se váží na Fce. RI mastocytů a bazofilů ("antigenně specifické receptory") q navázání multivalentního antigenu ( mnohobuněčného parazita) pomocí Ig. E na vysokoafinní Fc receptor pro Ig. E (Fc RI) q agregace několika molekul Fc RI

q iniciace degranulace mastocytu ( fúze cytoplazmatických granulí s povrchovou membránou a uvolnění jejich obsahu) – uvolnění histaminu q Histamin způsobuje vasodilataci, zvýšení vaskulární permeability, erytém, edém, svědění, kontrakci hladké svaloviny bronchů, zvýšení peristaltiky střev, zvýšení sekrece hlenu slizničními žlázkami v respiračním traktu a GITu. q aktivace metabolismu kyseliny arachidonové (leukotrien C 4, prostaglandin PGD 2) - amplifikace zánětlivé reakce q zahájení produkce cytokinů (TNF, TGF , IL-4, 5, 6…) mastocytem

q v pozdějších stádiích se aktivují TH 1 a jsou produkovány protilátky dalších tříd q eosinofily fagocytují komplexy parazitárních částic s Ig. E prostřednictvím svých receptorů pro Ig. E q eosinofily proti parazitům používají extracelulární baktericidní látky uvolněné z granulí (eosinofilní katoinický protein, proteázy)

Možnosti léčebného ovlivnění imunitního systému

Kauzální léčba a) transplantace kmenových buněk - u závažných vrozených poruch imunitního systému (některá lymfoproliferativní a myeloproliferativní onemocnění) - komplikace : infekční komplikace reakce štěpu proti hostiteli - získání kmenových buněk - odběrem z lopaty kosti kyčelní - z pupečníkové krve - z periferní krve po stimulaci GM-CSF

b) genová terapie - pomocí vhodného expresního vektoru je do lymfocytů nebo kmenových buněk vnesen funkční gen, který nahrazuje nefunkční gen - použito jako léčba některých případů SCID

Substituční léčba - autologní transplantace kmenových buněk po chemoterapii a radioterapii - léčba intravenózními imunoglobulíny (pochází z plazmy dárců krve) - substituce C 1 inhibitoru u hereditárního angioedému - substituce erytropoetinu u pacientů s chronickým renálním selháním - substituce G-CSF u agranulocytózy (Kostmannova syndromu)

Nespecifická imunomodulační léčba Imunomodulace = léčebný postup směřující k úpravě narušených imunitních funkcí a) nespecifická imunosupresivní léčba nespecifická = postihuje nejen nežádoucí autoreaktivní a aloreaktivní lymfocyty, ale i ostatní složky imunity (riziko snížení antiinfekční a protinádorové imunity) - používá se u léčby autoimunitních chorob, závažných stavů alergií a u orgánových transplantací

kortikoidy - protizánětlivý, imunosupresivní účinek - blokují aktivitu transkripčních faktorů (AP-1, NFk. B) - potlačují expresi genů (IL-2, IL-1, fosfolipáza A, MHCgp. II, adhezivních molekuly) - inhibice uvolnění histaminu z bazofilů - vyšší koncentrace indukují apoptózu - Prednison, metylprednison imunosupresiva zasahující do metabolismu DNA - cyklofosfamid (alkylační látky) - methotrexát (antimetabolit) - azathioprim (purinový analog)

imunosupresiva selektivně inhibující T lymfocyty - cyklosporin A (potlačuje expresi IL-2 a IL-2 R v aktivovaných T lymfocytech) - takrolimus - rapamycin - monoklonální protilátka anti-CD 3 (imunosuprese po transplantacích, léčba rejekčních krizí) Intravenozní imunoglobulinová terapie v imunosupresivní terapii

b) protizánětlivá a antialergická léčba nesteroidní protizánětlivé léky antihistaminika - blokují H 1 receptor - snižují expresi adhezivních molekul - snižují sekreci histaminu. . . - I. , II. a III. generace inhibitory zánětlivých cytokinů - antagonista receptoru pro IL-1 - monoklonální protilátky proti TNF - thalidomid (inhibitor TNF)

c) nespecifická imunostimulační léčba imunostimulancia - stimulují imunitní systém syntetické imunomodulátory - Methisoprinol (Isoprinosine) – užíván u virových infekcí s těžším nebo recidivujícím průběhem bakteriální extrakty a lyzáty - Broncho-Vaxom - prevence recidivujících infekcí dýchacích cest - Ribomunyl produkty imunitního systému - IL-2 - renální adenokarcinom - IFNa, IFN - virové hepatitidy, některé leukemie - erytropoetin - G-CSF, GM-CSF - neutropenie - transfer faktor - thymové hormony

Antigenně specifická imunomodulační léčba specifická imunomodulace = navození imunitní reakce či tolerance vůči určitému antigenu a) Aktivní imunizace b) Pasivní imunizace c) Specifická imunosuprese

a) aktivní imunizace = využití antigenu k vyvolání imunitní reakce, která může později chránit před patogenem nesoucím daný antigen (nebo antigen jemu podobný) q imunizace vakcinami vyrobenými z inaktivovaných nebo oslabených mikroorganismů nebo jejich antigenů (polysacharidová pouzdra, toxiny) q vzniká dlouhotrvající imunita, aktivována buněčná i protilátková imunita q podání injekční nebo orální q profalyktická q riziko vyvolání infekce nebo anafylaktických reakcí

b) pasivní imunizace - přirozená - přestup mateřských protilátek do krve plodu - terapeuticky - použití zvířecích protilátek proti různým toxinům (hadí jedy, tetanický toxin, botulotoxin) - profylakticky - lidský imunoglobulín z imunizovaných jedinců (hepatitida A, vzteklina, tetanus) - anti-Rh. D protilátky - zabránění imunizace matky Rh. D+ plodem - poskytuje dočasnou (3 týdny) specifickou humorální imunitu - riziko vyvolání anafylaktických reakcí

c) specifická imunosuprese = navození tolerance vůči určitému antigenu probíhají klinické studie: - navození tolerance perorálním podáním antigenu - alergenová imunoterapie (pyly, hmyzí jedy)

DĚKUJI ZA POZORNOST