Antibiticos DR CARLOS N DEL RIO ALMENDAREZ CENTRO

Antibióticos DR. CARLOS N DEL RIO ALMENDAREZ CENTRO DE ESPECIALIDADES PEDIATRICAS
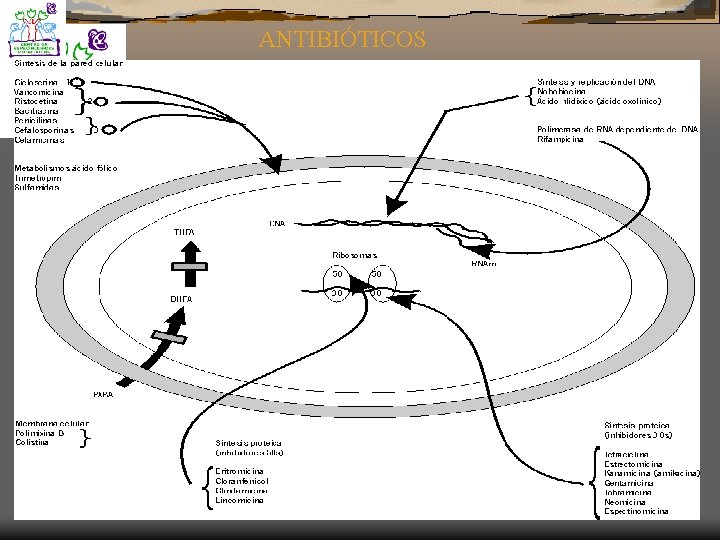
ANTIBIÓTICOS

INTRODUCCIÓN Ü Se inicia el uso de antibióticos hace más de 60 años Ü Uso y abuso de ellos Ü Administración inapropiada Ü Juicio y criterio clínico

SELECCIÓN INICIAL FACTORES: Ü Ü Ü Ü Conocimiento que no todas las infecciones son de etiología bacteriana Conocimiento de los microorganismos que causen la infección Conocimiento de la evolución natural de la enfermedad infecciosa Conocimiento de la vía de administración, dosis, duración del tratamiento, susceptibilidad bacteriana a los antibióticos que se van a utilizar Que el fármaco llegue al sitio de la infección en las concentraciones adecuadas Tener presente la edad, anomalías metabólicas, función hepática ó renal Datos de cultivos y sensibilidad deben guiar al clínico para continuar o modificar el régimen medicamentoso empírico pero esto no sustituye a la evolución clínica Evitar hasta donde sea posible el uso de combinaciones de atb

Conceptos generales Drogas sintéticas ó Quimioterapeuticos Son obtenidos por la mano del hombre. Creados en el Laboratorio El quimioterapeutico se define como: Una sustancia química sintética, obtenida para tratar infecciones mediante destrucción de los microorganismos infectantes, cuando se administra al huésped, sin dañar sus tejidos. Ü Antibióticos Son elaborados, en su metabolismo propio, por seres vivos: Plantas, animales, bacterias y hongos. Se define como una sustancia derivada de un organismo vivo, generalmente un microorganismo ó una modificación química de la misma, que inhibe la reproducción, crecimiento ó incluso destruye otros microorganismos y células anormales de animales Ü

CONCEPTOS GENERALES Agente Bacteriostático: Aquel que tiene la propiedad de inhibir la multiplicación bacteriana, misma que se reanuda cuando se retira el agente Ü Agente Bactericida: Aquel que tiene la propiedad de matar a las bacterias, es irreversible Las siguientes leyes de Jawest nos indican el efecto de la utilización conjunta de dos antimicrobanos: Ü Sinergismo: ( Bactericida + Bactericida): El resultado terapéutico es superior a la suma de sus efectos aislados Ü Suma de Efectos: ( Bacteriostático + Bacteriostático ): El resultado terapéutico es igual a las suma de sus efectos Ü Antagonismo: ( Bactericida + Bacteriostático ). El resultado terapéutico es inferior a la suma de sus efectos aislados. Ü

CLASIFICACIÓN GENERAL Ü BETALACTÁMICOS: Ü 1. Penicilinas naturales Penicilinas semisintéticas P. Resistentes a betalactamasas(isoxazolilpenicilinasas) Aminopenicilinas Carboxipenicilinas Ureidopenicilinas Inhibidores de betalactamasas 1. 2. 3. 4. 5. 6. 7. 2. 3. 4. Ü 1. 2. AMINOGLUCOSIDOS: Amikacina Gentamicina Estreptomicina Netilmicina LINCOSAMIDAS: Cindamicina Lincomicina

Clasificación general Ü 1. 2. Ü Ü 1. Ü GLUCOPÉPTIDOS: Vancomicina Teicoplanina POLIMIXINA FENICOLES: Cloranfenicol TETRACICLINAS Ü 1. 2. 3. 4. Ü Ü 1. 2. 3. 4. MACROLIDOS: Eritromicina Claritromicina Azitromicina Roxitromicina RIFAMICINAS QUIMIOTERÁPICOS: Nitrofuranos Imidazoles Quinolonas Sulfonamidas

PENICILINAS Ü ACTIVIDAD ANTIMICROBIANA: Anillo betalactamico+ anillo tiazolidínico+ una cadena de ácido 6 -aminopenicilinico. Ü MECANISMO DE ACCIÓN: Inhiben la síntesis de la pared bacteriana ( Bactericidas) Unión a las PBP

PENICILINAS Ü 1. 2. 3. 4. FARMACOCINÉTICA: Buen absorción oral Distribución Tisular y penetración adecuada en SNC. Eliminación renal Vida media variable ( 30 min PSC – hasta 24 hrs)

TOXICIDAD Alergia a Penicilina: 1 a 10% Ü Lesiones cutáneas maculopapulares: 20% Ü Reacciones Anafilácticas: 0. 004 a 0. 015% Ü EFECTOS ADVERSOS: 1. Síntomas gastrointestinales 2. Lesiones cutáneas 3. Neutropenia y alteraciones en agregación plaquetaria 4. Insuficiencia Renal 5. Encefalopatía o Crisis convulsivas Ü

MECANISMOS DE RESISTENCIA Ü DEGRADACIÓN ENZIMATICA BETALACTAMASAS : Plásmidos ó por cromosomas Ü IMPOSIBILIDAD DE PENETRACIÓN ALTERACIONES DE LAS PORINAS Ü ALTERACIONES DEL SITIO BLANCO PROTEÍNAS LIGADORAS DE PENICILINA ( PBP)

CEFALOSPORINAS Ü Cefalosporina Ü Estructura C básica: Anillo de Dihidrotiazina unido a un anillo Betalactámico

CEFALOSPORINAS Ü Ü 1. 2. 3. 4. Orales: Cefixima y Ceftibuten Parenterales: Primera generación Segunda generación Tercera generación Cuarta generación
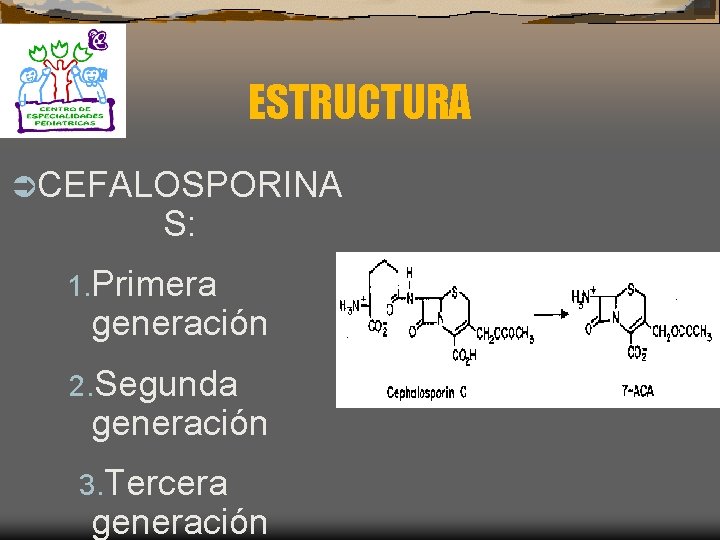
ESTRUCTURA ÜCEFALOSPORINA S: 1. Primera generación 2. Segunda generación 3. Tercera generación

Mecanismo de acción Las cefalosporinas impiden la síntesis de la pared celular bacteriana a través de la inactivación de una ó varías proteínas ligadoras de penicilina ( PBP) MECANISMOS DE RESISTENCIA: Ü Disminución de penetración Ü Producción de betalactamasas

FARMACOCINETICA Vía Parenterales: 1. Intramuscular 2. Intravenosa 3. Unión a proteínas desde el 17% hasta 95% 4. Penetran en la mayoría de los tejidos (SNC) Ü Vía oral 1. Buenas concentraciones séricas principalmente con el Ceftibuten Ü

ANTIBIÓTICOS BETALACTÁMICOS EN COMBINACIÓN CON UN INHIBIDOR DE BETALACTAMSAS Actividad antimicrobiana: 1. Ácido clavulanico. . 1981 2. Sulbactam 3. Tazobactam Estos inhibidores combinados aumentan la actividad antibacteriana de los betaláctamicos 4 a 32 veces más Ü

MECANISMOS DE ACCIÓN Ü Los inhibidores de betaláctamasas se unen a algunas proteínas que ligan penicilina ejerciendo una doble actividad antibacteriana Ü La actividad principal incluye la inhibición irreversible ( SUICIDA) de las betaláctamasas

MECANISMOS DE RESISTENCIA Ü 1. Producción de Betaláctamasas: Mutaciones cromosomicas

FARMACOCINÉTICA Ü Ü Ü Presenta el Ac. Clavulánico una absorción oral del 89 al 97% Sulbactam se absorbe bien solo en combinación con ampicilina 68% ( Profarmaco=Sultamicilina) Se unen a las proteínas 20% AC. Clavulánico, 38% el sulbactam Buena penetración a los tejidos Su vía de eliminación principal: 1. Riñón 2. Hígado

TOXICIDAD Ü Reacciones de Hipersensibilidad Ü Náuseas Ü Diarrea

MONOBACTÁMICOS Ü AZTREONAM: Es el único miembro de esta clase que es activo exclusivamente contra Pseudomonas aeruginosa. Ü MECANISMO DE ACCIÓN: Se une a las PBP impidiendo su función normal
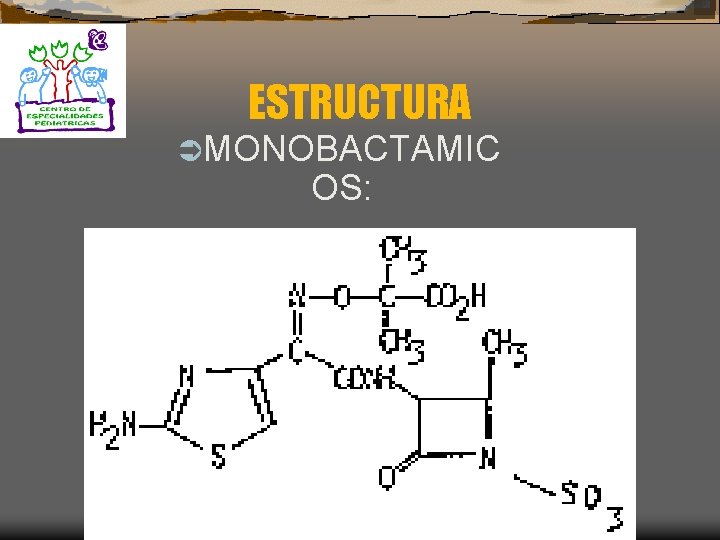
ESTRUCTURA ÜMONOBACTAMIC OS: 1. Aztreonam

MONOBACTÁMICOS Ü Mecanismo de resistencia: Es resistente a la hidrólisis por betalactámasas Ü Farmacocinética: Se administra solo por vía intravenosa Vida media de 2 horas El 56% se une a las proteínas Penetra a la mayoría de los tejidos Se elimina por vía Renal

MONOBACTÁMICOS Ü Toxicidad: Misma toxicidad que otros betalactámicos Ü Efectos adversos: Flebitis Elevación de las aminotransferasas Diarrea Náuseas Vómitos

CARBAPENEMS (Tienamicinas) Ü 1. 2. 3. 4. 5. Actividad antimicrobiana: Son antibióticos bicíclicos que comparten el núcleo carbapenem Descubiertos en 1975 El Imipenem es metabolizado activamente por la dehidropeptidasa renal I Asociación con Cilastatina un inhibidor de la dehidropeptidasa renal I que le da la estabilidad en soluciones concentradas El meropenem es estable a la acción de dehidropeptidasa I y puede administrarse solo
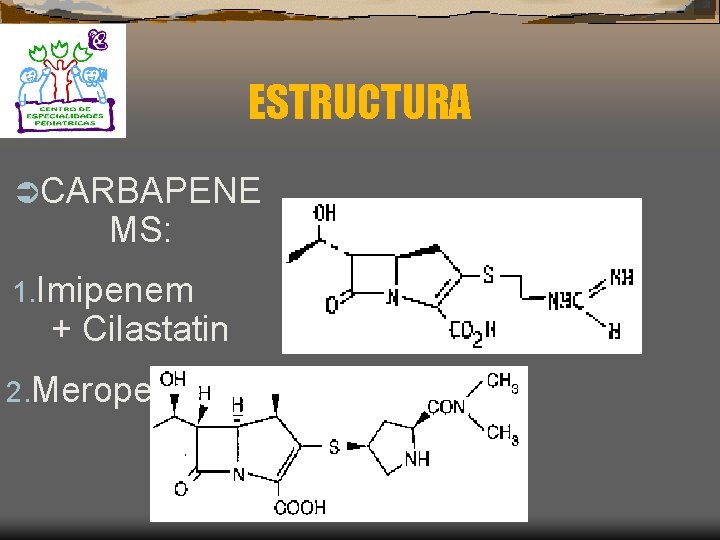
ESTRUCTURA ÜCARBAPENE MS: 1. Imipenem + Cilastatin 2. Meropenem

CARBAPENEMS 6. - Activos contra Enterobacterias gram negativas 7. - Activos con bacterias gram positivas 8. - La mayoría de los anaerobios son sensibles a estos antibióticos Ü Mecanismo de acción: Se unen a las PBP causando inhibición del crecimiento bacteriano, inhibición de la división celular, pérdida de la biosíntesis de mucopéptidos de pared celular causando lisis celular

CARBAPENEMS Ü Farmacocinética: No se absorben por vía oral Se distribuyen en todos los tejidos y líquidos corporales Vida media de una hora El 70% se excreta por vía renal.

CARBAPENEMS Ü Toxicidad: Crisis convulsivas: 1 – 7% por inhibición de los receptores GABA con disminución de la neurotransmisión inhibitoria Nauseas Vómitos Diarrea Flebitis

AMINOGLÍCOSIDOS Ü Ü 1. 2. 3. El primer atb la Estreptomicina ( 1944) Actividad antimicrobiana: Bacterias aerobias gram negativas Bacterias aerobias gram positivas Micobacterias

MECANISMOS DE ACCIÓN Ü Los aminoglicósidos son inhibidores de la biosíntesis de proteína al unirse al ribosoma bacteriano. Ü Sitio blanco de unión es la Unidad 30 S que contiene el r. RNA 16 s Ü Daño de la membrana externa Ü Bloqueo de la replicación inicial del DNA Ü Captación irreversible ?
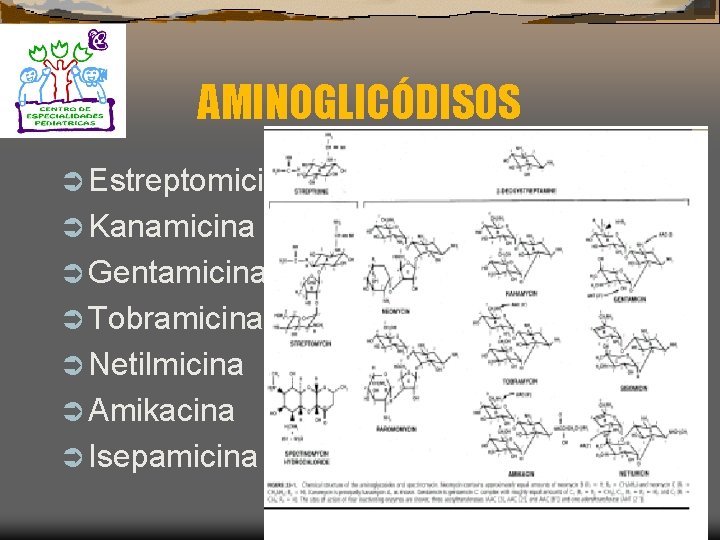
AMINOGLICÓDISOS Ü Estreptomicina Ü Kanamicina Ü Gentamicina Ü Tobramicina Ü Netilmicina Ü Amikacina Ü Isepamicina

MECANISMOS DE RESISTENCIA Son tres los mecanismos principales de resistencia Ü Disminución en la captación: 1. Sistema de transporte de electrones Ü Modificación del sitio blanco en el ribosoma: 1. Mutaciones genéticas ribosómicas Ü Modificación enzimática: 1. Acetiltransferasas Adenil/nucleotidil-transferasas Fosfotransferasas 2. 3.

FARMACOCINÉTICA Ü Absorción pobre por vía oral Ü Vía Intramuscular Ü Vía Intravenosa Ü Poca unión a proteínas séricas Ü Buena distribución en líquidos intersticial y extracelular Ü Eliminación renal

TOXICIDAD Ü Ototoxicidad: Auditiva Vestibular Irreversible Ü Nefrotoxicidad

MACRÒLIDOS Ü Son antibióticos naturales y Semisintéticos Ü Espectro medio Ü Bacteriostáticos
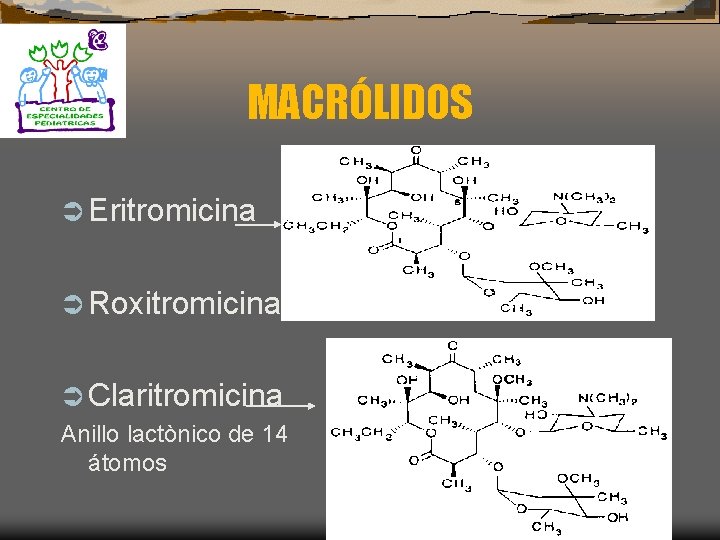
MACRÓLIDOS Ü Eritromicina Ü Roxitromicina Ü Claritromicina Anillo lactònico de 14 átomos
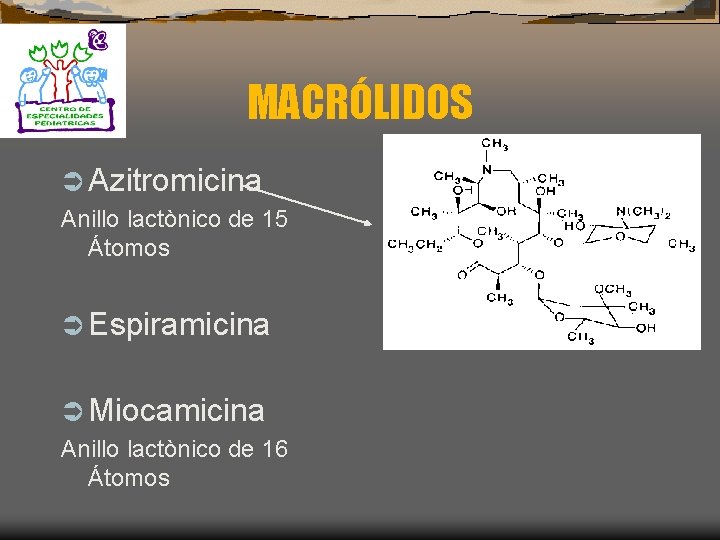
MACRÓLIDOS Ü Azitromicina Anillo lactònico de 15 Átomos Ü Espiramicina Ü Miocamicina Anillo lactònico de 16 Átomos

MACRÓLIDOS Mecanismo de Acción: Ü Inhiben la Síntesis de Proteínas: 1. Sub – Unidades 50 s ribosomal Pueden llegar a ser Bactericidas si se aumenta la concentración en el medio, densidad de la población bacteriana y fase de crecimiento Ü

MACRÓLIDOS Ü Mecanismo de resistencia: Por alteración de la permeabilidad de la pared bacteriana ( Cierre de porinas ) 2. Plàsmidos (modificación de RNA ribosomal) 3. Producción enzimático - Esterasas - Metilasas Existe resistencia cruzada entre macròlidos y lincosamidas 1.

MACRÓLIDOS Efectos colaterales: 1. Ototoxicidad 2. Irritación gástrica 3. Ictericia transitoria : Colestàsis. - Dolor Ü abdominal, Fiebre, Prurito y Hepatomegalia Erupción cutánea 5. Aplicación IM es muy dolorosa 4.

LINCOSAMIDAS Son Bacteriostáticos Ü Espectro medio: 1. Lincomicina 2. Clindamicina Ü Ü MECANISMO DE ACCIÒN: 1. Inhiben la síntesis de proteínas: Sub. U 50 s Ribosomal A concentraciones altas pueden ser bactericidas 2.
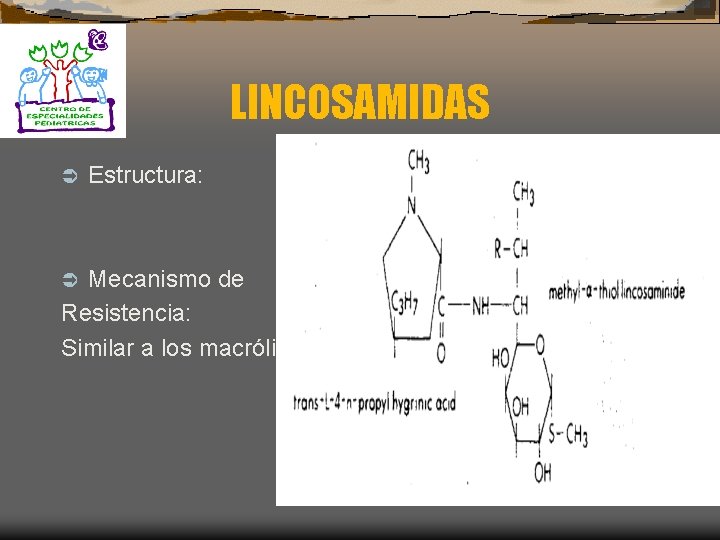
LINCOSAMIDAS Ü Estructura: Mecanismo de Resistencia: Similar a los macrólidos Ü

LINCOSAMIDAS Ü 1. 2. 3. 4. 5. Efectos colaterales: Irritación gástrica Erupciones cutáneas Colitis pseudomembranosa Flebitis Hepatotoxicidad

LINCOSAMIDAS Ü 1. 2. 3. 4. 5. Farmacocinética: Se admistra Vía oral, Intramuscular e Intravenosa Vida media de 3 horas Penetra en la mayoría de los tejidos En amígdalas, esputo, bronquios, pulmón, pleura, líquido pleural, apéndice y piel alcanza niveles superiores a la del suero Se elimina por el hígado

METRONIDAZOL Ü Actividad Antimcrobiana: Es activo contra protozooarios Gérmenes anaerobios + H. Pyori Ü Mecanismo de acción: Es reducido después de su penetración por un sístema oxidoreductasa de piruvato-ferredoxina presente en los anaerobios, generando productos tóxicos y muerte celular.

METRONIDAZOL Ü 1. 2. 3. 4. 5. Farmacocinética: Buena absorción oral Vía intravenosa se une a proteínas 1 – 20% Penetra a todos los tejidos y líquidos corporales Se metaboliza en el Hígado 6 -8% es eliminado en orina.

METRONIDAZOL Ü Mecanismos de Resistencia: Principal es la disminución del Sístema de oxidoreductasa. Es rara para anaerobios Puede ocurrir para H. pylori

METRONIDAZOL Toxicidad: 1. Gastrointestinales: * Dolor abdominal * Anorexia * Náusea 2. - Pancreatitis 3. - Hepatitis Ü

VANCOMICINA Ü Actividad antimicrobiana: Es el prímer glícopeptido contra bacterias aerobicas: S. aureus ( meticilino sensible y resistente), Estafilococo coagulasa negativo S. epidermidis, estreptococos como el S. Pneumoniae y contra Enterococo. Ü Mecanismo de acción: La vancomicina daña la permeabilidad de membranas y la síntesis de RNA en conjunto con la inhibición de la formación de Peptidoglicano

VANCOMICINA Ü 1. 2. 3. 4. Farmacocinética: Solo se puede administrar vía intravenosa No se absorbe vía oral Penetra a Hígado, riñon, bazo, pulmón y corazón, muy poca penetración a SNC Excretado por los riñones

VANCOMICINA Ü Mecanismo de resistencia: 1. Modificación del sitio blanco principal 2. Existen genes de resistencia: VAN A, VAN B, VAN C, VAN D como responsables de la resistencia a glucopéptidos 3. El gen Van A es el mas frecuente

VANCOMICINA Ü 1. 2. Toxicidad: Ototóxica Nefrotóxica: Aumento con el uso de aminoglucoósidos, diúreticos y anfotericina B 3. Síndrome del Hombre Rojo: Es dependiente de la dosis y velocidad de administración 4. 5. 6. 7. Disnea Mialgias Espasmos musculares Trombocitopenia, neutropenia y flebitis

TEICOPLANINA Ü Actividad antimicrobiana: Es el segundo glicopéptido que se limita a bacterias grampositivas Ü Mecanismo de acción. Inhibe la síntesis de pared celular impidiendo la polimerización del peptidoglicano. Ü Mecanismos de resistencia: Cambios en el sitio blanco principal

TEICOPLANINA Ü 1. 2. 3. 4. 5. Farmacocinética: Uso Intravenosos Vida media de 40 – 70 hrs Se une al 90% de las proteínas Depuración renal lenta Se excreta por vía renal

TEICOPLANINA Ü 1. 2. 3. 4. 5. Toxicidad: Hipersensibilidad Anormalidades hematológicas Ototoxicidad Nefrotoxicidad Síndrome del Hombre rojo ( rara)

CLORANFENICOL Actividad antimicrobiana: 1. Es bacteriostático 2. Es activo contra aerobios y anaerobios 3. Acividad bactericida contra S. Penumoniae, H influenzae y N. Meningitidis Ü

CLORANFENICOL Ü 1. 2. 3. Mecanismo de acción: Interfiere en la síntesis de proteínas al unirse a la subunidad ribosomica 50 S Farmacocinética: Penetra en todos los tejidos y líquidos Penetración al SNC 40 -65% con o sin inflamación La vida media es de 3 -4 hrs

CLORANFENICOL Mecanismo de resistencia: 1. Mecanismo enzimático: acetiltransferasa Ü 2. Perdída de la proteína bacteriana de la membrana externa responsable de la penetración intracelular

CLORANFENICOL Ü 1. 2. 3. 4. 5. 6. Toxicidad: Síndrome de Niño gris Daño hematológico Mielosupresión Trombocitopenia Neuritis óptica Neurotoxicidad

TRIMETROPIN - SULFAMETOXAZOL Actividad antimicrobiana: 1. Combinación de dos inhibidores de la síntesis de ácido dihidrofólico 2. Actividad contra gram positivos y gram negativos Ü

TRIMETROPIN - SULFAMETOXAZOL Ü Mecanismo de acción: 1. SMX inhibe la síntesis de ácido dihidroptérico 2. TMP se une a la reductasa del dihidrofolato impidiendo la transformación del ácido dihidrofólico en ácido tetrafólico

TRIMETROPIN - SULFAMETOXAZOL Ü 1. 2. 3. 4. Farmacocinética: Absorción oral es mayor de 85% La vida media es de 10 -12 hrs Buena distribución en todos los tejidos y líquidos corporales Su eliminación es por la orina

TRIMETROPIN - SULFAMETXOZAL Ü 1. 2. 3. 4. 5. Toxicidad: Náusea, vómito y diarrea. . . 0. 6 al 4% Efectos Hematológicos Hiperbilurribinemia en RN Hepatitis, Cefalea, Confusión, Depresión y daño renal transitorio Lesiones dermatológicas: Sx de Steven. Jhonson, eritema nodoso, fotodermatitis, urticaria, síndrome de piel escaldada, dermatitis exfoliativa
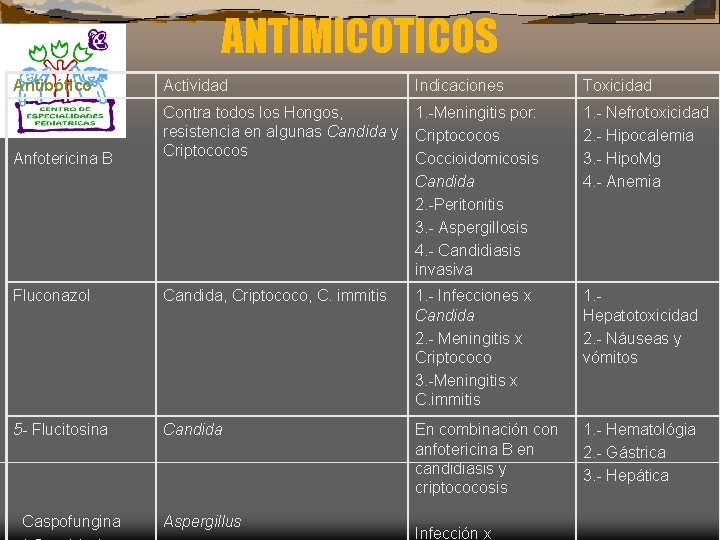
ANTIMICOTICOS Antibótico Actividad Indicaciones Toxicidad Anfotericina B Contra todos los Hongos, resistencia en algunas Candida y Criptococos 1. -Meningitis por: Criptococos Coccioidomicosis Candida 2. -Peritonitis 3. - Aspergillosis 4. - Candidiasis invasiva 1. - Nefrotoxicidad 2. - Hipocalemia 3. - Hipo. Mg 4. - Anemia Fluconazol Candida, Criptococo, C. immitis 1. - Infecciones x Candida 2. - Meningitis x Criptococo 3. -Meningitis x C. immitis 1. Hepatotoxicidad 2. - Náuseas y vómitos 5 - Flucitosina Candida En combinación con anfotericina B en candidiasis y criptococosis 1. - Hematológia 2. - Gástrica 3. - Hepática Caspofungina Aspergillus Infección x

- Slides: 68