Antibiotiques Une des grandes russites dans le traitement

Antibiotiques Une des grandes « réussites » dans le traitement des maladies au XX° siècle Un usage abusif, un mésusage actuel Un problème pour l’ avenir: résistances, infections nosocomiales,

Antibiotiques agir sur l’ agent infectieux Donnés à l’hôte, Pour détruire un agent Qui infecte l’hôte, Une pharmacologie particulière, où les effets « cliniques » attendus s’appliquent à un agent infectant et les effets sur l’hôte ne peuvent être qu’indésirables, non attendus,

Slide 13 of 147

Choix d’un ATB et modalités d'administration Choisir un antibiotique dont le spectre est adapté aux bactéries infectantes (identifiées ou supposées) (Bactériologie) Il faut qu'il puisse diffuser jusque là où est le germe (Pharmacocinétique) Un mode d'administration pragmatique, qui donne la meilleure efficacité, pour un risque « acceptable » . en s'appuyant sur les données pharmacocinétiques, pharmacodynamiques, les modèles animaux, et le bon sens on peut proposer des modes d'administration chez l'Homme, susceptibles d'avoir un bon rapport bénéfice / risque, qu'on teste dans le cadre d'essais cliniques comparatifs (PK/PD). La durée nécessaire pour le traitement ne doit pas être choisie au hasard ; ce sont aussi les essais cliniques comparatifs qui, après comparaison de durées différentes, déterminent la durée qui a, dans une indication donnée, en moyenne, le meilleur rapport efficacité-effets indésirables. C'est grâce à de tels essais que la durée du traitement d'une première infection urinaire basse de la femme est passé de 8 j, à des traitements en une seule prise, dits « minute » (PK/PD). Prévenir les résistances tant au niveau des bactéries responsables de l’infection que de la flore commensale: appliquer les données PK/PD et bon usage… Ne pas oublier l’état du malade!

Antibiotiques classification ? structure chimique mode d’action antibactérienne Choix « hybride » action ->structure exception: antituberculeux -> action antibactérienne
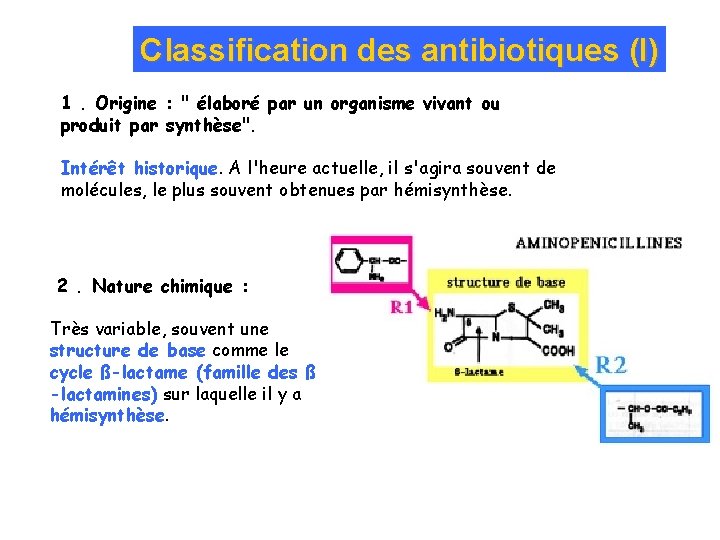
Classification des antibiotiques (I) 1. Origine : " élaboré par un organisme vivant ou produit par synthèse". Intérêt historique. A l'heure actuelle, il s'agira souvent de molécules, le plus souvent obtenues par hémisynthèse. 2. Nature chimique : Très variable, souvent une structure de base comme le cycle ß-lactame (famille des ß -lactamines) sur laquelle il y a hémisynthèse.

Classification des antibiotiques (II) Pourquoi ? * Nombre de molécules élevé, donc faciliter le choix thérapeutique. * A une parenté structurale s'associera un mode d'action semblable ainsi qu'une modalité d'action et un spectre d'action, donc classification en famille au sein desquels peuvent exister des groupes ou sous-groupes. Néanmoins, il existe des antibiotiques "orphelins": acide fusidique, fosfomycine, triméthoprime. Critères de classification ?

ANTIBIOTIQUES MECANISMES D’ACTION 1) Inhibent la synthèse de la membrane cellulaire (synthèse des peptidoglycans) : -lactamines 2) Inhibent la réplication de l’ADN : quinolones : 3) Inhibent la synthèse des protéines: aminoglycosides tétracyclines, macrolides, chloramphénicol
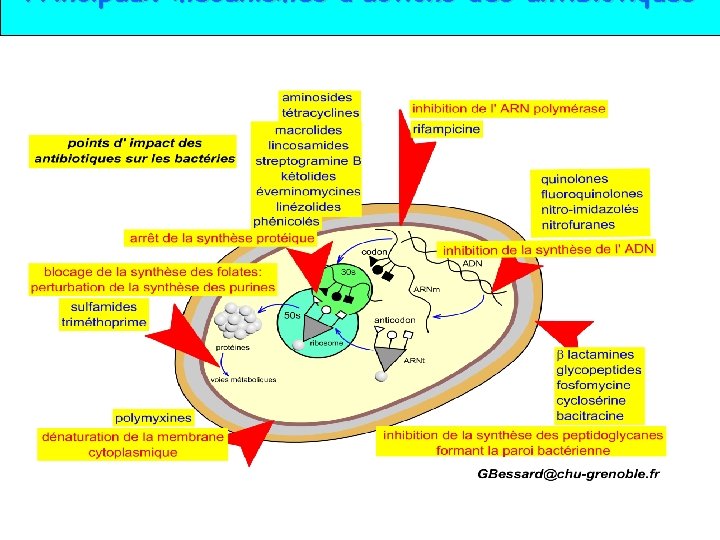
Principaux mécanismes d’actions des antibiotiques Mécanismes d’action des antibiotiques,

RESISTANCES AUX ANTIBIOTIQUES Mécanismes • Diminution de la concentration intracellulaire (tétracyclines) Diminution de la concentration intracellulaire 1. diminution de la perméabilité membranaire 2. excrétion active • Modification de l ’agent : -lactamases ( -lactamines) -lactamases • Modifications de la cible : par mutations (quinolones) Modifications de la cible : par mutations

Résistances aux antibiotiques : mécanismes Diminution de la concentration cellulaire : voir MDR (multidrug resistance)
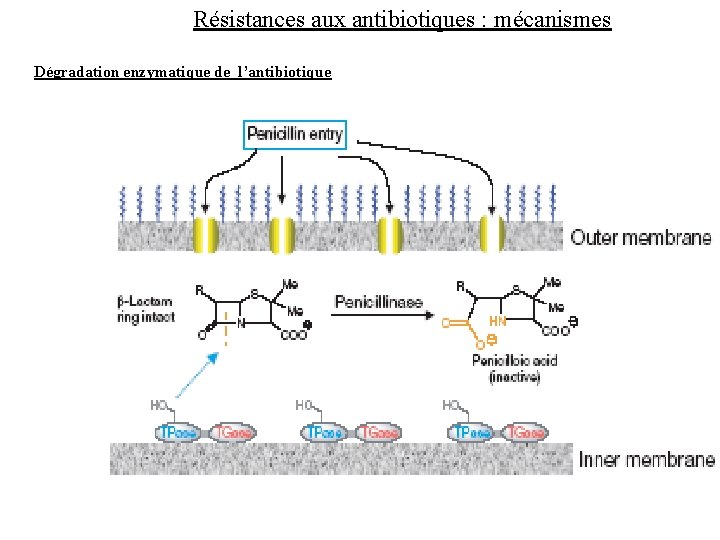
Résistances aux antibiotiques : mécanismes Dégradation enzymatique de l’antibiotique
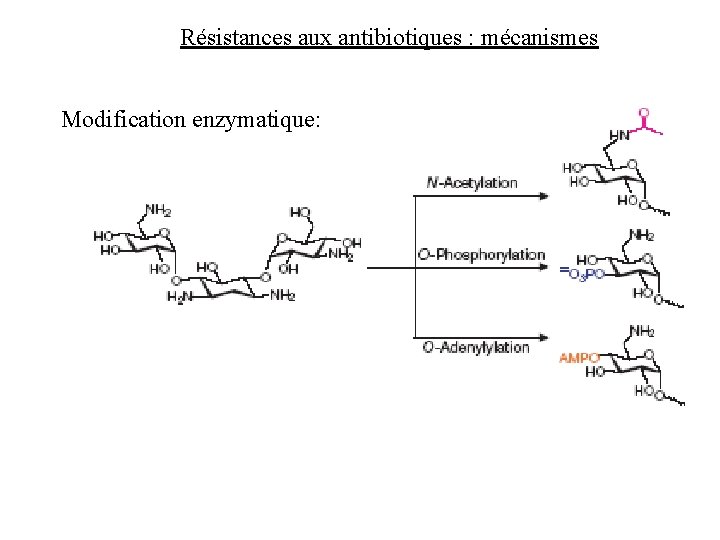
Résistances aux antibiotiques : mécanismes Modification enzymatique:

Modifications de la cible : par mutations Stratégies: • séléction locale • transfert de matériel génétique: transformation (ADN libre), conjugaison (plasmides), transduction (phages)
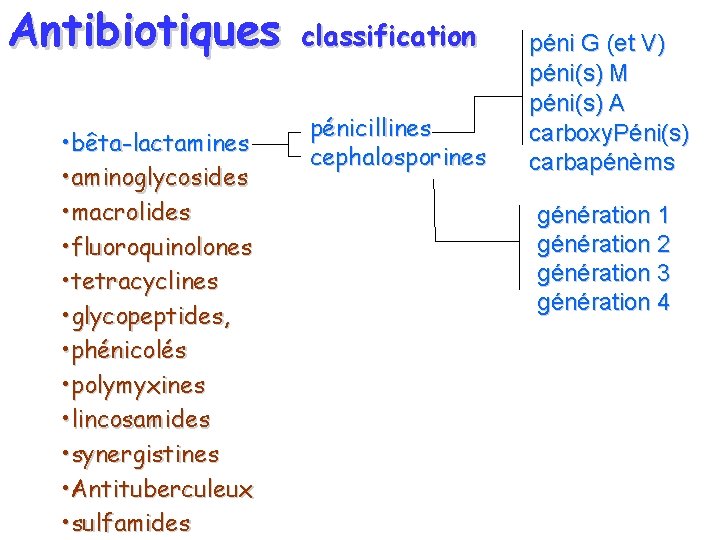
Antibiotiques • bêta-lactamines • aminoglycosides • macrolides • fluoroquinolones • tetracyclines • glycopeptides, • phénicolés • polymyxines • lincosamides • synergistines • Antituberculeux • sulfamides classification pénicillines cephalosporines péni G (et V) péni(s) M péni(s) A carboxy. Péni(s) carbapénèms génération 1 génération 2 génération 3 génération 4

Antibiotiques : mécanismes d’action • Action sur la paroi bactérienne bêta-lactamines, glycopeptides • Inhibition réversible de la synthèse protéique macrolides, tétracyclines, (chloramphénicol) • Inhibition irréversible de la synthèse protéique aminosides • Inhibition de la synthèse des acides nucléiques fluoroquinolones, rifampicine • antimétabolites sulfamides • Action sur la membrane cellulaire polymyxines,

ANTIBIOTIQUES MECANISMES D’ACTION 1) Inhibent la synthèse de la membrane cellulaire (synthèse des peptidoglycans) : -lactamines 2) Inhibent la réplication de l’ADN : sulfamides, quinolones 3) Inhibent la synthèse des protéines: aminoglycosides, tétracyclines, macrolides, chloramphénicol
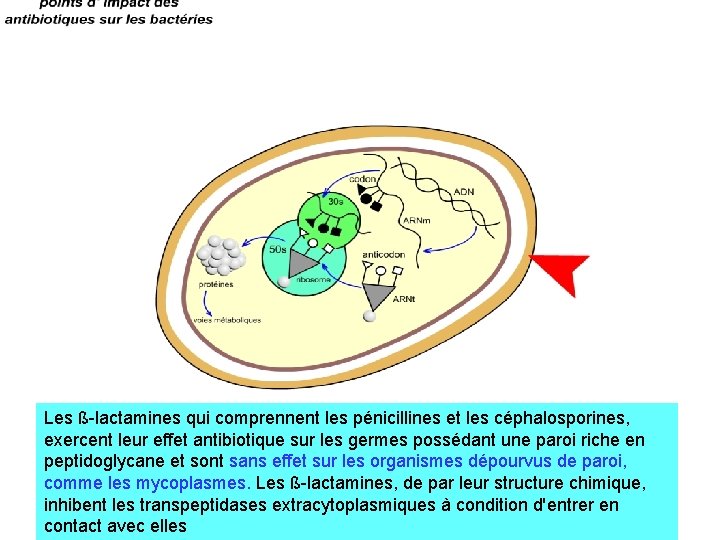
Les ß-lactamines qui comprennent les pénicillines et les céphalosporines, exercent leur effet antibiotique sur les germes possédant une paroi riche en peptidoglycane et sont sans effet sur les organismes dépourvus de paroi, comme les mycoplasmes. Les ß-lactamines, de par leur structure chimique, inhibent les transpeptidases extracytoplasmiques à condition d'entrer en contact avec elles
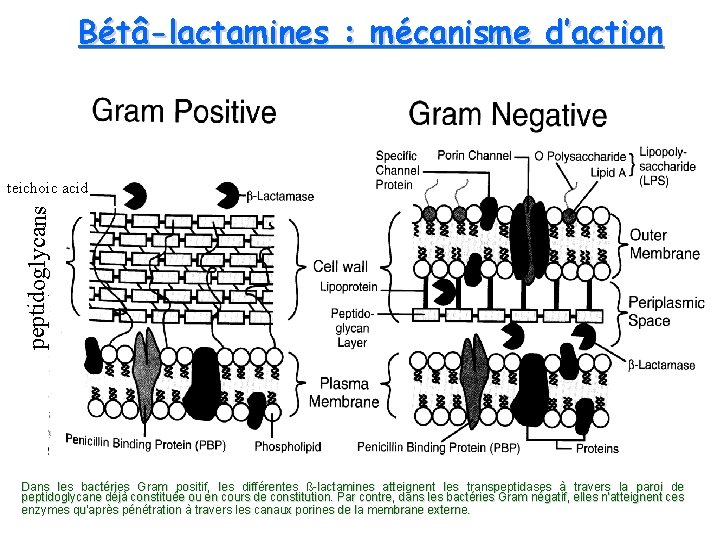
Bétâ-lactamines : mécanisme d’action peptidoglycans teichoic acid Dans les bactéries Gram positif, les différentes ß-lactamines atteignent les transpeptidases à travers la paroi de peptidoglycane ou en en cours de de constitution. Par contre, dans les bactéries Gram négatif, elles n'atteignent ces peptidoglycane déjà constituée ou enzymes qu'après pénétration à travers les canaux porines de la membrane externe.
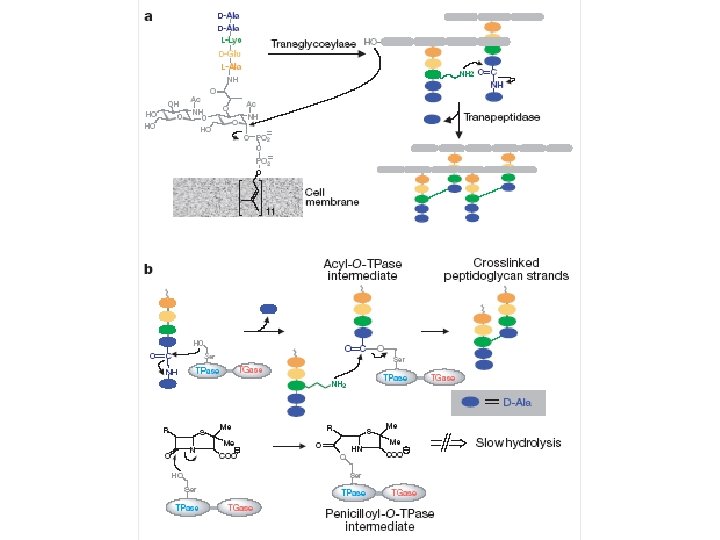

Bétâ-lactamines : mécanisme d’action La synthèse du peptidoglycane est complexe et nécessite l'activité d'environ trente enzymes différentes. Elle comporte trois étapes principales : a. une étape intracytoplasmique aboutissant à la synthèse d'UDPintracytoplasmique acétylmuramyl-pentapeptide, terminé par un dipeptide, le D-alanyl-D-alanine La synthèse de ce dipeptide nécessite l'intervention de la phosphoénolpyruvate transférase, d'une racémase et d'une synthétase. b. une deuxième étape membranaire aboutissant à la formation d'un membranaire polymère acétylglucosamine et de l'UDP-acétylmuramyl-dipeptide. Ce UDP-acétylmuramyl-dipeptide polymère sort du cytoplasme à travers la membrane cytoplasmique. c. une troisième étape extracytoplasmique comportant une polymérisation par extracytoplasmique une polymérisation transpeptidation (liaison peptidique entre acides aminés) sous l'effet d'une transpeptidation transpeptidase fixée à la partie externe de la membrane cytoplasmique et par transglycosylation (liaison glucidique).
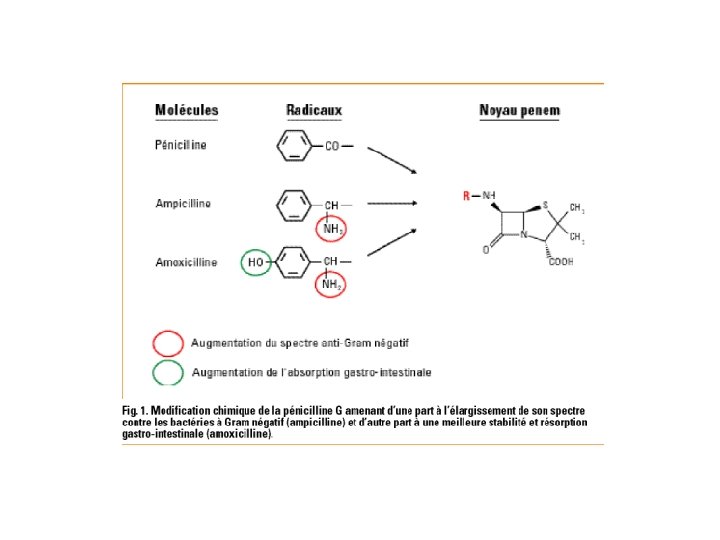

Pénicillines 1. benzylpénicilline (G), phénoxyméthylpénicilline • actif contre Gram + • inactif contre majorité de Staph. aureus • rapidement hydrolysé par pénicillinase 2. pénicillines résistantes contre pénicillinase flucloxacilline méticilline 3. Pénicillines à large spectre (Gram -) ampicilline, amoxicilline : hydrolysée par -lactamases ticarcilline : contre Pseudomonas, entérobactérie piperacilline : contre Pseudomonas, Klebsiella.
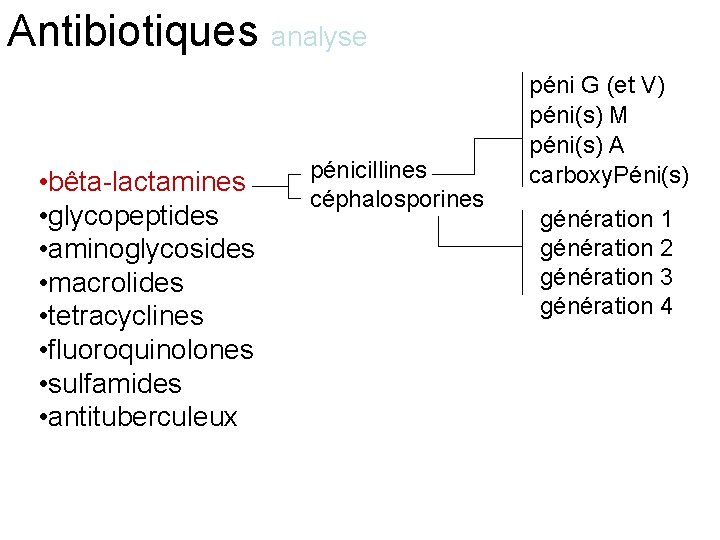
Antibiotiques analyse • bêta-lactamines • glycopeptides • aminoglycosides • macrolides • tetracyclines • fluoroquinolones • sulfamides • antituberculeux pénicillines céphalosporines péni G (et V) péni(s) M péni(s) A carboxy. Péni(s) génération 1 génération 2 génération 3 génération 4
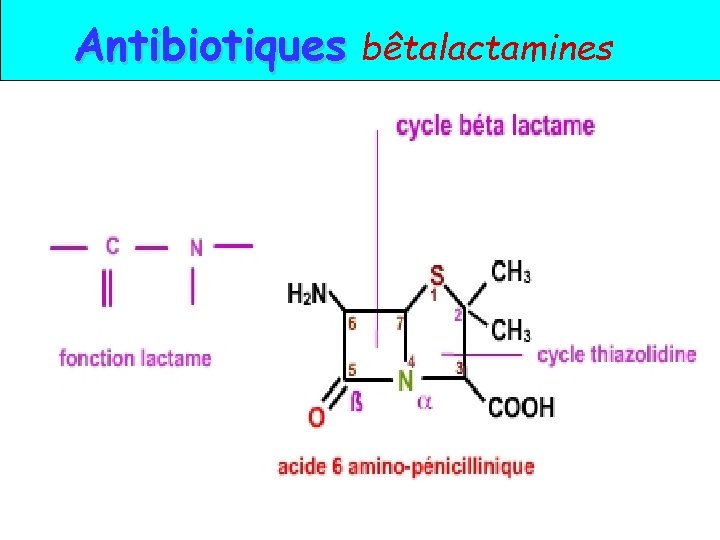
Antibiotiques bêtalactamines
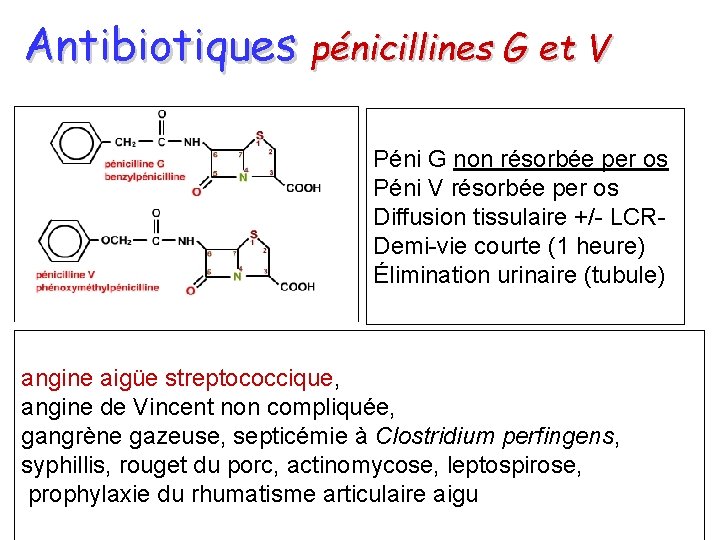
Antibiotiques pénicillines G et V Péni G non résorbée per os Péni V résorbée per os Diffusion tissulaire +/- LCRDemi-vie courte (1 heure) Élimination urinaire (tubule) angine aigüe streptococcique, angine de Vincent non compliquée, gangrène gazeuse, septicémie à Clostridium perfingens, syphillis, rouget du porc, actinomycose, leptospirose, prophylaxie du rhumatisme articulaire aigu

Antibiotiques pénicillines G et V Formes retard: Benzathine-pénicilline, Procaïne- pénicilline,
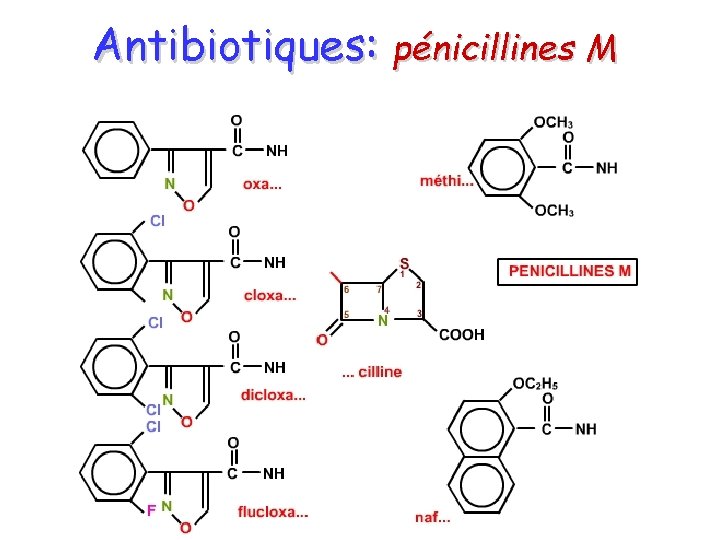
Antibiotiques: pénicillines M

Antibiotiques pénicillines M seules cloxa, dicloxa et flucloxacilline sont résorbées par voie entérale, méthicilline, oxacilline, cloxacilline, dicloxacilline, flucloxacilline, nafcilline, résistent à la ß lactamase des staphylocoques sécréteurs de cette "pénicillinase".
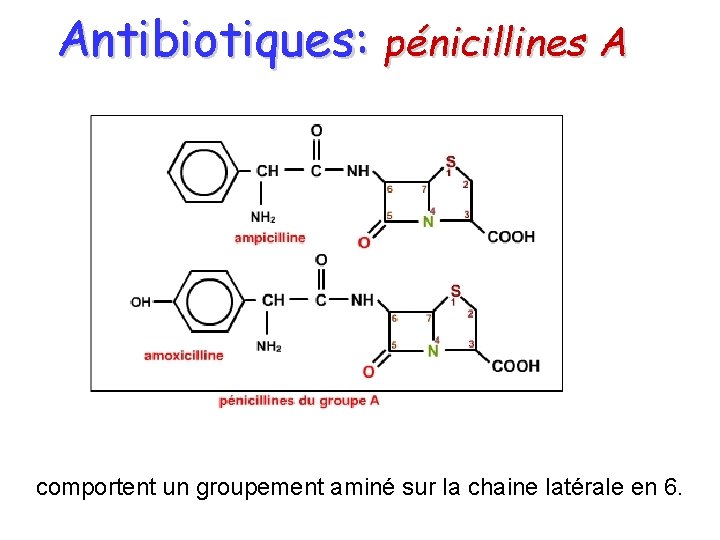
Antibiotiques: pénicillines A comportent un groupement aminé sur la chaine latérale en 6.

Antibiotiques: pénicillines A améliorations cinétiques, résorption orale, diffusion tissulaire, (LCR) moindre toxicité, amélioration du spectre d’ activité,

Antibiotiques: pénicillines A association aminopénicilline/acide clavulanique permet de combattre l’action des bétalactamases

Antibiotiques: carboxypenicillines uréidopénicillines activité anti-pyocyanique Ils sont présentés seulement sous forme injectable par voie intraveineuse et sont utilisés en milieu hospitalier. Ticarcilline TICARPEN* Inj Mezlocilline BAYPEN* « Pipéracilline PIPÉRILLINE* «

Antibiotiques: pénicillines • pénicilline G, la première • pénicilline V, la même mais per os • Procaïne pénicilline, IM, longue action • Pénicillines M, contre les staph résistants • Aminopénicillines, per os, à bonne diffusion, spectre élargi, • Asso. Ampi/a. clavulinique • Et: carboxi, uréïdo, ….
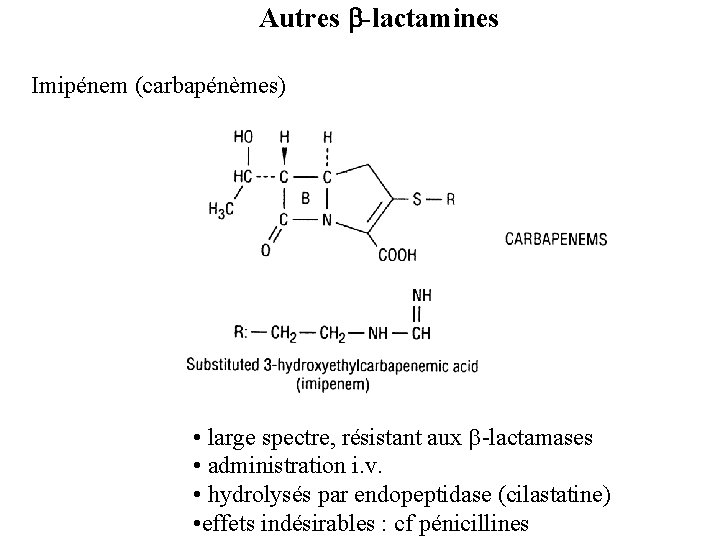
Autres -lactamines Imipénem (carbapénèmes) • large spectre, résistant aux -lactamases • administration i. v. • hydrolysés par endopeptidase (cilastatine) • effets indésirables : cf pénicillines

Carbapénèmes et monobactams Les carbapénèmes et les monobactams sont des dérivés proches des céphalosporines. L'imipénem (thiénamycine) a un spectre large et est associé à un inhibiteur de son catabolisme, la cilastine. La cilastine est un inhibiteur d'une enzyme rénale, la déhydropeptidase I qui métabolise et inactive l'imipénem Les ß-lactamines monocycliques, ou monobactams, comme l'aztréonam, sont actifs seulement contre les germes Gram négatif

Pharmacocinétique. · lipide-insoluble (amoxicilline: VD = 0. 2 l/kg) · absorption orale variable (pénicilline G ) · large distribution tissulaire, sauf: SNC, prostate, faible dans LCR · élimination rénale: filtration, sécrétion · ½ vie plasmatique courte (~1 -2 h)

Résistance, mécanismes. • Diminution de la permabilité membranaire • Augmentation de l ’efflux (Gram-) • Pénicillinases, -lactamases (Gram +) Voir acide clavulanique • Différences structurelles et d'affinité entre PBPs (pneumocoques, méningocoques
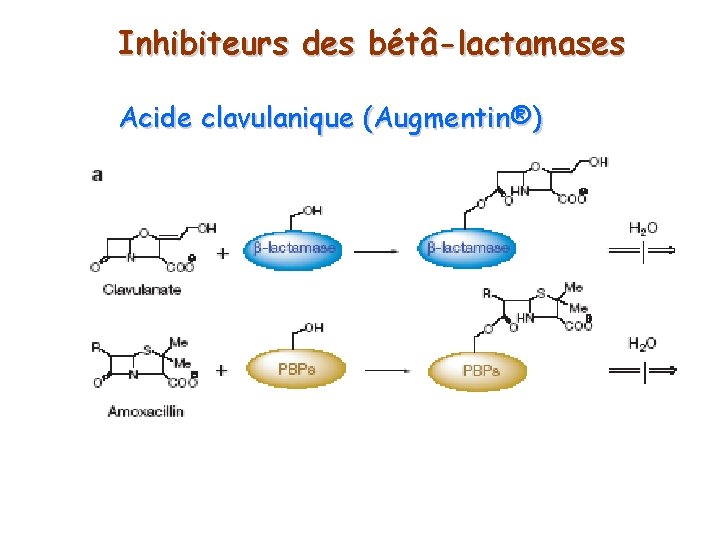
Inhibiteurs des bétâ-lactamases Acide clavulanique (Augmentin®)

Sulbactam En plus de son effet inhibiteur irréversible sur les ß-lactamases, le sulbactam a une activité antibiotique intrinsèque sur quelques germes, mais il est toujours utilisé en association avec les antibiotiques détruits par les -lactamases. Le sulbactam s'administre par voie parentérale, en perfusion. Il s'élimine par voie rénale. Il existe un ester sulbactam-ampicilline. L'hydrolyse de la liaison ester dans l'organisme libère le sulbactam et l'ampicilline Sulbactam + ampicilline estérifiée UNACIM* Inj Sulbactam (seul) BÉTAMAZE* Tazobactam Le tazobactam est un dérivé de l'acide pénicillanique qui a des propriétés proches de celles de l'acide clavulanique et du sulbactam. Il est associé à la pipéracilline. Tazobactam+ pipéracilline TAZOCILLINE* Inj

Effets indésirables des pénicillines ·toxicité directe faible, grande marge thérapeutique irritation locale, thrombophlébites nausées, vomissement, diarrhées convulsions (insuffisance rénale) · hypersensibilité (ac. pénicilloïque): érythème, anaphylaxie, vasculite éosinophilie, anémie hémolytique arthralgie rares néphrites interstitielles.
Antibiotiques analyse • bêta-lactamines • glycopeptides, • aminoglycosides • macrolides • tetracyclines • fluoroquinolones • Antituberculeux • sulfamides pénicillines céphalosporines péni G (et V) péni(s) M péni(s) A carboxy. Péni(s) génération 1 génération 2 génération 3 génération 4
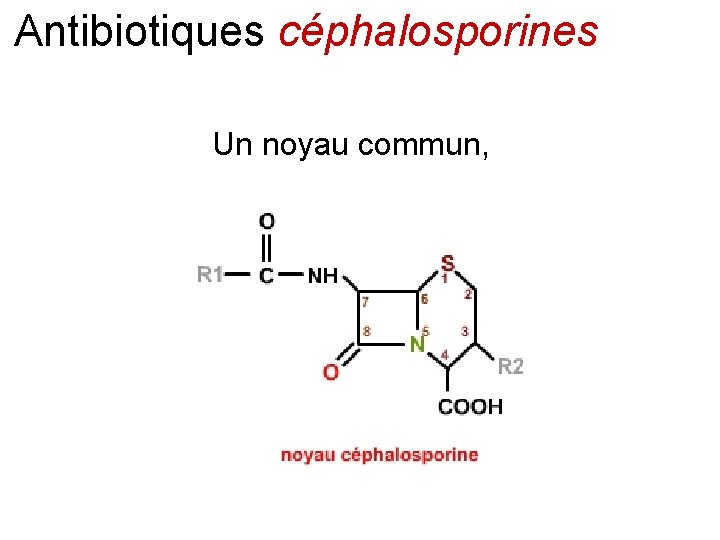
Antibiotiques céphalosporines Un noyau commun,

Céphalosporines 1. première génération: ·céfalexine, ·large spectre: Gram+ > Gram – ·inf. urinaires, prophylaxie chirurgie, peau, tissus mous 2. deuxième génération: ·céfamandole (Mandokef), céfuroxime, céfaclor (Céclor), céfoxitine ·plus actif contre Gram- que 1ère génération ·administration orale possible. 3. troisième génération ·céfotaxime (Claforam), ceftriaxone (Rocéphine), ceftazidime, ·large spectre contre Gram - et Gram + ·sensibles aux -lactamases ·ceftriaxone : élimination biliaire ·adm. iv , passe barrière hémato-encéphalique, infections graves 4. quatrième génération ·céfépime (Maxipime) ·spectre comparable à 3ème génération ·résistant à quelques -lactamases (Entérobacter) ·ttt empirique, infections nosocomiales

Antibiotiques céphalosporines Génération 1: céfalotine, céfalexine, active sur les souches Gram +, de façon limitée les Gram Génération 2: céfamandole, céfoxitine, céfuroxime, activité accrue sur les germes Gram - certains dérivés actifs sur Bacterioides fragilis Génération 3: céfotaxime, céftriaxone, céftazidime, céfopérazone, . . . activité moindre sur les Gram + mais meilleure activité sur les entérobactéries, y compris souches productrices de béta-lactamases. Céftazidime et céfopérazone sont actives sur Pseudomonas aeruginosa mais moins actives sur les coccis Gram + Génération 4: céfépime, stabilité sur plasmides et bétalactamases. Intérêt: infections à bacilles Gram - résistantes aux autres céphalosporines.
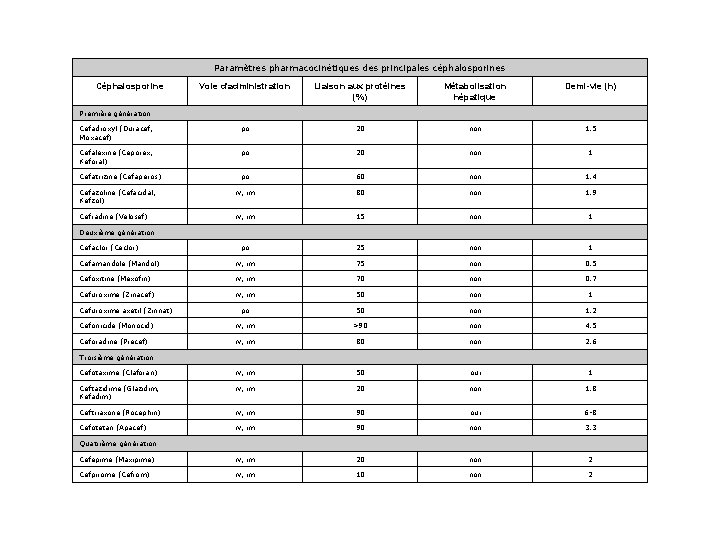
Paramètres pharmacocinétiques des principales céphalosporines Céphalosporine Voie d'administration Liaison aux protéines (%) Métabolisation hépatique Demi-vie (h) Cefadroxyl (Duracef, Moxacef) po 20 non 1. 5 Cefalexine (Ceporex, Keforal) po 20 non 1 Cefatrizine (Cefaperos) po 60 non 1. 4 Cefazoline (Cefacidal, Kefzol) iv, im 80 non 1. 9 Cefradine (Velosef) iv, im 15 non 1 po 25 non 1 Cefamandole (Mandol) iv, im 75 non 0. 5 Cefoxitine (Mexofin) iv, im 70 non 0. 7 Cefuroxime (Zinacef) iv, im 50 non 1 po 50 non 1. 2 Cefonicide (Monocid) iv, im >90 non 4. 5 Ceforadine (Precef) iv, im 80 non 2. 6 Cefotaxime (Claforan) iv, im 50 oui 1 Ceftazidime (Glazidim, Kefadim) iv, im 20 non 1. 8 Ceftriaxone (Rocephin) iv, im 90 oui 6 -8 Cefotetan (Apacef) iv, im 90 non 3. 3 Cefepime (Maxipime) iv, im 20 non 2 Cefpirome (Cefrom) iv, im 10 non 2 Première génération Deuxième génération Cefaclor (Ceclor) Cefuroxime axetil (Zinnat) Troisième génération Quatrième génération

ANTIBIOTIQUES MECANISMES D’ACTION 1) Inhibent la synthèse de la membrane cellulaire (synthèse des peptidoglycans) : -lactamines 2) Inhibent la réplication de l’ADN : sulfamides, quinolones 3) Inhibent la synthèse des protéines: aminoglycosides, tétracyclines, macrolides, chloramphénicol
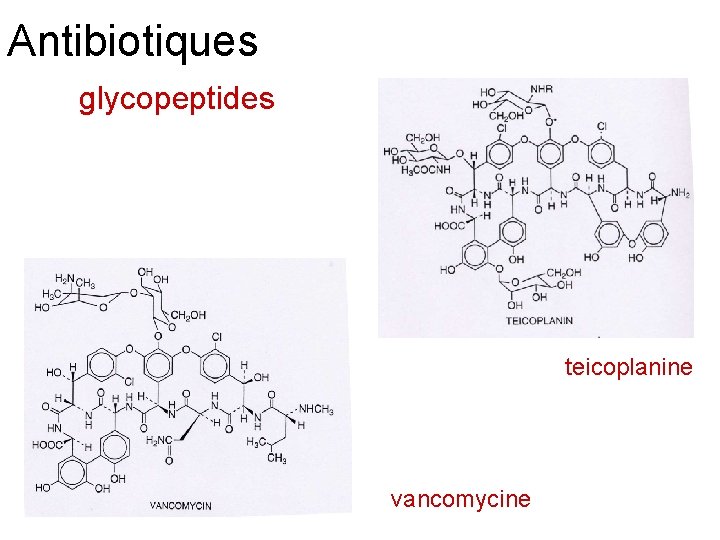
Antibiotiques glycopeptides teicoplanine vancomycine

Antibiotiques: glycopeptides La vancomycine est un glycopeptide tricyclique de poids moléculaire élevé, environ 1500, qui, en se fixant étroitement par cinq liaisons hydrogène à la terminaison D-alanyl-D-alanine, inhibe la transpeptidation, altère la synthèse de la paroi bactérienne et modifie la perméabilité de la membrane cytoplasmique. Elle inhibe aussi la synthèse du RNA. Elle est active contre les bactéries Gram positif comme les staphylocoques, les streptocoques, les Elle est active contre les bactéries Gram positif pneumocoques et est utilisée en particulier dans le traitement des infections à staphylocoques résistants aux autres antibiotiques. Sur le plan pharmacocinétique, elle est peu absorbée par voie orale et son administration se fait par voie intraveineuse pour traiter des infections générales. La voie buccale est réservée au traitement de certaines colites, à Clostridium difficile par exemple. Les principaux effets indésirables de la vancomycine sont de type allergique, mais son accumulation, chez l'insuffisant rénal notamment, entraîne une néphrotoxicité et une ototoxicité. La teicoplanine, glycopeptide proche de la vancomycine, est active sur les germes Gram positif. teicoplanine Des entérocoques ont développé une résistance à la vancomycine en acquérant la capacité de remplacer la D-alanine par l'acide D-lactique, ce qui empêche la fixation de la vancomycine. On peut craindre que les entérocoques puissent transmettre leur résistance aux staphylocoques.
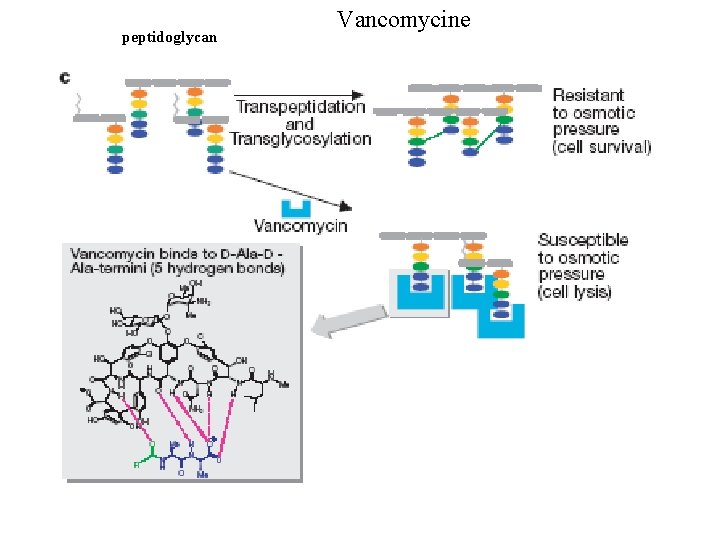
peptidoglycan Vancomycine

Glycopeptides Vancomycine · inhibition de transpeptidation et transglycosylation , prévient l’élongation de la chaîne de peptidoglycan · spectre: Gram +, Staph. dorés résistants à flucloxacilline · effets indésirables: réactions anaphylactoïdes néphrotoxicité, ototoxicité · administration I. V, passe dans LCR · élimination rénale. Autre : Teicoplanine (dose de charge, LP +++, T 1/2 longue

Antibiotiques: glycopeptides teicoplanine usage hospitalier oral (colites et préparations digestives) et parentéral (germes sensibles) vancomycine usage hospitalier parentéral germes sensibles Utilisées sur germes méthicilline résistants. Pratique d’un suivi des concentrations plasmatiques,

Antibiotiques inhibant la synthèse protéique Antibiotiques agissant au niveau de la sous-unité ribosomale 30 s Les inhibiteurs de la sous-unité ribosomale 30 S ont des propriétés antibiotiques. On y classe les tétracyclines et les aminosides. Antibiotiques agissant au niveau de la sous-unité ribosomale 50 s Les médicaments qui perturbent le fonctionnement des sous-unités ribosomales 50 S ont des propriétés antibiotiques; ce sont les macrolides, le chloramphénicol et l'acide fusidique.
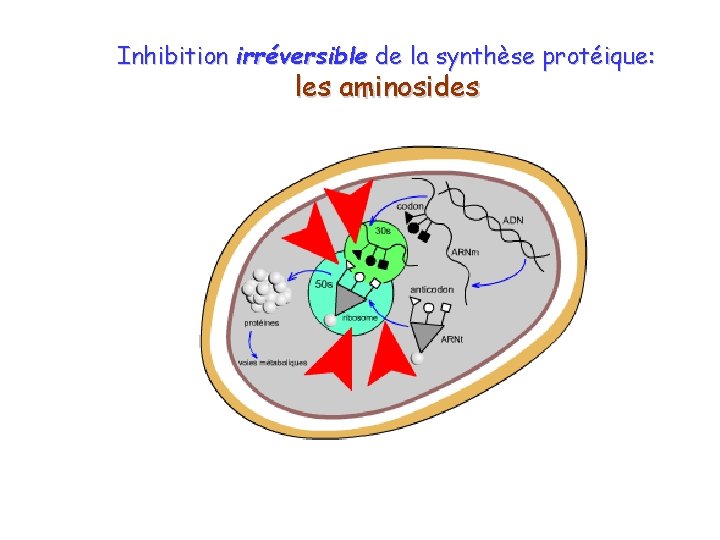
Inhibition irréversible de la synthèse protéique: les aminosides
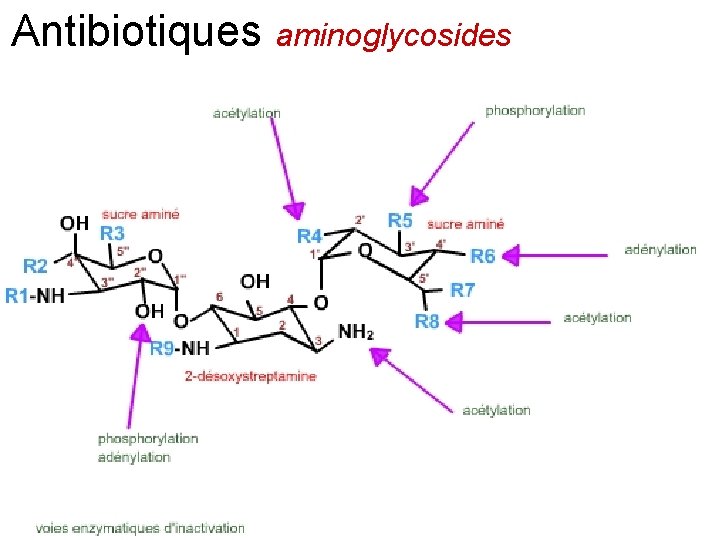
Antibiotiques aminoglycosides

Antibiotiques aminoglycosides 1943, la streptomycine 1949, la néomycine (usage externe) 1957, la kanamycine en 1963, gentamicine - GENTALLINE ® puis: tobramycine - NEBCINE ® - (1967), sisomicine - SISOLINE ® - (1970), dibékacine - DIBEKACYL ® - (1971), amikacine - AMIKLIN ® - (1972), nétilmicine - NETROMICINE ® - (1974). les dérivés des streptomyces sont à suffixe "mycine", les dérivés d'actinomycètes monospores sont à suffixe "micine".

Les aminoglycosides Les aminosides, antibiotiques bactéricides, diffusent dans les bactéries à travers les canaux porines jusqu'à l'espace périplasmique. Leur pénétration à travers la membrane cytoplasmique est active et nécessite un apport d'énergie et la présence d'oxygène. Lorsque l'aminoside est en permanence présent au contact d'un germe sensible, il y a inhibition de sa pénétration à travers la membrane cytoplasmique. Cette constatation explique l'intérêt de l'administration discontinue des aminosides Les aminosides perturbent la synthèse protéique bactérienne en se fixant sur les ribosomes de la sous-unité 30 S. L'altération de la membrane bactérienne est la conséquence de la perturbation de la synthèse protéique. La résistance aux aminosides peut provenir d'un défaut de leur pénétration dans le La résistance défaut de leur pénétration cytoplasme bactérien, de leur inactivation par biotransformations sous l'influence de leur inactivation d'enzymes, phosphorylase, acétylase, synthétisées sous la dépendance de plasmides, d'une modification de la structure des ribosomes empêchant la fixation de l'antibiotique. modification de la structure des ribosomes

Antibiotiques: aminoglycosides infections sévères à germes gram négatifs anaérobies infections à Pseudomonas aeruginosa infections systémiques à Staphylocoques méthi-S endocardites streptococciques états fébriles sur terrain neutropénique, immunodéprimé. listériose, Mycobactérium tuberculosis

Antibiotiques aminoglycosides propriétés cinétiques communes: non résorbés par voie orale, peu liés aux protéines plasmatiques, Ils diffusent de façon limitée dans les tissus (sauf dans le parenchyme rénal) et peu dans le LCR, ne sont pas biotransformés, demi vie plasmatique de 2 à 3 heures, filtration glomérulaire sous forme de produit parent. Une réabsorption tubulaire explique les concentrations parenchymateuses rénales, traversent le placenta,

Antibiotiques aminoglycosides Effets indésirables atteinte de l'oreille interne: irréversible, cumulative traduite par une perte de l'audition les troubles de l'équilibre (risque spécifique pour l'administration locale éviter l'association de médicaments ototoxiques: furosémide) atteinte rénale néphropathie tubulo-intersticielle aigue à diurèse conservée le plus souvent réversible à l'arrêt du traitement. situations à risque: sujet âgé, insuffisant rénal, médicaments néphrotoxiques associés, hypersensibilité, effet curare-like.

Antibiotiques aminoglycosides Propriétés cinétiques communes: - Non résorbés par voie orale, - peu liés aux protéines plasmatiques, leur distribution est essentiellement extracellulaire : de fortes concentrations sont trouvées dans le rein, l'endolymphe et la périlymphe de l'oreille interne, ce qui explique leur toxicité rénale et cochléaire ils diffusent de façon limitée dans les tissus (sauf dans le parenchyme rénal) et peu dans le LCR < 10% plasma), traversent le placenta - ne sont pas biotransformés, - filtration glomérulaire sous forme de produit parent. Une réabsorption tubulaire explique les concentrations parenchymateuses rénales, demi vie plasmatique de 2 à 3 heures…, -Dans la mesure où les aminosides ne diffusent pas dans les tissus graisseux, l'adaptation de leur posologie devrait tenir compte seulement du volume de la masse maigre.
Antibiotiques macrolides un cycle macro-lactonique,
Antibiotiques macrolides

Antibiotiques macrolides Indications principales: angines aigües: en seconde intention lors d'intolérance à la pénicilline infections bronchiques, pulmonaires à germes intra-cellulaires, infections uro-génitales ( en seconde intention après les cyclines pour C. trachomatis, U. urealyticum) infections à Mycobacterium avium au cours du SIDA éradication d' Helicobacter pylori. toxoplasmose de la femme enceinte

Antibiotiques macrolides Les principaux macrolides sont l'érythromycine, la spiramycine, la midécamycine, la josamycine, la roxithromycine, la dirithromycine, la clarithromycine et l’ azithromycine Ils pénètrent dans les bactéries sous la forme non ionisée qui est prédominante à p. H alcalin. Les bactéries Gram positif accumulent environ 100 fois plus de macrolides que les germes Gram négatif, ce qui explique leur action prédominante sur les germes Gram positif Les macrolides ont une activité bactériostatique ou bactéricide selon leur concentration et la sensibilité des germes. Ils sont efficaces sur les cocci Gram positif aérobies et anaérobies, les Gram positif aérobies et anaérobies cocci gram négatif, comme les gonocoques et les méningocoques, les bacilles gram négatif comme Hélicobacter pylori, et des germes comme Legionella pneumophilia, Mycoplasma, Clamydia. En France, actuellement, un quart des pneumocoques sont résistants aux macrolides. La résistance aux macrolides est la conséquence d'une diminution de leur pénétration cellulaire, de leur hydrolyse par des estérases et de modifications ribosomales

Antibiotiques macrolides Pharmacocinétique Forte pénétration intracellulaire Les macrolides inhibent la synthèse d'enzymes hépatiques de biotransformation des médicaments: association contre indiquée avec: carbamazépine, dérivés de l'ergot de seigle (risque ischémique des extrémités), cisapride (risques de troubles du rythme), Effets indésirables Les macrolides sont des antibiotiques bien tolérés. intolérances digestives hépatites cholostatiques (érythromycine) troubles de l'audition (érythromycine) peu fréquents,

ANTIBIOTIQUES MECANISMES D’ACTION 1) Inhibent la synthèse de la membrane cellulaire (synthèse des peptidoglycans) : -lactamines 2) Inhibent la réplication de l’ADN : sulfamides, quinolones 3) Inhibent la synthèse des protéines: aminoglycosides, tétracyclines, macrolides, chloramphénicol
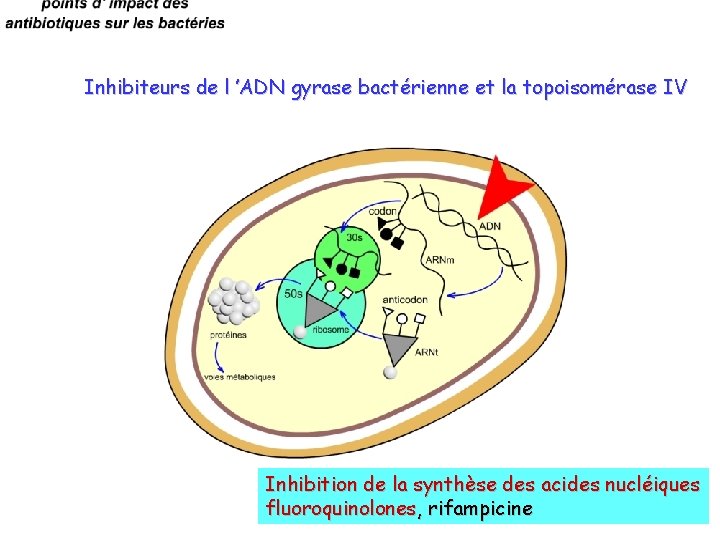
Inhibiteurs de l ’ADN gyrase bactérienne et la topoisomérase IV Inhibition de la synthèse des acides nucléiques fluoroquinolones, rifampicine
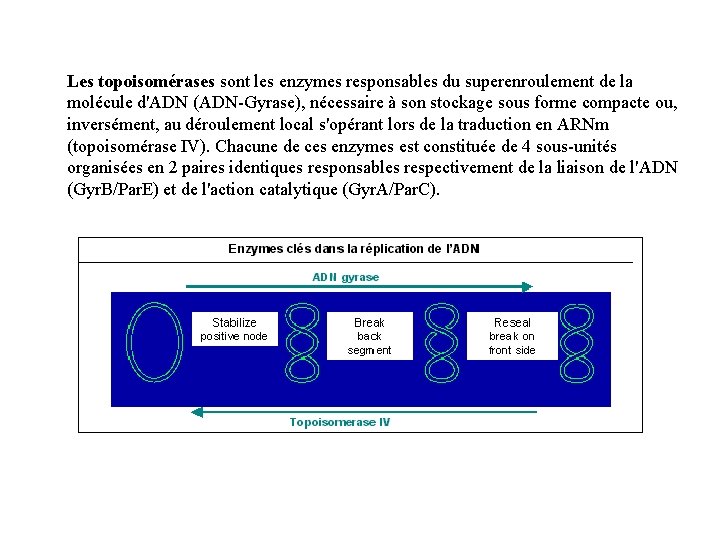
Les topoisomérases sont les enzymes responsables du superenroulement de la molécule d'ADN (ADN-Gyrase), nécessaire à son stockage sous forme compacte ou, inversément, au déroulement local s'opérant lors de la traduction en ARNm (topoisomérase IV). Chacune de ces enzymes est constituée de 4 sous-unités organisées en 2 paires identiques responsables respectivement de la liaison de l'ADN (Gyr. B/Par. E) et de l'action catalytique (Gyr. A/Par. C).
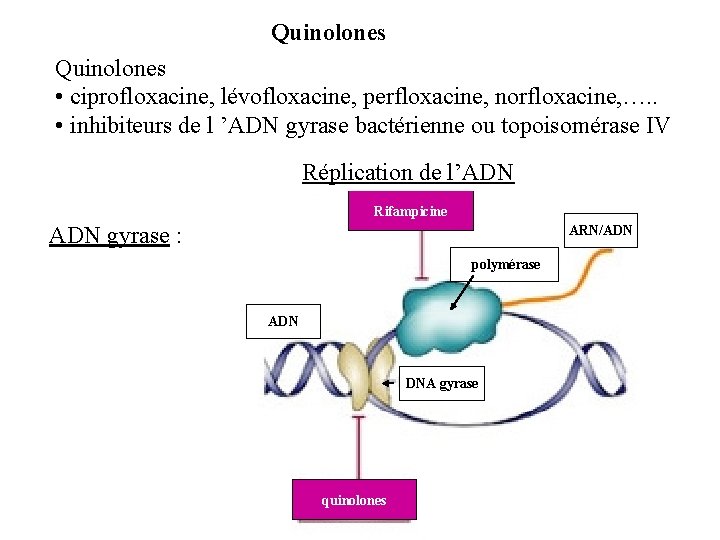
Quinolones • ciprofloxacine, lévofloxacine, perfloxacine, norfloxacine, …. . • inhibiteurs de l ’ADN gyrase bactérienne ou topoisomérase IV Réplication de l’ADN Rifampicine ADN gyrase : ARN/ADN polymérase ADN DNA gyrase quinolones

Les gyrases de l’ADN ou topoisomérase II • catalyse (ATP-dépendant) l’introduction de ‘negative supercoils’ dans l’ADN

Antibiotiques fluoroquinolones Les fluoroquinolones bloquent le fonctionnement de l'ADN gyrase et empêchent la replication de l' ADN bactérien. Une action sur la topoisomérase IV empêche le partage de l'ADN chromosomique repliqué entre les cellules filles.

Antibiotiques: fluoroquinolones La topo-isomérase II, composée chez Escherichia coli d'une sous-unité a et de deux sous-unités ß, coupe les deux brins de DNA pour réduire leur surenroulement et permettre leur séparation, nécessaire à la replication et à la transcription. Cette enzyme assure ensuite la réparation du DNA en position de surenroulement, ce qui rend le DNA beaucoup plus compact à l'intérieur de la cellule. Les quinolones s'intercalent sous forme de complexe de magnésium entre les deux brins du DNA bactérien. Elles empêchent la soudure des brins de DNA dans un état sur-enroulé, et donc la formation de chromosomes à l'état compact. Les différences qui existent entre les chromosomes bactériens et humains sont susceptibles d'expliquer l'absence habituelle d'effet des quinolones, dans les conditions thérapeutiques, sur le fonctionnement du DNA humain alors que le DNA bactérien est perturbé.
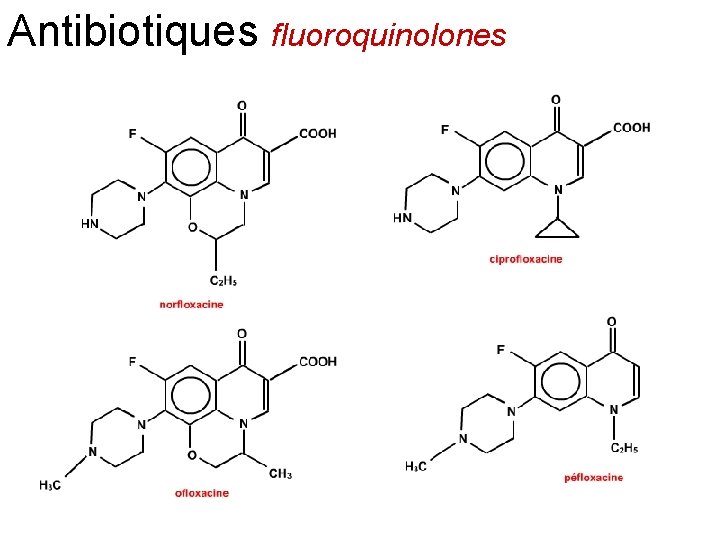
Antibiotiques fluoroquinolones
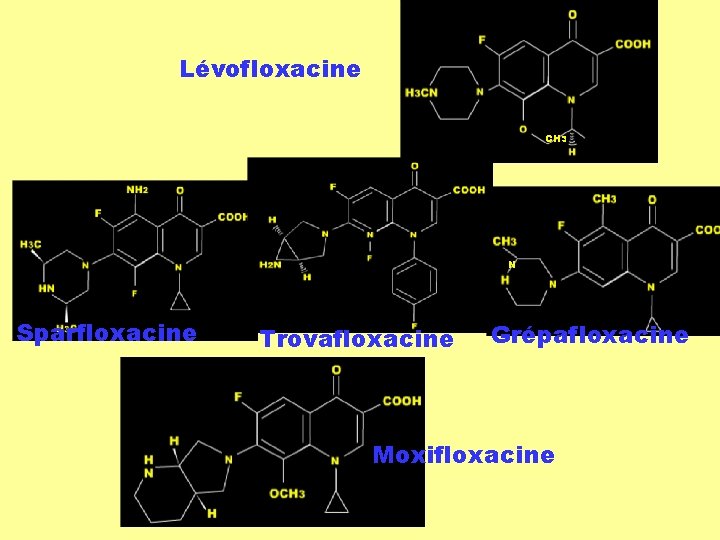
Lévofloxacine CH 3 N Sparfloxacine Trovafloxacine Grépafloxacine Moxifloxacine
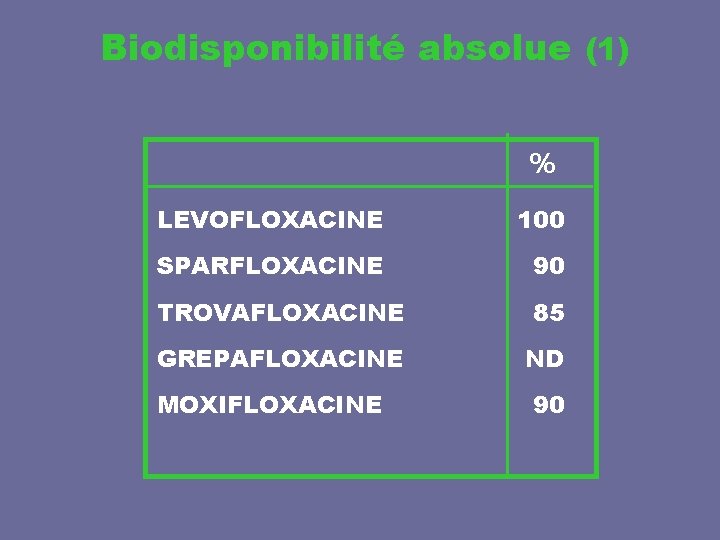
Biodisponibilité absolue (1) % LEVOFLOXACINE 100 SPARFLOXACINE 90 TROVAFLOXACINE 85 GREPAFLOXACINE ND MOXIFLOXACINE 90

Effets de l’alimentation
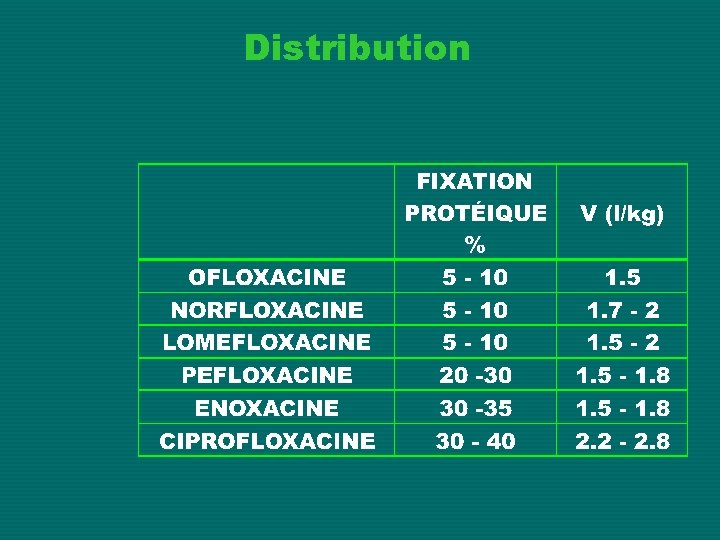
Distribution
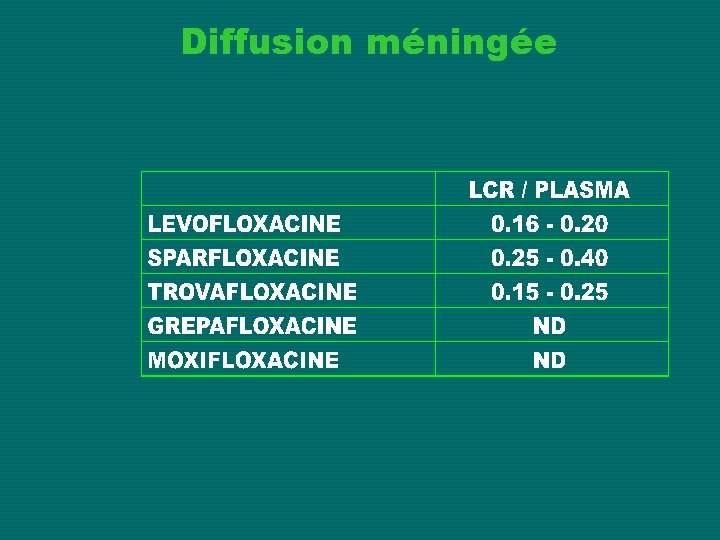
Diffusion méningée
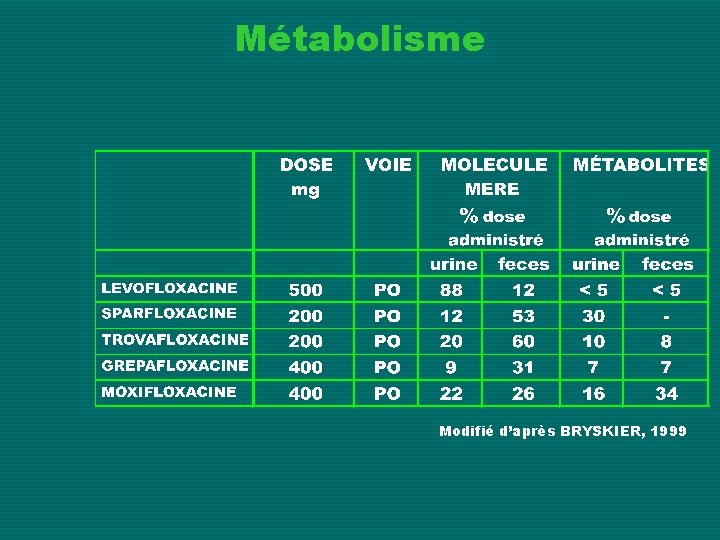
Métabolisme Modifié d’après BRYSKIER, 1999
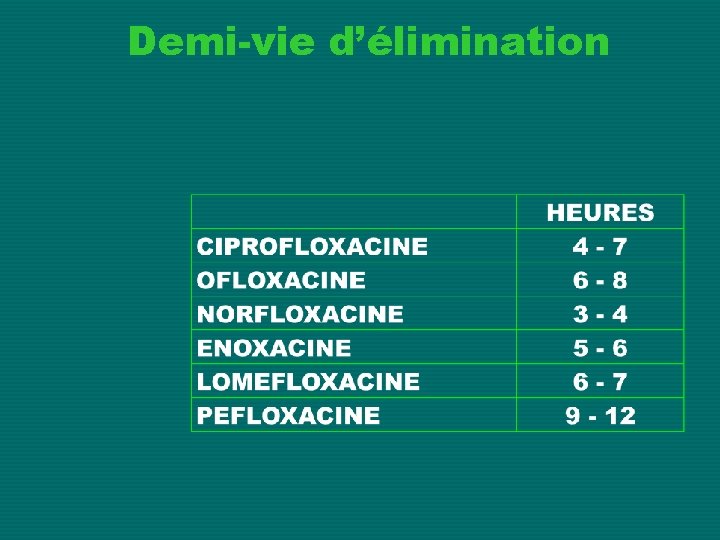
Demi-vie d’élimination

Antibiotiques fluoroquinolones principales indications: infections urinaires avec ou sans pyélo-néphrite. infections génitales (homme femme) gonococcie. infections gastro-intestinales (typhoïde, certaines diarrhées bactériennes). certaines infections ORL: sinusites chroniques et otites chroniques à germe documenté. pneumonies à germe documenté, ou de surinfection, ou nosocomiale. mucoviscidose. légionellose. infections ostéo-articulaires à germe documenté.

Fluoroquinilones Pharmacocinétique: · Bonne biodisponibilité · Large volume de distribution · ½ vie plasmatique: 3 -5 h : ciprofloxacin 10 h : perfloxacine • Elimination rénale, hépatique ou mixte Effects indésirables. · en général : bien tolérées · nausées, céphalées · arthralgies, anomalies du cartilage de croissance · Allongement du QT
- Slides: 84