Antibiotikaresistens ystein Sbstad Konsekvenser av den kte resistensen

Antibiotikaresistens Øystein Søbstad

Konsekvenser av den økte resistensen • Økte kostnader for helsetjenesten • Lengre sykehusopphold og flere • Behandlingssvikt med følgende • Økt antall dødsfall • I USA • > 2 mill personer syke • > 23000 dødsfall • EU > 25. 000 dødsfall med økte kostnader på 1, 5 milliard Euro • Globalt > 350. 000 mill premature dødsfall de neste 35 år.

Historien • Pesten i Aten 430 f. kr. • Den justinianske pesten ca 541 • Div «pester» i historien. Svartedøden • Syfilis • Lepra • Kolera • Gastroenteritter – dysenteri • Tuberkulose
Kolera

Historien – Kampen mot infeksjoner • • • 2000 F. kr Bønn til høyere makter Ulike remedier og tryllekunster. Fra Søramerika Alkaloider fra kinabark ipecacuanhabusken. Paul Ehrlich: Salvarsan , 1909, George Domagks sulfonamider Flemming og penicillin Fra 1940 årene endret forskningstartegi: fremstilling av antibiotika fra jordbakterier og en rekke nye preparater. 1956 Eisenhower til Kongressen: « I hereby declare………» Resistens påvist allerede i 1940 Mindre oppmerksomhet fra på antibiotika fra 70årene og utover 2030 Bønn til høyere makter?
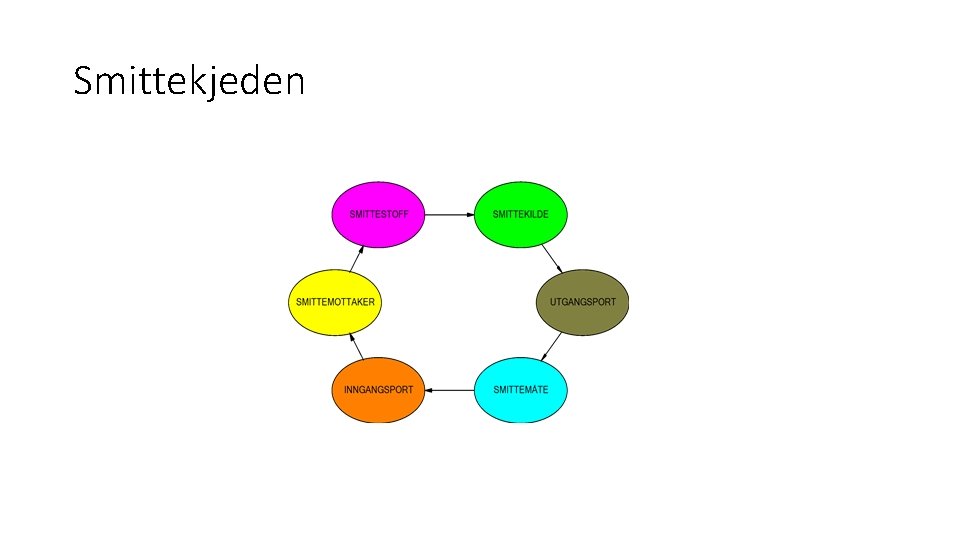
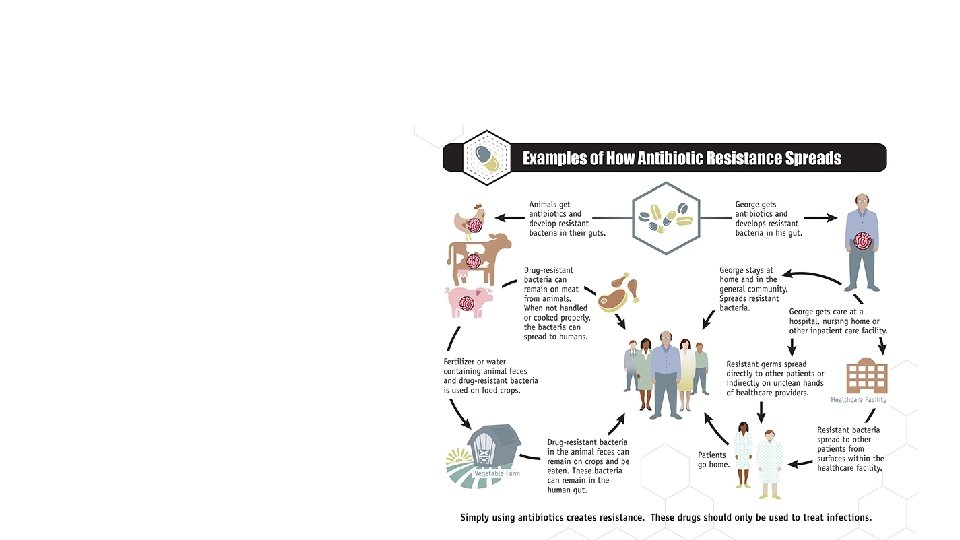
Smittekjeden

Smittestoffene • Bakterier • Sopp • Andre parasitter • Protozooer • Plasmodier • M. fl. • Virus

Antibiotika • Gresk ord anti = mot, bios = liv • I utgangspunktet stoffer produsert av mikroorganismer mot andre mikroorganismer, f. eks. sopp produserer penicillin mot bakterier. Noen bakterier produserer amfotericin mot sopp. • Antiviralia er ikke antibiotika fordi virus ikke kan sies å være «liv» .
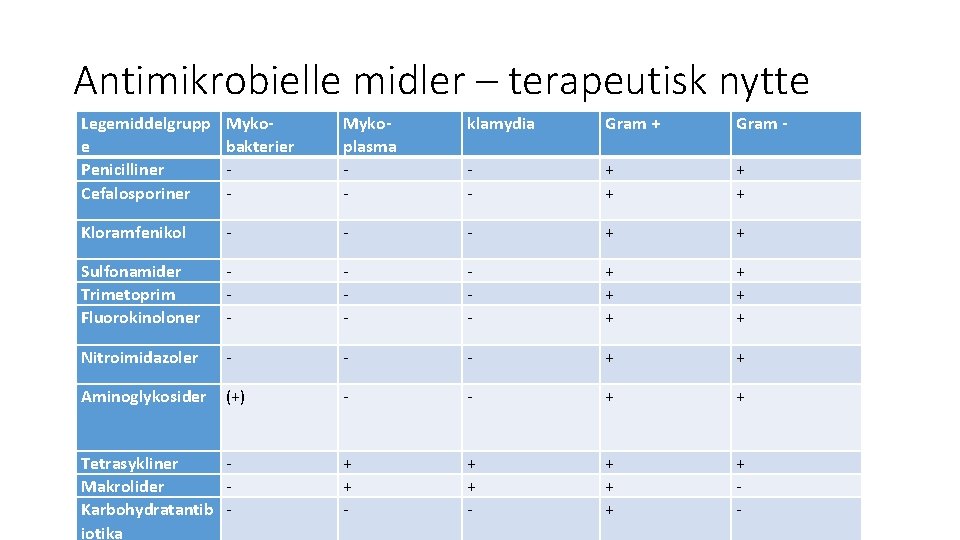
Antimikrobielle midler – terapeutisk nytte Legemiddelgrupp e Penicilliner Cefalosporiner Mykobakterier - Mykoplasma - klamydia Gram + Gram - - + + Kloramfenikol - - - + + Sulfonamider Trimetoprim Fluorokinoloner - - - + + + Nitroimidazoler - - - + + Aminoglykosider (+) - - + + + + - Tetrasykliner Makrolider Karbohydratantib iotika

Om bruk av antibiotika • Antibiotika brukes til behandling av infeksjoner ved å hemme eller ødelegge mikrobene som forårsaker sykdom. Antibiotika omfatter medikamenter som brukes mot bakterier (antibakterielle midler), sopp (antimykotiske midler) og parasitter (antiparasittære midler). Midler som påvirker virus kalles antivirale midler. • Kan brukes terapeutisk eller profylaktisk • Målet for antibiotika er å virke selektivt hemmende eller drepende på den patogene parasitten - et smalspektret middel med bactericid virkning og minst mulig bivirkninger. • Rett indikasjon – rett bruk. • Bredspektret – smalspektret. • Hensyn til klinisk farmakologiske parametre

Hvordan virker antibiotika? Substans virkningsmekanisme • Penicillin • Bactericid ved åhemme bakterienescelleveggsyntese • Bakteriocid/bakteriostatisk Bindes til ribosomer hemmer proteinsyntesen. • Bakteriostatisk. Hemmer proteinsyntesen • Bact. cid mot Begge former for tb hemmer RNA syntesen • Makrolider • Tetrasyklin • Rifampicin

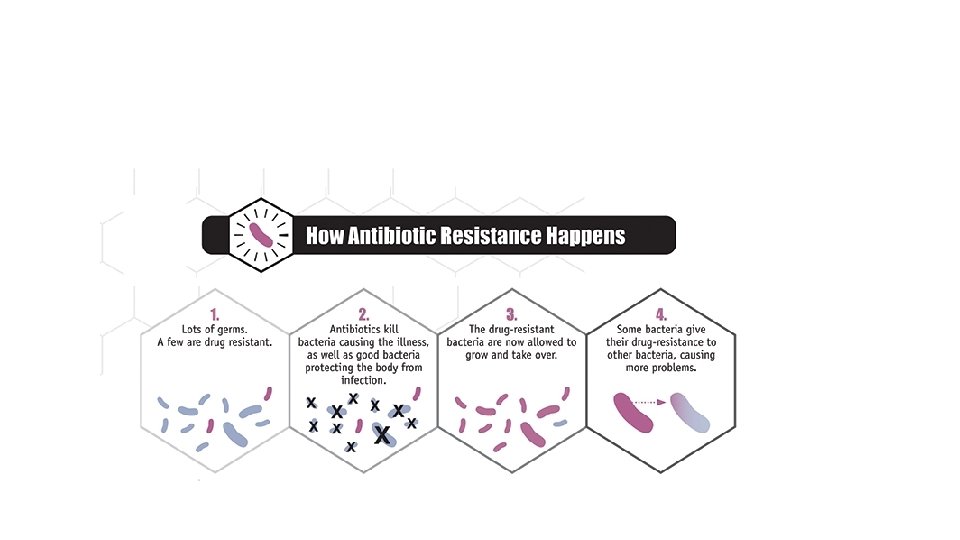
Resistens • Antibiotikaresistens innebærer at bakterier kan leve videre og formere seg selv om de utsettes for antibiotika. • Enkelte bakterier har en naturlig resistens • Andre utvikler resistens - ervervet resistens • Bakterier kan ha eller utvikle resistens mot to eller flere antibiotika og kalles da multiresistent

Måle antibiotikas effektivitet.

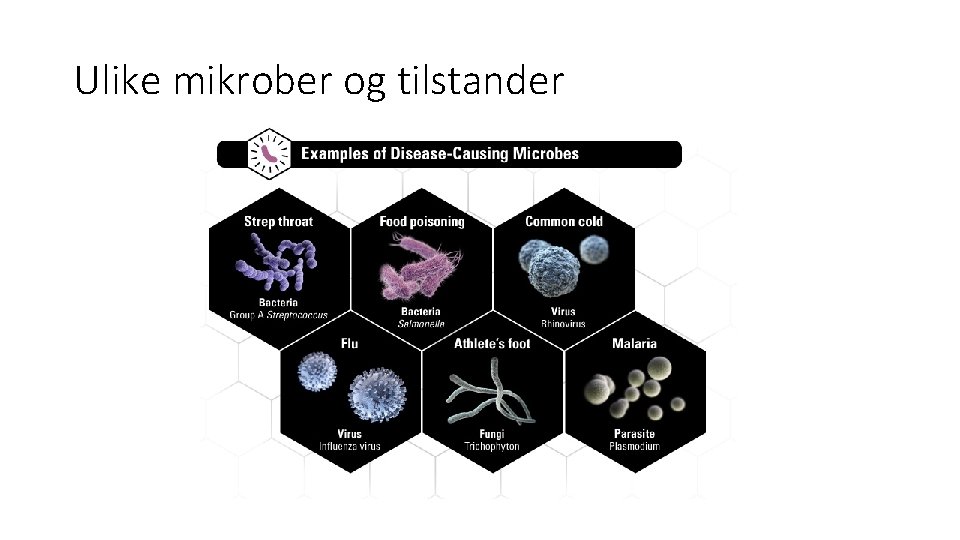
Ulike mikrober og tilstander
Bakterier med kjent resistens • Karbapenemresistent Enterobacteriaceae • Multiresistent Acinetobacter

Alvorlig resistens • Fluconazolresistens candiada albicans • Extended Spectrum Beta. Lactamase produserende Enterobacteriaceae (ESBL)

VRE – lokalt velkjent. • Vancomycinresistenterokokker • Candida albicans


Hvordan erverves resistens? • Med antibiotikaresistens menes en mikrobes evne til å motstå virkningen av antibiotika. Det kan bety at bruken av antibiotika ikke vil ha den ønskete kliniske effekt, og det kan få konsekvenser både for den enkelte pasient, helsetjenesten og samfunnet • Endringer i arvestoffet (DNA); såkalte mutasjoner. Slike mutasjoner kan oppstå når antibiotika spres i miljøet og påvirker bakterier. • Å hente resistensgener fra andre bakterier. Dette kalles horisontal genoverføring. For eksempel kan såkalte mobile genetiske elementer med resistensgener overføres mellom bakterier. • Slike endringer kan skje i bakteriene hos den enkelte som bruker antibiotika, og i bakterier i miljø som utsettes for antibiotika.

Resistensmekanismer • Enzymatisk ødeleggelse av det antibiotiske middelet • Endring av bakteriestrukturen slik at a. b. ikke lenger kan binde seg ( opptak av arvestoff med påfølgende endring av målmolekyl i bakterien. ) • Noen bakterier kan hindre at det antibakterielle middelet når fram til målmolekylet inne i bakteriecellen
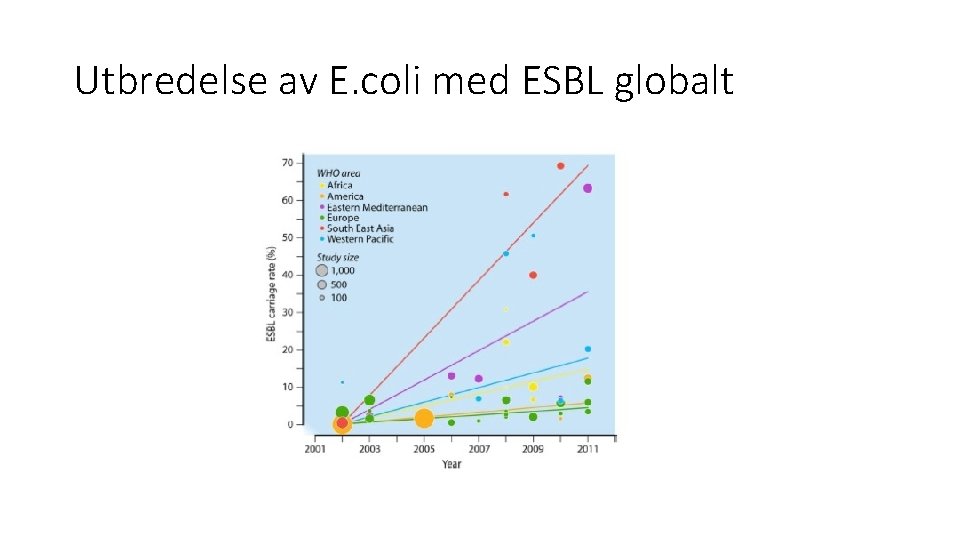
Utbredelse av E. coli med ESBL globalt

Aktuelle bakterier • Problemene med antibiotikaresistens er ofte knyttet til noen viktige bakteriearter (penicillinresistens hos Streptococcus pneumoniae (pneumokokker), meticillin-resistens hos gule stafylokokker (MRSA), vankomycin-resistens hos enterokokker (VRE), resistens mot bredspektrede betalaktamer (ESBL), aminoglykosider og fluorokinoloner hos enterobakterier (E. coli, Klebsiella etc. ). • Utviklingen de siste årene har særlig vært bekymringsfull hos enterobakteriene • En nylig publisert oversiktsartikkel (Woerther et al. , 2013) viser at det i enkelte studier i Asia er funnet ESBLpositive E. coli i tarmflora hos 30 -70% av personene som ble undersøkt. Tilsvarende tall for Europa er 5 -10%. Hos personer som har vært på turistreise til Midtøsten eller Syd-øst Asia finner man ofte at 30 -50% er friske bærere ved hjemkomst
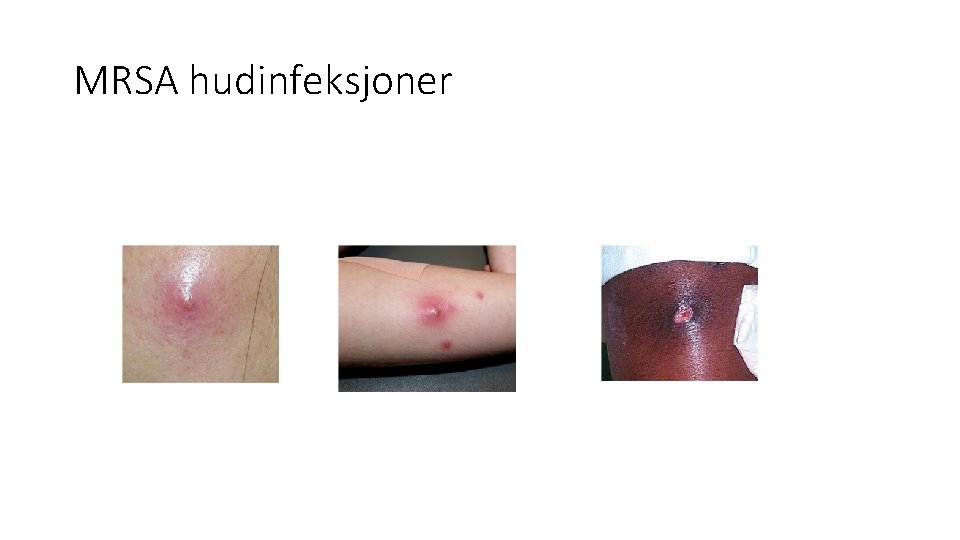
MRSA hudinfeksjoner

Risikofaktorer for MRSA • MRSA skal ikke etablere seg og bli en fast del av bakteriefloraen ved norske sykehus og sykehjem • Kronisk hudsykdom • Sår • Proteser • Immunsvikt • Diabetes
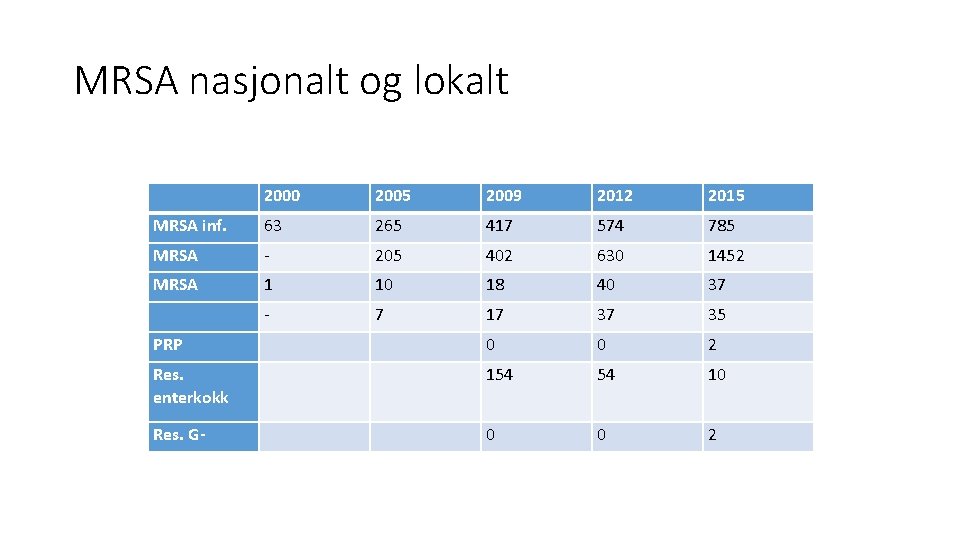
MRSA nasjonalt og lokalt 2000 2005 2009 2012 2015 MRSA inf. 63 265 417 574 785 MRSA - 205 402 630 1452 MRSA 1 10 18 40 37 - 7 17 37 35 PRP 0 0 2 Res. enterkokk 154 54 10 Res. G- 0 0 2
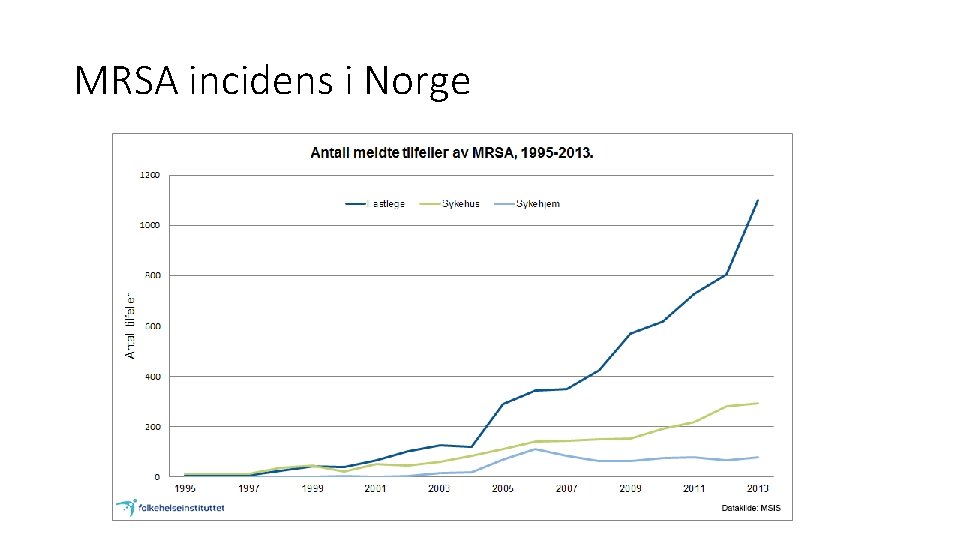
MRSA incidens i Norge

Ca-MRSA • Overføres i samfunnet utenfor helseinstitusjoner • Oppdaget i Chicago 1998 blant skoleelever • Ulike andre Staf. Aureus stammer • Genetisk mer pussproduserende • Medfører økt antall hudinfeksjoner med staf. Aur.

Risikofaktorer for ca-MRSA • Fattigdom • Fedme • Sosiale minoriteter • Flyktninger bl. a. flyktningeleire. • Kontaktsport. • Bringes hjem etter utenlandsreiser etter kontakt med lokalbefolkningen
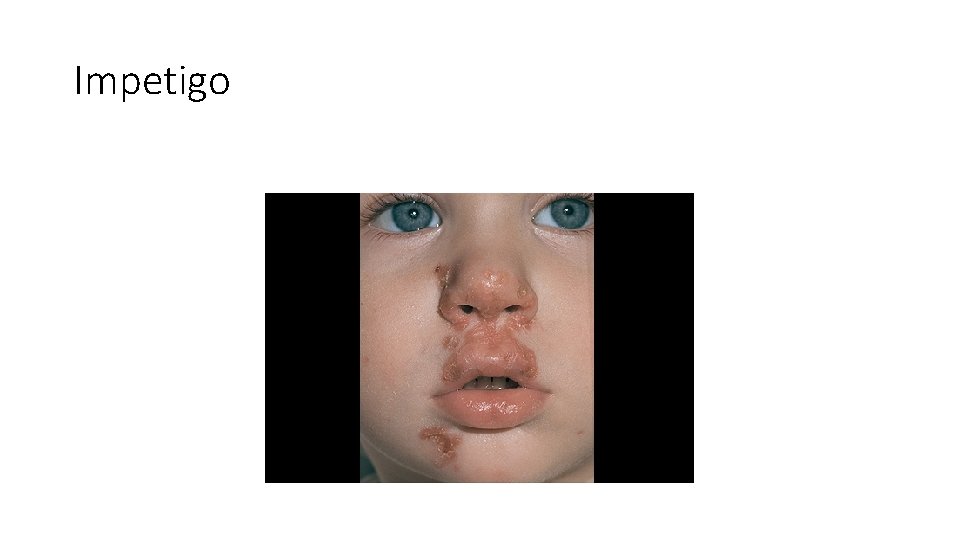
Impetigo

LA-MRSA • Norge ble LA-MRSA (CC 398) påvist i prøver fra griser første gang i 2011 • I 2013 har det imidlertid vært to geografisk atskilte utbrudd av LAMRSA i norske svinebesetninger, som begge inkluderer flere besetninger. Det er også påvist smitte til flere personer som har hatt kontakt med disse besetningene. • Det er pr juni 2014 påvist LA-MRSA smitte til 30 personer i dette utbruddet, og den samme varianten er påvist i 24 svinebesetninger. Det anses mest sannsynlig at smitten har kommet inn via MRSAinfiserte gjestearbeidere.
CDC - Strategier

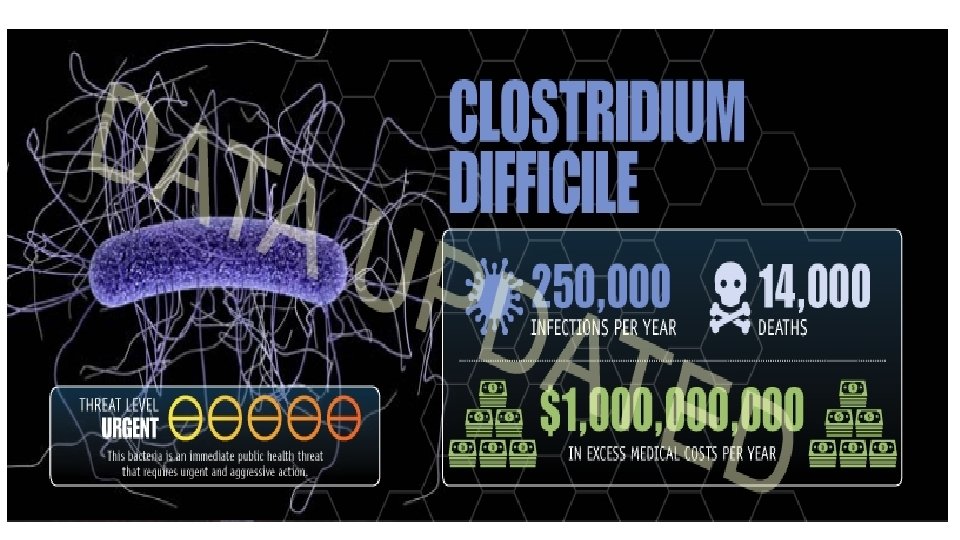
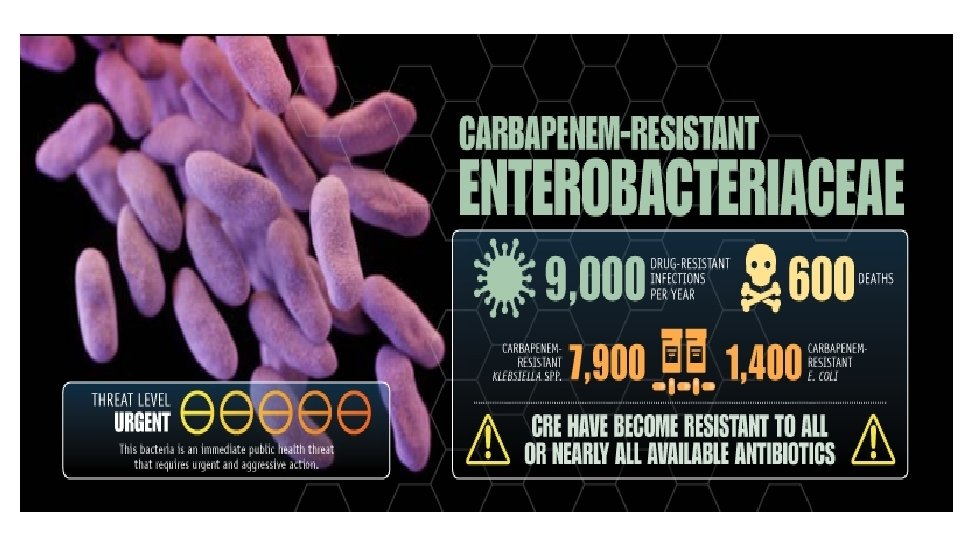
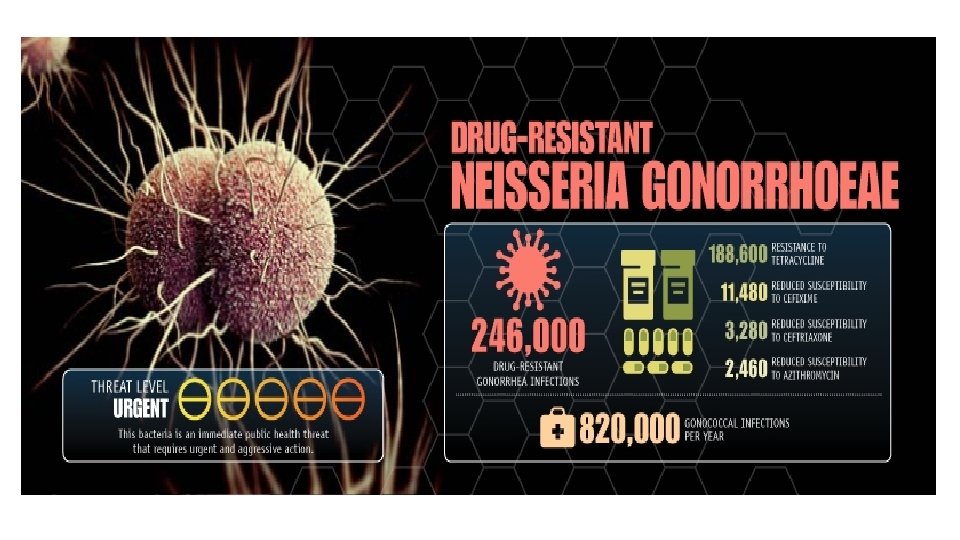

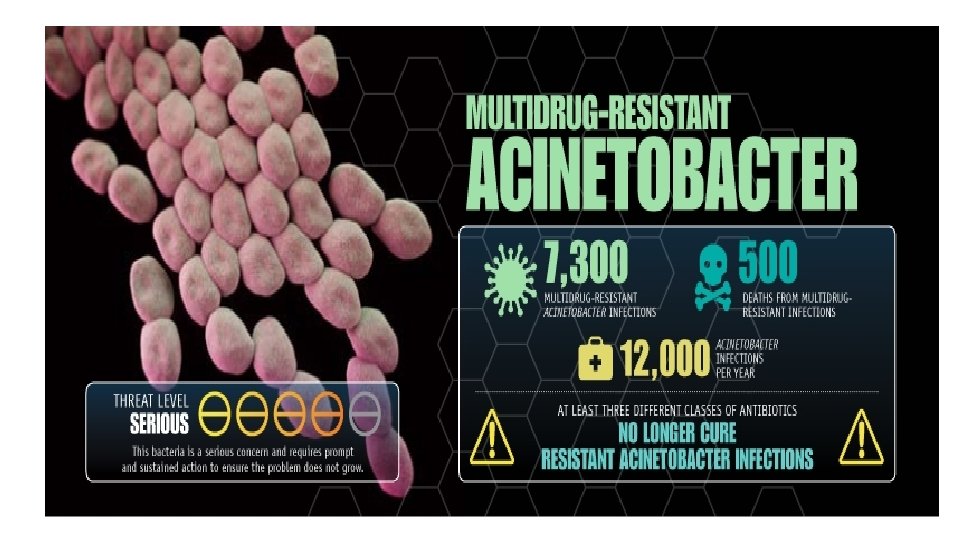

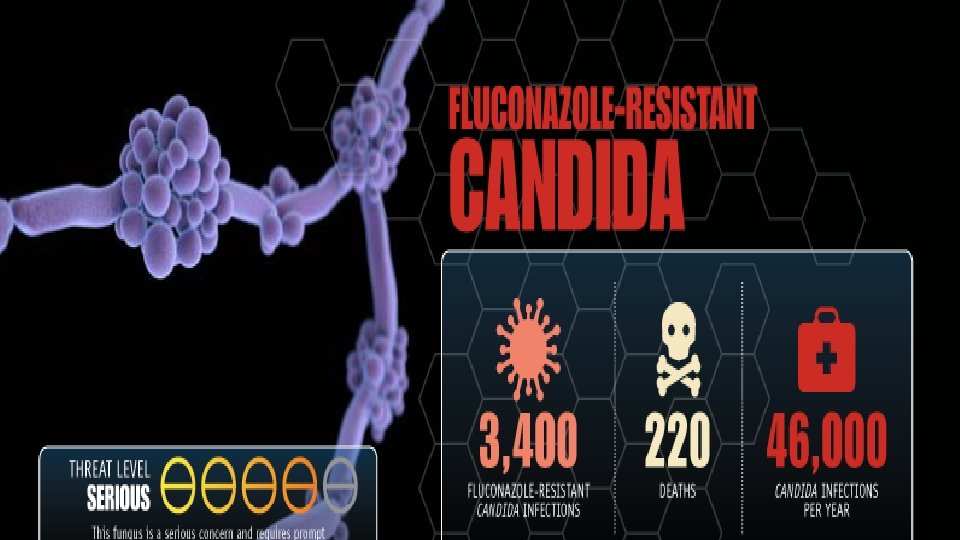
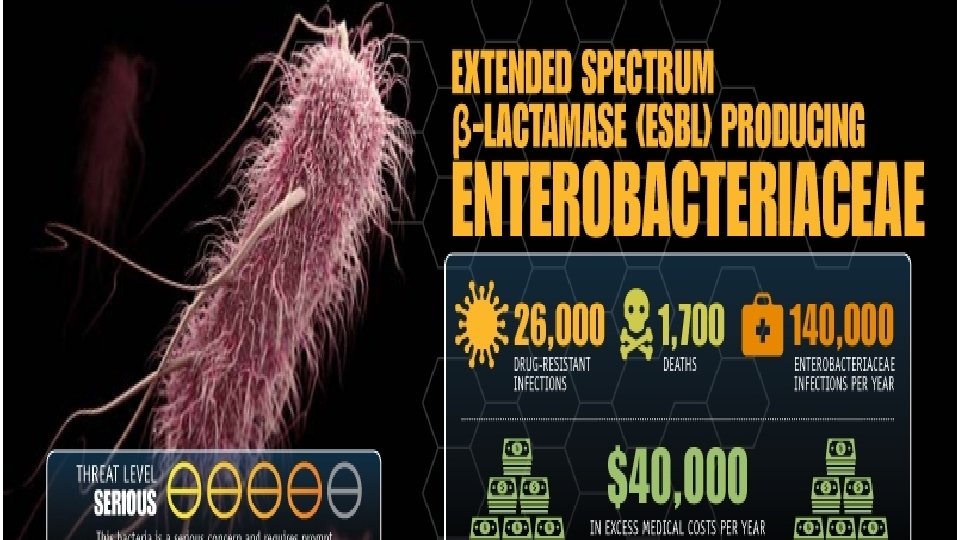

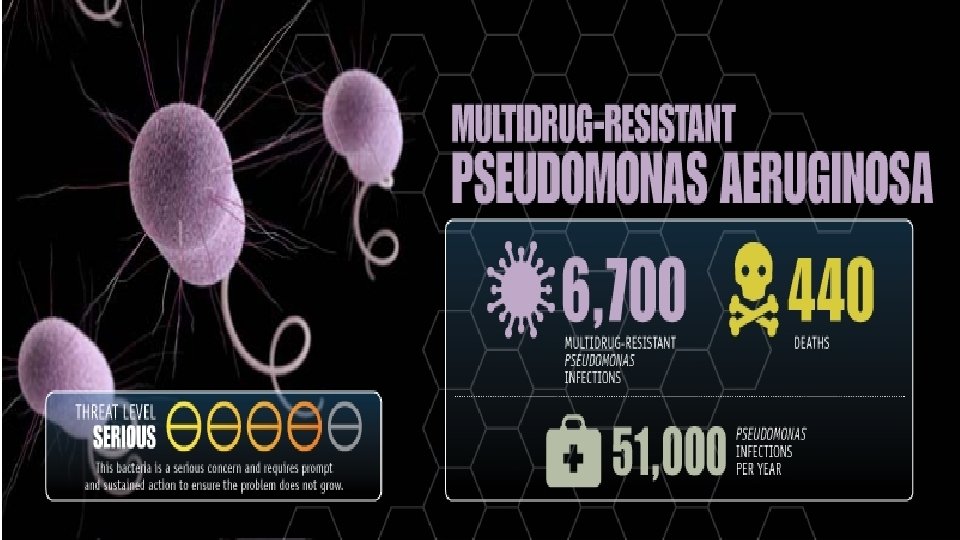
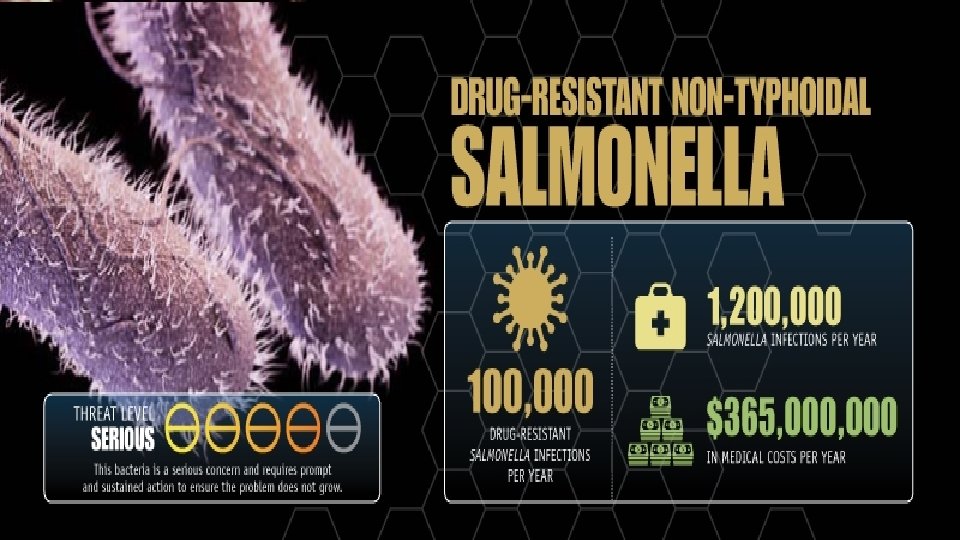
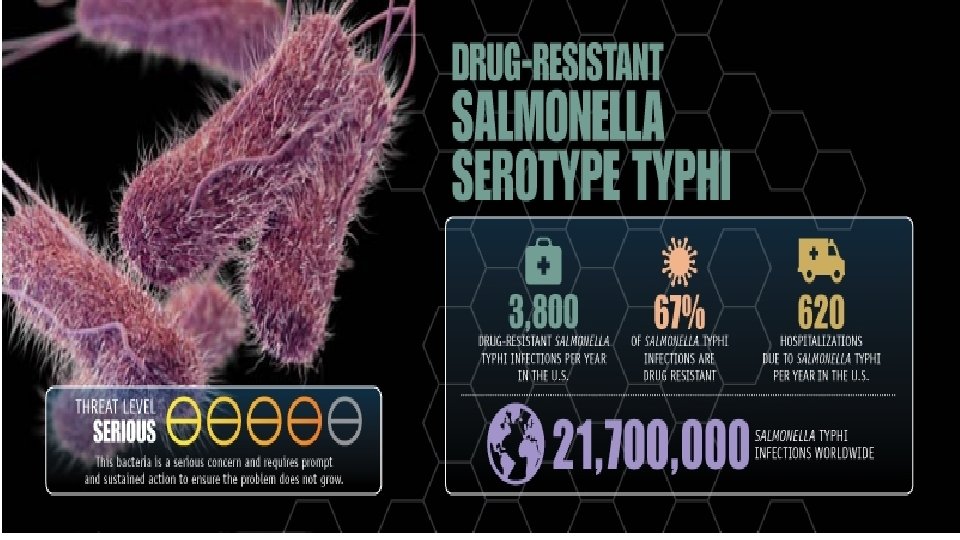





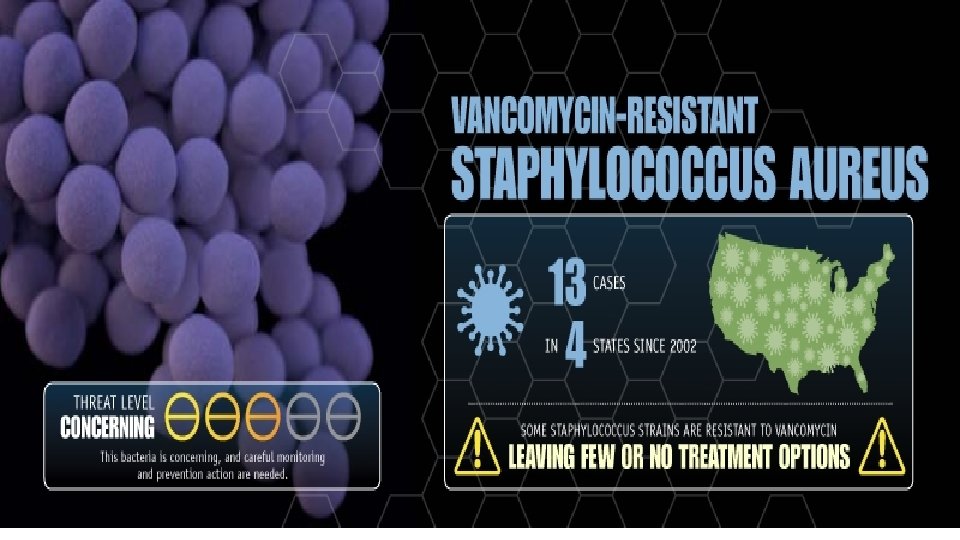
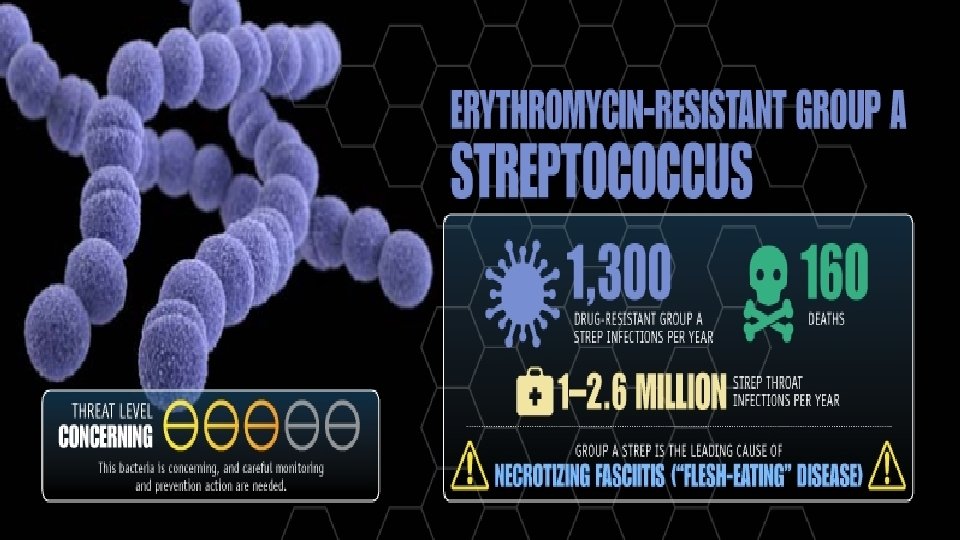

Kjerneoppgaver for å hindre resistensutvikling • Forebygge infeksjoner • Hindre spredning av resistens • Smitteoppsporing • Veiledning i forskrivning av antibiotika • Utvikle nye diagnostiske prøver • Utvikle nye behandlingsmidler.

Nasjonal strategi mot antibiotikaresistens 2015 -2020 • Overordnede mål • 1. Redusere den totale bruken av antibiotika. • 2. Riktigere bruk av antibiotika. • 3. Økt kunnskap om hva som driver utvikling og spredning av antibiotikaresistens. • 4. Være en pådriver i internasjonalt, normativt arbeid for å styrke tilgang, ansvarlig bruk og utvikling av nye antibiotika, vaksiner og bedre diagnostiske hjelpemidler.

Sektorspesifikke mål - helse 1. Antibiotikabruken i befolkningen er redusert med 30 prosent målt i DDD 7 /1000 innb/døgn sammenlignet med 2012. 2. Norge er blant de tre landene i Europa som bruker minst antibiotika til mennesker, målt i DDD/1000 innbyggere/døgn. 3. Gjennomsnittlig forskrivning av antibiotika er redusert fra dagens 450 resepter til 250 resepter per 1000 innbyggere per år. 4. Forskrivningen av antibiotika ved luftveisinfeksjoner er redusert med 20 prosent målt i DDD /1000 innb/døgn sammenlignet med 2012. 5. Det er gjennomført studier av sykdomsbyrde ved antibiotikaresistens, konsekvenser av eventuelt for lavt antibiotikabruk og effekt av smitteverntiltak

Matproduserende landdyr og kjæledyr 1. Det er utarbeidet oversikt over oppsamlingssteder for antibiotikaresistente bakterier i de mest relevante dyrepopulasjonene og planter av betydning for mattryggheten. 2. 2. LA-MRSA 8 er ikke etablert i norsk svinehold. 3. Forekomsten av ESBL 9 i norske fjørfebesetninger er redusert til et minimum. 4. Forbruket av antibiotika til matproduserende landdyr er redusert med minst 10 prosent sammenlignet med forbruket i 2013. 5. Forbruket av antibiotika til kjæledyr er redusert med minst 30 prosent sammenlignet med forbruket i 2013. 6. Narasin og andre koksidiostatika med antibakteriell virkning er faset ut av kyllingproduksjonen forutsatt at dette ikke går utover dyrehelse og dyrevelferd eller øker bruken av antibiotika til behandling.
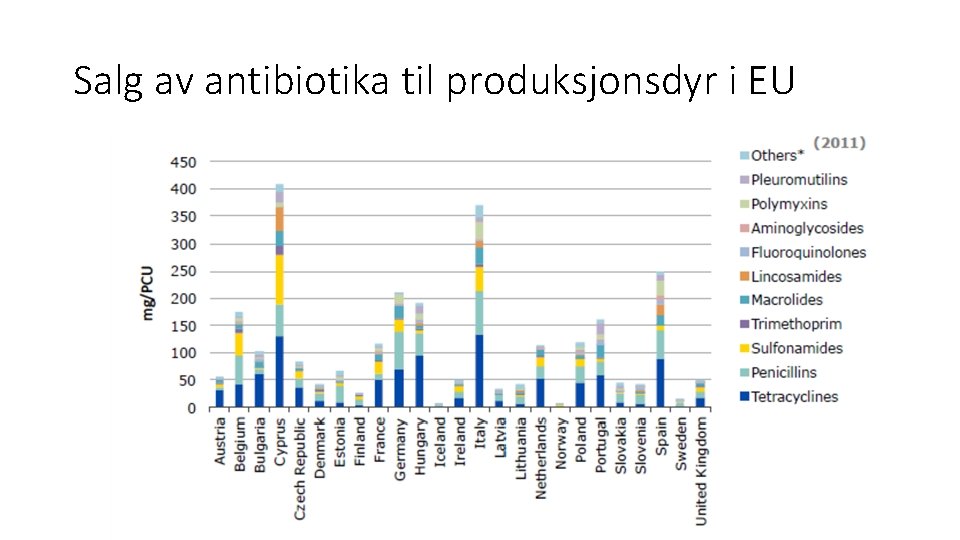
Salg av antibiotika til produksjonsdyr i EU

Fisk 1. Totalbruken av antibiotika i fiskeoppdrett er i 2020 på samme nivå eller lavere enn for perioden 2004 - 2014, målt i antall kilo antibiotika.

Klima og miljø 1. En kartlegging av antibiotikaresistente bakterier er gjennomført i representative miljøer og på utvalgte organismer av dyr, vann og jord med ulik grad av eksponering for antibiotika. 2. Det er initiert studier for å undersøke effekten av andre resistensdrivere enn antibiotika i naturen, deriblant desinfeksjonsmidler, biocider og tungmetaller.
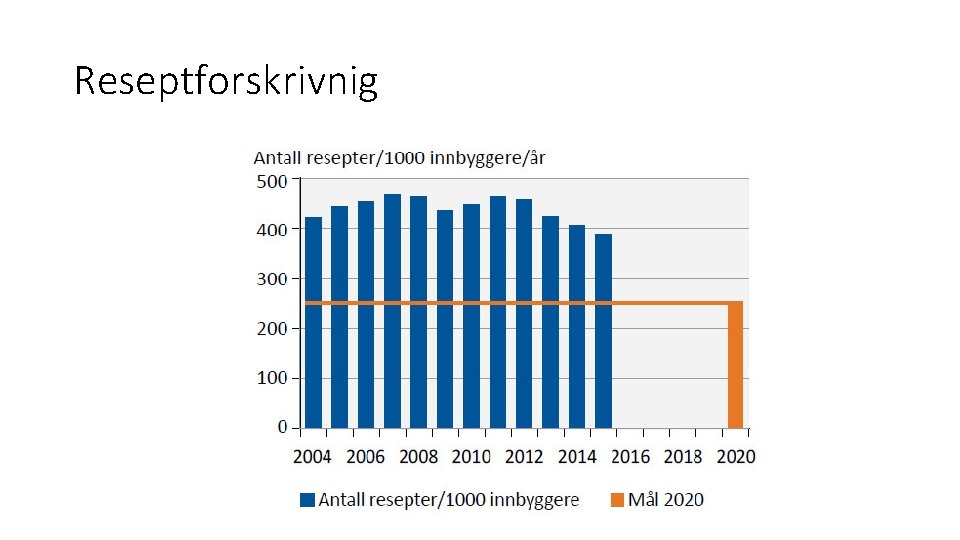
Reseptforskrivnig
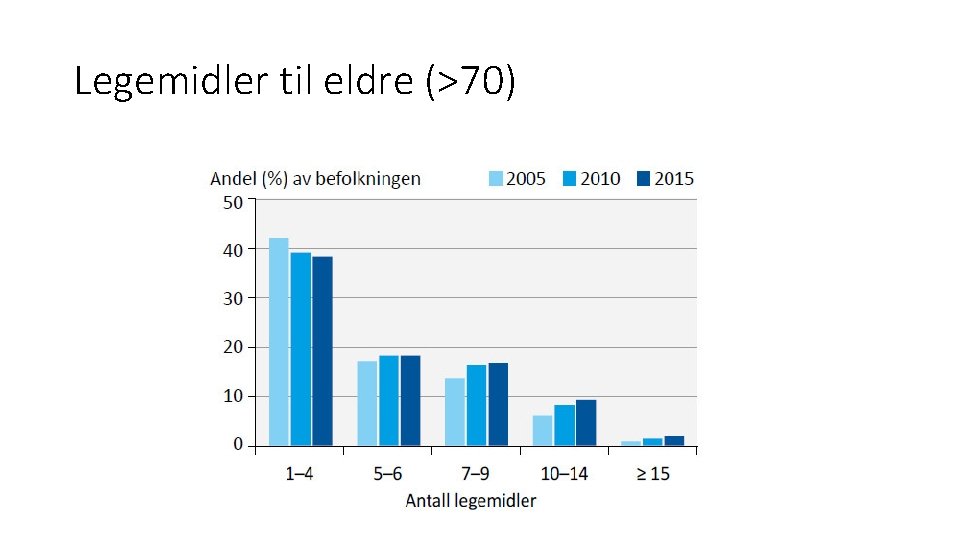
Legemidler til eldre (>70)
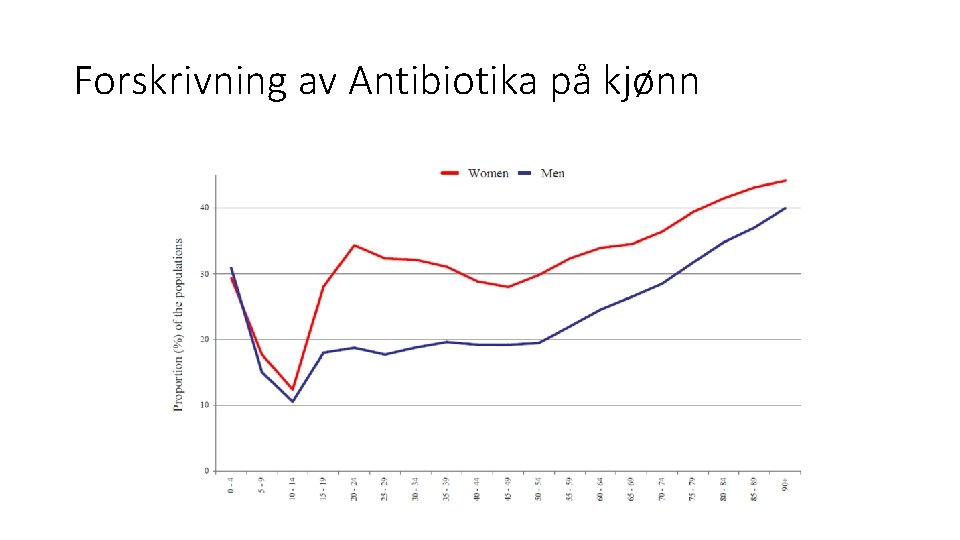
Forskrivning av Antibiotika på kjønn
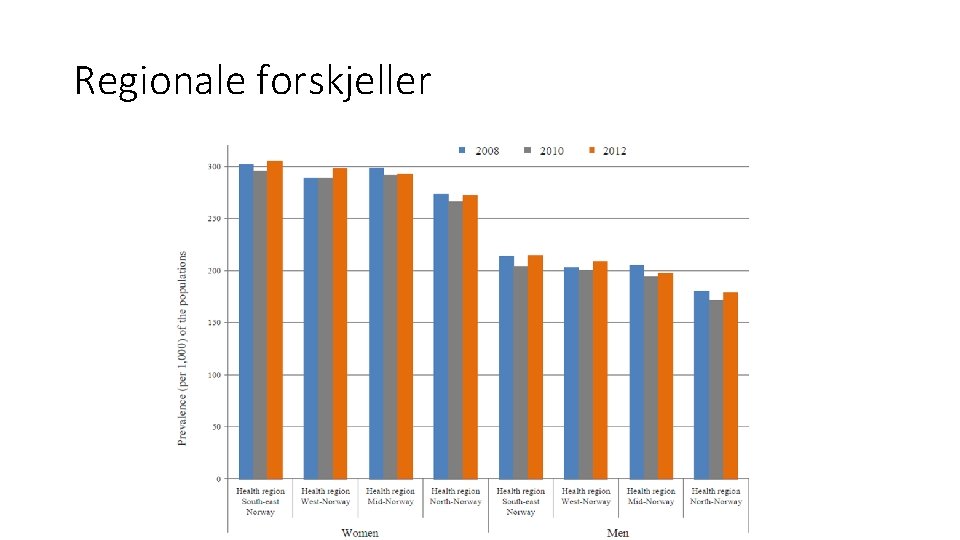
Regionale forskjeller

Tilbake til forebygging • Forebyggingens paradoks • På pasientnivå • • Kunnskap og holdninger Hygiene Pasientadferd Vaksinasjon? ? • På behandlernivå • • Kunnskap og holdninger Rask og sikker diagnostikk Rett antibiotikabruk i rette mengder Kontroller?

Forskrivningsmål o. a. mål • • • Redusere a. b. i befolkningen med 30% i DDD/1000 i f. t. 2012 Norge skal være blant de tre beste i Europa m. h. t. a. b. forskrivn. Redusere fra 450 til 280 rp pr 1000/år Kartlegge sykd. Byrde v resistens som følge av a. b. bruk og smitteverntiltak A. b. skal ikke ha neg. Effekt i befolkningen Forebygge hvor mulig i stedet for å behandle. Bruke a. b. på rett måte Forskrivere – befolkning- IT-løsninger Friske bærere Vaksiner.

Dagens situasjon • Internasjonalt har man sett en akselererende økning av forekomsten av resistente, sykdomsfremkallende mikrober hos dyr og mennesker. • Blant land som overvåker MRSA, har Norge sammen med Island den laveste forekomsten i verden. • I de fleste andre land i Europa er andelen MRSA av blodkulturisolater med S. aureus over 20%, i andre verdensdeler ofte over 50%, mens i Norge er andelen under 1%. • Økt reisevirksomhet – og da særlig økt kontakt med utenlandske sykehus for helsearbeidere og pasienter – øker smittepresset mot Norge og norske helseinstitusjoner.

Dagens situasjon forts. • Det foregår trolig en betydelig og kontinuerlig utveksling av mikrobeflora mellom ulike økologiske nisjer, men man er de senere år i enda større grad blitt oppmerksom på at det totale økosystemet sannsynligvis er svært viktig for spredning av antibiotkaresistens. • Bruk av antibiotika til mennesker og dyr vil dessuten påvirke mikrobefloraen utenfor det syke individ ved at fortsatt aktiv substans lekker til det ytre miljø via avrenning og kloakk. • Bruk av antibakterielle midler gir grunnlag for positiv seleksjon av resistens og er regnet som hovedårsak til utviklingen og økningen av andel av resistens i mange bakteriepopulasjoner de siste 70 årene • Også andre stoffer, som tungmetaller, plantevernmidler, desinfeksjonsmidler og noen farmasøytiske midler og stoffer i kosmetikk kan via sammenfallende seleksjon (ko-seleksjon) bidra til spredning og opprettholdelse av resistens

Utfordringer • Det er kunnskapshull knyttet til forståelsen av slike kostnader for bakteriene, og hvordan disse kan kvantifiseres og hvordan de påvirkes av kompensatoriske mutasjoner. Slik forståelse er nødvendig for å kunne forutsi i hvilken grad ervervet resistens er reversibel • Kunnskap om populasjonsstrukturen til mikrober er sentralt også med hensyn på forståelsen av mulige ”utvaskingseffekter” hvor repetert tilførsel av konkurrerende bakteriepopulasjoner, f. eks som fôrtilskudd til husdyr, påvirker etablerte resistente populasjoner. • Systematisk overvåkning av antibiotikaresistens ble startet i 2000 med etablering av NORM og NORM-Vet. • Ekspertgruppen har ikke løsning på AMR-problemet, men påpeker at bedre oversikt over problemets reelle størrelse er en forutsetning for tiltak som kan begrense videre utvikling av antibiotikaresistens

Anbefaling fra odontologiske læresteder • Basale smittevernrutiner er tilstrekkelig der det ikke foreligger akutt infeksjon forårsaket av MRSA. • Ved kjent bærerskap av MRSA kan det vurderes å behandle pasienten på slutten av dagen. • Kirurgiske operasjonsenheter må ha retningslinjer for å håndtere pasienter med kjent MRSAbærerskap eller pasienter som har hatt sykehusopphold utenlands de siste 12 måneder, og som ikke er undersøkt for mulig MRSA-bærerskap. • Pasienter med økt sekresjon fra MRSA-infiserte sår bør, om mulig, utsette behandling som ikke er akutt.

Risikopasienter - Spørsmål til pasienter før behandling ved norske sykehus: Har du tidligere fått påvist MRSA, eller har du i løpet av de siste 12 måneder: - fått behandling i sykehus eller annen behandlingsinstitusjon utenfor Norge? – fått tannlegebehandling utenfor Norge? – arbeidet ved sykehus eller legekontor utenfor Norge? – arbeidet eller vært i barnehjem eller flyktningleir utenfor Norge? – arbeidet ved sykehus, sykehjem eller andre institusjoner med utbrudd av MRSA? – hatt nær kontakt med personer smittet av MRSA uten beskyttelsesutstyr? – vært mer enn 6 uker sammenhengende i land utenfor Norge OG har – hud- eller andre sårinfeksjoner - kroniske hudlidelser eller – innlagt medisinsk utstyr (venekanyle, urinkateter, o. l. ) gjennom hud/slimhinner? – fått utført tatovering eller piercing i utlandet

Hvis du svarer ja på et eller fler av spørsmålene ta kontakt med din fastlege for å ta en MRSA-test - fastlegen sender kopi av svaret - dersom testen er negativ møter du til timen som avtalt – - dersom du får påvist MRSA, ber vi deg kontakte sykehuset i god tid før oppsatt ti

Ekspertkomiteens 8 anbefalinger 1. Mer kunnskap om antibiotikaresistens i ulike miljøer, spesielt i tarm hos mennesker og dyr, i jord og hav. 2. Bedre overvåking av resistente mikrober i matvarer produsert nasjonalt og internasjonalt. 3. Smittevern i vid forstand. Mennesker og dyr, gjødsel, strukturendringer i norsk landbruk 4. Vaksiner til mennesker, dyr og fisk 5. Bedre diagnostiske hjelpemidler 6. Ansvarlig bruk, forskrivning av antibiotika 7. Bedre oversikt over kostnader ved manglende kontroll av resistensproblemene. 8. Resistens er et globalt problem. Derfor nødvendig med nasjonalt og internasjonalt samarbeid.

Fremtiden ? ?

Nettadresser • https: //www. regjeringen. no/no/dokumenter/nasjonal-strategi-motantibiotikaresistens • https: //www. regjeringen. no/contentassets/915655269 bc 04 a 47928 fc e 917 e 4 b 25 f 5/handlingsplan-antibiotikaresistens. pdf • https: //www. regjeringen. no/no/aktuelt/mindre-og-riktigere-bruk-avantibiotika/id 2424608/ • https: //www. fhi. no/sv/antibiotikaresistens/ • www. CDC. gov • http: //ecdc. europa. eu/en/Pages/home. aspx

Takk for oppmerksomheten!
- Slides: 78