Antibiothrapie raisonne Lapproche PKPD et les recommandations actuelles

Antibiothérapie raisonnée L’approche PK/PD et les recommandations actuelles A Bousquet-Mélou Ecole Nationale Vétérinaire de Toulouse Oniris – Nantes – 25 Octobre 2016

Antibiothérapie raisonnée : quels objectifs ? 1. Efficacité maximale contre les bactéries pathogènes 2. Minimiser l’émergence et la sélection des résistances bactériennes – Pour les pathogènes cibles : enjeux d’efficacité / santé animale – Pour les bactéries non cibles: enjeux de santé humaine • Bactéries zoonotiques • Flores commensales des animaux (réservoirs de gènes de résistance)

Comment déterminer un schéma posologique ?
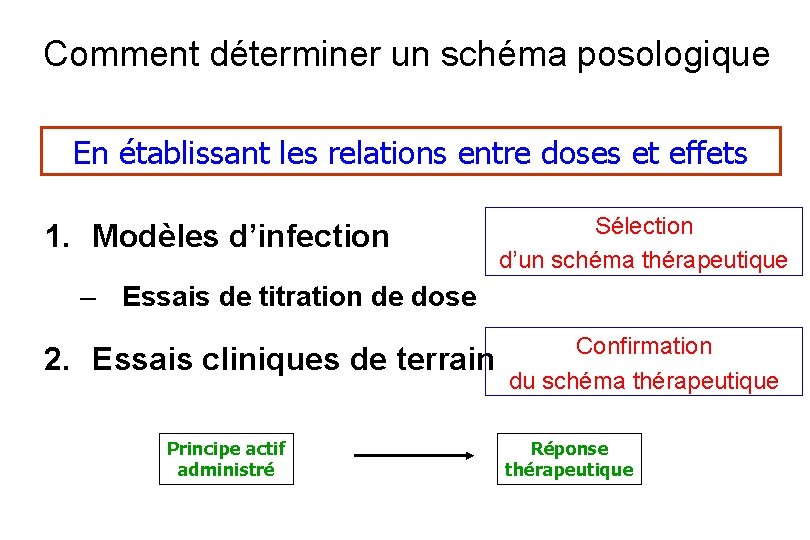
Comment déterminer un schéma posologique En établissant les relations entre doses et effets 1. Modèles d’infection Sélection d’un schéma thérapeutique – Essais de titration de dose 2. Essais cliniques de terrain Principe actif administré Confirmation du schéma thérapeutique Réponse thérapeutique

Comment déterminer un schéma posologique En établissant les relations entre doses et effets 1. Modèles d’infection – Essais de titration de dose 2. Essais cliniques de terrain 3. Approche PK/PD
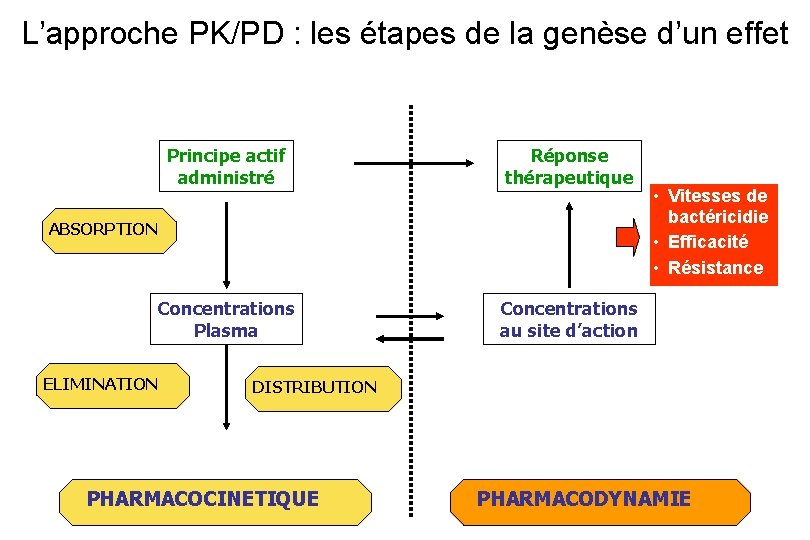
L’approche PK/PD : les étapes de la genèse d’un effet Principe actif administré Réponse thérapeutique Concentrations Plasma Concentrations au site d’action ABSORPTION ELIMINATION • Vitesses de bactéricidie • Efficacité • Résistance DISTRIBUTION PHARMACOCINETIQUE PHARMACODYNAMIE
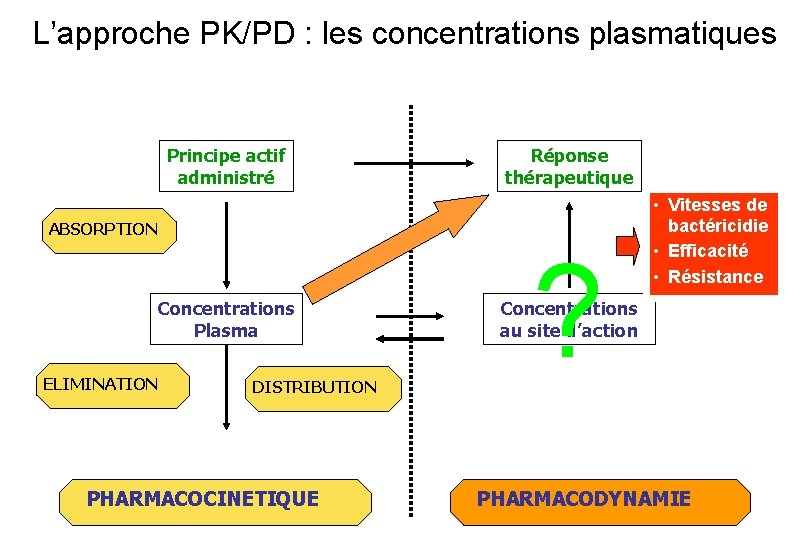
L’approche PK/PD : les concentrations plasmatiques Principe actif administré Réponse thérapeutique ABSORPTION Concentrations Plasma ELIMINATION DISTRIBUTION PHARMACOCINETIQUE ? • Vitesses de bactéricidie • Efficacité • Résistance Concentrations au site d’action PHARMACODYNAMIE
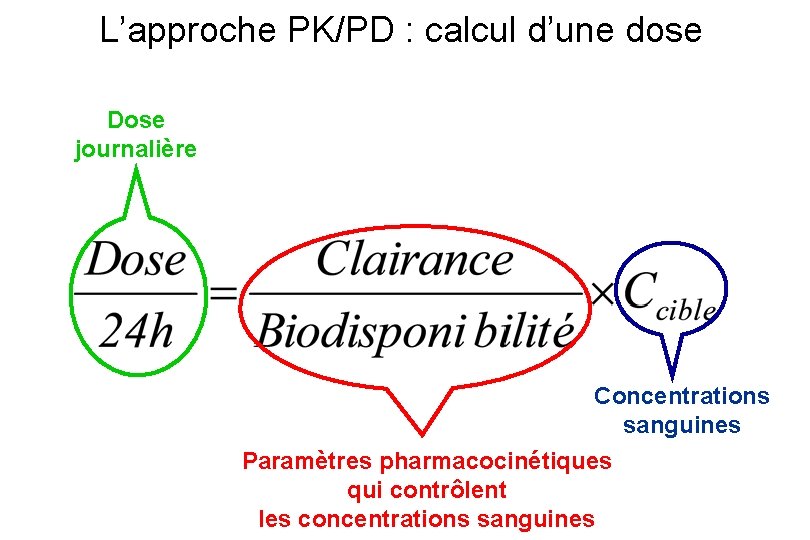
L’approche PK/PD : calcul d’une dose Dose journalière Concentrations sanguines Paramètres pharmacocinétiques qui contrôlent les concentrations sanguines

L’approche PK/PD : calcul d’une dose La clairance click

Pourquoi les concentrations plasmatiques ? • Parce que c’est facile à mesurer • Mais est-ce pertinent ?

Où sont localisés les pathogènes ? • 3 localisations possibles des pathogènes Extracellulaires Streptococcus pneumoniae Escherichia coli Klebsiella pneumoniae Mannheimia haemolytica Pasteurella multocida Actinobacillus pleuropneumoniae Mycoplasma hyopneumoniae Bordetella bronchiseptica Intracellulaires (obligatoires) Chlamydiae Rickettsia Brucella Lawsonia intracellularis (enterite proliferative du porc) Intracellulaire (facultatifs) Staphylococcus aureus Salmonella typhi Listeria Mycobacterium tuberculosis Streptococcus suis
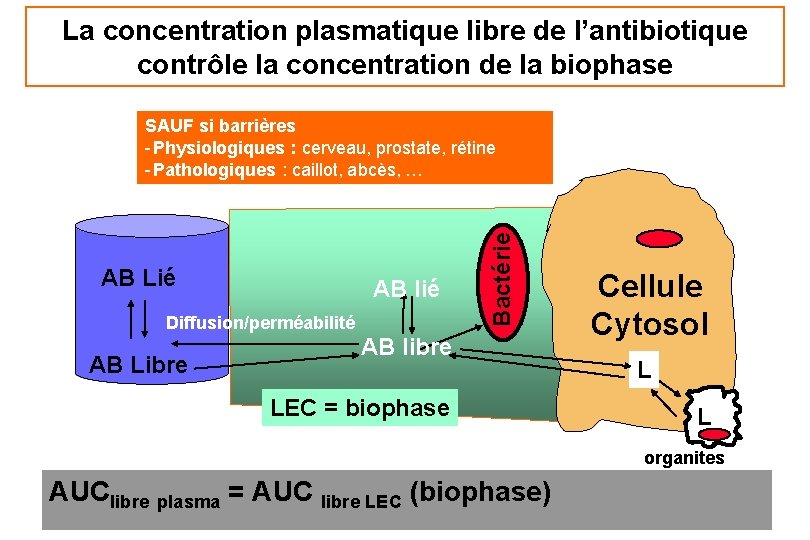
La concentration plasmatique libre de l’antibiotique contrôle la concentration de la biophase AB Lié AB lié Diffusion/perméabilité AB Libre Bactérie SAUF si barrières - Physiologiques : cerveau, prostate, rétine - Pathologiques : caillot, abcès, … AB libre LEC = biophase Cellule Cytosol L L organites AUClibre plasma = AUC libre LEC (biophase)

Pourquoi les concentrations plasmatiques ? • Parce que c’est facile à mesurer • Parce que c’est pertinent le plus souvent • Et les concentrations tissulaires ?

Concentrations tissulaires : pertinentes. . . ?

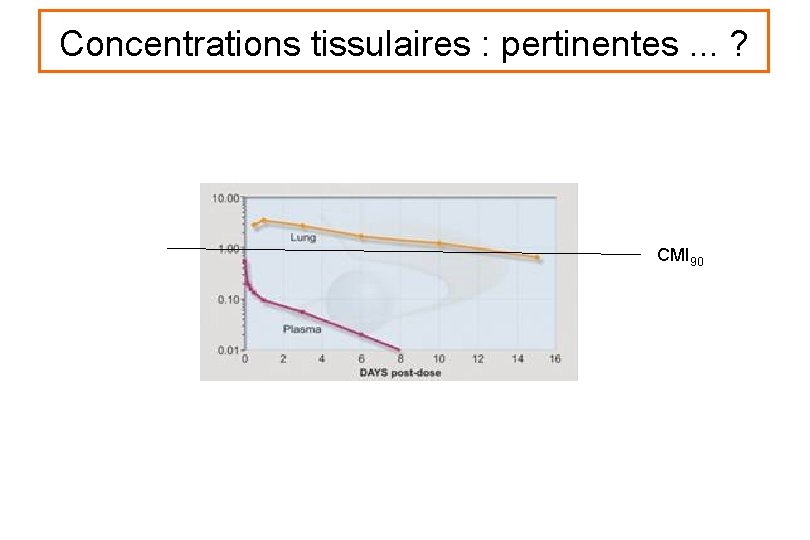
Concentrations tissulaires : pertinentes. . . ? CMI 90

Concentrations tissulaires : . . . ou pas ? • Les concentrations issues de broyats ne reflètent pas l’hétérogénéité des compartiments extracellulaire et intracellulaires • Les bactéries sont majoritairement extracellulaires • Microdialyse des liquides extracellulaires (LEC) • Concentrations libres LEC = concentrations libres plasma • Pas de modification par l’inflammation

Pourquoi les concentrations plasmatiques ? • Parce que c’est facile • Parce que c’est pertinent le plus souvent • Parce que les concentrations tissulaires ne sont pas pertinentes
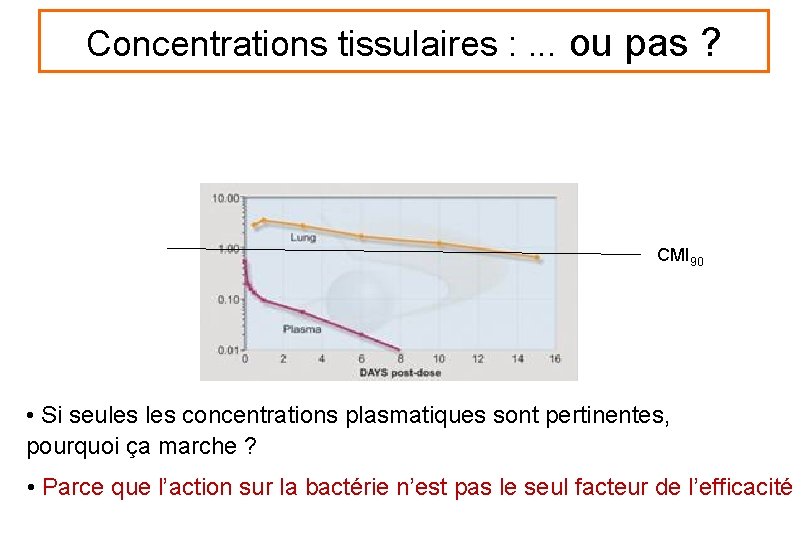
Concentrations tissulaires : . . . ou pas ? CMI 90 • Si seules concentrations plasmatiques sont pertinentes, pourquoi ça marche ? • Parce que l’action sur la bactérie n’est pas le seul facteur de l’efficacité
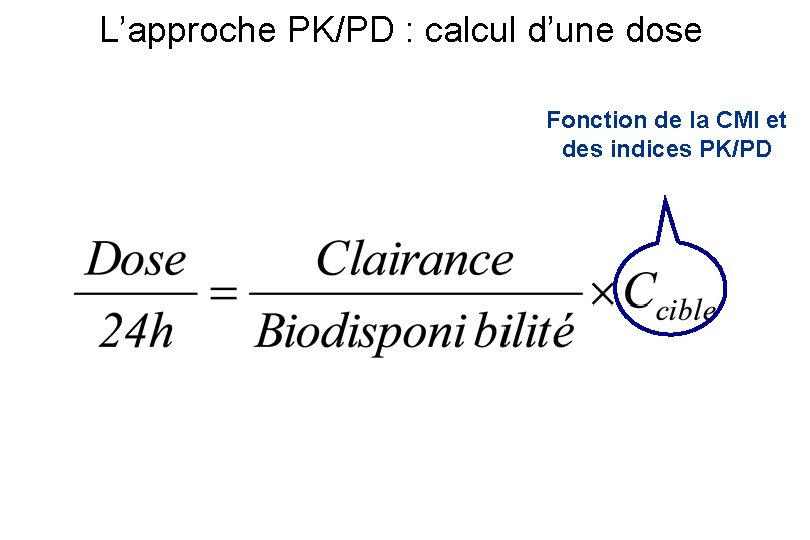
L’approche PK/PD : calcul d’une dose Fonction de la CMI et des indices PK/PD

Antibiothérapie raisonnée : quels objectifs ? 1. Efficacité maximale contre les bactéries pathogènes

L’approche PK/PD pour les antibiotiques Les indices d’efficacité des antibiotiques ou indices PK/PD • Des critères de substitution pour la guérison clinique ou bactériologique • Des manières de standardiser l’exposition sanguine, relativement à la sensibilité du pathogène (la CMI) – Exposition exprimée en termes d’Intensité et/ou de Durée • Des valeurs seuils ( « breakpoints » ) de ces indices garantissent la guérison avec une certaine probabilité, >80 -90%
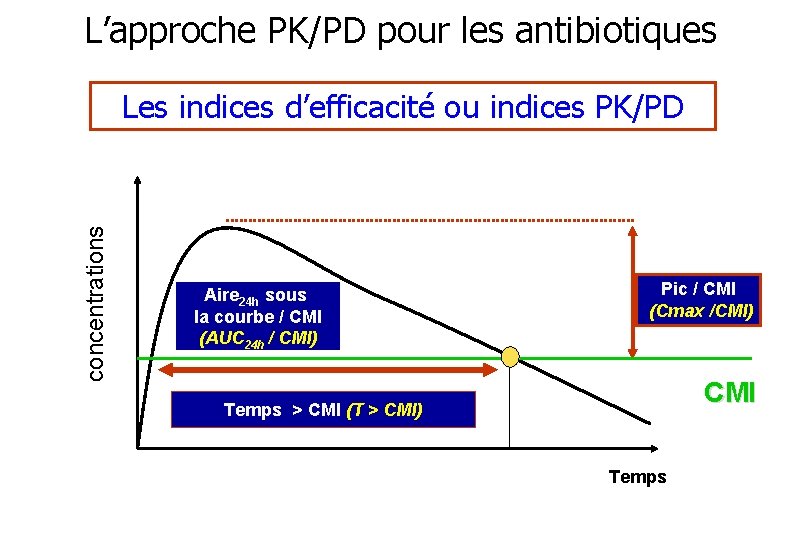
L’approche PK/PD pour les antibiotiques concentrations Les indices d’efficacité ou indices PK/PD Aire 24 h sous la courbe / CMI (AUC 24 h / CMI) Pic / CMI (Cmax /CMI) CMI Temps > CMI (T > CMI) Temps

Le type d’indice PK/PD en corrélation avec l’efficacité dépend de la classe d’antibiotique
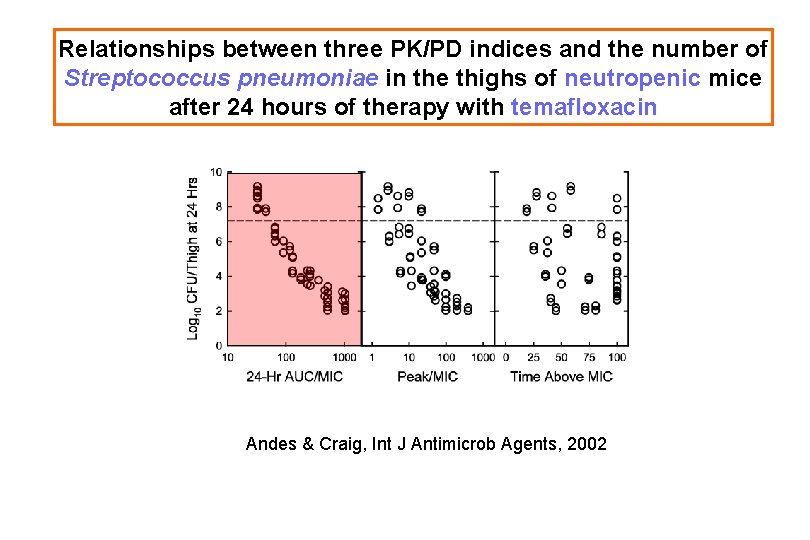
Relationships between three PK/PD indices and the number of Streptococcus pneumoniae in the thighs of neutropenic mice after 24 hours of therapy with temafloxacin Andes & Craig, Int J Antimicrob Agents, 2002
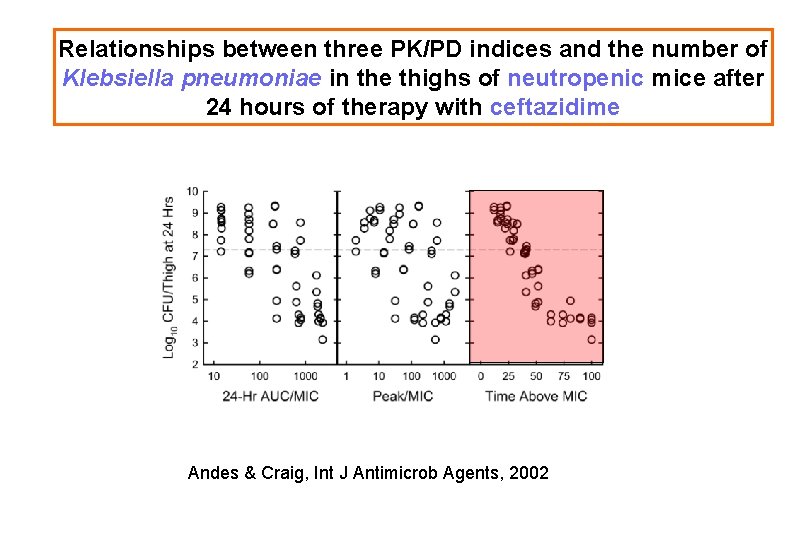
Relationships between three PK/PD indices and the number of Klebsiella pneumoniae in the thighs of neutropenic mice after 24 hours of therapy with ceftazidime Andes & Craig, Int J Antimicrob Agents, 2002

Les indices PK/PD corrélés avec l’efficacité sont fonction de la famille d’antibiotique et du type d’activité antibactérienne From Lees, Svenden & Wiuff, In : Guide to Antimicrobial Use in Animals. Ed. Guadabassi, jensen & kruse, 2008
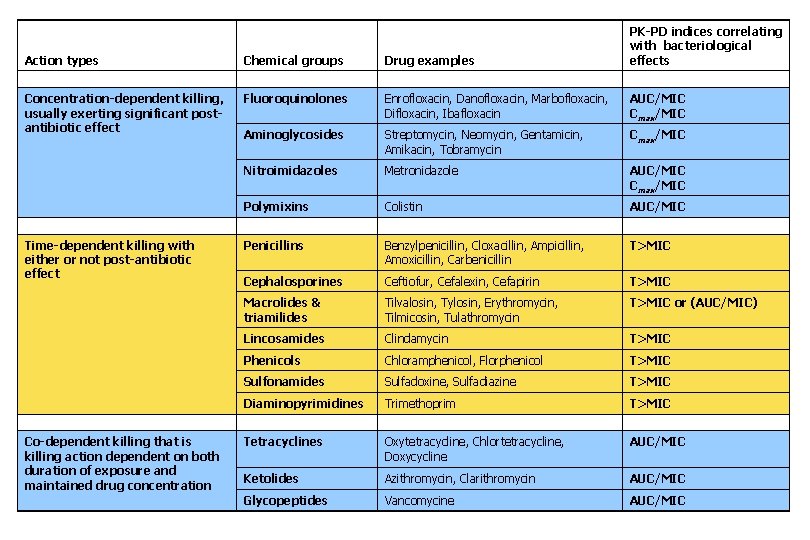
Action types Chemical groups Drug examples PK-PD indices correlating with bacteriological effects Concentration-dependent killing, usually exerting significant postantibiotic effect Fluoroquinolones Enrofloxacin, Danofloxacin, Marbofloxacin, Difloxacin, Ibafloxacin AUC/MIC Cmax/MIC Aminoglycosides Streptomycin, Neomycin, Gentamicin, Amikacin, Tobramycin Cmax/MIC Nitroimidazoles Metronidazole AUC/MIC Cmax/MIC Polymixins Colistin AUC/MIC Penicillins Benzylpenicillin, Cloxacillin, Ampicillin, Amoxicillin, Carbenicillin T>MIC Cephalosporines Ceftiofur, Cefalexin, Cefapirin T>MIC Macrolides & triamilides Tilvalosin, Tylosin, Erythromycin, Tilmicosin, Tulathromycin T>MIC or (AUC/MIC) Lincosamides Clindamycin T>MIC Phenicols Chloramphenicol, Florphenicol T>MIC Sulfonamides Sulfadoxine, Sulfadiazine T>MIC Diaminopyrimidines Trimethoprim T>MIC Tetracyclines Oxytetracycline, Chlortetracycline, Doxycycline AUC/MIC Ketolides Azithromycin, Clarithromycin AUC/MIC Glycopeptides Vancomycine AUC/MIC Time-dependent killing with either or not post-antibiotic effect Co-dependent killing that is killing action dependent on both duration of exposure and maintained drug concentration

Valeurs des indices PK/PD requises pour garantir une efficacité maximale Modèles d’infection chez les rongeurs Infections chez l’Homme
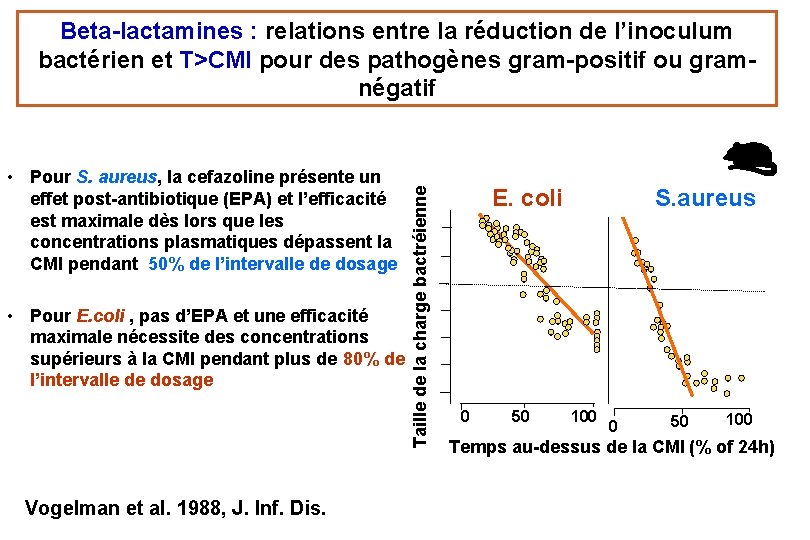
• Pour S. aureus, la cefazoline présente un effet post-antibiotique (EPA) et l’efficacité est maximale dès lors que les concentrations plasmatiques dépassent la CMI pendant 50% de l’intervalle de dosage • Pour E. coli , pas d’EPA et une efficacité maximale nécessite des concentrations supérieurs à la CMI pendant plus de 80% de l’intervalle de dosage Vogelman et al. 1988, J. Inf. Dis. Taille de la charge bactréienne Beta-lactamines : relations entre la réduction de l’inoculum bactérien et T>CMI pour des pathogènes gram-positif ou gramnégatif E. coli 0 50 S. aureus 100 0 50 100 Temps au-dessus de la CMI (% of 24 h)
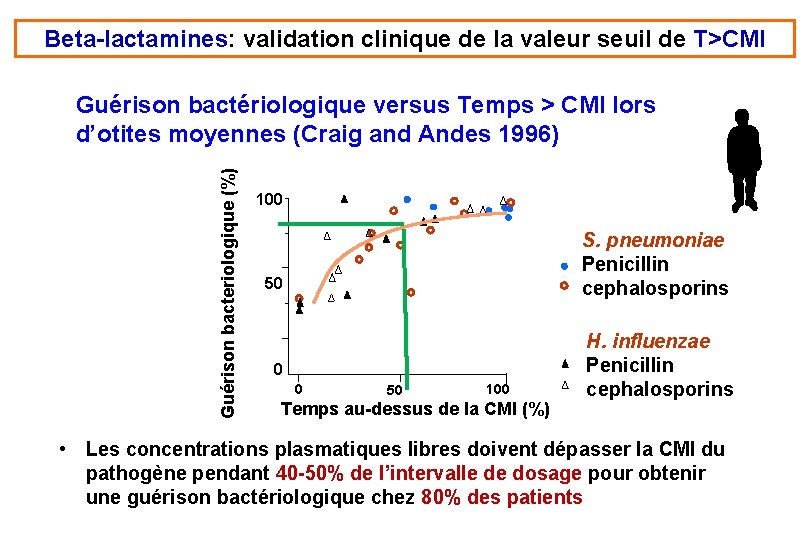
Beta-lactamines: validation clinique de la valeur seuil de T>CMI Guérison bacteriologique (%) Guérison bactériologique versus Temps > CMI lors d’otites moyennes (Craig and Andes 1996) 100 S. pneumoniae Penicillin cephalosporins 50 0 0 50 100 Temps au-dessus de la CMI (%) H. influenzae Penicillin cephalosporins • Les concentrations plasmatiques libres doivent dépasser la CMI du pathogène pendant 40 -50% de l’intervalle de dosage pour obtenir une guérison bactériologique chez 80% des patients
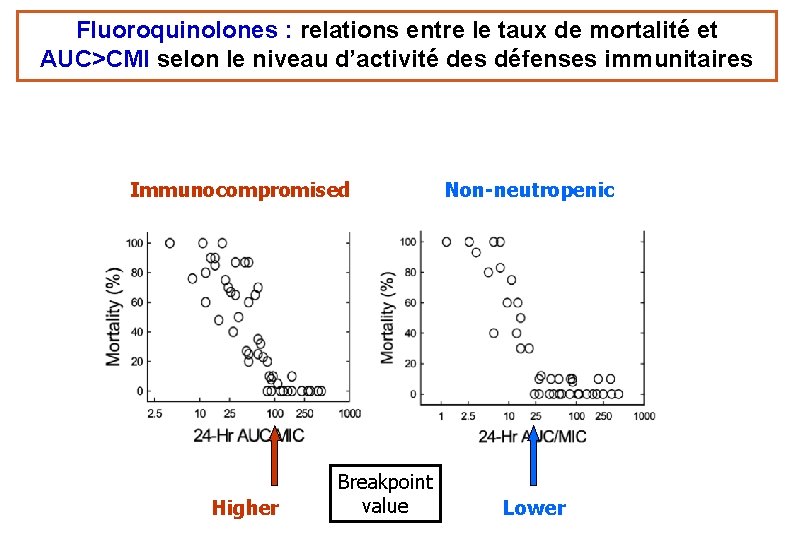
Fluoroquinolones : relations entre le taux de mortalité et AUC>CMI selon le niveau d’activité des défenses immunitaires Immunocompromised Higher Breakpoint value Non-neutropenic Lower

Fluoroquinolones: validation clinique de la valeur seuil de AUC/CMI Infections pulmonaires (nosocomiales) traitées avec la ciprofloxacine en IV AUC/CMI fortement prédictif du % d’éradication bactérienne et de son délai d’obtention % patients remaining culture positive • AUC/CMI>125 : très fort % d’éradication • AUC/CMI>250 : éradication obtenue dès le premier jour de traitement 100 AUC/CMI < 125 50 AUC/CMI 125 -250 0 AUC/CMI > 250 8 12 4 Days after start of therapy AUC/CMI > 125 = Conc moy = 5 x. CMI

Action types Schémas posologiques Concentration-dependent killing, usually exerting significant postantibiotic effect Chemical groups Drug examples PK-PD indices correlating with bacteriological effects Fluoroquinolones Enrofloxacin, Danofloxacin, Marbofloxacin, Difloxacin, Ibafloxacin AUC/MIC Cmax/MIC Aminoglycosides Streptomycin, Neomycin, Gentamicin, Amikacin, Tobramycin Nitroimidazoles Doses journalières C /MIC élevées / en une fois Metronidazole AUC/MIC C /MIC Qui peuvent être espacées max Time-dependent killing with either or not post-antibiotic effect Polymixins Colistin AUC/MIC Penicillins Benzylpenicillin, Cloxacillin, Ampicillin, Amoxicillin, Carbenicillin T>MIC Cephalosporines Ceftiofur, Cefalexin, Cefapirin Sulfonamides Doses journalières T>MIC Tilvalosin, Tylosin, Erythromycin, T>MIC or (AUC/MIC) fractionnées / perfusion Tilmicosin, Tulathromycin Clindamycin ou T>MIC Chloramphenicol, Florphenicol T>MIC (Très) longue-action Sulfadoxine, Sulfadiazine T>MIC Diaminopyrimidines Trimethoprim T>MIC Tetracyclines Oxytetracycline, Chlortetracycline, Doxycycline AUC/MIC Ketolides Azithromycin, Clarithromycin AUC/MIC Glycopeptides Vancomycine AUC/MIC Macrolides & triamilides Lincosamides Phenicols Co-dependent killing that is killing action dependent on both duration of exposure and maintained drug concentration

Pour résumer • Le type d’indice PK/PD corrélé avec l’efficacité : – Dépend du mécanisme d’action de l’antibiotique vis-à-vis du pathogène : homogène au sein d’une même famille – Intensité de l’exposition (AUC/CMI, Cmax/CMI) pour les antibiotiques concentration-dependants et durée de l’exposition (T>CMI) pour les antibiotiques temps-dépendants – Est le même quel que soit l’hôte infecté : animaux, humains • Les valeurs des indices PK/PD associées à une forte probabilité de guérison: – Dépendent de divers facteurs : bactéries (Gram+ vs Gram-), antibiotiques (beta-lactamines), niveau des défenses immunitaires, sites infectieux

Antibiothérapie raisonnée : quels objectifs ? 1. Efficacité maximale contre les bactéries pathogènes 2. Minimiser l’émergence et la sélection des résistances bactériennes – Pour les pathogènes cibles : enjeux d’efficacité / santé animale Les gros inoculums bactériens sont hétérogènes
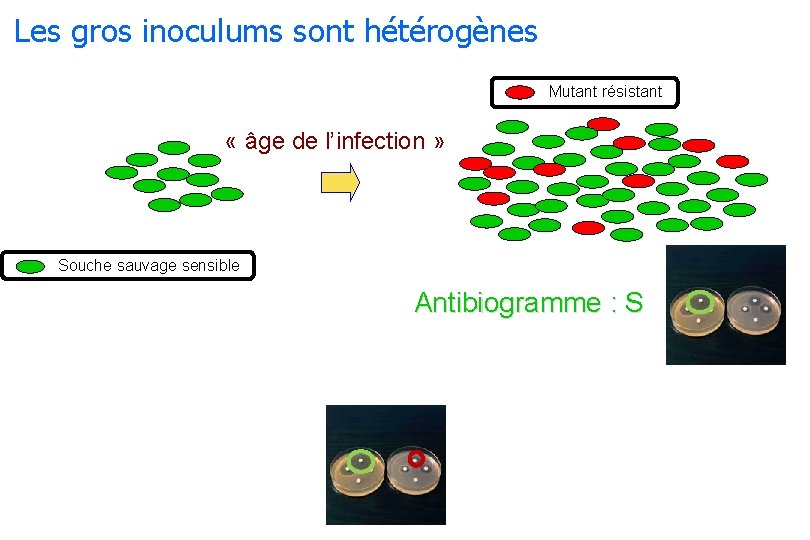
Les gros inoculums sont hétérogènes Mutant résistant « âge de l’infection » Souche sauvage sensible Antibiogramme : S

Sélection ou prévention des résistances : la notion de fenêtre de sélection Fluoroquinolones : Résistances apparaissent par mutation (10 -8 -10 -9) sur les gènes codant pour les cibles des antibiotiques (gyrases, topoisomérases) Doses fortes
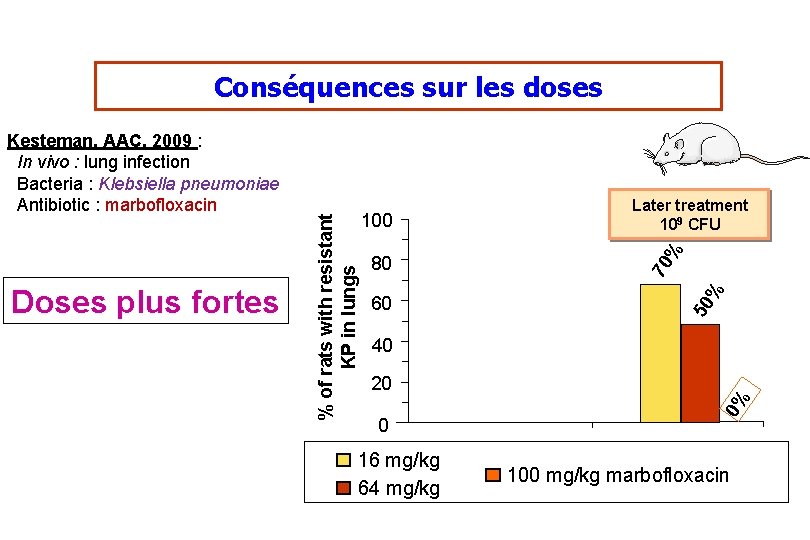
% 60 % 80 50 40 20 0 16 mg/kg 64 mg/kg 0% Doses plus fortes 100 Later treatment 109 CFU 70 Kesteman, AAC, 2009 : In vivo : lung infection Bacteria : Klebsiella pneumoniae Antibiotic : marbofloxacin % of rats with resistant KP in lungs Conséquences sur les doses 100 mg/kg marbofloxacin

De l’intérêt de traiter vite
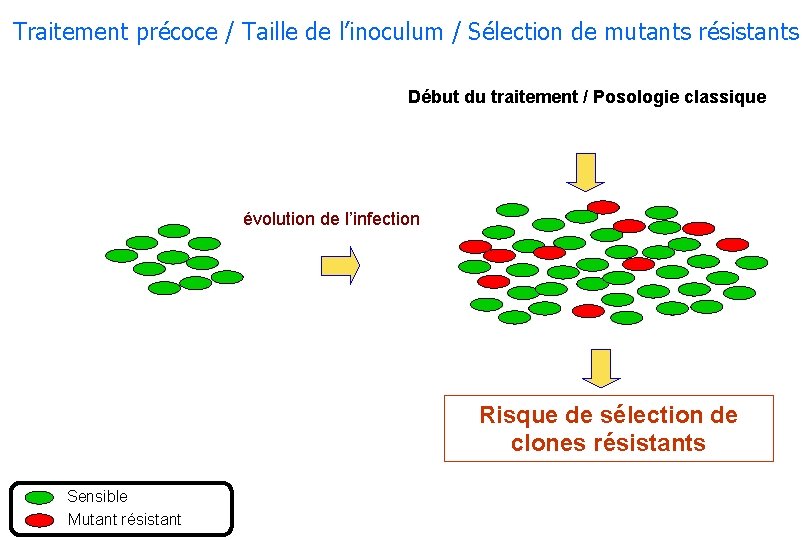
Traitement précoce / Taille de l’inoculum / Sélection de mutants résistants Début du traitement / Posologie classique évolution de l’infection Risque de sélection de clones résistants Sensible Mutant résistant
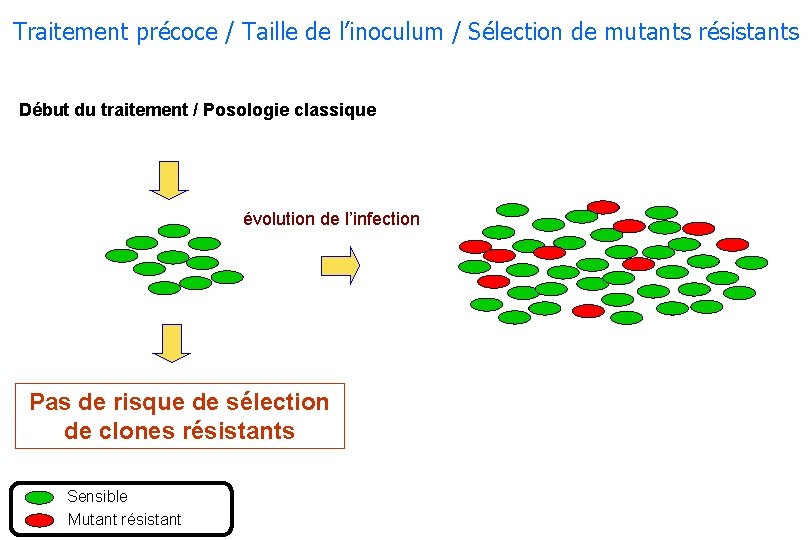
Traitement précoce / Taille de l’inoculum / Sélection de mutants résistants Début du traitement / Posologie classique évolution de l’infection Pas de risque de sélection de clones résistants Sensible Mutant résistant
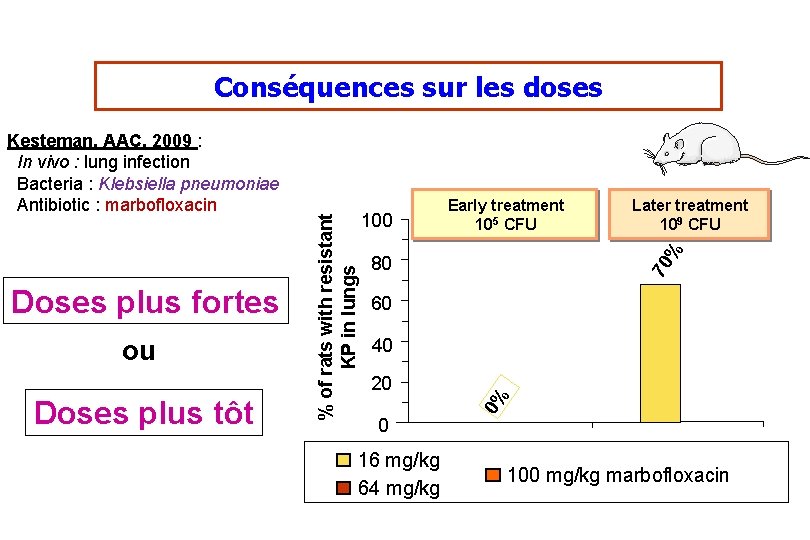
Doses plus fortes ou Doses plus tôt Later treatment 109 CFU % 100 Early treatment 105 CFU 70 80 60 40 20 0 16 mg/kg 64 mg/kg 0% Kesteman, AAC, 2009 : In vivo : lung infection Bacteria : Klebsiella pneumoniae Antibiotic : marbofloxacin % of rats with resistant KP in lungs Conséquences sur les doses 100 mg/kg marbofloxacin

De l’intérêt de traiter vite 1. Réduire le risque de présence de mutants résistants
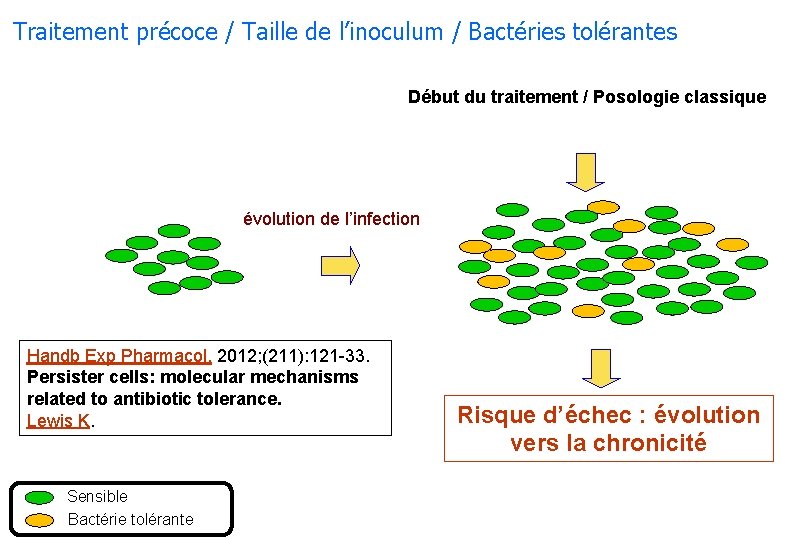
Traitement précoce / Taille de l’inoculum / Bactéries tolérantes Début du traitement / Posologie classique évolution de l’infection Handb Exp Pharmacol. 2012; (211): 121 -33. Persister cells: molecular mechanisms related to antibiotic tolerance. Lewis K. Sensible Bactérie tolérante Risque d’échec : évolution vers la chronicité
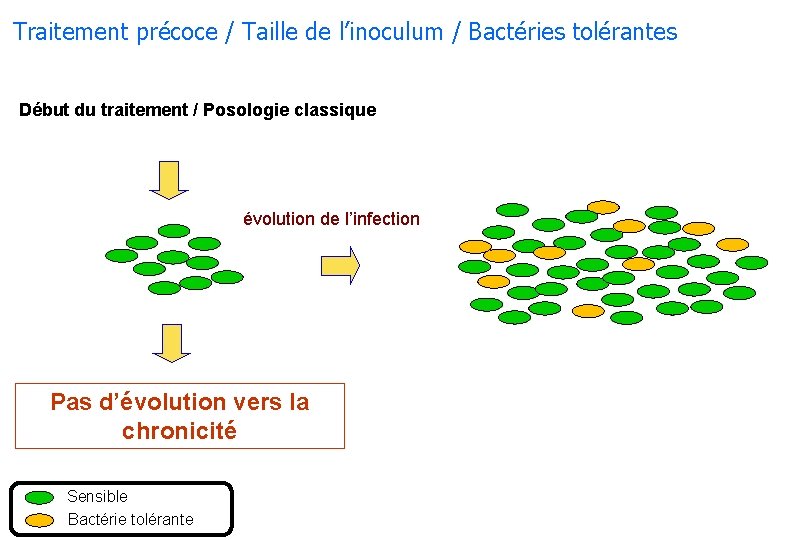
Traitement précoce / Taille de l’inoculum / Bactéries tolérantes Début du traitement / Posologie classique évolution de l’infection Pas d’évolution vers la chronicité Sensible Bactérie tolérante

De l’intérêt de traiter vite 1. Réduire le risque de présence de mutants résistants 2. Eviter la présence de bactéries tolérantes ( «persisteurs» )
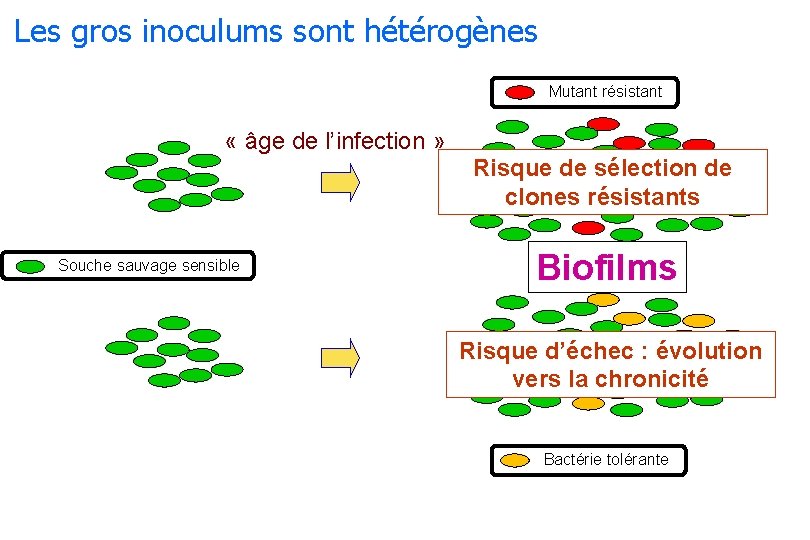
Les gros inoculums sont hétérogènes Mutant résistant « âge de l’infection » Risque de sélection de clones résistants Souche sauvage sensible Biofilms Risque d’échec : évolution vers la chronicité Bactérie tolérante
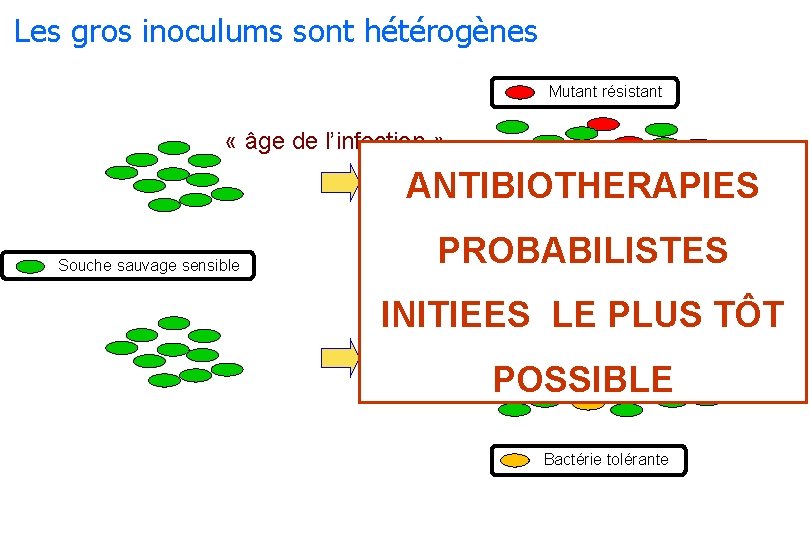
Les gros inoculums sont hétérogènes Mutant résistant « âge de l’infection » Risque de sélection de ANTIBIOTHERAPIES clones résistants Souche sauvage sensible PROBABILISTES INITIEES LE PLUS TÔT Risque d’échec : évolution vers la chronicité POSSIBLE Bactérie tolérante

Pour résumer • Traiter Vite et Fort est une combinaison favorable pour : – guérison clinique – prévention de la sélection de résistance au site infectieux

Antibiothérapie raisonnée : quels objectifs ? 1. Efficacité maximale contre les bactéries pathogènes 2. Minimiser l’émergence et la sélection des résistances bactériennes – Pour les pathogènes cibles : enjeux d’efficacité / santé animale – Pour les bactéries non cibles: enjeux de santé humaine • Bactéries zoonotiques • Flores commensales des animaux (réservoirs de gènes de résistance)
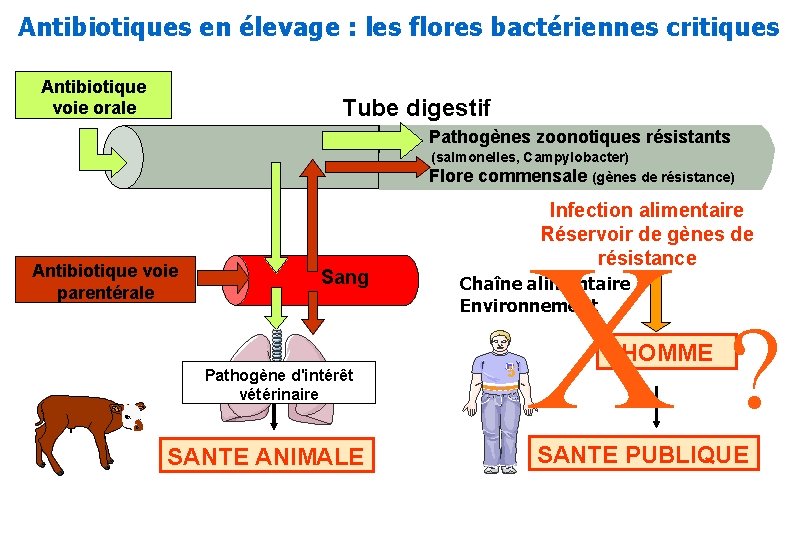
Antibiotiques en élevage : les flores bactériennes critiques Antibiotique voie orale Tube digestif Pathogènes zoonotiques résistants (salmonelles, Campylobacter) Flore commensale (gènes de résistance) Antibiotique voie parentérale Sang Pathogène d'intérêt vétérinaire SANTE ANIMALE Infection alimentaire Réservoir de gènes de résistance X? Chaîne alimentaire Environnement 5 HOMME SANTE PUBLIQUE
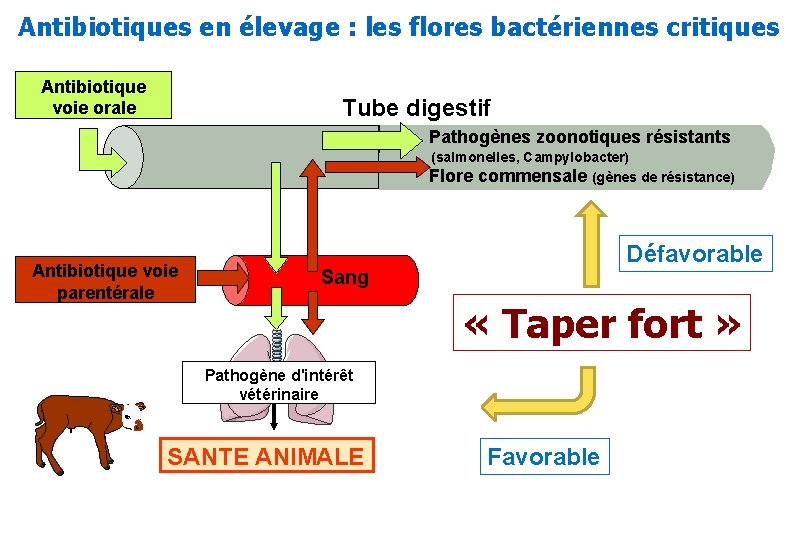
Antibiotiques en élevage : les flores bactériennes critiques Antibiotique voie orale Tube digestif Pathogènes zoonotiques résistants (salmonelles, Campylobacter) Flore commensale (gènes de résistance) Antibiotique voie parentérale Défavorable Sang « Taper fort » Pathogène d'intérêt vétérinaire SANTE ANIMALE Favorable
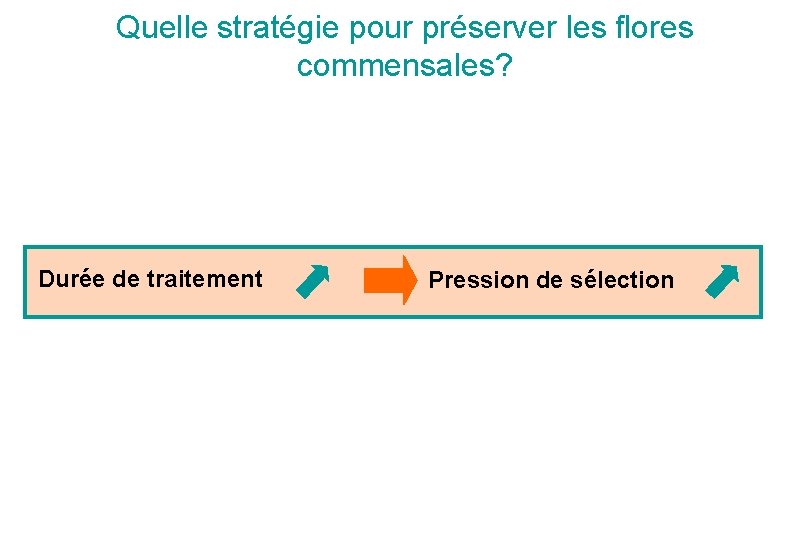
Quelle stratégie pour préserver les flores commensales? Durée de traitement Pression de sélection

Quelle stratégie pour préserver les flores commensales? Absence d’essais cliniques comparatifs en médecine vétérinaire qui valident les durées de traitements Durée de traitement = CHOIX SOUVENT EMPIRIQUE « la durée précise du traitement n’est pas confortée par une preuve solide » « pas suffisamment d’essais cliniques contrôlés » d’après Organisation Mondiale de la Santé

Quelle stratégie pour préserver les flores commensales? Impact de la durée du traitement sur le succès clinique FLUOROQUINOLONE, BETA-LACTAMINE, MACROLIDE traitement exacerbations aiguës de bronchite chronique 5 jours de traitement = 7 -10 jours de traitement Falagas et al. JAC 2008: 62 442 -450 FLUOROQUINOLONE (levofloxacine) traitement pneumonies 750 mg pendant 5 jours = Dunbar et al. CID 2003: 37 752 -760 500 mg pendant 10 jours

Quelle stratégie pour préserver les flores commensales? Impact de la durée du traitement sur le succès clinique AMOXICILLINE – AC CLAVULANIQUE traitement exacerbations aiguës de bronchite chronique Après ré-évaluation à 3 jours : groupe placebo ou amox-clav 7 jours 3 jours de traitement = 10 jours de traitement Falagas et al. Clin Microb Infect 2007: 13 284 -290 RE-EVALUATIONS 3 -5 JOURS POUR DECISION RE-EVALUATIONS LORS DE TRANSITIONS : Injectable / Voie orale Sortie d’hospitalisation

Quelle stratégie pour préserver les flores commensales? Impact de la durée du traitement sur l’émergence résistance : la flore commensale du rhynopharynx AMOXICILLINE : 90 mg/kg pendant 5 j vs 40 mg/kg pendant 10 j Isolement de S. pneumoniae résistants à la pénicilline chez des enfants moins fréquent Schrag et al. JAMA 2001: 286 49 -56 PENICILLINE : durée de traitement supérieure à 5 jours Isolement de S. pneumoniae résistants à la pénicilline chez des enfants plus fréquent Guillemot et al. JAMA 1998: 279 365 -370
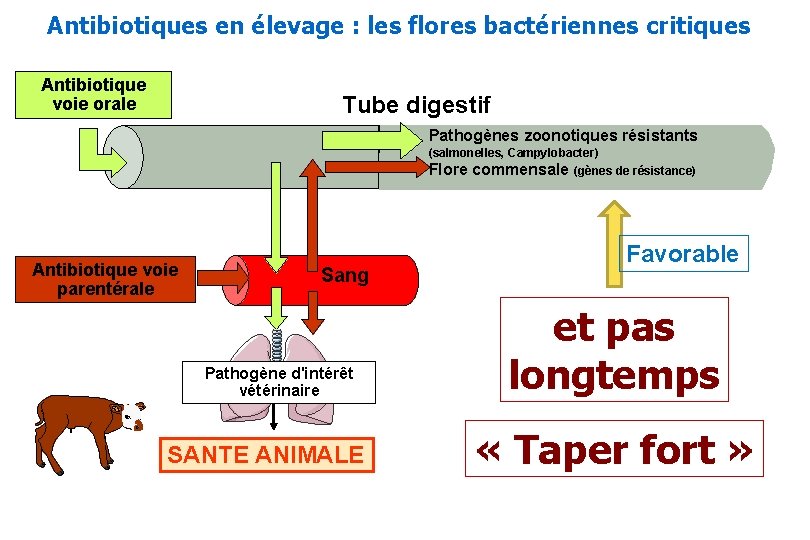
Antibiotiques en élevage : les flores bactériennes critiques Antibiotique voie orale Tube digestif Pathogènes zoonotiques résistants (salmonelles, Campylobacter) Flore commensale (gènes de résistance) Antibiotique voie parentérale Sang Pathogène d'intérêt vétérinaire SANTE ANIMALE Favorable et pas longtemps « Taper fort »
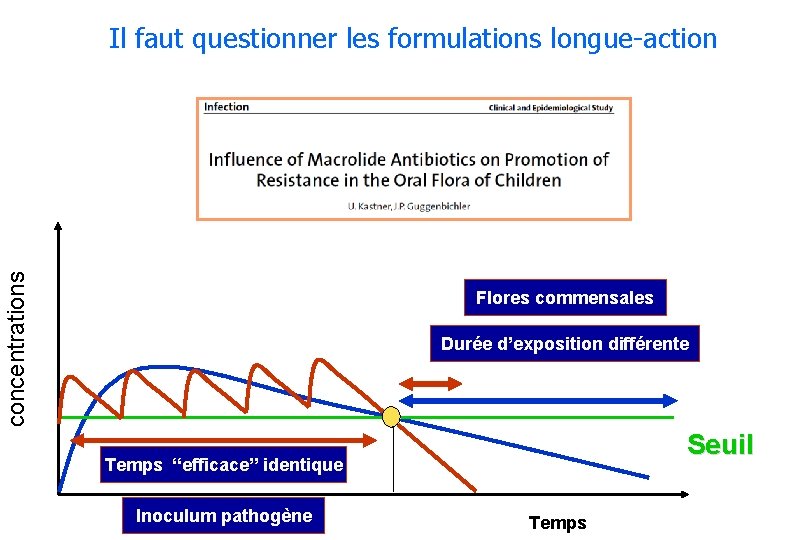
concentrations Il faut questionner les formulations longue-action Flores commensales Durée d’exposition différente Seuil Temps “efficace” identique Inoculum pathogène Temps

Conclusion • Traiter vite et fort pour – Éradiquer les bactéries – Prévenir la sélection de résistances au site infectieux • Traiter brièvement pour – Limiter la pression de sélection sur les flores commensales « Hit hard and fast … then leave as soon as possible » Clinical cornerstone 2003 S 3 (S 21 -S 28) « Hit hard and stop early » Clinical Infectious Disease 2004

Troisième partie : Quelques défis à venir pour l’antibiothérapie en élevage
- Slides: 62