ANTIANGIOGNICOS INDICACIONES Y PERFIL DE TOXICIDAD DE LOS












- Slides: 17

ANTIANGIOGÉNICOS INDICACIONES Y PERFIL DE TOXICIDAD DE LOS TKIs INMA GALLEGO JIMÉNEZ. MIR 4º ONCOLOGÍA. HOSPITAL NUESTRA SEÑORA DE VALME. SEVILLA.

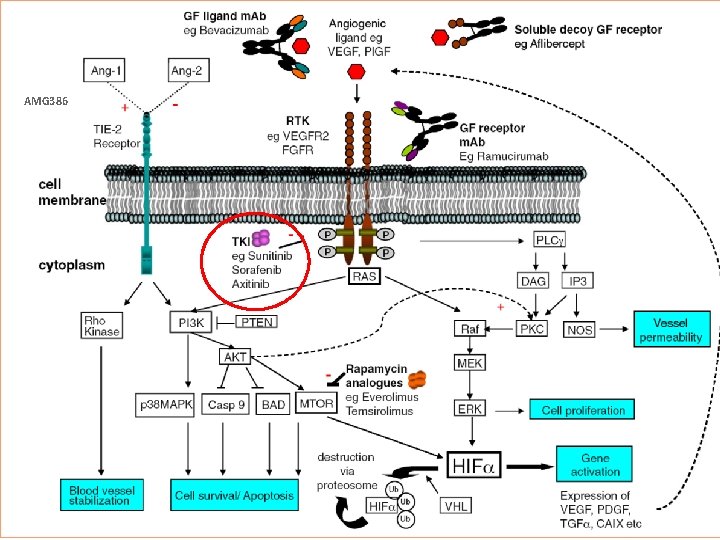
Angiogénesis y cáncer AMG 386

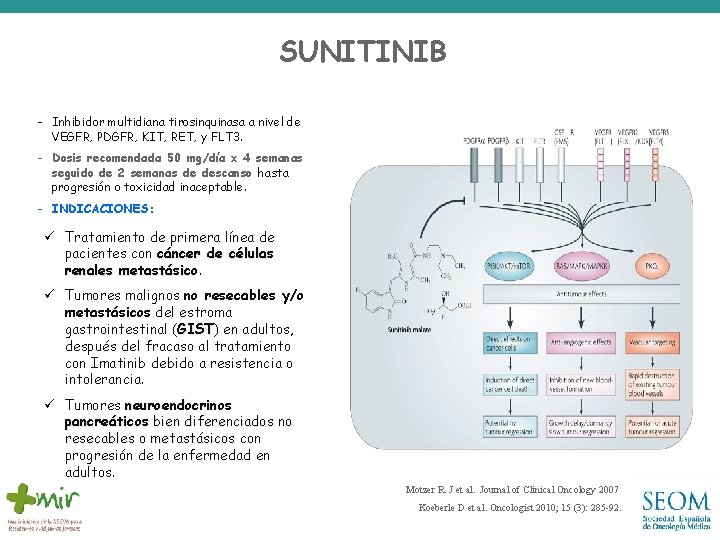
SUNITINIB - Inhibidor multidiana tirosinquinasa a nivel de VEGFR, PDGFR, KIT, RET, y FLT 3. - Dosis recomendada 50 mg/día x 4 semanas seguido de 2 semanas de descanso hasta progresión o toxicidad inaceptable. - INDICACIONES: ü Tratamiento de primera línea de pacientes con cáncer de células renales metastásico ü Tumores malignos no resecables y/o metastásicos del estroma gastrointestinal (GIST) GIST en adultos, después del fracaso al tratamiento con Imatinib debido a resistencia o intolerancia. ü Tumores neuroendocrinos pancreáticos bien diferenciados no resecables o metastásicos con progresión de la enfermedad en adultos. Motzer R. J et al. Journal of Clinical Oncology 2007 Koeberle D et al. Oncologist 2010; 15 (3): 285 -92.

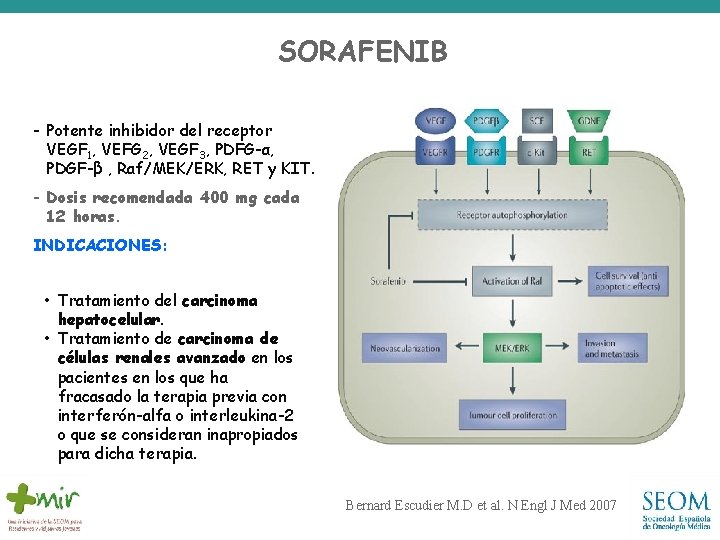
SORAFENIB - Potente inhibidor del receptor VEGF 1, VEFG 2, VEGF 3, PDFG-α, PDGF-β , Raf/MEK/ERK, RET y KIT. - Dosis recomendada 400 mg cada 12 horas. INDICACIONES: • Tratamiento del carcinoma hepatocelular. • Tratamiento de carcinoma de células renales avanzado en los pacientes en los que ha fracasado la terapia previa con interferón-alfa o interleukina-2 o que se consideran inapropiados para dicha terapia. Bernard Escudier M. D et al. N Engl J Med 2007

PAZOPANIB - Inhibidor múltiple tirosinquinasa de VEGFR 1, VEGFR 2, VEGFR 3, PDFG-α, PDGF-β, FGFR-1 y 3 y c-kit. También tiene actividad frente al receptor de la interleuquina-2, frente a la quinasa inducible de células T (ITK), Proteína tirosinquinasa específica de los leucocitos (Lc. K) y del receptor de la tirosinquinasa de glicoproteínas de transmembrana (c-FMS) - Dosis recomendada 800 mg/24 horas. - INDICACIONES: ü Tratamiento de primera línea del carcinoma de células renales avanzado en adultos y para los pacientes con enfermedad avanzada que han recibido tratamiento previo con citoquinas. ü Determinados subtipos de Sarcomas de tejidos blandos avanzado que hayan recibido previamente tratamiento con quimioterapia para tratar su enfermedad metastásica o en aquellos pacientes adultos cuya enfermedad haya progresado en los 12 meses siguientes tras recibir tratamiento neoadyuvante y/o adyuvante. FDA. Center for drug evaluation and research. Medical Review. Votrient (Pazopanib). Clinical NDA. Review. Hutson T et al. J Clin Oncol 2012; 28: 475 -480.

AXITINIB - Inhibidor múltiple tirosinquinasa de VEGFR 1, VEGFR 2, VEGFR 3, PDFGR -α y c-kit. - Indicado en el tratamiento de carcinoma avanzado de células renales tras fracaso a un tratamiento previo con sunitinib o citoquinas. - La dosis de inicio de Axitinib es de 5 mg dos veces al día. Si lo tolera durante dos semanas, la dosis puede subir a 7 mg dos veces al día. La dosis máxima es de 10 mg dos veces al día. Rini BI et al. Comparative effectiveness of axitinib versus sorafenib in advanced renal cell carcinoma (AXIS): a randomised phase 3 trial. 2012; 188 (2): 188: 412 -3.

VANDETANIB - Inhibidor múltiple tirosinquinasa de VEGFR 2, VEGFR 3, EGFR y RET. - Indicado en el tratamiento de carcinoma medular de tiroides avanzado no resecable o metastásico. - La dosis recomendada es de 300 mg una vez al día hasta intolerancia o progresión de la enfermedad. Thornton et al. Clin Cancer Res 2012

VEGFR 1 VEGFR 2 VEGFR 3 PDGFR c. KIT RET Otros SUNITINIB - + + + FLT 3 SORAFENIB - + + + RAF PAZOPANIB + + + - FGFR AXITINIB + + + - - VANDETANIB EGFR

EFECTOS SECUNDARIOS q EFECTOS SECUNDARIOS HTA Toxicidad Cardiaca Síndrome mano-pie Mucositis Diarrea Toxicidad Hematológica Astenia

TOXICIDAD CARDIACA ü La disfunción ventricular izquierda es el principal efecto adverso (12% de los pacientes), G 3 -4 en el 1 -2% de los pacientes. ü En el 27% de los pacientes se produce un descenso de la FEVI. ü Las arritmias, y la prolongación del intervelo PR y QT son menos del 1% de los casos. ü Se ha de realizar un estudio basal cardiológico que incluye FEVI y ECG. Durante el tto se ha de monitorizar trimestralmente la FEVI. ü Se pueden utilizar IECAs y betabloqueantes. Si aparecen signos de Insuficiencia Cardiaca se puede utilizar furosemida 80 mg/día. García Álvarez A, et al. Cardiovascular and Hematological agents in Medicinal Chemistry 2010; 8: 11 -21

SÍNDROME MANO-PIE Más frecuente con Sunitinib y Sorafenib. Consiste en la formación de lesiones hiperqueratósicas en las zonas de presión. Suelen ser molestas y dolorosas. Lacouture ME et al. The Oncologist 2008; 13: 1001 -1011.

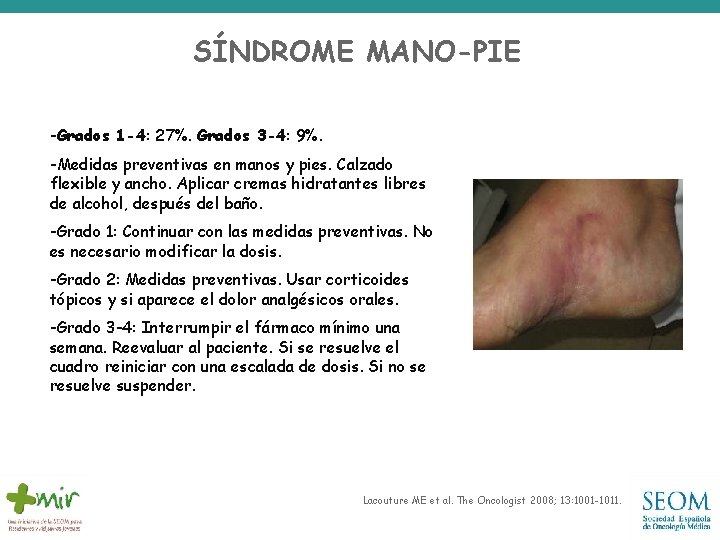
SÍNDROME MANO-PIE -Grados 1 -4: 27%. Grados 3 -4: 9%. -Medidas preventivas en manos y pies. Calzado flexible y ancho. Aplicar cremas hidratantes libres de alcohol, después del baño. -Grado 1: Continuar con las medidas preventivas. No es necesario modificar la dosis. -Grado 2: Medidas preventivas. Usar corticoides tópicos y si aparece el dolor analgésicos orales. -Grado 3 -4: Interrumpir el fármaco mínimo una semana. Reevaluar al paciente. Si se resuelve el cuadro reiniciar con una escalada de dosis. Si no se resuelve suspender. Lacouture ME et al. The Oncologist 2008; 13: 1001 -1011.

MUCOSITIS ü Se produce en el 10 -30% de los pacientes en tratamiento con ITK, siendo G 3 -G 4 sólo en el 2% de los pacientes. ü En ocasiones aparece estomatitis sin lesiones aparentes. ü Mejoran rápidamente durante dos semanas de descanso, pero suelen reaparecer en los siguientes ciclos. Tto: Enjuagues con colutorios sin alcohol, con anestésicos tópicos como lidocaína, y vaselina para las queilitis. Si aparece candidiasis oral: enjuagues con nistatina 5 ml 4 veces al día. Y si es necesario tratamiento oral: Fluconazol 100 mg al día durante 7 días. Ivanyi P et al. Dtsch Arztebl Int 2008; 105 (13); 232 -7.

ASTENIA • Ocurre en el 65 -73% de los pacientes, aunque sólo el 10% experimenta astenia severa que interfiere con la actividad diaria (grado 3). • Normalmente aparece entre la 2ª y 3ª semana de iniciar el tto. • Los síntomas pueden mejorar durante las dos semana de descanso, sobre todo en pacientes con baja carga tumoral. Medidas Preventivas: Identificar posibles causas como dolor, depresión, hipotiroidismo, anemia, hipofosfatemia, hipomagnesemia, malnutrición. Si la calidad de vida se ve comprometida por la astenia reducir dosis. Tibes, R. , Trent, J. , y Kurzrock, R. Annu Rev Pharmacol Toxicol 2005; 45, 357 -384.

DIARREA Todos los grados: 50%. Especialmente con Sunitinib y Pazopanib. Al contrario de lo que ocurre con la diarrea inducida por la quimioterapia, que generalmente es continua, la diarrea inducida por sunitinib puede ocurrir de forma irregular. La diarrea G 1 -G 2 puede mejorarse con hidratación oral y antidiarreicos orales como la loperamida. Si la diarrea es importante y empeora con la ingesta de alimentos, se puede administrar loperamida 30 minutos antes de la comida y colestiramina antes de las comidas.

TOXICIDAD HEMATOLÓGICA - Inducen anemia, neutropenia y trombocitopenia en un 45% de los pacientes. - Sólo el 5 -8% de los pacientes presentaron neutropenia o trombocitopenia grado 3 -4. No hubo ningún caso de neutropenia febril en los estudios fase II y fase III. - Recomendaciones: - Neutropenia G 3 -G 4: Reducir 1 nivel de dosis en el siguiente ciclo. - Anemia G 3 -G 4 generalmente no requiere reducción ni interrupción. - Si la trombopenia es de grado 3 se reduce la dosis. Bhojani N, Jeldres C, Patard JJ et al. European Urology 2008; 53: 917 -930.

CONCLUSIONES: - La inhibición de la angiogénesis mediante TKIs ha demostrado su eficacia en términos de respuesta y supervivencia en el contexto del tratamiento del cáncer renal, GIST, CMT, tumores neuroendocrinos de origen pancreático, hepatocarcinoma y algunos subtipos de sarcomas de tejidos blandos. - Su perfil de toxicidad especifico (HTA, toxicidad cardíaca, diarrea, mucositis, astenia y síndrome mano-pie) debe ser conocido y manejado para un buen cumplimiento terapéutico. - Importante señalar la ausencia de marcadores pronósticos y predictivos de respuesta a esta modalidad de tratamiento. - Considerar la relación coste-eficacia y la posibilidad de desarrollo de mecanismos de resistencia. - Numerosos estudios con nuevos fármacos frente a esta vía de señalización en desarrollo.