Anorganick nekovov materily Keramika Sklo Stavebn pojiva vpno

Anorganické nekovové materiály

• Keramika • Sklo • Stavební pojiva – vápno beton sádra (asfalt) • Geopolymery
Keramika

Keramika • Kdy - 9000 let př. n. l. – mladší doba kamenná (neolit). • Kde - oblast Blízkého východu. • Co - nádoby z jílu, které byly po vysušení vytvrzeny v ohni. • K čemu – k uskladňování úrody.

Keramika • Ve střední Evropě první neolitická sídliště asi 6000 let př. n. l. – typickým znakem je lineární keramika. • Samotné slovo keramika pochází z řeckého slova keramos = hrnčířská hlína, zboží.

Keramika • Časem mnohá zlepšení technologie (vypalované cihly, porcelán). • Základní „mokrý“ pracovní postup se zachoval dodnes. • Formováním za mokra se vyrábí také keramika pro různé průmyslové aplikace (teplotně odolné vyzdívky pecí, vysokonapěťové izolátory). • V posledních 30 - ti letech keramika zažívá nový vzestup, změna výrobních technologií.

Keramika • Na rozdíl od užitkové, kuchyňské a umělecké keramiky se vyrábí progresivní technická keramika lisováním prášku za vysoké teploty – sintrování (spékání). • Důležitá je příprava výchozích materiálů spolu s technologií (jemné prášky, dokonalé promísení hmoty, optimalizace podmínek – teplota, tlak). • Částice se propojí vzájemnou difúzí atomů v místech dotyku částic.

Keramika Nová keramika vyniká: Současné cíle jsou: • Vysokou tvrdostí • Oděruvzdorností • Pevností v tlaku • Zjemnění mikrostruktury • Lepší propojení částic • Zlepšení mechanických vlastností

Keramika • Kluzné prvky a ventily v automobilových motorech a v turbínách • Jaderné a chemické reaktory • Počítače a jejich přídavná zařízení • Solární kolektory • Raketoplány, vesmírné projekty • Náhrada lidských kostí, kloubů a zubů

Keramika • Z chemického hlediska lze keramické materiály rozdělit na: • Oxidy • Karbidy • Nitridy • Boridy • Titanáty • Niobáty

Keramika Mezi oxidy patří: • • • Al 2 O 3 Cr 2 O 3 Mg. O Zr. O 2 Li. Al 2 Si. O 6 • Tyto oxidy jsou podstatou tzv. sklokeramiky.

Keramika • Sklokeramika se připravuje řízenou krystalizací z taveniny. • Zvláštním teplotním režimem se sklovitá tavenina převede do krystalického stavu. • Vzniklé krystaly jsou tak drobné, že nerozptylují viditelné světlo a proto je sklokeramika poměrně dobře průhledná a také teplotně velmi odolná.

Keramika Z karbidů jsou prakticky významné: • • Zr. C – karbid zirkonia Ti. C – karbid titanu Si. C – karbid křemíku WC – karbid wolframu Většinou jde o velmi tvrdé materiály. Jsou vhodné na řezné a brusné nástroje a trysky odolávající oděru a vysokým teplotám.

Keramika Mezi nitridy patří: • SIALON – slitina křemíku, hliníku, kyslíku a dusíku • Ti. N – nitrid titanu • Tyto materiály jsou využívány na řezné nástroje, lopatky plynových turbín, slévárenské kelímky a licí trysky. Boridy stejně jako nitridy se používají v elektrotechnice.

Keramika Funkční keramika: • Čidla na měření různých fyzikálních veličin. • Keramické polovodiče (v základním stavu se chovají jako izolátory, jsou-li excitovány, dovolují průchod elektronů). • Varistory (odporové součástky jejichž elektrický odpor se mění s velikostí protékajícího proudu).

Keramika • Piezoelektrická keramika (vyvolává vybuzení elektrickým polem mechanickou deformaci nebo změnu krystalové modifikace a naopak, mechanická deformace vyvolá na protilehlých ploškách keramické destičky elektrický náboj). • Takové chování vykazuje např. nerost perovskit – Ca. Ti. O 3.

Keramika • Jednou z aplikací piezoelektrické keramiky jsou kanálky tryskových tiskáren k počítačům – elektrickými signály se s vysokou frekvencí otevírají a zase uzavírají a tak se podle povelů počítače řídí průchod tiskové barvy.

Keramika • Keramické snímače citlivě registrují mechanické kmity – používají se např. pro snímání akustické emise v průběhu namáhání materiálů – lze získat včas informaci o místních lomových procesech, vzniku a růstu trhliny. • Titanáty zirkonia a lanthanu reagují elektrickým signálem na dopadající světlo – využití v optoelektronice.

Keramika Konstrukční keramika: • Zahrnuje nitridy, karbidy, oxidy. • Hlavní předností oproti kovům je podstatně vyšší teplotní odolnost, nižší teplotní roztažnost, vysoká odolnost proti korozi a oděru. • Mechanické vlastnosti jsou uspokojivé i nad teplotou 1000 o. C, hustota je přibližně poloviční než u kovů (snížení hmotnosti, úspora paliva – dopravní technika).

Keramika Nevýhody keramiky: • 1) velmi křehká (má nízkou houževnatost) • 2) špatná reprodukovatelnost vlastností (mnohem větší rozptyl pevnostních vlastností než u odpovídajících kovových strojních součástí)

Keramika • Příčinou obou nedostatků je struktura. • Struktura je tvořená vzájemně propojenými drobnými částečkami s množstvím slabých míst, defektů a pórů. • Keramika se porušuje křehkou trhlinou, která se šíří vždy podél rozhraní mezi zrny. • Pro zvýšení houževnatosti se používá tzv. transformačního zpevnění, při kterém se využívá specifického chování oxidu zirkoničitého.

Keramika • Zr. O 2 přechází do rovnovážné a stabilní krystalové struktury, pokud je vystaven velké elastické deformaci (jde o tzv. martenzitický strukturní přechod, při kterém krystalky skokem zvětší svůj objem). • Oxid zirkoničitý v nestabilní formě se může používat dvěma způsoby:

Keramika • 1) Jemné částice se rovnoměrně rozptýlí v jiném keramickém materiálu – např. Al 2 O 3. Když se v základním keramickém materiálu vytvoří trhlina, částice Zr. O 2 v okolí jejího vrcholu expandují a vzniklý tlak trhlinu opět uzavírá a brání jí v růstu. Výsledkem je vyšší houževnatost.

Keramika • 2) Přísně řízeným teplotním režimem se vydělí nestabilní částice Zr. O 2 v matrici ze stabilní formy téže látky. Velikost a podíl nestabilních částic lze poměrně dobře nastavit. Z takové houževnaté zirkoničité keramiky se vyrábějí např. nemagnetické nože a nůžky.

Keramika Keramické kompozitní materiály: keramická vlákna + keramická matrice = > materiál s typickou tvrdostí keramiky s teplotní odolností keramiky s odolností proti teplotním šokům s odolností proti deformaci při extrémně vysokých teplotách s vyšší pevností oproti samotné keramické matrici

Keramika • Smyslem výroby keramických kompozitních materiálů oproti kompozitům s polymerní matricí je zvýšení houževnatosti (u polymerních zvýšení pevnosti). • Vyztužení vlákny nebo mikroskopickými destičkami může celou strukturu lépe propojit a zpevnit a zlepšit její chování. • Kompozity využívají i uhlíkové nanotrubičky.
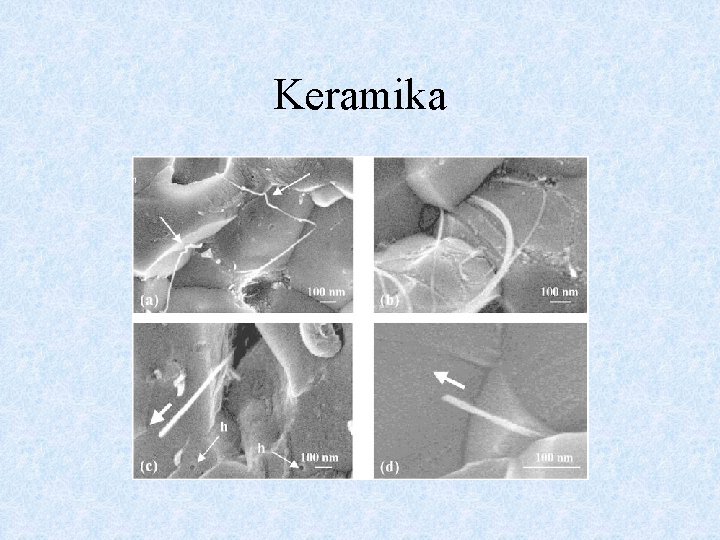
Keramika

Keramika Aplikace: • • Keramické nástroje Biokeramika Keramický motor Keramika ve vesmíru

Keramika Keramické nástroje • Keramické řezné nástroje • Ložiska • Keramické povlaky kovových řezných nástrojů

Keramika Biokeramika – překonává plasty i kovy. • Je lehká, biologicky snášenlivá, nekoroduje. Může být připravena s řízenou pórovitostí, takže kostní tkáň do keramické protézy postupně vrůstá. • Náhrady zubů, kostí, částí kloubů.

Keramika Keramický motor • V Japonsku bylo již ověřováno – motor však zatím neschopen běžného provozu. • Z termodynamických zákonů vyplývá, že účinnost tepelných strojů roste s provozní teplotou. • Keramický motor by mohl pracovat při vyšší teplotě při snížené spotřebě paliva. • Schůdnější cesta – dílčí náhrady exponovaných dílů nebo keramické povlaky.

Keramika ve vesmíru • Keramické destičky vyvinuté pro tepelnou ochranu přistávání raketoplánu – teplota přistávání 1400 o až 1500 o. C – přesahuje teplotu tání oceli. • Strukturu destiček tvoří velmi jemná křemenná vlákna pokrytá keramickým povlakem. Asi 95% objemu destiček zaujímá prázdný prostor – nízká hustota.

Sklo

Sklo • Z fyzikálního hlediska je sklo každý amorfní, homogenní a tuhý materiál. • Vzniká nejčastěji ochlazením taveniny takovým způsobem, že nezkrystalizuje a přitom dosáhne tak vysoké viskozity, že se chová jako pevná látka. • Materiál ve sklovitém stavu lze získat také za stálé teploty (např. tavenina selenu) při dostatečně vysokém tlaku.

Sklo • Sklovité materiály nemají ostrý bod tání, v taveninu přecházejí postupně v určitém teplotním rozmezí. • V nižší teplotní oblasti vykazují další přechodovou teplotu – teplota skelného přechodu (transformační) – výrazně se mění - tuhost amorfního materiálu - koeficient teplotní roztažnosti - teprve pod touto teplotou se materiál skutečně chová jako sklo

Sklo • • • Křemenné sklo – 1330 o. C Křemičitá skla – 400 – 550 o. C Plexisklo – 105 o. C Silikonový kaučuk – -120 o. C Schopnost „zamrznutí“ neuspořádané kapaliny do sklovitého stavu záleží na : - chemické struktuře dané látky - rychlosti chlazení - tloušťce ochlazované vrstvy
![Sklo • Kritická rychlost chlazení [o. C/s] • Kritická tloušťka [cm] • Si. O Sklo • Kritická rychlost chlazení [o. C/s] • Kritická tloušťka [cm] • Si. O](http://slidetodoc.com/presentation_image_h/b79a0c917cad8e184d3b986a99226dae/image-37.jpg)
Sklo • Kritická rychlost chlazení [o. C/s] • Kritická tloušťka [cm] • Si. O 2 – 2. 10 -4 • Ge. O 2 – 7. 10 -2 • Ag – 10 10 • Si. O 2 – 4. 10 2 • Ge. O 2 – 7 • Ag – 10 -5

Sklo Křemenné sklo • Vyrábí se ze samotného roztaveného křemene – křemenného písku (1720 – 2000 o. C) – energie a technologie! • Vynikající fyzikální a chemické vlastnosti. • Bod tání křemene lze podstatně snížit přidáním tavících přísad (tavidel = soda).

Sklo

Sklo Křemičitá skla • Sodné sklo – obsahuje 25% Na 2 O, taví se při 850 o. C, příměsí je soda Na 2 CO 3 • Mnohem snáze se tvaruje za horka. • Použití sody – výrobní tajemství starověkých sklářů.

Sklo

Sklo Přírodní sklo – vltavíny (moldavity) • Jde s největší pravděpodobností o ztuhlé kapičky roztavených hornin, které byly nejprve vymrštěny do stratosféry po dopadu meteoritu v Bavorsku. • Při zpětném průletu vzdušným obalem Země se roztavily a jako horký skelný déšť dopadly do míst dnešních nalezišť, kde do nich kyselé písky za miliony let vyleptaly jemný reliéf.

Sklo • Nejstarší doklady o uměle vyrobeném skle – 5000 let před Kristem archeologická naleziště v Sýrii. • Egypt – 1000 let před Kristem vynalezena sklářská píšťala. • Staří Římané – tvarování skla do forem nebo do volného prostoru, zdobení.

Sklo • 13. století – na byzantskou tradici navázali skláři v Benátkách – ostrov Murano (požáry), křišťálové sklo.

Sklo • České sklárny – 17. století, Jablonecko, Železnobrodsko (Nový Amsterodam). • Středověk i doba renesance – vzácný a drahý materiál, průsvitnost a průhlednost skla důležitá pro jeho aplikace. • 15. století – Nizozemí – skleněné čočky – brýle, dalekohledy, mikroskopy (1606). • Dnes celosvětová výroba skla dosahuje ¼ objemu výroby železa.

Sklo • • • Sklenice Láhve Umělecké předměty Stavebnictví Chemické aparatury

Sklo • • Optické prvky Solární články Světlovodná vlákna Skelné tkaniny

Sklo • Pro každý typ skleněných výrobků byla vyvinuta nejvhodnější technologie. • Všechny výrobní technologie využívají skutečnosti, že viskozita skloviny se s teplotou plynule mění. • Tažení – ploché sklo – svislé tažení (v Čechách po 80 letech výroba ukončena) • Lití – novější technologie FLOAT – lití skloviny na vodorovnou hladinu roztaveného kovu • Lisování • Foukání

Sklo • Pozvolné chlazení každého výrobku – zabránění vzniku vnitřního pnutí. • Kompaktní sklo neobsahuje žádné vnitřní rozhraní ani vyztužující elementy – ideální prostředí pro šíření trhlin – sklo je křehké – má malou houževnatost. • Lom nastává v nejslabším místě struktury materiálu.

Sklo • Rm v tahu běžných skleněných předmětů je cca 100 MPa. • Tenká skleněná vlákna – i několik GPa. • Zvýšení pevnosti: • Pro zvýšení pevnosti se odleptává povrchová vrstva (HF) – na určitou dobu se odstraní povrchové vady.

Sklo • Další úpravy vedoucí ke zvýšení pevnosti: • Do povrchové vrstvy výrobku ze sodného skla mohou být iontovou difúzí vpraveny atomy draslíku. Protože K má rozměrnější atomy než Si, vznikne v povrchové vrstvě tlakové pnutí, které zabrání rozběhnutí trhliny. • Prudké zakalení výrobku vytvoří na povrchu tlakové pnutí kompenzované tahovým napětím v hlubších vrstvách, což vede k vyšší pevnosti.

Sklo • Po rozbití vzniknou místo velkých střepů drobné úlomky. • Částečné nahrazení atomů kyslíku v běžném skle atomy dusíku. Mezi Si a N vzniknou kovalentní vazby, sklo je pevnější v celém průřezu. • Kompozity – sklovitá matrice vyztužená drátky nebo kovovou síťkou.

Sklo • • Výroba skla: Směs surovin =„ sklářský kmen“ Hlavní součástí je křemenný písek cca 70 % + Na 2 CO 3 – soda, K 2 CO 3 – potaš, Ca. CO 3 – vápenec. • Další přísady: oxidy boru, fosforu, hliníku, hořčíku, barya, olova. • Případně střepy z recyklací – „sklářská vsádka“. • Liší se chemické složení – liší se i vlastnosti skel.

Sklo Křemenné sklo – čirý sklovitý Si. O 2 • • • Vysoká teplotní odolnost (do 1200 o. C) Nízký koeficient roztažnosti Odolné vůči teplotním rázům Vysoký elektrický odpor i při zvýšené teplotě Mimořádně odolné vůči kyselinám

Sklo Ploché sklo FLOAT • 73% Si. O 2 + 14% Na 2 O + 4% Mg. O + další příměsi • Podobné složení má lahvové sklo. • Zelené nebo hnědé zabarvení je způsobeno příměsí cca 0, 4%Fe 2 O 3 a oxidačně redukčními podmínkami.
Sklo Tepelně odolná skla • SIMAX nebo PYREX • 80% Si. O 2 + 13% B 2 O + 3% Na 2 O + 1% K 2 O

Sklo Křišťálové sklo • Složení je voleno tak, aby bylo dosaženo co nejvyššího indexu lomu. • K 2 O – Ca. O – Si. O 2 český křišťál • K 2 O – Pb. O – Si. O 2 olovnatý = anglický křišťál • Pravý olovnatý křišťál – 24% Pb. O. • Dekorativní vlastnosti olovnatého křišťálu jsou v jeho vysokém indexu lomu a výrazné závislosti indexu lomu na vlnové délce světla.

Sklo • Skleněná světlovodná vlákna. • Princip světlovodného vlákna s vnitřní vrstvou s vyšším indexem lomu. • Úplným odrazem na rozhraní mezi vnitřní a vnější vrstvou se světelný paprsek udržuje podél osy vlákna.

Sklo Skleněná vlákna pro kompozity • E – sklo neobsahuje alkálie – koroze! • Vlákna pružná, ohebná, velmi pevná, při výrobě povrchová úprava podle předpokládané aplikace. • Z materiálového hlediska důležitá pevnost v kombinaci s hustotou. • d = 0, 1 mm – Rm = 300 MPa strukturní vady! • d = 1 µm – Rm =10 GPa

Sklo • Vlákna, tkaniny, rohože, kombinace s uhlíkovými vlákny.

Stavební pojiva - maltoviny

Stavební pojiva - maltoviny • Egypt – 4000 let před Kristem – vápenosádrové malty. • Maltoviny se vyrábějí z nerostných surovin, před zpracováním jsou sypké, zrnité či práškovité. • Po přidání vody získávají pastovitou konzistenci a poté se mění v kompaktní tvrdý materiál. • V průběhu zpevňování maltovin se rozlišují 2 etapy – 1. tuhnutí – roste viskozita maltoviny • 2. tvrdnutí – maltovina je v pevném stavu, dále roste její pevnost a tvrdost.

Vápno

Vápno • Je nejstarší ze všech stavebních pojiv. • V současnosti - 19% stavebnictví • 80% jako průmyslová chemikálie v metalurgii ocelí, neželezných kovů, výroba papíru, skla. • „nehašené vápno“ = Ca. O s příměsí oxidů (Mg. O) • Příprava: tepelný rozklad přírodního vápence při teplotě větší než 800 o. C • Ca. CO 3 + teplo –> Ca. O + CO 2 „pálení vápna“ ve vápenkách

Vápno • Vápenec + koks 1: 10, 20 – 32 hodin => vzdušné vápno – tuhne na vzduchu • Hydraulické vápno – tuhne i pod vodou • Před použitím do malty nebo omítky se musí nehašené vápno „hasit“. • Ca. O + H 2 O –> Ca(OH)2 + teplo • Nedostatečně vyhašené vápno je příčinou materiálových vad. (vápno se spálí nebo utopí)

Vápno • Z hašeného vápna, písku a vody se připravují vápenné malty na zdění a omítání. • Při postupném tuhnutí a tvrdnutí na vzduchu probíhá reakce: Ca(OH)2 + CO 2 –> Ca. CO 3 + H 2 O • Kruh chemických rovnic se tak uzavírá a konečným produktem je opět tvrdý materiál jako na začátku s rozdílem, že pevně spojuje stavební prvky.

Vápno • Písek se na chemické reakci přímo nepodílí, ale přispívá k pórovitosti výsledného materiálu. • Póry usnadňují pronikání CO 2 dovnitř a H 2 O ven.

Beton

Beton • Znali už Římané – římský Pantheon postaven v letech 115 – 125 jako válcová betonová stavba zevně obložená cihlami a překrytá betonovou kupolí s průměrem 43, 2 m – nebylo překonáno dalších 1300 let. • Podstatou tuhnutí betonu je celá řada chemických reakcí cementu s vodou. • Cement (v současnosti portlandský cement) - je práškovitá směs řady anorganických látek, jejichž poměr se může značně lišit.

Beton • • Rozlišují se 3 složky cementu: alit – 3 Ca. O. Si. O 2 belit – 2 Ca. O. Si. O 2 celit – spojovací hmota s vysokým podílem železa a s krystalickým brownmilleritem 4 Ca. O. Al 2 O 3. Fe 2 O 3 Směs těchto minerálních látek vzniká v cementárně vypálením vápence Ca. CO 3 společně s hlínami a jíly v rotační peci při teplotě cca 1450 o. C.

Beton • Vzniklý „slínek“ se pak rozemele na jemný prášek, ke kterému se poté přidává ještě sádrovec Ca. SO 4. 2 H 2 O, popř. rozemletá vysokopecní struska. • Složky cementu reagují s vodou za vzniku tepla. • Reakce mohou být poměrně složité, dohromady se označují jako hydratace. • Po 28 dnech se beton považuje za uspokojivě tvrdý, ve skutečnosti tvrdnutí a zpevňování probíhá celá léta a vlastně nikdy nekončí.

Beton • Vlastní beton se připraví smícháním cementu s vodou a pískem, popř. hrubým kamenivem. • Optimální množství vody: málo – nízká pevnost betonu, mnoho – pevnost klesá, smršťování betonu, optimální množství vody je cca 0, 45 – 0, 55 • Beton obsahuje i určité množství vzduchu – pórovitost.

Beton Parametry: • Vysoká pevnost v tlaku. • Malá pevnost v tahu. • Vyztužování ocelovými tyčemi, dráty, rohožemi, v současnosti i polymerní vlákna. • Předepjatý beton – výztuž se napne do rámu ještě před ztuhnutím betonové směsi a po dokončení ztuhnutí se opět uvolní.

Sádra

Sádra • Sádrová pojiva se připravují částečnou nebo úplnou dehydratací sádrovce Ca. SO 4. 2 H 2 O. • Při teplotě 95 – 130 o. C přechází nerost sádrovec na polohydrát Ca. SO 4. ½ H 2 O. • Při 150 – 300 o. C na anhydrit Ca. SO 4, který je rozpustný ve vodě. • Podstatou sádry je polohydrát s malým podílem anhydritu.

Sádra • S vhodným množstvím vody přechází sádra zpět na sádrovec, tuhne a tvrdne. • Výchozí krystalky hemihydrátu se rozpustí ve vodě, poté se začnou vytvářet krystalky dihydrátu, které mají oproti výchozímu nižší rozpustnost ve vodě. • Výsledkem je poměrně pevná struktura tvořená vzájemně propletenými krystalky. • Tuhnutí sádry lze zpomalit – malířský klih, mléko. • Urychlit – kuchyňská sůl, síran sodný.

Sádra Uplatnění: • Stavebnictví • Umělecké předměty • Odsiřování elektráren – sádrovec – sádrokartonové desky (kompozit s vrstevnatou strukturou – kombinace papírové hmoty a sádry)

Asfalt

Asfalt • Všechny přírodní tuhé a tekuté uhlovodíky se zahrnují pod obecný termín „živice“. • Asfalt je za normální teploty tuhý, zahříváním kapalní. • Těží se přímo ze země – asfaltové jezero na ostrově Trinidad – přírodní asfalt. • Ropný asfalt – zbytek po destilaci ropy. • Podstatou asfaltu je směs uhlovodíků s vysokou molekulovou hmotností.

Asfalt • Pro vlastnosti asfaltu používaného na povrchy vozovek je důležitý poměr kameniva a pojiva. • Ideální struktura obsahuje hranaté částice různé velikosti propojené stejnoměrnou vrstvou asfaltového pojiva (5 – 10%), póry (2 – 5%) – důležité – při tlakovém namáhání asfalt vyplňuje póry místo aby byl vytlačován z prostoru mezi částicemi.

Asfalt • Novinka – asfalt plněný drcenými skleněnými střepy – využití odpadu z nevratných lahví. • Modifikace asfaltu odpady z PE – zvýšení pružnosti a odolnosti praskání za nízkých teplot – využití v místech vyššího dynamického namáhání – např. mostní vozovky.

Asfalt – Zikkurat v Uru – původní asfalt

Geopolymery
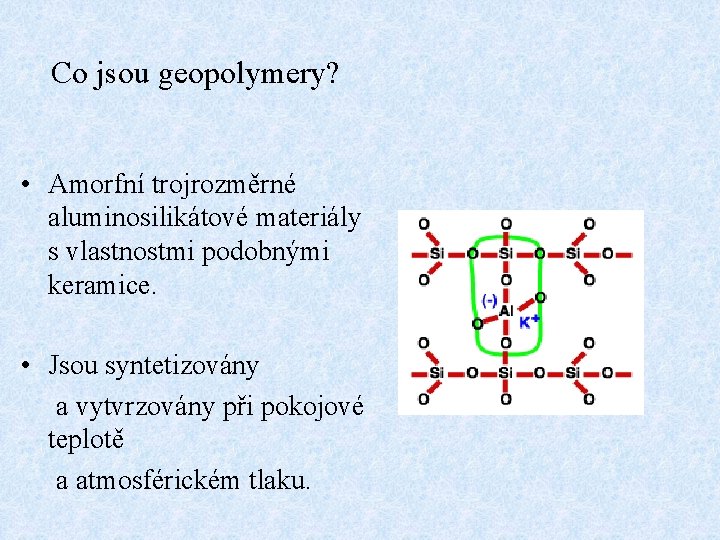
Co jsou geopolymery? • Amorfní trojrozměrné aluminosilikátové materiály s vlastnostmi podobnými keramice. • Jsou syntetizovány a vytvrzovány při pokojové teplotě a atmosférickém tlaku.
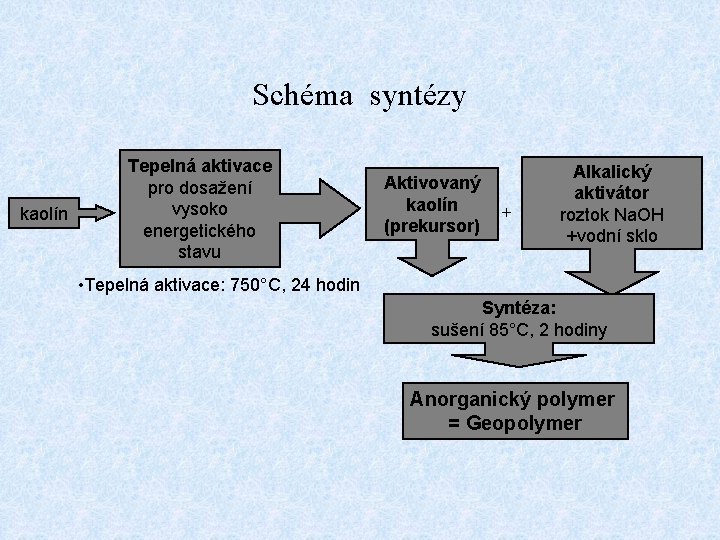
Schéma syntézy kaolín Tepelná aktivace pro dosažení vysoko energetického stavu Aktivovaný kaolín (prekursor) + Alkalický aktivátor roztok Na. OH +vodní sklo • Tepelná aktivace: 750°C, 24 hodin Syntéza: sušení 85°C, 2 hodiny Anorganický polymer = Geopolymer

Chemická struktura a aplikace

Aplikace • Nová generace materiálů, které mohou být použité čisté, s plnivy nebo vyztužujícími vlákny pro různé aplikace. • Automobilový a letecký průmysl, formy pro odlévání kovů, zapouzdření odpadů, dekorace, opravy budov.

Aplikace

Děkuji za pozornost.
- Slides: 89