Aniones Empaquetamiento compacto Cbico Hexagonal o cbico simple

Aniones – Empaquetamiento compacto (Cúbico ó Hexagonal) o cúbico simple Cationes – Huecos cúbicos, octaédricos o tetraédricos -La clasificación de Lima de Faria se basa en definir ambas cuestiones mediante superíndices sobre fórmulas tipo Ej. cb o t Na. Cl Ca. F 2 } AX AX 2 Cationes (ocupan los huecos octaédricos) A 2 o. Xh (Doble de cationes que de aniones) -No todas las combinaciones son posibles. - Ej. A 2 o. Xh no lo es. (¿Por qué? ) { Aniones (en EHC) c h sc
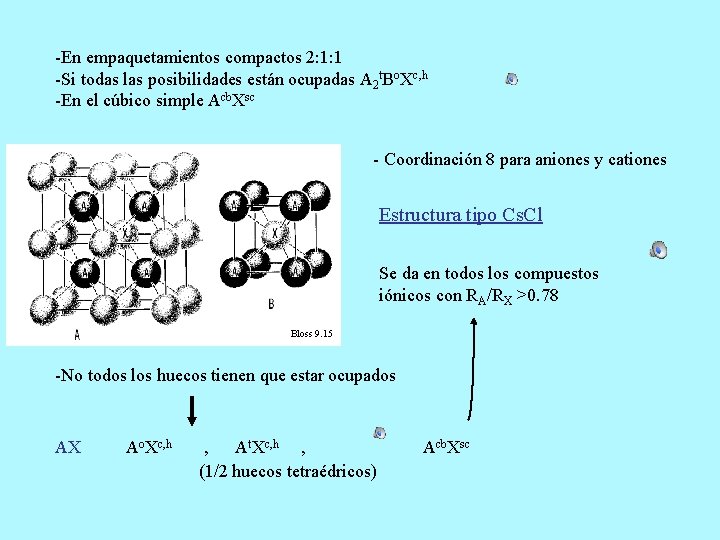
-En empaquetamientos compactos 2: 1: 1 -Si todas las posibilidades están ocupadas A 2 t. Bo. Xc, h -En el cúbico simple Acb. Xsc - Coordinación 8 para aniones y cationes Estructura tipo Cs. Cl Se da en todos los compuestos iónicos con RA/RX >0. 78 Bloss 9. 15 -No todos los huecos tienen que estar ocupados AX Ao. Xc, h , At. Xc, h , (1/2 huecos tetraédricos) Acb. Xsc
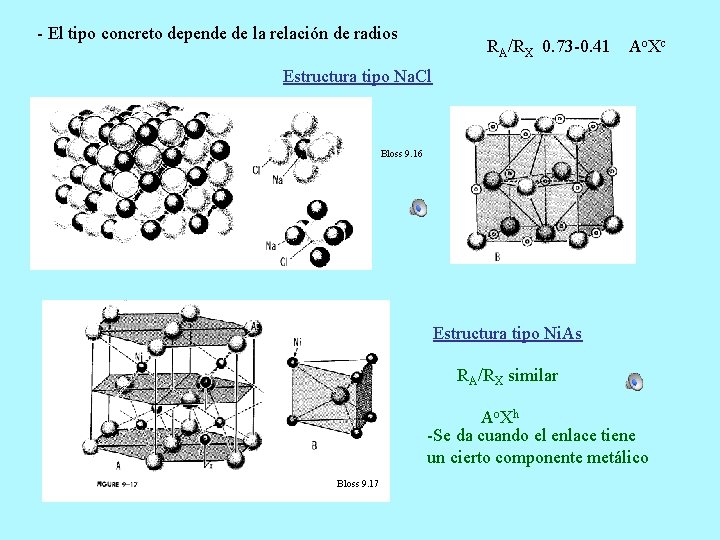
- El tipo concreto depende de la relación de radios RA/RX 0. 73 -0. 41 Ao Xc Estructura tipo Na. Cl Bloss 9. 16 Estructura tipo Ni. As RA/RX similar Ao Xh -Se da cuando el enlace tiene un cierto componente metálico Bloss 9. 17
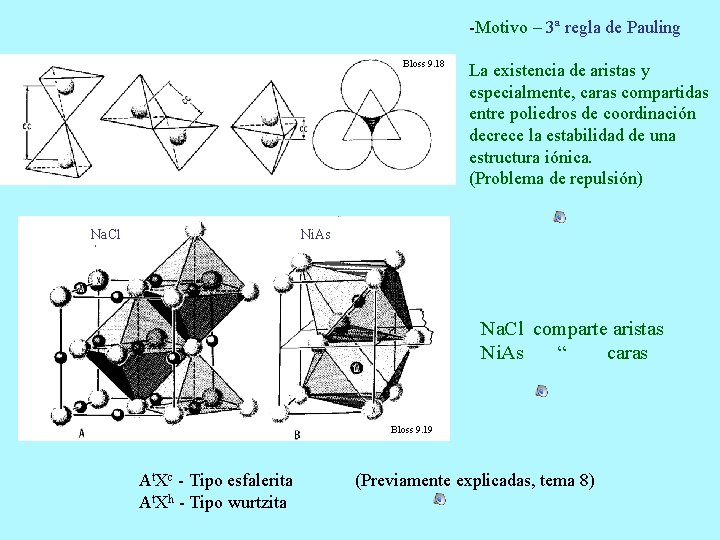
-Motivo – 3ª regla de Pauling Bloss 9. 18 Na. Cl La existencia de aristas y especialmente, caras compartidas entre poliedros de coordinación decrece la estabilidad de una estructura iónica. (Problema de repulsión) Ni. As Na. Cl comparte aristas Ni. As “ caras Bloss 9. 19 At. Xc - Tipo esfalerita At. Xh - Tipo wurtzita (Previamente explicadas, tema 8)
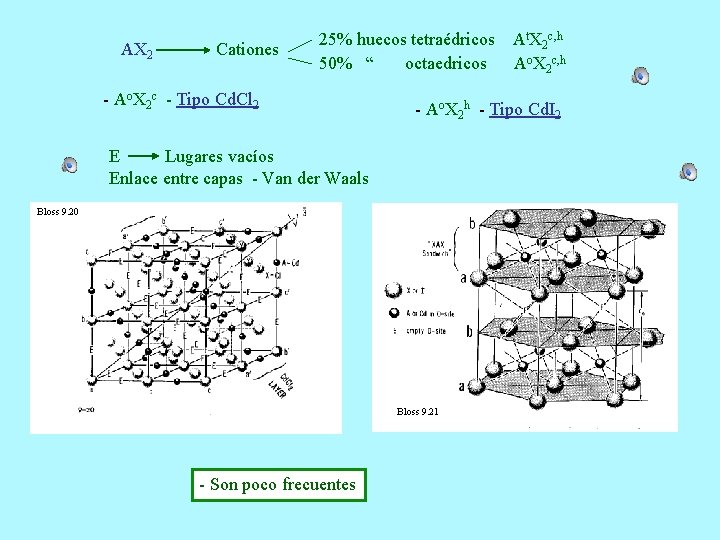
AX 2 Cationes 25% huecos tetraédricos 50% “ octaedricos - Ao. X 2 c - Tipo Cd. Cl 2 - Ao. X 2 h - Tipo Cd. I 2 E Lugares vacíos Enlace entre capas - Van der Waals Bloss 9. 20 Bloss 9. 21 - Son poco frecuentes At. X 2 c, h Ao. X 2 c, h
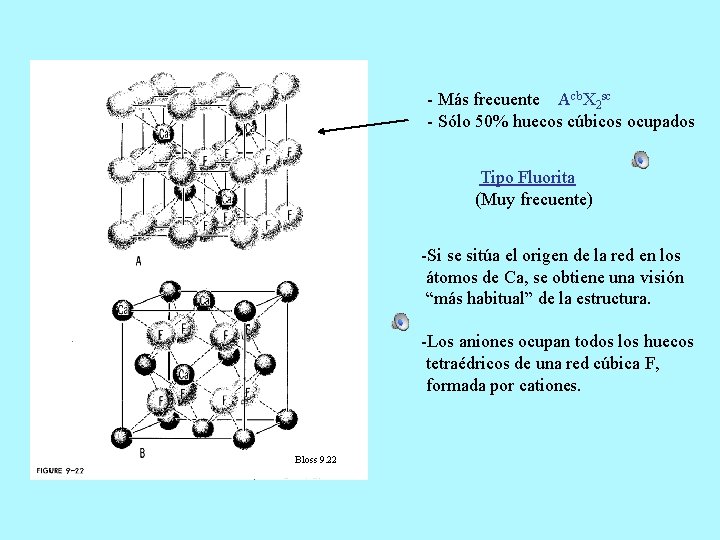
- Más frecuente Acb. X 2 sc - Sólo 50% huecos cúbicos ocupados Tipo Fluorita (Muy frecuente) -Si se sitúa el origen de la red en los átomos de Ca, se obtiene una visión “más habitual” de la estructura. -Los aniones ocupan todos los huecos tetraédricos de una red cúbica F, formada por cationes. Bloss 9. 22
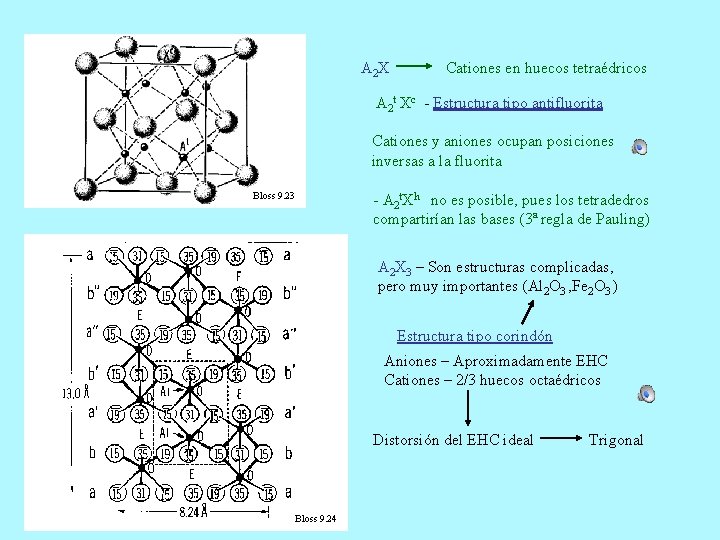
A 2 X Cationes en huecos tetraédricos A 2 t Xc - Estructura tipo antifluorita Cationes y aniones ocupan posiciones inversas a la fluorita Bloss 9. 23 - A 2 t. Xh no es posible, pues los tetradedros compartirían las bases (3ª regla de Pauling) A 2 X 3 – Son estructuras complicadas, pero muy importantes (Al 2 O 3 , Fe 2 O 3 ) Estructura tipo corindón Aniones – Aproximadamente EHC Cationes – 2/3 huecos octaédricos Distorsión del EHC ideal Bloss 9. 24 Trigonal
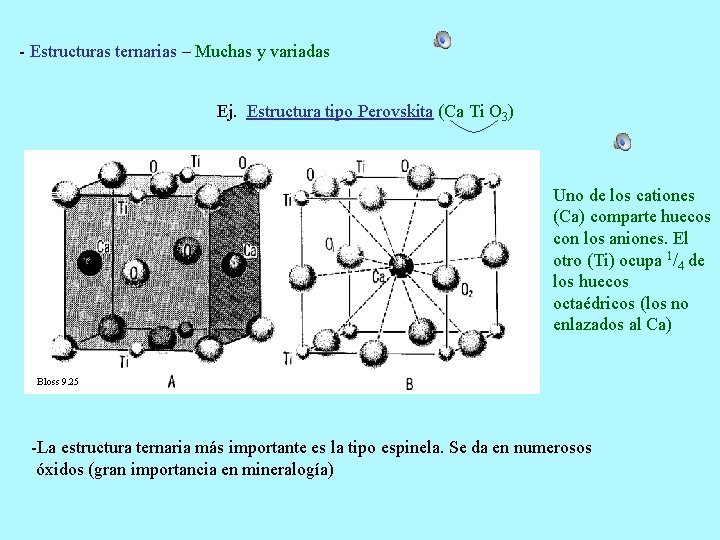
- Estructuras ternarias – Muchas y variadas Ej. Estructura tipo Perovskita (Ca Ti O 3) Uno de los cationes (Ca) comparte huecos con los aniones. El otro (Ti) ocupa 1/4 de los huecos octaédricos (los no enlazados al Ca) Bloss 9. 25 -La estructura ternaria más importante es la tipo espinela. Se da en numerosos óxidos (gran importancia en mineralogía)

Una estructura derivada se obtiene mediante la supresión de algún elemento de simetría de la estructura básica de la que deriva Subgrupo de simetría - Dos tipos Esfalerita Estructuras de substitución Calcopirita Zn Cu Fe (Cu Fe S 2) - Celdilla de arriba celdilla de abajo Una celdilla completa de la derivada necesita dos de la básica Bloss 9. 28 Cúbico Tetragonal (parámetro c doble)
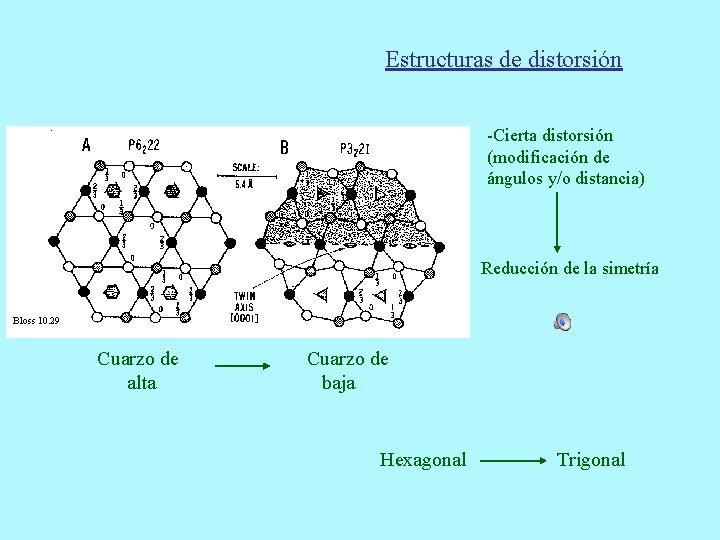
Estructuras de distorsión -Cierta distorsión (modificación de ángulos y/o distancia) Reducción de la simetría Bloss 10. 29 Cuarzo de alta Cuarzo de baja Hexagonal Trigonal
- Slides: 10