ANALISIS KARBOHIDRAT dan SERAT MAKANAN Copyright Dr Joko

ANALISIS KARBOHIDRAT dan SERAT MAKANAN Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 1

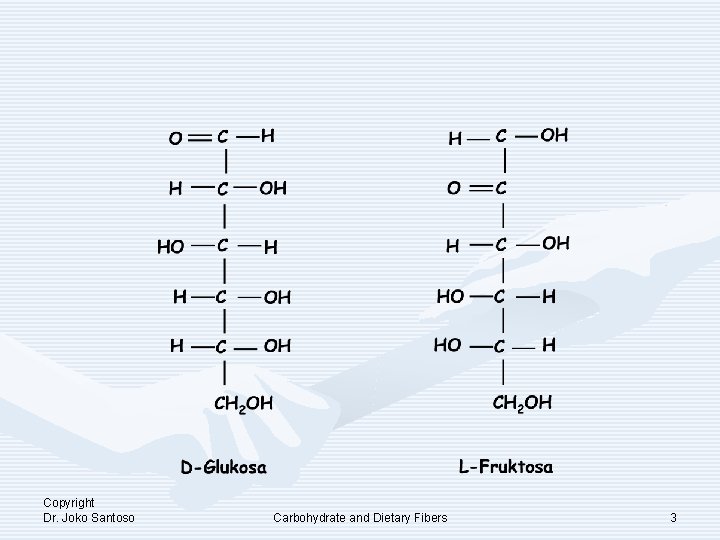
ANALISIS KARBOHIDRAT KH adalah polihidroksi ALDEHID atau polihidroksi KETONE atau kalau dihidrolisis menghasilkan salah satu atau keduanya (polihidroksi aldehid dan atau polihidroksi keton) Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 2
Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 3

Klasifikasi karbohidrat: 1. Monosakarida: suatu molekul yang terdiri dari lima atau enam atom C. 2. Oligosakarida: polimer dari 2 -10 monosakarida. 3. Polisakarida: polimer >10 monosakarida. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 4

• Karena struktur monosakarida hydroxyaldehida atau ketone terbuka maka monosakarida sangat reaktif. • Monosakarida maupun oligosakarida dengan demikian mudah mengalami ENOLISASI sehingga dapat mereduksi Cu 2+ dan Fe(CN)63 GULA PEREDUKSI. • Polisakarida (KH) bila dihidrolisis akan menghasilkan: – MONOSAKARIDA – HIDROKSI ALDEHIDE – HIDROKSI KETONE Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 5

Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 6

• Dalam proksimat analisis: Total KH selalu dihitung dengan % BY DIFFERENCE % KH = 100% - (%Air + %Abu + %Lemak + %Protein) Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 7
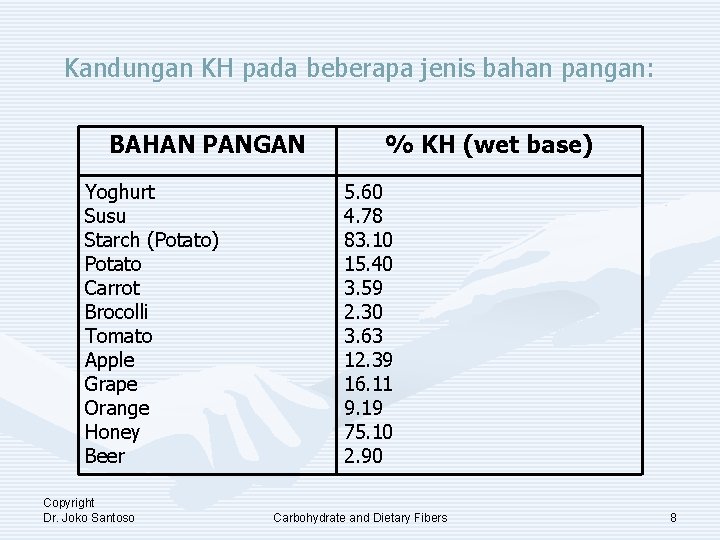
Kandungan KH pada beberapa jenis bahan pangan: BAHAN PANGAN Yoghurt Susu Starch (Potato) Potato Carrot Brocolli Tomato Apple Grape Orange Honey Beer Copyright Dr. Joko Santoso % KH (wet base) 5. 60 4. 78 83. 10 15. 40 3. 59 2. 30 3. 63 12. 39 16. 11 9. 19 75. 10 2. 90 Carbohydrate and Dietary Fibers 8

Untuk analisis gula dapat digunakan berbagai metode: 1. Metode Reduksi: (a). LANE-EYNON (b). MUNSEN-WALKER (c). NELSON-SOMOGYI (d). ALKALINE-FERRICYANIDE (e). PHENOL-SULFURIC (f). ANTHRONE (g). COLORIMETRY Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 9

Untuk analisis gula dapat digunakan berbagai metode: 2. 3. 4. 5. Polarimetri Metode FISIK Densimetri Refraktometri Lain-lain (Enzimatik, Kromatografi, Instrument). Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 10
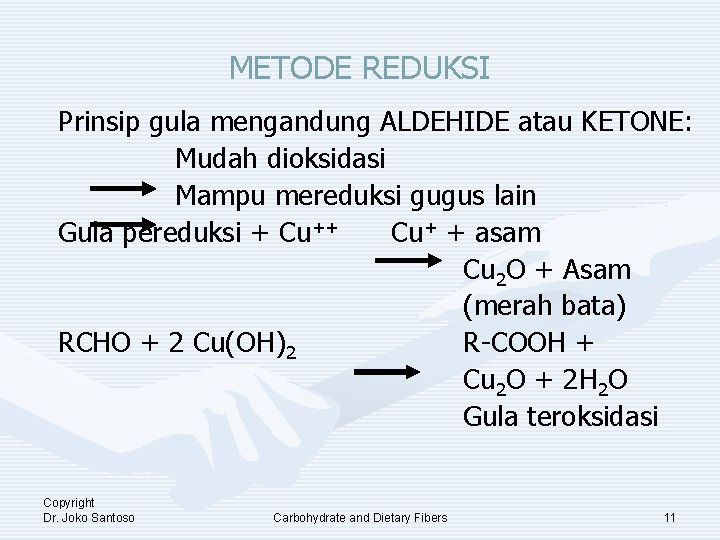
METODE REDUKSI Prinsip gula mengandung ALDEHIDE atau KETONE: Mudah dioksidasi Mampu mereduksi gugus lain Gula pereduksi + Cu+ + asam Cu 2 O + Asam (merah bata) RCHO + 2 Cu(OH)2 R-COOH + Cu 2 O + 2 H 2 O Gula teroksidasi Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 11

METODE REDUKSI Analisis dengan: Gravimetri Titrasi/Volumetri Spektrofotometri Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 12

Persiapan sampel: • Sampel dalam bentuk cair dibuat basa + Ca. CO 3 agar asam-asam yang terdapat dalam sampel tidak menghidrolisis gula yang ada selama pemanasan. Pemanasan menginaktivasi enzim-enzim penghidrolisa gula. • Untuk menghilangkan pigmen, SENYAWA BERWARNA dan SENYAWA KOLOID + Pb-asetat basa. Kelebihan Pb-asetat dihilangkan dengan penambahan Na/K-OKSALAT Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 13

Persiapan sampel: • Jika sampel berbentuk padat, perlu dilakukan ekstraksi dengan alcohol 80 % untuk mengekstrak gula yang ada disampel. Kebanyakan gula sensitive terhadap alcohol dengan konsentrasi tinggi alkohol perlu dihilangkan dengan pemanasan rendah. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 14

METODE NELSON-SOMOGYI adalah modifikasi dari Metode MUNSON-WALKER Prinsip: • Reaksi antara Cu 2 O dengan Arseno-molybdate (Ammonium molybdate = ((NH 4)6 Mo 7 O 24) + Sodium Arsenate Na 2 HAs. O 7 didalam H 2 SO 4. • Menghasilkan warna biru, ukur λ 500 -520 nm. Pereaksi: (i) Pereaksi tembaga sulfat (ii) Pereaksi arsenomolibdat (iii) Larutan glukosa standar Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 15

METODE FERISIANIDA BASA Prinsip : Pada p. H>10. 5, gula akan mereduksi FERISIANIDA FEROSIANIDA yang akan bereaksi dengan ion feri membentuk senyawa biru Prussian yang dapat diukur intensitasnya λ 700 nm. Pereaksi: 1. Larutan Sianida basa 2. Larutan Pottasium ferisianida 0. 05% (w/v) dalam air 3. Larutan feriamonium sulfat. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 16

PHENOL SULFURIC ACID Metode ini: - sederhana - cepat - Universal Untuk total KH dalam pangan baik untuk gula pereduksi dan nonpereduksi Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 17

• Prinsip: Reaksi KH dengan phenol dalam keadaan asam kuat, menghasilkan panas, diikuti pemanasan 25 -30 o. C selama 20 menit Terjadi dehidrasi KH sehingga terbentuk FURFURAL dan HYDROXYMETHYL FURFURAL, produk ini berkondensasi dengan PHENOL muncul warna YELLOWORANGE λ 480 nm = PENTOSE λ 490 NM = HEXOSE Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 18

Metode VOLUMETRIK (MUNSON- WALKER) • Titrasi Cuprouse oxide dengan permanganate: Cu 2 O + Fe 2(SO 4)3 2 Fe. SO 4 + Cu. SO 4 +Cu. O 10 Fe. SO 4 + 2 KMn. O 4 + 8 H 2 SO 4 5 Fe 2(SO 4)3 + K 2 SO 4 + 2 Mn. SO 4 + 8 H 2 O • Konversi Cu. O terhadap gula dapat dilihat dari tabel. • Metode ini kurang sensitive (> 5 mg glukosa/5 ml). Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 19
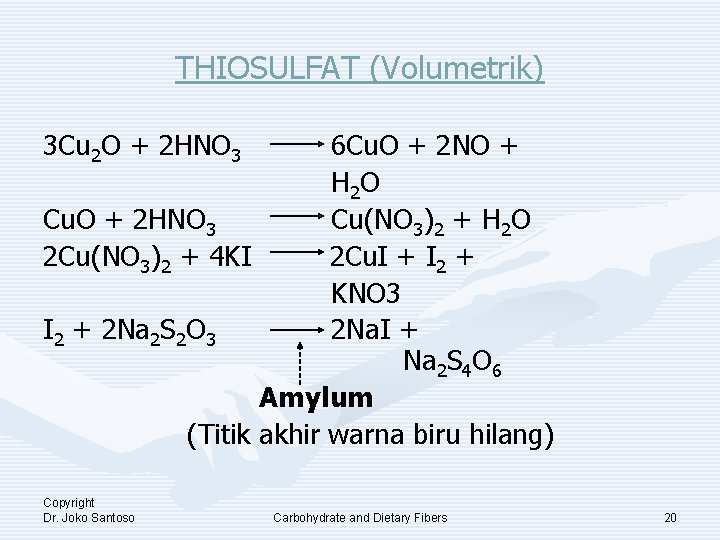
THIOSULFAT (Volumetrik) 3 Cu 2 O + 2 HNO 3 6 Cu. O + 2 NO + H 2 O Cu. O + 2 HNO 3 Cu(NO 3)2 + H 2 O 2 Cu(NO 3)2 + 4 KI 2 Cu. I + I 2 + KNO 3 I 2 + 2 Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 Amylum (Titik akhir warna biru hilang) Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 20

LANE-EYNON (Volumetrik) • Biasanya digunakan untuk penentuan LAKTOSA (anhidrat atau monohidrat) GLUKOSA, FRUKTOSA, MALTOSA (anhidrat atau monohidrat). • Penetapan gula pereduksi dengan metode ini didasarkan atas pengukuran volume larutan gula pereduksi standar yang dibutuhkan untuk mereduksi pereduksi tembaga basa yang diketahui volumenya. • Titik akhir titrasi ditunjukkan dengan Metilen Biru yang warnanya akan hilang, karena kelbihan gula pereduksi diatas jumlah yang dibutuhkan untuk mereduksi semua tembaga. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 21

Pereduksi: (i) Larutan tembaga sulfat (ii) Larutan tartrat basa (iii) Larutan Fehling (iv) Larutan Dekstrosa standar (v) Larutan Metilen Blue 0, 2% dalam air Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 22

COLORIMETRI • Gula pereduksi bereaksi dengan 2. 3. 5 Triphenyl Tetrazolium Bromide atau Chloride > p. H 12. 5 yang menghasilkan warna kompleks TRIPHENYL FORMAZON (Pink-Violet-Blue) λ 485 nm. • Gula pereduksi bereaksi dengan 3. 5 Dinitrosalicylate dalam keadaan basa menghasilkan warna Red-Brown. • Karbohidrat dapat bereaksi dengan Resorcinol warna kompleks • Karbohidrat dapat bereaksi dengan Orcinol warna kompleks Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 23

METODE SHAFFER-SOMOGYI • Segala jenis bahan pangan terutama yang mengandung sedikit gula pereduksi Prinsip: • Gula pereduksi akan mereduksi Cu 2+ Cu+ • Cu+ dioksidasi oleh I 2 (hasil oksidasi KI oleh KIO 3 dalam asam) Cu 2+ kembali • Kelebihan I 2 dititrasi dengan Na 2 S 2 O 3 Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 24

Pereaksi: (1) Larutan Tembaga sulfat (2) Larutan Kalium Iodat 0. 1 N (3) Pereaksi Shaffer-Somogyi (4) Larutan Iodida-kalium oksalat (5) Larutan Natrium tiosulfat standar (6) Larutan asam sulfat (7) Larutan pati untuk indikator Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 25

METODE ANTHRONE • Prinsip: – Anthrone (9, 10 -dihydro-9 -oxanthra-cene) merupakan hasil reduksi anthraquinone – Anthrone bereaksi secara spesifik dengan KH dalam asam sulfat pekat menghasilkan warna biru kehijauan khas Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 26

METODE CLEG-ANTHRONE untuk TOTAL AVAILABLE CARBOHYDRATE Prinsip: Bahan di-digest dengan menggunakan asam perklorat, pati yang terhidrolisa bersama-sama dengan gula yang larut dapat bereaksi dengan anthrone membentuk warna biru kehijauan dapat ditentukan jumlahnya secara kolorimetrik (dinyatakan sebagai persen glukosa). Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 27

METODE DNS Prinsip: Dalam suasana alkali gula pereduksi akan mereduksi 3, 5 -dinitrosolisilat (DNS) membentuk senyawa yang dapat diukur absorbannya pada λ 550 nm Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 28

METODE ENZIMATIS 1. Metode D-Sorbitol 2. Metode Lactose-D-galactose – Lactose β-galactose – D-Galactose + D-Glucose β-galactose Dehydrogenase D-Galactonic acid + NADH + H+ NADH diukur pada 334, 340 atau 365 nm. 3. Metode Maltose/Sucrose/D-glucose Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 29
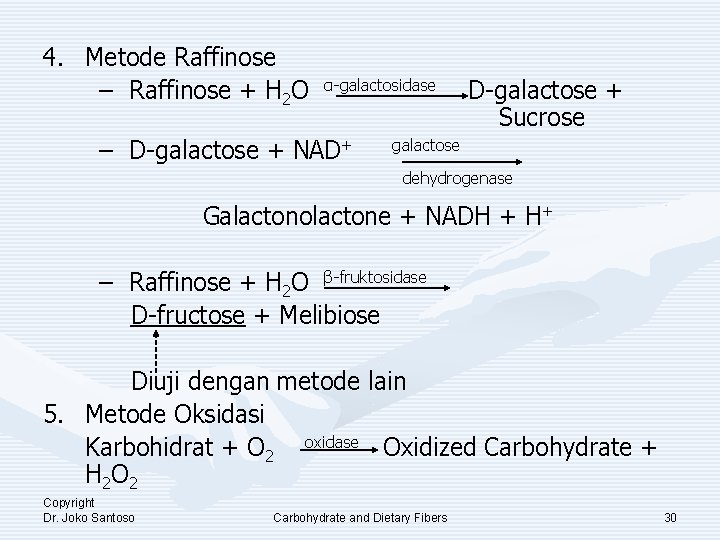
4. Metode Raffinose – Raffinose + H 2 O α-galactosidase – D-galactose + NAD+ D-galactose + Sucrose galactose dehydrogenase Galactonolactone + NADH + H+ – Raffinose + H 2 O β-fruktosidase D-fructose + Melibiose Diuji dengan metode lain 5. Metode Oksidasi Karbohidrat + O 2 oxidase Oxidized Carbohydrate + H 2 O 2 Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 30

PENETAPAN SERAT KASAR • Serat kasar merupakan residu dalam bahan makanan atau pertanian setelah diperlakukan dengan asam dan alkali mendidih dan terdiri dari sellulosa dengan sedikit lignin dan pentosan. Pereaksi: (1). Antifoam Agent (2). Asbes (3). Larutan H 2 SO 4 (4). Na. OH (5). Larutan K 2 SO 4 (6). Alkohol Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 31

PENETAPAN DIETERY FIBER • Bagian dari komponen bahan pangan nabati yang tidak dapat dicerna oleh saluran pencernaan manusia. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 32

Berdasarkan fungsinya dalam tanaman DF dibagi menjadi 3 fraksi utama: 1. POLISAKARIDA STRUKTURAL: terdapat dalam dinding sel dan terdiri dari selulosa dan polisakarida non-selulosa (hemiselulosa dan substansi pektat). 2. NON POLISAKARIDA STRUKTURAL: lignin. 3. POLISAKARIDA NON STRUKTURAL: termasuk gum dan mucilage serta polisakarida lain seperti karagenan dan agar. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 33

METODE VAN SOEST dan modifikasinya Masih banyak digunakan (mudah dan relatif cepat). Kadar ADF (Acid Detergent Fiber) Kadar NDF (Neutral Detergent Fiber) Penetapan komponen dietery fiber lainnya dapat ditentukan dengan metode lain. § METODE KLASON Penetapan lignin § METODE SPEKTROFOTOMETRI Substansi pelarut § Kadar Hemiselulosa selisih Kadar NDF dengan ADF § Kadar Selulosa selisih kadar NDF dengan lignin § Total DF Kadar NDF + Substansi Pektat. Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 34

PENETAPAN ADF Prinsip: • Sampel diekstrak dengan larutan ADF (Setiltrimetil ammonium bromide dalam H 2 SO 4 1 N) sehingga seluruh komponen selain komponen ADF larut. • Komponen yang tidak larut disaring, dikeringkan, ditimbang, dan dikoreksi dengan kandungan mineral yang ada dalam komponen tersebut dengan cara menyabunkan sehingga yang tinggal hanya mineral saja. Pereaksi: i. Larutan ADF (20 g setil trimetil ammonium bromide dalam 1 lt H 2 SO 4 1 N) ii. Aseton Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 35

PENETAPAN NDF Prinsip: • Sampel diekstrak dengan larutan NDF sehingga seluruh komponen selain komponen NDF larut. • Komponen yang tidak larut disaring, dikeringkan, ditimbang dan dikoreksi dengan kandungan mineral. • Untuk sampel yang mengandung pati, maka patinya harus dihidrolisa dengan enzim α-amilose, jika tidak pati tersebut akan menyulitkan dalam pengeringan. Pereaksi: 1. Larutan NDF (18, 61 g EDTA-2 Na, 6. 81 g Na 2 B 4 O 7. 10 H 2 O, 30 g Sodium Lauril Sulfat, 4. 56 g Na 2 HPO 4 dan 10 ml 2 -etoksi-etanol dilarutkan sampai 1 liter sehingga p. H 6, 4 -7, 1). 2. Larutan α-amilase (1 g α-amilase dimasukkan dalam 1 liter buffer phospat). 3. Aseton Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 36

PENETAPAN LIGNIN Prinsip: Mula-mula sampel diekstrak dengan larutan ADF sehingga seluruh komponen selain selulosa dan lignin larut. Selulosa yang ada dalam residu diihidrolisa dengan H 2 SO 4 72% sehingga yang tertinggal hanya residu lignin. Pereaksi: (1). Larutan ADF (2). Larutan H 2 SO 4 72% (w/v) (3). Aseton Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 37

PENETAPAN SUBSTANSI PEKTAT (a). Metode Kolorimetrik – Mc. Cready dan Mc Comb (1952) yang dimodifikasi oleh Blumenkrentz-dan Arboc Hansen (1973). – Penetapannya didasarkan pada reaksi antara ohidroksidifenil dengan anhidrogalakturonat yang menghasilkan warna dan diukur pada λ 520 nm. Pereaksi: 1. Larutan versen 0. 5% 2. Larutan tetraborat dalam sulfat 3. Larutan o- hidroksidifenil 4. Na. OH 0. 05 N Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 38

(b). Metode Gravimetrik – Pektin yang telah diekstrak disaponifikasi dengan alkali dan diendapkan sebagai kalium pektat dengan penambahan kalsium klorida dalam suasana asam. – Endapan kalsium pektat dicuci sampai bebas klorida, dikeringkan ditimbang. Pereaksi: 1. Asam asetat 1 N 2. Kalsium klorida 1 N 3. Perak nitrat 1% 4. HCl 0. 05 N Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 39
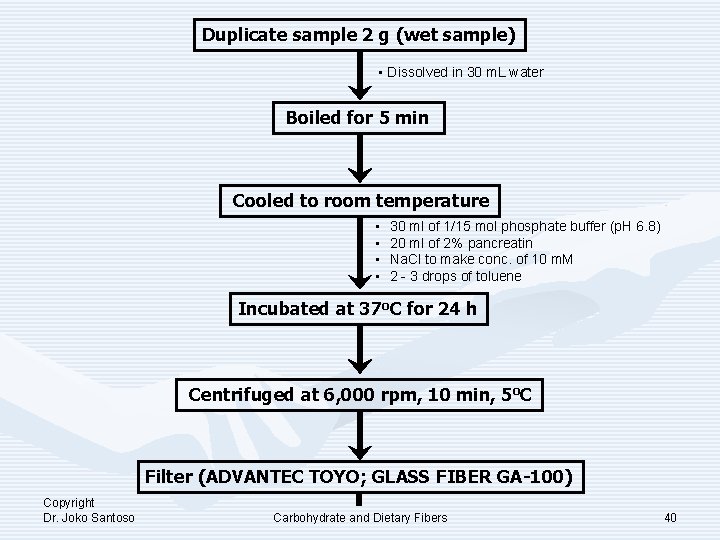
Duplicate sample 2 g (wet sample) • Dissolved in 30 m. L water Boiled for 5 min Cooled to room temperature • • 30 ml of 1/15 mol phosphate buffer (p. H 6. 8) 20 ml of 2% pancreatin Na. Cl to make conc. of 10 m. M 2 - 3 drops of toluene Incubated at 37 o. C for 24 h Centrifuged at 6, 000 rpm, 10 min, 5 o. C Filter (ADVANTEC TOYO; GLASS FIBER GA-100) Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 40
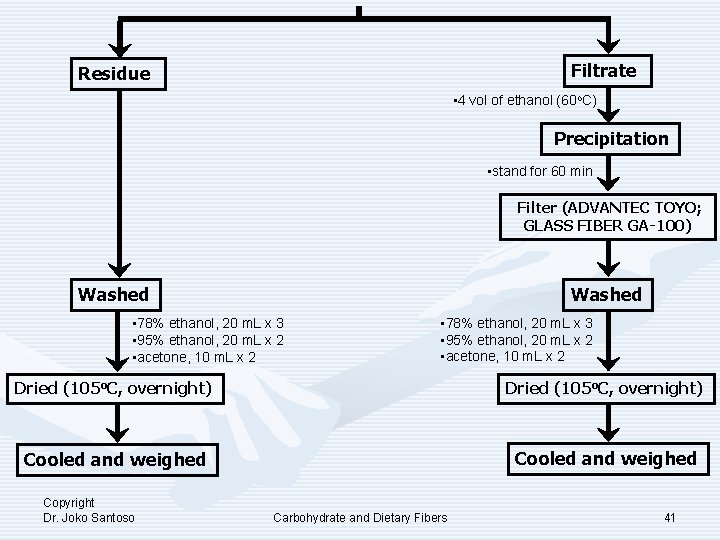
Filtrate Residue • 4 vol of ethanol (60 o. C) Precipitation • stand for 60 min Filter (ADVANTEC TOYO; GLASS FIBER GA-100) Washed • 78% ethanol, 20 m. L x 3 • 95% ethanol, 20 m. L x 2 • acetone, 10 m. L x 2 Dried (105 o. C, overnight) Cooled and weighed Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 41
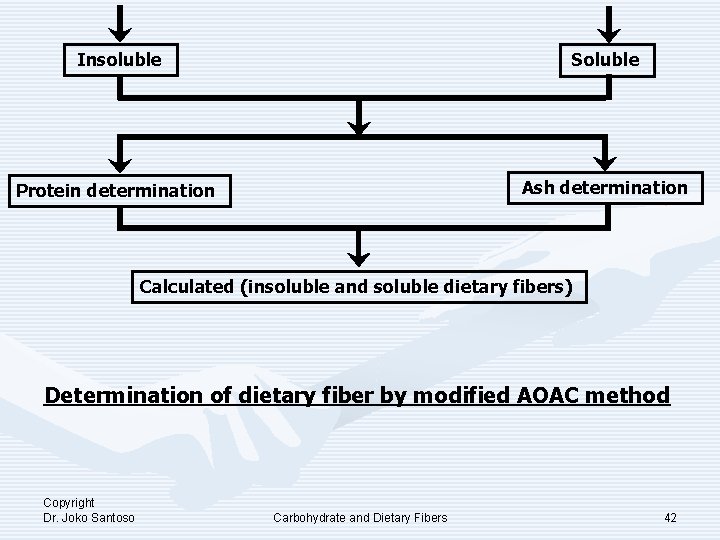
Insoluble Soluble Protein determination Ash determination Calculated (insoluble and soluble dietary fibers) Determination of dietary fiber by modified AOAC method Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 42

TERIMA KASIH Copyright Dr. Joko Santoso Carbohydrate and Dietary Fibers 43
- Slides: 43