Analisador Submersvel de Rendimento Fotossinttico DIVINGPAM Informaes Gerais

Analisador Submersível de Rendimento Fotossintético DIVING-PAM

Informações Gerais • Avaliação rápida e confiável do rendimento da conversão da energia luminosa em energia química durante a fotossíntese – Chamado de rendimento quântico (RQ) • Efetivo (RQE) • Potencial (RQP) – Analisa efetivamente apenas as reações luminosas da fotossíntese (fase “clara”) • PS II λ < 670 ηm

• Ideal para atividades de campo – Princípio PAM permite tolerar uma razão de sinal de 1: 105 entre a fluorescência da amostra e o ruído de fundo – Varreduras rápidas do desempenho fotossintético – Suporta até 50 m de profundidade

• Iluminação com pulso de luz de amplitude modulada (PAM) = saturação aplicada em frequência – Detecção seletiva do rendimento da fluorescência da clorofila • Determinação do RQ • Determinação da taxa de transporte de elétrons relativa (r. ETR) • Determinação de parâmetros fotossintéticos – Aplicação de pulso saturante • Suprime rendimento fotoquímico a zero • Induz máximo rendimento da fluorescência • Dispersão de energia por calor não varia

Operação Básica • Fácil • Tela de cristal líquido e um teclado foto-sensível com 8 teclas • Após a execução de uma função, todos os dados gerados são armazenados na memória
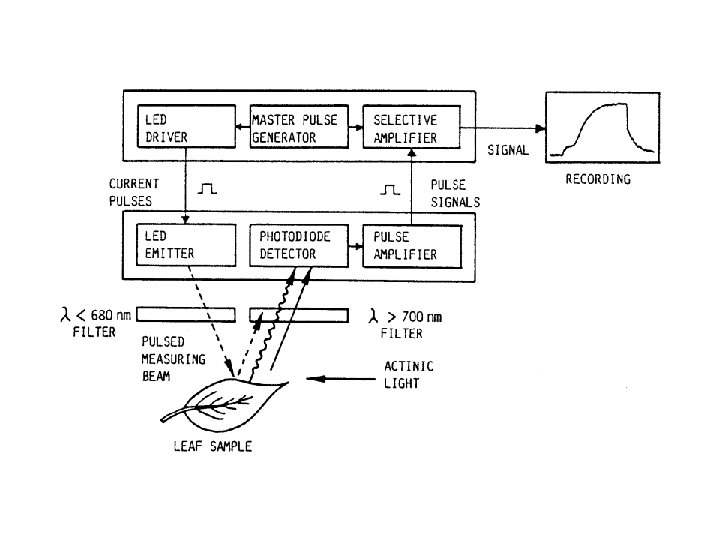

Condições para uma Boa Análise • Necessidade de ajuste dos parâmetros de iluminação às características do modelo investigado – – – Intensidade da luz basal Ganho Intensidade do pulso saturante Tempo de aplicação do pulso saturante Outros

• Distância amostra : fibra óptica aprox. 10 mm • Durante as leituras, a disposição entre o cabo de fibra óptica e a amostra não pode variar • Ajustar função auto-zero, evitando ruídos • Medidas de rendimento quântico só fazem sentido se as condições de iluminação forem bem controladas – Tomada de dados em condição “steady-state” – Iluminação abaixo da condição de saturação

• Temperatura e intensidade luminosa devem ser registradas • Em campo: – Local de coleta de dados sobre fluorescência = às de intensidade luminosa pelo fotômetro • Bateria com voltagem inferior a 8. 0 V – Problema! – Medidas tornam-se errôneas
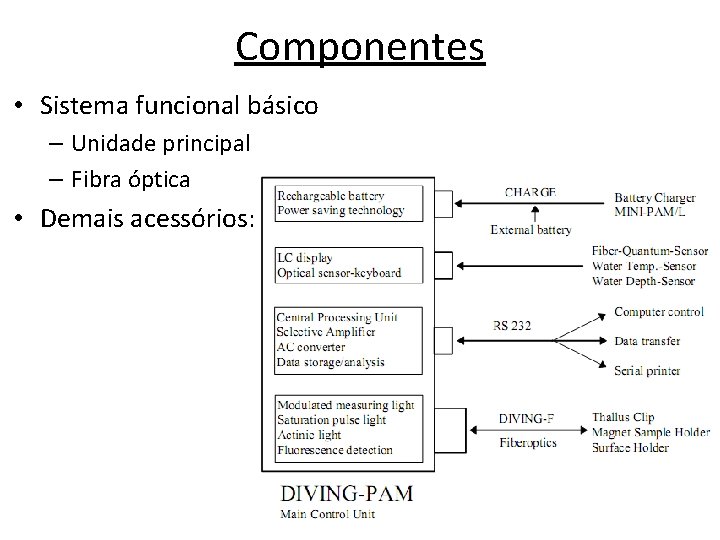
Componentes • Sistema funcional básico – Unidade principal – Fibra óptica • Demais acessórios:

Medidas de Fluorescência da Clorofila com o Diving-PAM • Equipamento inovador: permitiu extender o estudo in situ da fotossíntese para o universo subaquático • Por quê a fluorescência da clorofila pode ser indicadora da qualidade do aparato fotossintético de organismos fotossintetizantes?
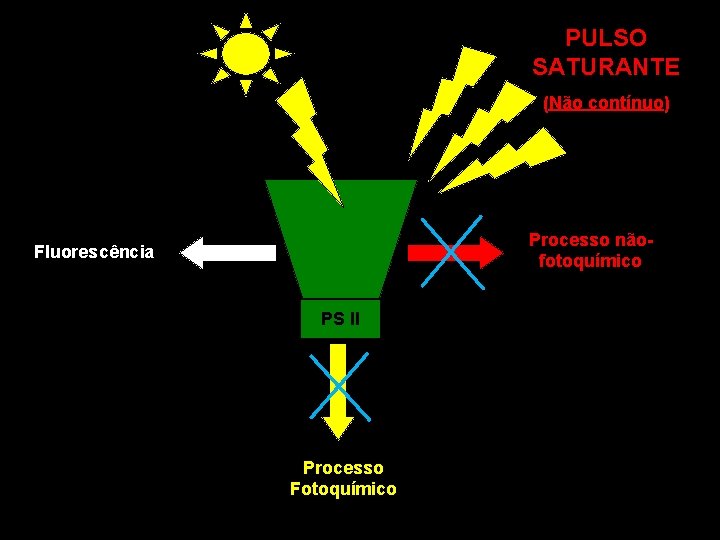
PULSO SATURANTE (Não contínuo) Processo nãofotoquímico Fluorescência PS II Processo Fotoquímico
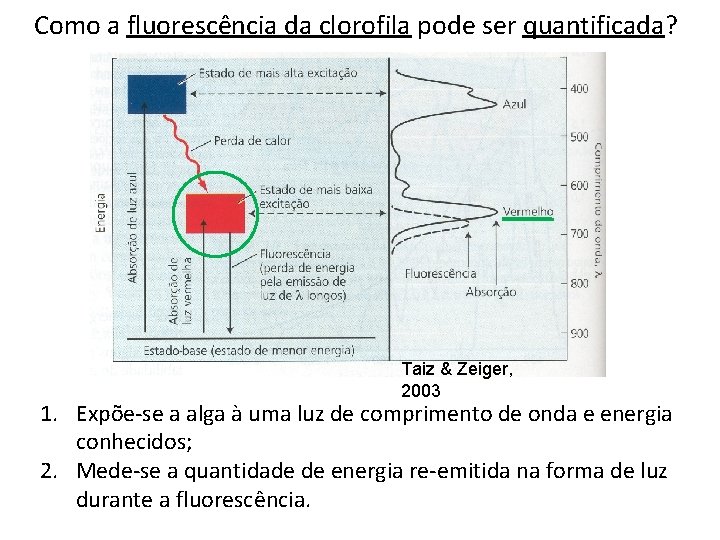
Como a fluorescência da clorofila pode ser quantificada? Taiz & Zeiger, 2003 1. Expõe-se a alga à uma luz de comprimento de onda e energia conhecidos; 2. Mede-se a quantidade de energia re-emitida na forma de luz durante a fluorescência.
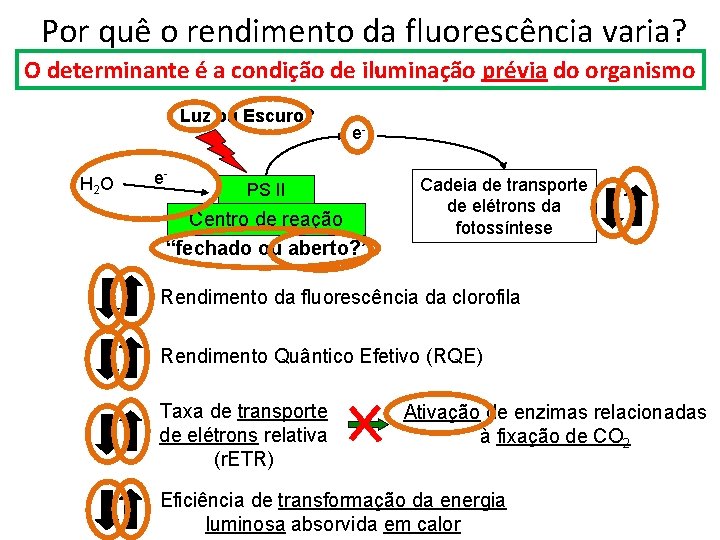
Por quê o rendimento da fluorescência varia? O determinante é a condição de iluminação prévia do organismo Luz ou Escuro? H 2 O e- e- PS II Centro de reação “fechado ou aberto? ” Cadeia de transporte de elétrons da fotossíntese Rendimento da fluorescência da clorofila Rendimento Quântico Efetivo (RQE) Taxa de transporte de elétrons relativa (r. ETR) Ativação de enzimas relacionadas à fixação de CO 2 Eficiência de transformação da energia luminosa absorvida em calor

Aplicações da Fluorescência da Clorofila • pode detectar variações de maneira rápida e pouco invasiva • útil no estudo de aclimatação à diferentes microambientes

• pode fornecer informações sobre a eficiência fotossintética de algas expostas a estressores ambientais – – – – Alta irradiância UV Temperatura Hídrico Toxinas Depleção de nutrientes Outros
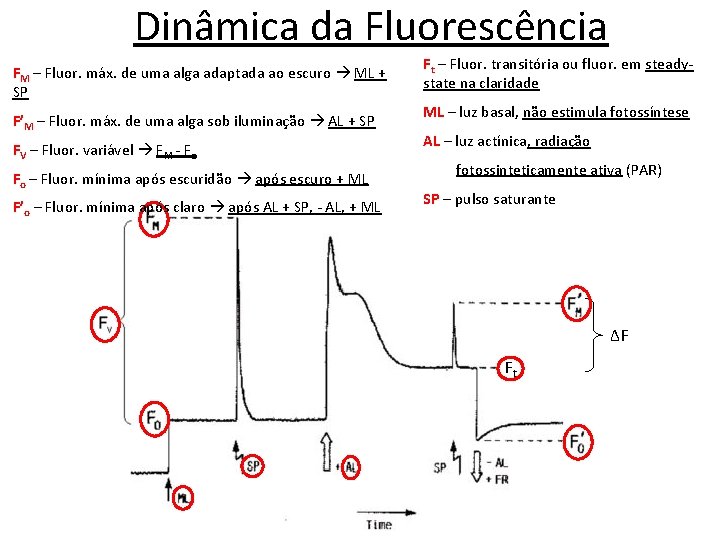
Dinâmica da Fluorescência FM – Fluor. máx. de uma alga adaptada ao escuro ML + SP F’M – Fluor. máx. de uma alga sob iluminação AL + SP FV – Fluor. variável FM - Fo Fo – Fluor. mínima após escuridão após escuro + ML F’o – Fluor. mínima após claro após AL + SP, - AL, + ML Ft – Fluor. transitória ou fluor. em steadystate na claridade ML – luz basal, não estimula fotossíntese AL – luz actínica, radiação fotossinteticamente ativa (PAR) SP – pulso saturante ΔF Ft

1. Rendimento Quântico Potencial – ●RQP Eficiência fotoquímica máxima do fotossistema II - Obtenção desse parâmetro: - Adaptação ao escuro – 5 a 20 min - Centros de reação abertos - Função do Diving-PAM: Start - Pulso de saturação - Equação: Fv/Fm ≠ valor de RQP ≠ eficiência do NPQ - Fotoinibição
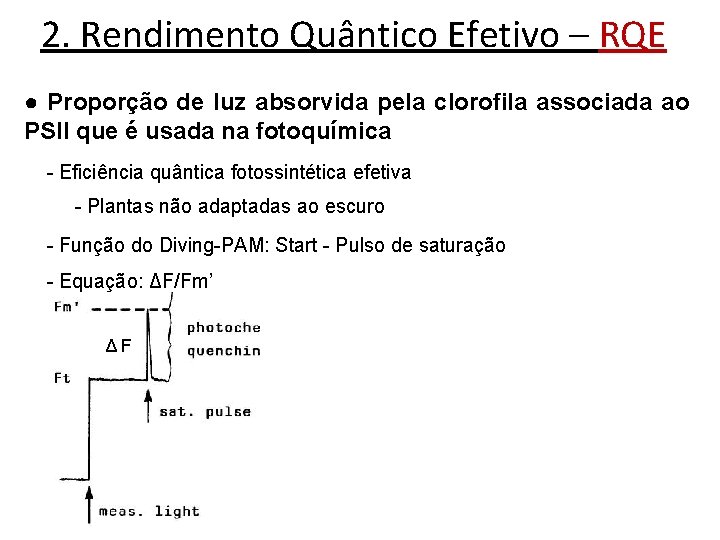
2. Rendimento Quântico Efetivo – RQE ● Proporção de luz absorvida pela clorofila associada ao PSII que é usada na fotoquímica - Eficiência quântica fotossintética efetiva - Plantas não adaptadas ao escuro - Função do Diving-PAM: Start - Pulso de saturação - Equação: ΔF/Fm’ ΔF

3. Extinção Fotoquímica – q. P ● Centros de reação do FS II abertos - Equação ΔF/Fm’ – F 0’ ΔF Ft ● RQP x RQE X q. P - RQE – Eficiência fotossintética alcançada em dado momento - RQP e q. P – Processos fundamentais que alteram a eficiência fotossintética

4. Taxa de Transporte de Elétrons – ETR Q PSII é Chl P 680 Cyt. b 3 PSI PQ Cyt. f Chl PC P 700 ● Equação ΔF/ Fm’ x PAR x coef. de absorção x 0, 5 -ΔF/ Fm’ = RQE - PAR = luz actínica (μmol fótons m-2 s-1) = fluxo de fótons fotossinteticamente ativo (FFFA) - Coeficiente de absorção = % de quanta absorvida pela planta -0, 5 = fator que explica a divisão de energia entre FSII e FSI oeficiente de absorção = % de quanta absorvida pela planta ● Relação direta c/ a taxa de fixação de CO 2 e liberação de O 2
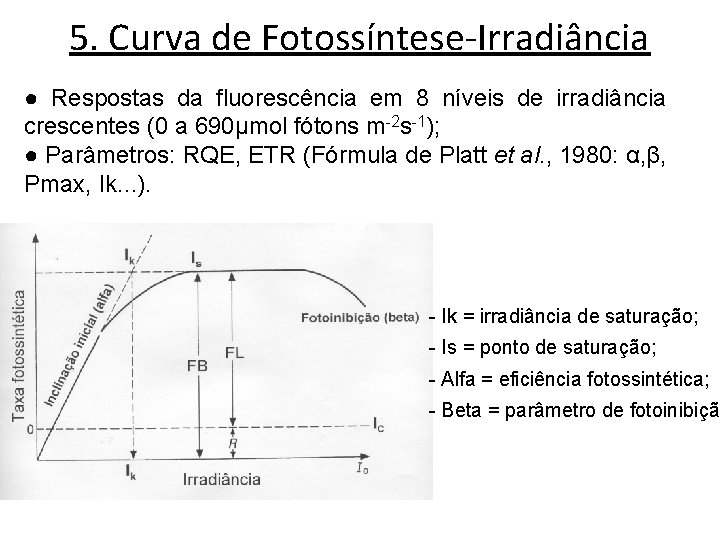
5. Curva de Fotossíntese-Irradiância ● Respostas da fluorescência em 8 níveis de irradiância crescentes (0 a 690μmol fótons m-2 s-1); ● Parâmetros: RQE, ETR (Fórmula de Platt et al. , 1980: α, β, Pmax, Ik. . . ). - Ik = irradiância de saturação; - Is = ponto de saturação; - Alfa = eficiência fotossintética; - Beta = parâmetro de fotoinibição
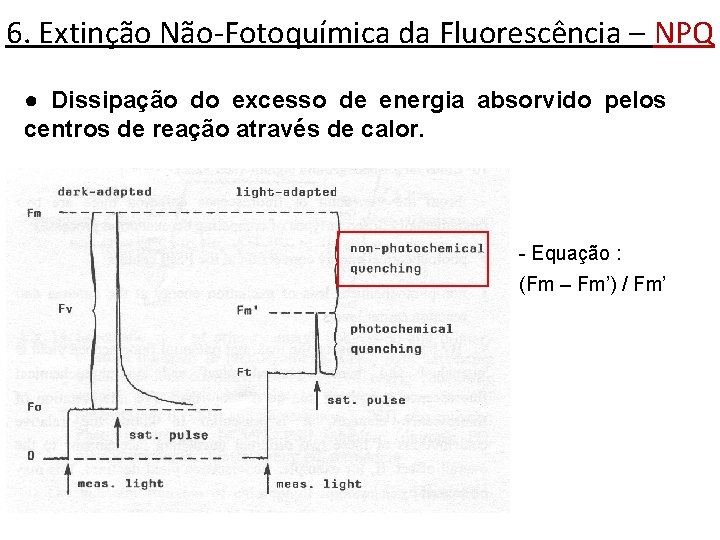
6. Extinção Não-Fotoquímica da Fluorescência – NPQ ● Dissipação do excesso de energia absorvido pelos centros de reação através de calor. - Equação : (Fm – Fm’) / Fm’

NPQ ● Processos que influenciam: q. E – quenching dependente de energização da membrana: relacionado com o gradiente de prótons da membrana do tilacóide. - É o principal componente do NPQ; - Processo rápido (minutos); - Essencial na proteção das plantas pelos danos induzidos pela luz; - Requer a presença de p. H baixo no lúmen do tilacóide; - Envolve a formação de zeaxantina; - Cessa em minutos quando a planta é colocada no escuro.

NPQ ● Processos que influenciam: q. I – Fotoinibição - Mecanismo fotoprotetor reversível contra altas irradiâncias relacionado a presença de zeaxantina; -Diminuição da atividade do FSII para controlar o excesso de energia (pigmentos antena do FSII); - Danos no centro de reação do FSII; - Processo lento (minutos a horas).
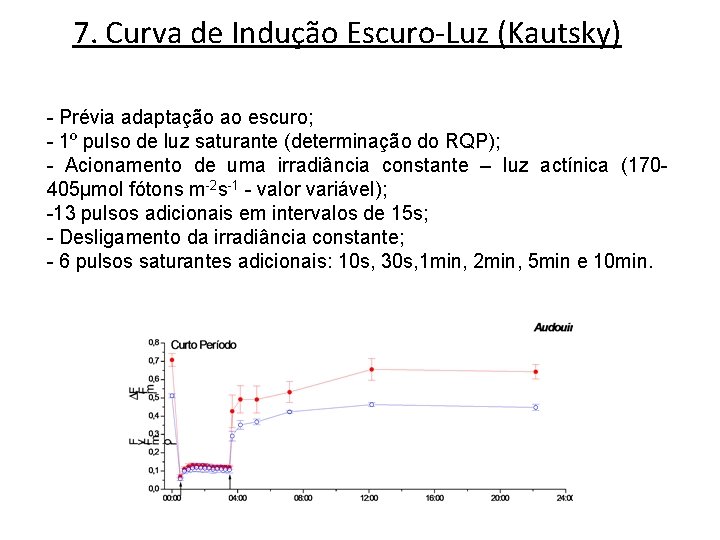
7. Curva de Indução Escuro-Luz (Kautsky) - Prévia adaptação ao escuro; - 1º pulso de luz saturante (determinação do RQP); - Acionamento de uma irradiância constante – luz actínica (170405μmol fótons m-2 s-1 - valor variável); -13 pulsos adicionais em intervalos de 15 s; - Desligamento da irradiância constante; - 6 pulsos saturantes adicionais: 10 s, 30 s, 1 min, 2 min, 5 min e 10 min.
- Slides: 26