Amostragem e Mtodos Analticos Qumica Ambiental Engenharia Ambiental

Amostragem e Métodos Analíticos Química Ambiental Engenharia Ambiental Prof. Alonso Goes Guimarães

Análise Química n n n Promovem relevantes informações a estudos ambientais; Monitoramento de espécies químicas em um determinado meio; Estudo e/ou pesquisa com propósito ambiental para obter resposta;

Análise Química n Estudo ambiental n Quais os diferentes compostos de mercúrio existentes em uma lagoa contaminada? n Quais os metais e suas respectivas concentrações no corpo hídrico?

Análise Química n Monitoramento ambiental n Obter dados analíticos que devem ser comparados com valores previamente estabelecidos; n Diagnosticar se critérios e/ou padrões de qualidade estão sendo obedecidos pelo objeto em estudo; n O efluente lançado pela indústria está dentro dos parâmetros permitidos pela legislação?

Química Analítica n n É o ramo da química que se debruça na identificação ou quantificação de espécies ou elementos químicos; Na sua qualidade de ciência metrológica, passa a ser cada vez mais importante em transações econômicas do tipo comercial.

Importância na Qualidade de Vida n n n Maior interesse em temas como saúde, segurança e o meio ambiente; Informes e discussões/decisões em temas como qualidade das águas, dos sedimentos, dos solos, do ar, de resíduos; evidências em casos de envenenamento ou ingestão de drogas envolvendo investigações policiais (medicina forense);

A Química Analítica e outras ciências Engenharias Medicina Nutrição Química Analítica Farmácia Geologia Oceanografia Direito Ciências ambientais


Segurança da qualidade na determinação dos resultados analíticos n n Normatização estabelecida internacionalmente. O custo de uma análise química equivocada: n n n em análises forenses: uma convicção injusta ou culpados impunes; na indústria e comércio pode levar a distribuição de mercadorias inferiores; no fornecimento de água para beber, contaminantes perigosos podem não ser detectados, ou aparecerem com níveis maiores do que o valor real;

Segurança da qualidade na determinação dos resultados analíticos n Em monitoramento ambiental, erros podem levar a não detecção de riscos ou a identificação de riscos irreais; n Os custos podem ser financeiros e/ou podem levar a perdas do valor intrínseco dos recursos naturais;

Química Analítica n O que é X na amostra Y? n Qual o teor do constituinte X na amostra Y ? n Qual a forma química e o teor que o constituinte X se apresenta na amostra Y? n Como o constituinte X esta distribuído na

Principais desafios da Química Analítica n Determinação de constituintes com teores cada vez menores; n Ganho em velocidade analítica; n Determinação com especiação; n Análise química em amostras sólidas e gasosas;

Análise Ideal n n n Métodos para determinação química diretamente no ambiente (in situ) e em tempo real; Poucas são as medidas que podem ser feitas desta forma; Normalmente, a espécie química deve sofrer transformações e purificação;

Alguns termos usados em Química Analítica n n n Analisar e determinar Análise de traços Exatidão e precisão n Seletividade n Sensibilidade n Pré-concentração n Efeito de matriz

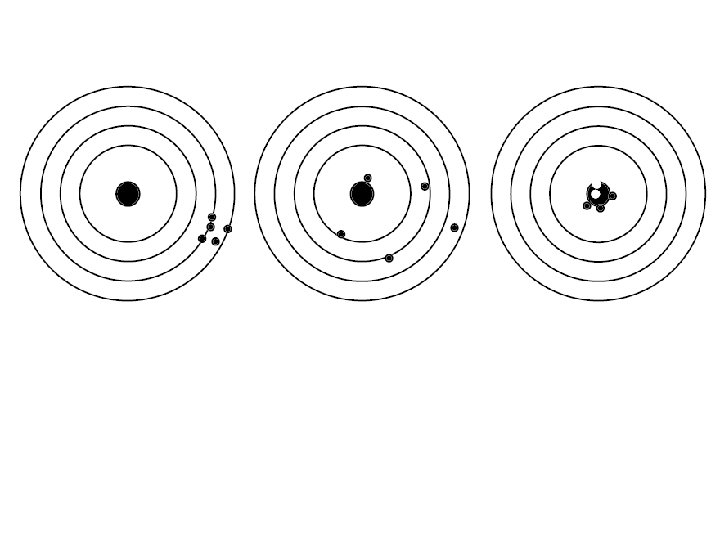
Exatidão e Precisão n n Exatidão: n Está relacionada com o erro absoluto da medida; n Proximidade do valor medido em relação ao valor verdadeiro da grandeza; Precisão: n Está relacionada com a concordância das medidas entre si; n Quanto maior a dispersão dos valores, menor a precisão.

Exatidão e Precisão n Exatidão: n n Precisão: pode ser expressa quanto a grandeza dos desvios n n Veracidade das medidas; Reprodutibilidade das medidas; PRECISÃO NÃO IMPLICA OBRIGATORIAMENTE EXATIDÃO!!!!!

Métodos Analíticos -Introdução n n Todo método analítico é baseado na medida de uma propriedade física; Os métodos analíticos são classificados de acordo com a propriedade física que o mesmo se baseia.

Principais Métodos de Análise
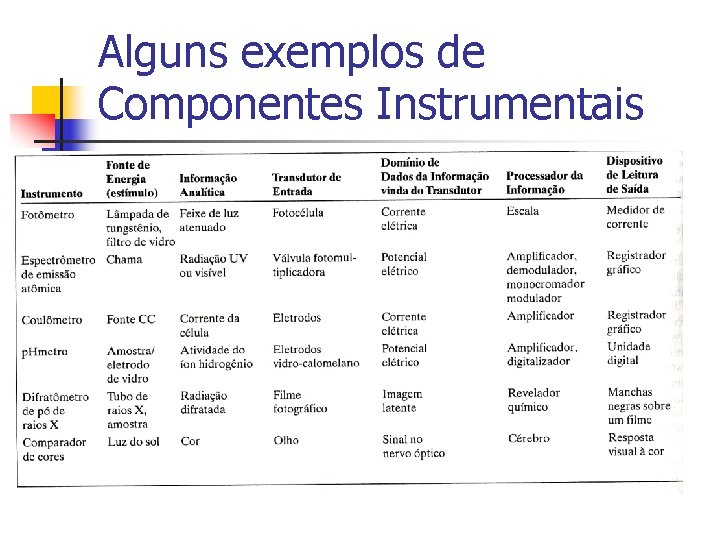
Alguns exemplos de Componentes Instrumentais

Métodos Analíticos Critérios de Seleção 1 - Objetivo da análise 2 - Exatidão requerida 3 - Teor do componente presente na amostra n n Componente maior conc. > 1% componente menor conc. 0, 1 a 1 % Micro ou traços conc. < 0, 1% Ultratraços conc. g L-1

Métodos Analíticos Critérios de Seleção 4567 - Recursos disponíveis Número de amostras a analisar Composição química da amostra Tamanho da amostra

Tipos de Análise n Qualitativa n n Quando se pretende determinar ou identificar as espécies ou elementos químicos presentes numa amostra. Quantitativa n Para se determinar a quantidade de uma espécie ou elemento químico numa amostra.

Amostragem n n É o processo de coleta de uma amostra representativa de um lote heterogêneo, ou seja, que represente a totalidade do material de interesse para que seja realizada a análise. Mesmo para a melhor amostra representativa, haverá sempre a necessidade de algum grau de PREPARAÇÃO DA AMOSTRA, quer para retirar interferentes, quer para dar forma disponível para a análise.

Amostragem Para Monitoramento ambiental: ambiental � Protocolos específicos de amostragens; � Normatizado por agências (ABNT); � Devem ser seguidos com rigor; Para Estudo Ambiental: Ambiental � Não acontece o mesmo; � Busca-se o desconhecido; � Bom senso; � Histórico do problema; � Experiência do analista pode ser melhor solução para elaboração do protocolo de amostragem

Amostragem de Líquidos n n n Garrafas de vidro, plástico e metal (depende da análise e do analito); Não existem grandes dificuldades; Não perturbar a água de forma significativa; Às vezes coletar em diferentes profundidades; Luz, calor, solubilidade de gases e contato com o leito influem nas concentrações dos compostos; Frasco amostrador em profundidades.

Garrafas de amostragem Garrafa de Van Dorn

Amostragem de Sólidos n n n Tratamento especial; Material é pouco homogêneo; Pode ser necessário coletar em vários pontos. Todo material misturado e homogeneizado; A profundidade pode ser relevante; Dependendo do problema usar brocas, trados, tubos ou equipamentos para cortar o solo; Cavar e recolher diretamente a amostra.

Amostragem de Sólidos

Amostragem de Gases n n n Frequentemente a matriz é a atmosfera; Propriedade de dispersar e homogeneizar a mistura; Amostra homogênea e muito diluída;

Amostragem de Gases n Fatores que influem nas propriedades e composição: n n n Pressão atmosférica; Temperatura; Vento; Chuva; Conhecer as condições ambientais pode ser necessário;

Amostragem de Gases n n Para ambientes fechados e concentração alta: n Pequenos tubos contendo reagente (mudam de cor na presença do poluente); Para ar atmosférico: n Baixas concentrações; n Não existem técnicas analíticas para determinação direta; n Pré-concentração: n Coletores capturam grande volume de ar por um meio sól. ou líq. e retem as espécies.

Amostragem de Gases n n Existem bombas aspiradoras disponíveis no mercado para uso específico; É possível adaptar: n n n Aspirador de pó; Compressores de aquários; Compressores para inalação.

Volumetria de neutralização n n n Método de análise baseado na reação entre íons H 3 O+ e OHH 3 O+ + OH 2 H 2 O Detecção do ponto final com uso de indicadores;

Análise Gravimétrica n n n Método analítico quantitativo cujo processo envolve a separação e pesagem de um elemento ou um composto do elemento na forma mais pura possível. Titulações que resultam na formação de compostos pouco solúveis; Usadas principalmente para determinação de haletos e de alguns íons metálicos;

Análise Gravimétrica n n Deve ser processada em tempo curto; Composto suficientemente insolúvel; Uso do indicador adequado; Construção da curva de titulação;

Características de um bom precipitado n n n Ter baixa solubilidade Ser fácil de recuperar por filtração Não ser reativo com o ar, a água;
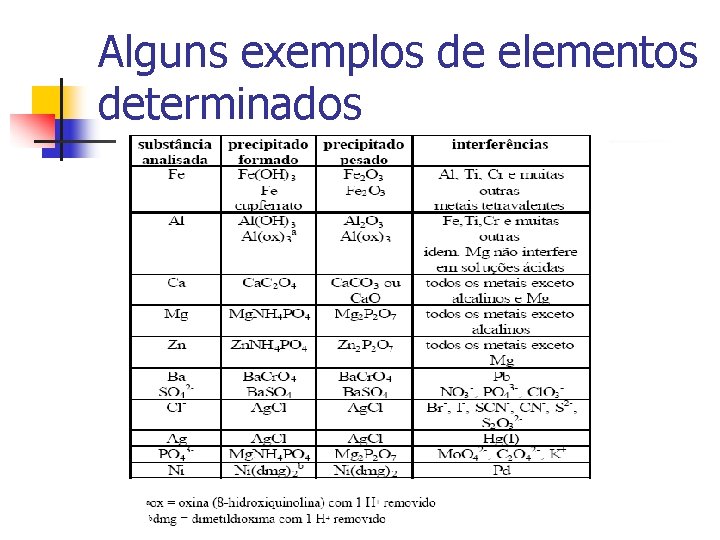
Alguns exemplos de elementos determinados

Exemplos de Análise n Determinação de ferro em solo n 0, 485 g de uma amostra de solo contendo ferro (II) e (III), foi oxidada e o ferro (III) precipitado como óxido de ferro hidratado (Fe 2 O 3. XH 2 O). O precipitado depois de filtrado, lavado e calcinado pesou 0, 248 g, com o ferro na forma de óxido (Fe 2 O 3).

Exemplos de Análise n n Determinação de cálcio em águas naturais O íon cálcio é precipitado na forma do sal orgânico oxalato de cálcio (pouco solúvel) com ácido oxálico H 2 C 2 O 4. O precipitado Ca. C 2 O 4 é coletado em papel de filtro (este será convertido em CO 2(gás) e H 2 O(vapor) pela ação oxidante do O 2 atmosférico, sendo estes então eliminados), seco e aquecido até o rubro (calcinação).

Exemplos de Análise n O processo converte o precipitado quantitativamente para óxido de cálcio (cal). O precipitado depois de calcinado é resfriado em dessecador e pesado. Usa-se um cadinho previamente aquecido, resfriado e pesado para a ignição do precipitado. O cálcio em 200 m. L de amostra de água natural foi determinado pela precipitação do cátion como Ca. C 2 O 4. O precipitado foi filtrado, lavado e calcinado em cadinho com massa de 26, 600 g. A massa do cadinho, mais o precipitado calcinado (Ca. O PM=56, 08 g/mol) foi de 26, 713 g.

Potenciometria n A potenciometria direta determina a concentração do íon ativo simplesmente medindo a f. e. m. da célula em condições que permitam conhecer o seu valor exato. Dessa exatidão dependerá a precisão dos resultados analíticos;

Potenciometria n n O potencial do eletrodo indicador (comparado com um eletrodo de referência) é medido inicialmente em soluções padrão da espécie química a ser determinada; Comparando-se a medição do potencial em amostras com os dados das soluções padrões, é possível avaliar-se a concentração da amostra.

p. Hmetros
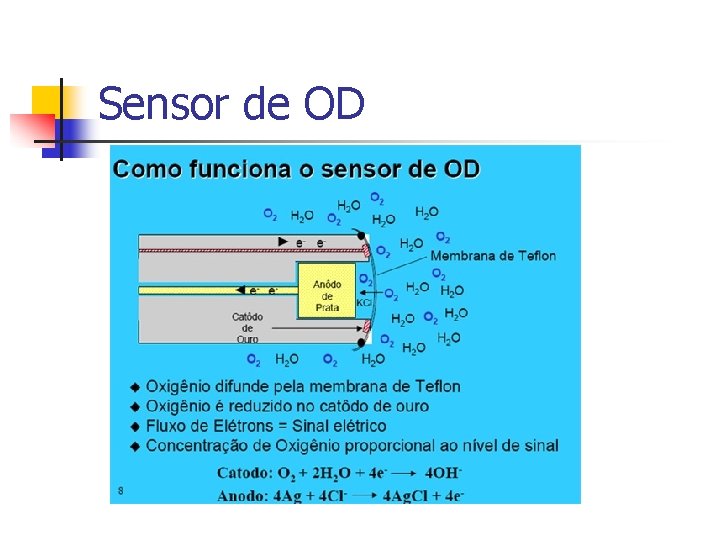
Sensor de OD

Aparelhos Portáteis Multiparâmetros

Analisador de Metais Pesados em Solos e Rocha - Fluorescência de Raio-X n n Análise qualitativa e quantitativa de mais de 20 metais pesados presentes no solo, em rocha e minério. Elementos Standard: Ba, Sb, Sn, Cd, Ag, Mo, Zr, Sr, U, Rb, Th, Pb, Se, As, Tl, Hg, Zn, Cu, Ni, Co, Fe, Mn, Cr, V, Ti, Sc, Ca, K, Cl, S, P.

Analisador de Metais Pesados em Solos e Rocha - Fluorescência de Raio-X

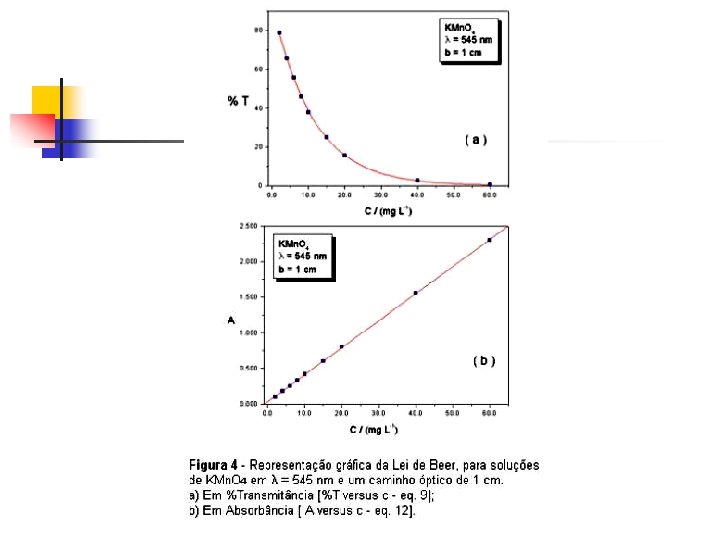
Espectrofotometria n n Dos métodos colorimétricos, o método mais exato para a determinação da concentração de substâncias em solução; Um espectrofotômetro pode ser considerado como um fotômetro fotoelétrico de filtro refinado que permite o uso de faixas de luz aproximadamente monocromáticas continuamente;

Espectrofotômetro n As partes essenciais de um espectrofotômetro são uma fonte de energia radiante, um monocromador, um dispositivo para o isolamento de luz monocromática, mais exatamente, faixas estreitas de energia radiante da fonte de luz, células de vidro ou de sílica e feixes de energia radiante que passam através do solvente ou solução.

Espectrofotômetro
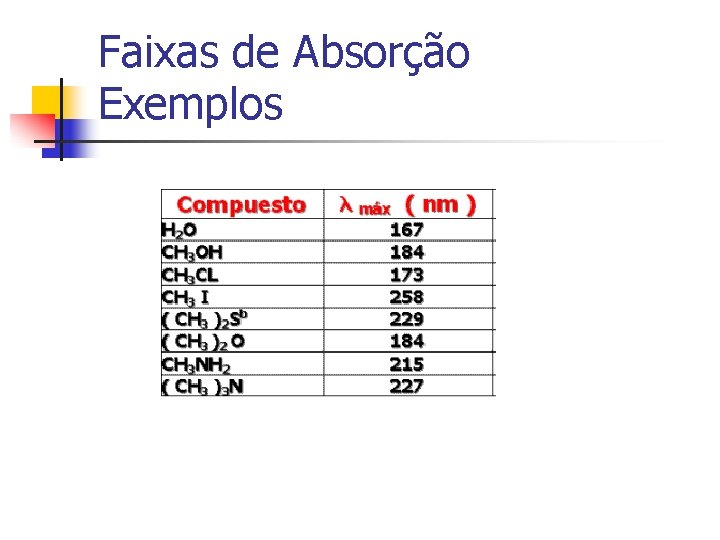
Faixas de Absorção Exemplos
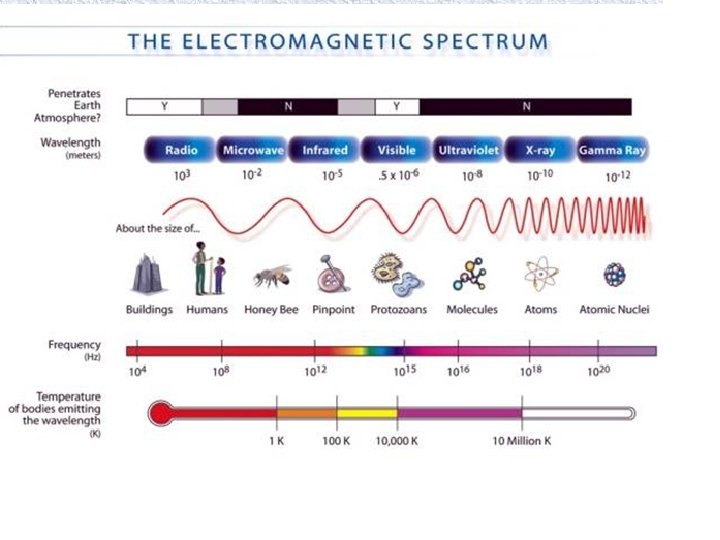

Espectro Visível

Cromatografia n Michael Tsewtt - botânico russo 1906 n n Separar subst. que dão cor a uma folha; Origem grega: escrever com cor (chromatus quer dizer cor e graphein, escrever)

Cromatografia n n É um processo físico de separação; Os componentes a serem separados se distribuem em duas fases: n n Fase estacionária: Sólido ou líquido sobre um suporte sólido com grande área superficial; Fases móvel: Gasosa, líquida ou fluido supercrítico. Passa pela estacionária arrastando os componentes da mistura.

Cromatografia n Tipos principais: n Cromatografia planar: n n n CP: em papel CCD: em camada delgada Cromatografia em coluna n n CG: gasosa CL: líquida

Cromatografia em papel n n n Compostos hidrossolúveis, ácidos orgânicos e íons metálicos Princípio: partição (solubilidade) Quantidade de amostra necessária: 10 -3 a 10 -6 g Tipos: ascendente, descendente, bidimensional, circular F. M. - Sistema de solventes


Cromatografia em Camada Delgada n n n n Método rápido (20 -40 min. ) Uso de diversos agentes cromogênicos Maior sensibilidade que C. P. (10 -9 g) Grande gama de compostos pode ser analisada Método simples e barato F. M. - sistema de solventes F. E - Adsorventes (sílica, alumina, celite,


Cromatografia Gasosa n n n Técnica com alto poder de resolução; Várias substâncias numa mesma amostra; Pode chegar a 10 -12 g/m. L de solução.

Cromatografia Gasosa n n Rapidez; Alto poder de separação; Separação de várias classes de compostos em uma análise; Sensibilidade (ppm n n n Amostras voláteis; Compostos termicamente estáveis; Técnicas auxiliares p/ identificação.

Cromatografia Gasosa: Aplicações n n n Análise de ácidos graxos e triglicerídeos; Análise de compostos voláteis responsáveis pelo aroma característico de alimentos; Análise de açúcares; Análise de aminoácidos; Análise de pesticidas; Análise de fármacos.

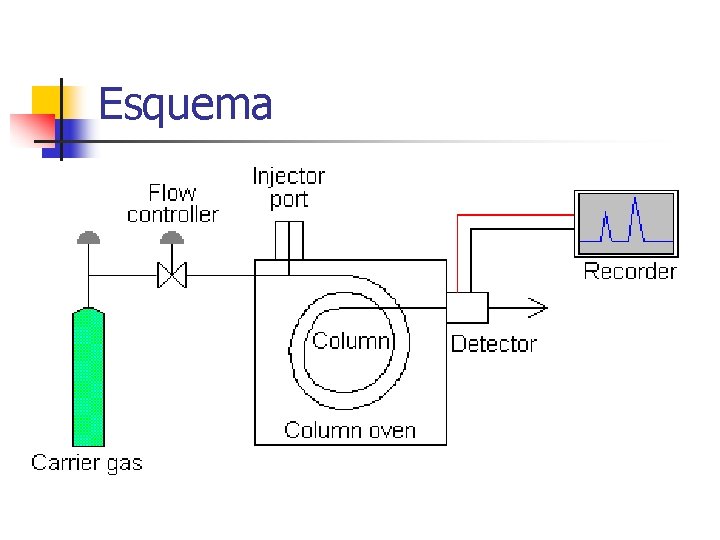
Esquema

Gás de arraste (FM) n n n H 2, N 2, He, Ar Função: transporte da amostra; Propriedades: inerte, compatível com o detetor, puro.

Cromatografia gasosa: Colunas - tipos n n Parâmetro Coluna capilar Diam. Int. (mm) 0, 15 - 0, 75 Comp. (m) 10 -100 Pratos teóricos 3000 empacotada 1 -4 1 -3 2400


Colunas - fase estacionária (FE) n n Apolar: hidrocarbonetos não aromáticos, silicones (ex. : SE 30) - P. E. Polar: contém grande quantidade de grupos polares (Ex. : Carbowax)- interações tipo lig. de hidrogênio Intermediária: grupos polares ou potencialmente polares em esqueleto apolar (Ex. SE-52) Escolha da coluna: n Polaridade da fase estacionária; n diâmetro e espessura do filme quantidade de amostras, tempo de análise, pressão (velocidade da FM), temperatura do forno n Comprimento pratos teóricos.

Detetor - requisitos n n n Alta sensibilidade; Baixo nível de ruído; Faixa linear ampla p/ a resposta; Resposta p/ os compostos de interesse (universais, seletivos, específicos); Insensível a pequenas mudanças de fluxo e temperatura; Destrutivos/ não destrutivos.

Detetor -Tipos n n Ionização de chamas FID (alta sensibilidade, resposta quase universal) FM = hidrogênio ou nitrogênio, destrutivo; Condutividade térmica (resposta universal, não destrói a amostra) - FM = Hélio ou hidrogênio, não destrutivo; Captura de elétrons (seletivo p/ halogênios orgânicos, nitrilas, nitratos e organometálicos) FM = nitrogênio, não destrutivo; Termiônico (seletivo p/ compostos contendo N e P)

Cromatografia gasosa: Cromatogramas Tr= tempo de retenção Tm = tempo morto- tempo que a FM leva para percorrer a coluna T´r = tempo de retenção corrigido = Tr-Tm

Cromatografia gasosa: Análise quantitativa Relação concentração x Área do pico
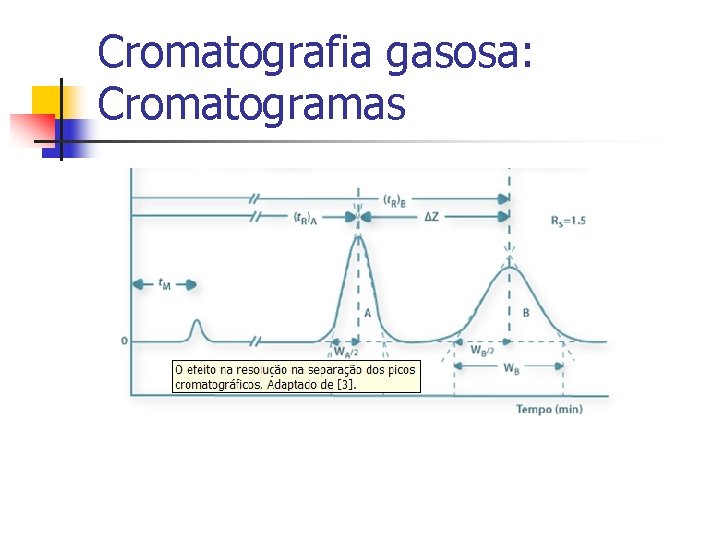
Cromatografia gasosa: Cromatogramas

Cromatografia gasosa: Cromatogramas Formação de íons pela combustão da amostra na presença de H 2 e O 2. Origina corrente elétrica no coletor gerando um sinal do qual a combustão do gás de arraste é descontada
- Slides: 78