Aminosyrer Proteinenes byggesteiner Aminosyrer Alle proteiner er dannet

Aminosyrer Proteinenes byggesteiner

Aminosyrer • Alle proteiner er dannet ved sammenkopling av 20 forskjellige aminosyrer • Alle levende organismer benytter de samme aminosyrene • Aminosyrene er proteinspråkets alfabet – Benevnes med trebokstavs- og enbokstavsforkortelser • F. eks. Alanin = Ala = A • Andre aminosyrer brukes ikke i proteinsyntese • Et fåtall aminosyrer modifiseres etter innkorporering i proteiner

Aminosyrenomenklatur • Aminosyrenes navne presenteres ofte som forkortelser
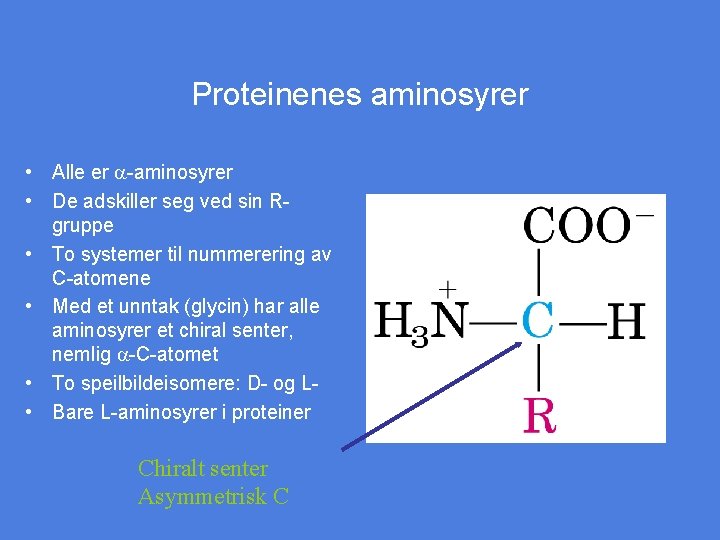
Proteinenes aminosyrer • Alle er a-aminosyrer • De adskiller seg ved sin Rgruppe • To systemer til nummerering av C-atomene • Med et unntak (glycin) har alle aminosyrer et chiral senter, nemlig a-C-atomet • To speilbildeisomere: D- og L • Bare L-aminosyrer i proteiner Chiralt senter Asymmetrisk C
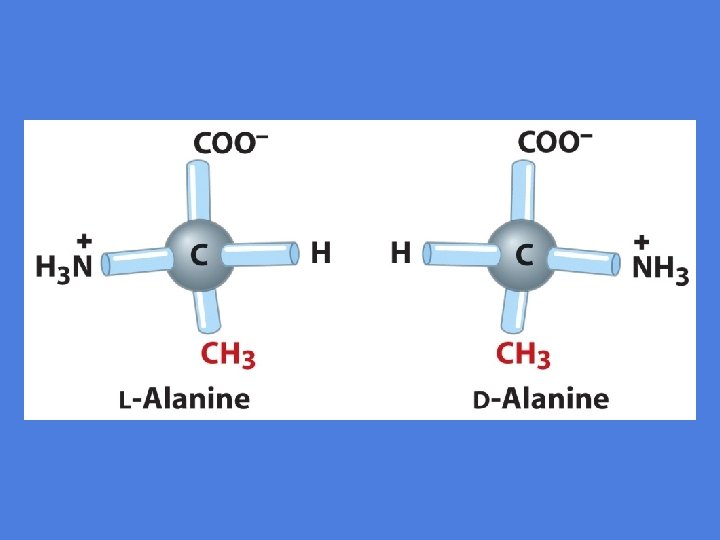
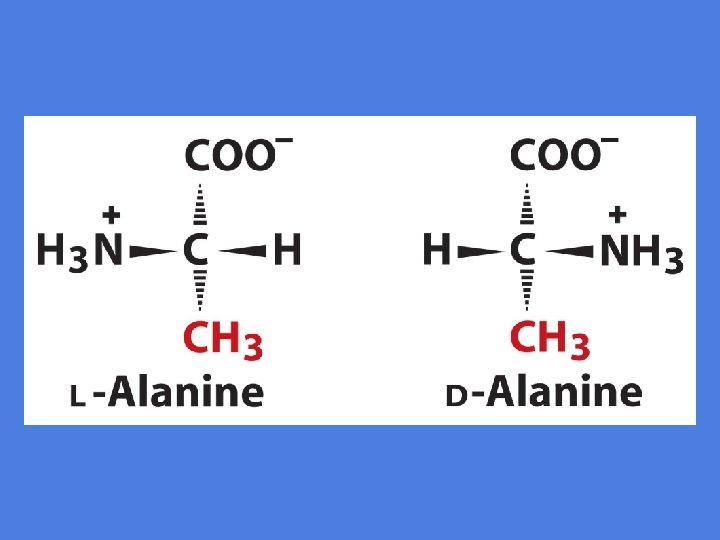
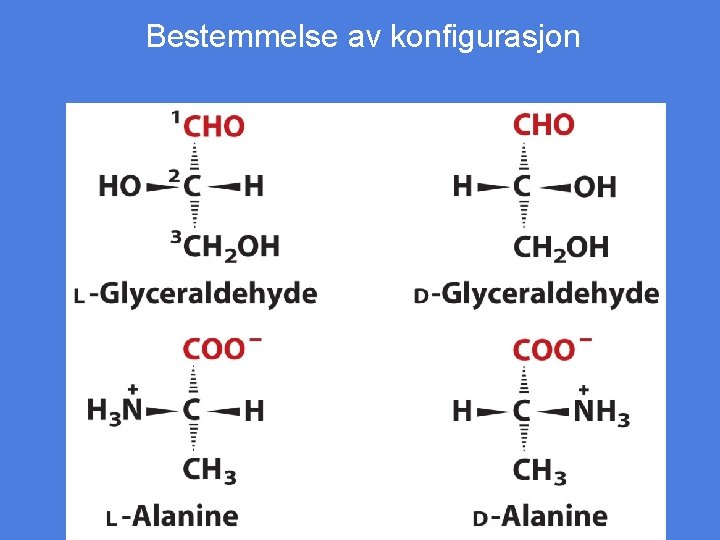
Bestemmelse av konfigurasjon

Aminosyrenes klassifisering • Basert på R-gruppenes/sidekjedenes kjemiske egenskaper – 1) upolare, alifatiske sidekjeder – 2) aromatiske sidekjeder (ofte upolare) – 3) polare, uladede sidekjeder – 4) positivt ladede – 5) negativt ladede
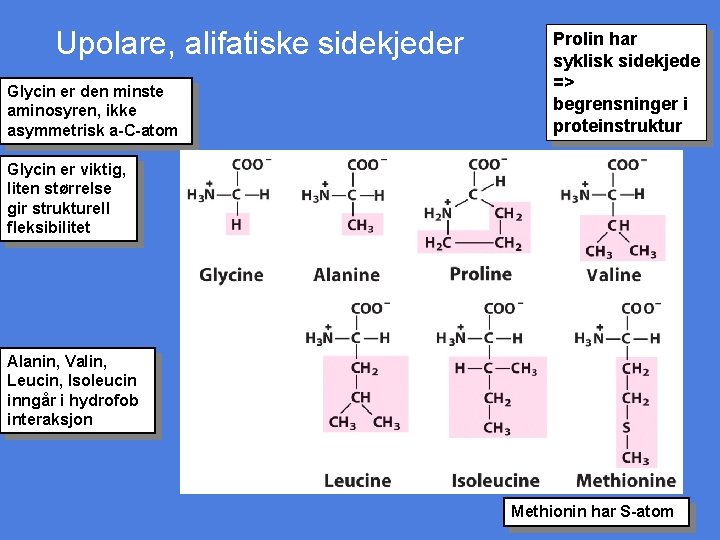
Upolare, alifatiske sidekjeder Glycin er den minste aminosyren, ikke asymmetrisk a-C-atom Prolin har syklisk sidekjede => begrensninger i proteinstruktur Glycin er viktig, liten størrelse gir strukturell fleksibilitet Alanin, Valin, Leucin, Isoleucin inngår i hydrofob interaksjon Methionin har S-atom
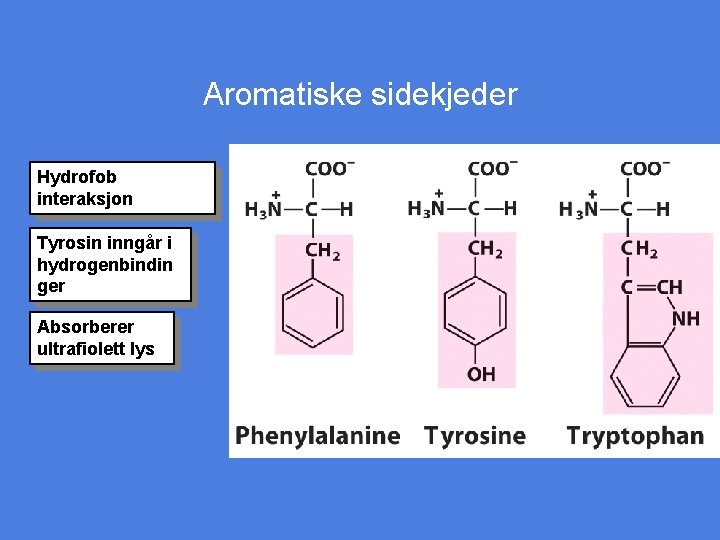
Aromatiske sidekjeder Hydrofob interaksjon Tyrosin inngår i hydrogenbindin ger Absorberer ultrafiolett lys
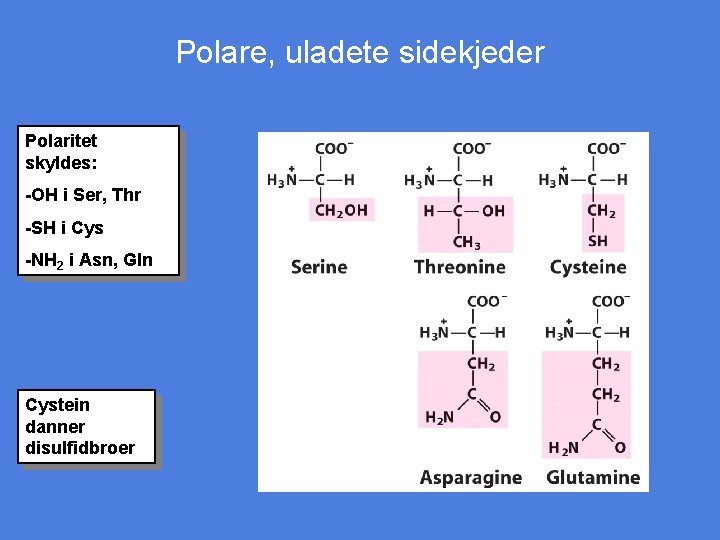
Polare, uladete sidekjeder Polaritet skyldes: -OH i Ser, Thr -SH i Cys -NH 2 i Asn, Gln Cystein danner disulfidbroer Slide 13
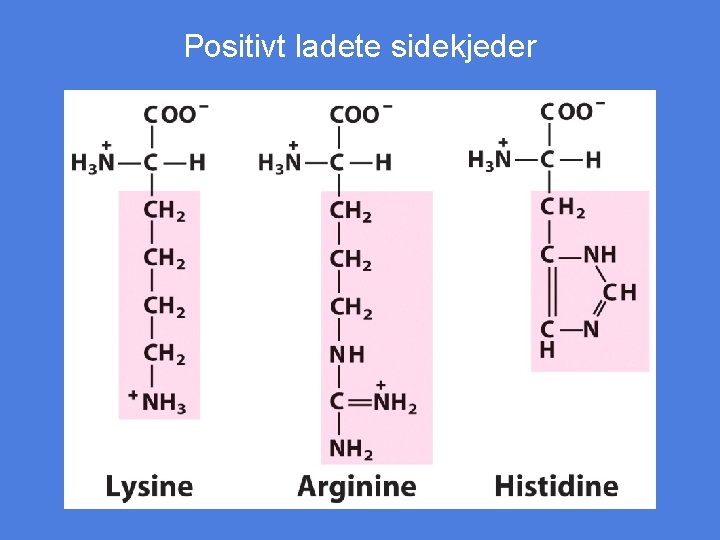
Positivt ladete sidekjeder
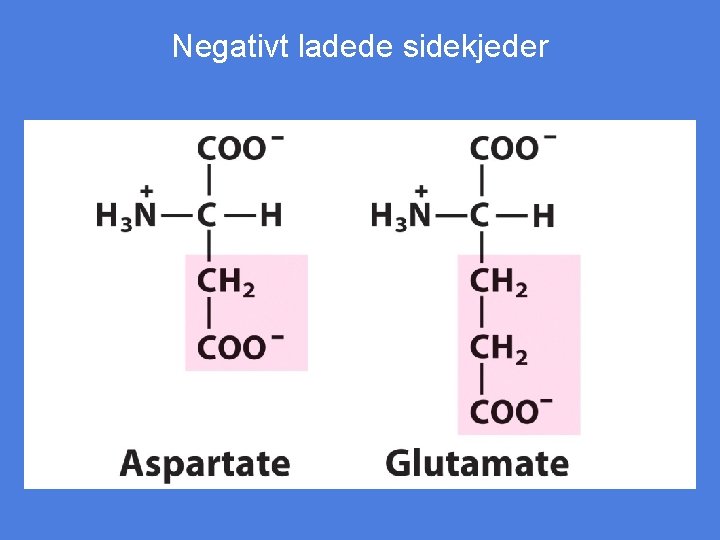
Negativt ladede sidekjeder
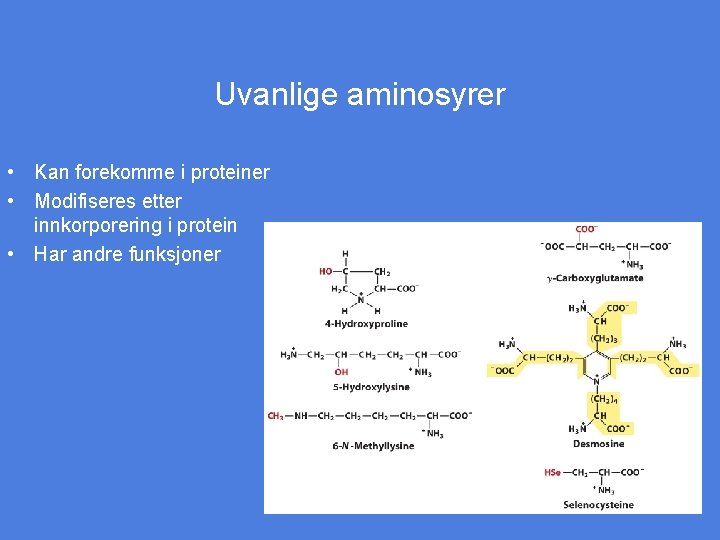
Uvanlige aminosyrer • Kan forekomme i proteiner • Modifiseres etter innkorporering i protein • Har andre funksjoner
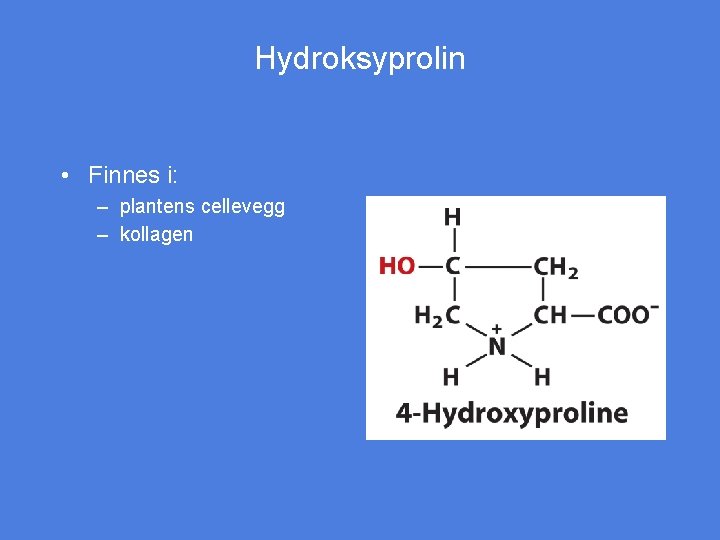
Hydroksyprolin • Finnes i: – plantens cellevegg – kollagen
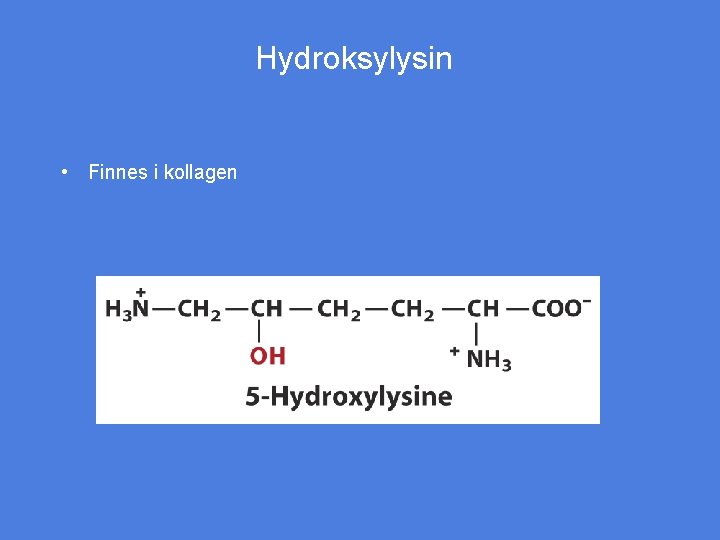
Hydroksylysin • Finnes i kollagen
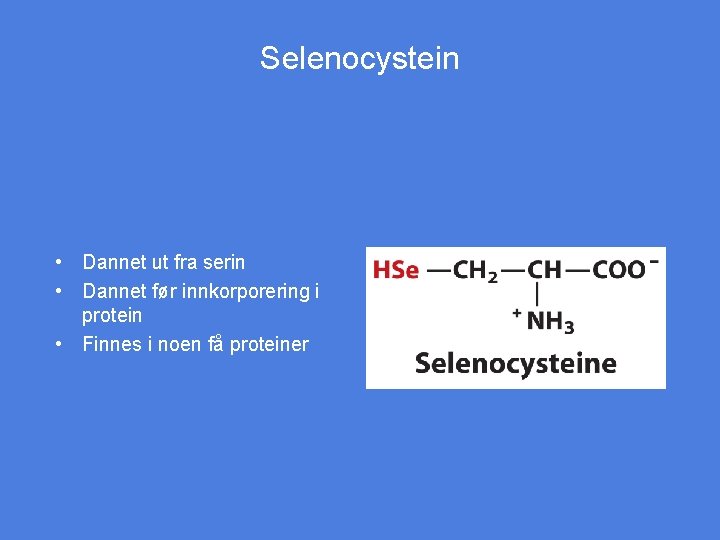
Selenocystein • Dannet ut fra serin • Dannet før innkorporering i protein • Finnes i noen få proteiner
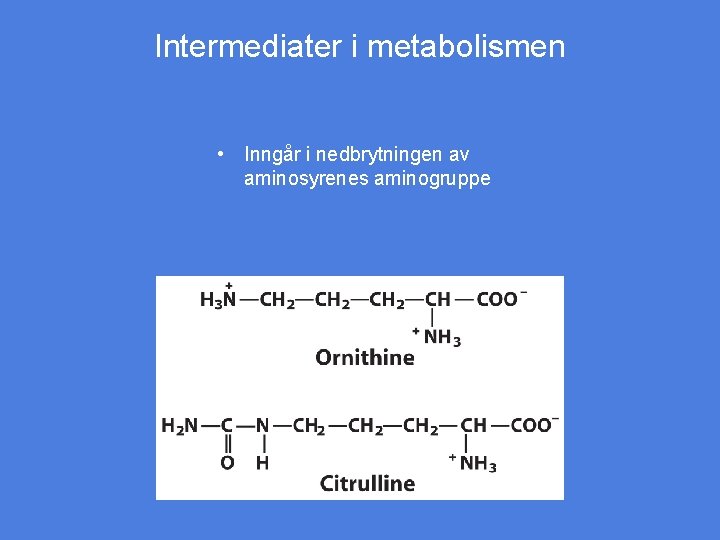
Intermediater i metabolismen • Inngår i nedbrytningen av aminosyrenes aminogruppe
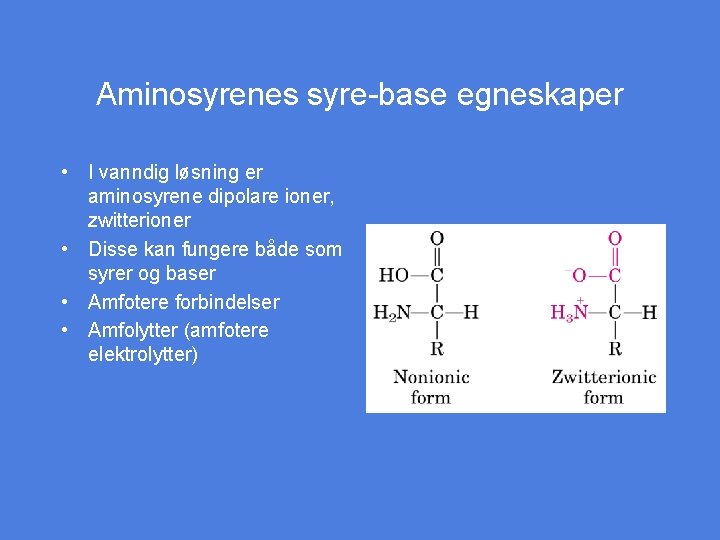
Aminosyrenes syre-base egneskaper • I vanndig løsning er aminosyrene dipolare ioner, zwitterioner • Disse kan fungere både som syrer og baser • Amfotere forbindelser • Amfolytter (amfotere elektrolytter)
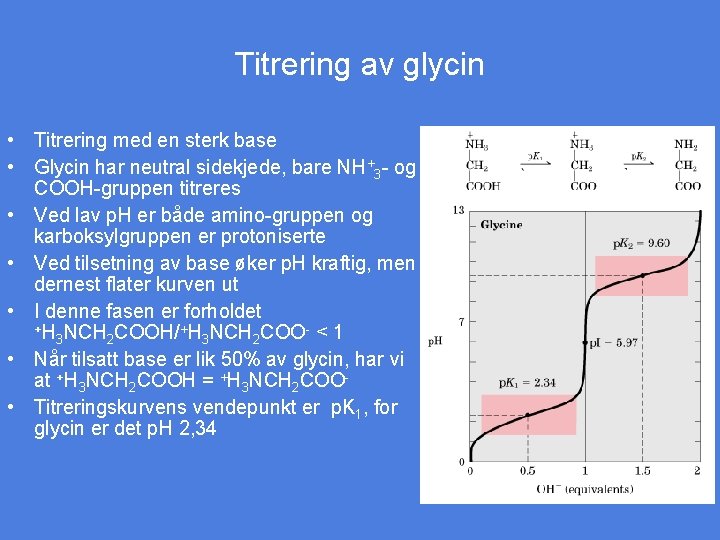
Titrering av glycin • Titrering med en sterk base • Glycin har neutral sidekjede, bare NH+3 - og COOH-gruppen titreres • Ved lav p. H er både amino-gruppen og karboksylgruppen er protoniserte • Ved tilsetning av base øker p. H kraftig, men dernest flater kurven ut • I denne fasen er forholdet +H NCH COOH/+H NCH COO- < 1 3 2 • Når tilsatt base er lik 50% av glycin, har vi at +H 3 NCH 2 COOH = +H 3 NCH 2 COO • Titreringskurvens vendepunkt er p. K 1, for glycin er det p. H 2, 34 Figur 5 -10
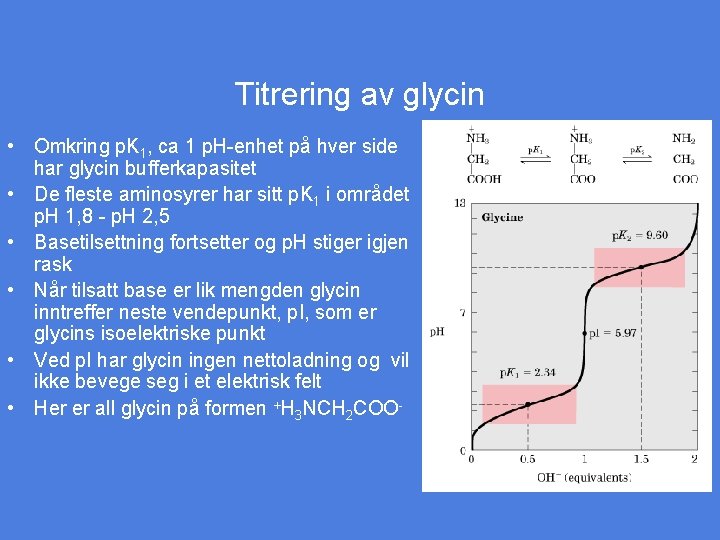
Titrering av glycin • Omkring p. K 1, ca 1 p. H-enhet på hver side har glycin bufferkapasitet • De fleste aminosyrer har sitt p. K 1 i området p. H 1, 8 - p. H 2, 5 • Basetilsettning fortsetter og p. H stiger igjen rask • Når tilsatt base er lik mengden glycin inntreffer neste vendepunkt, p. I, som er glycins isoelektriske punkt • Ved p. I har glycin ingen nettoladning og vil ikke bevege seg i et elektrisk felt • Her er all glycin på formen +H 3 NCH 2 COO- Figur 5 -10
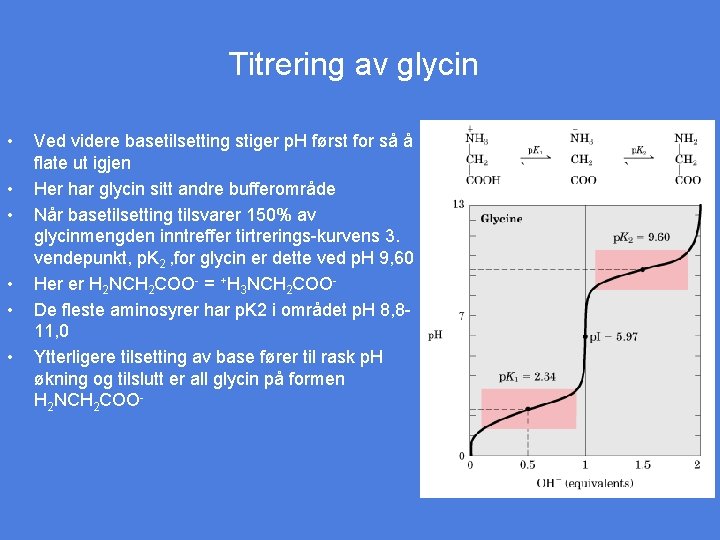
Titrering av glycin • • • Ved videre basetilsetting stiger p. H først for så å flate ut igjen Her har glycin sitt andre bufferområde Når basetilsetting tilsvarer 150% av glycinmengden inntreffer tirtrerings-kurvens 3. vendepunkt, p. K 2 , for glycin er dette ved p. H 9, 60 Her er H 2 NCH 2 COO- = +H 3 NCH 2 COODe fleste aminosyrer har p. K 2 i området p. H 8, 811, 0 Ytterligere tilsetting av base fører til rask p. H økning og tilslutt er all glycin på formen H 2 NCH 2 COO- Figur 5 -10
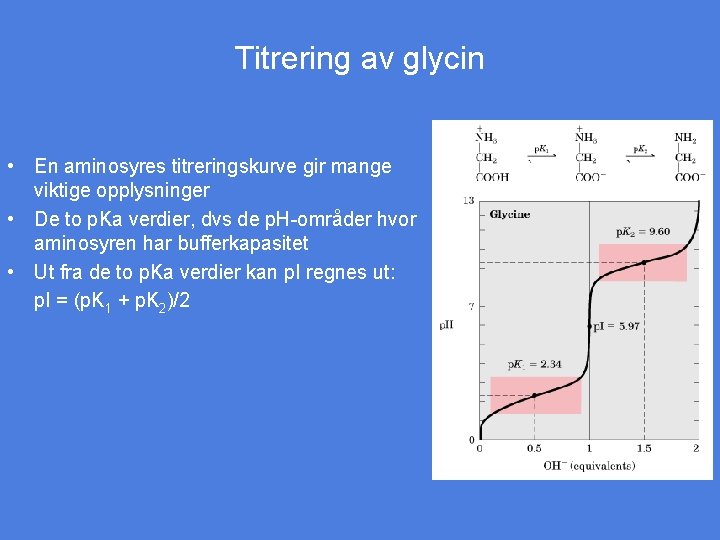
Titrering av glycin • En aminosyres titreringskurve gir mange viktige opplysninger • De to p. Ka verdier, dvs de p. H-områder hvor aminosyren har bufferkapasitet • Ut fra de to p. Ka verdier kan p. I regnes ut: p. I = (p. K 1 + p. K 2)/2 Figur 5 -10
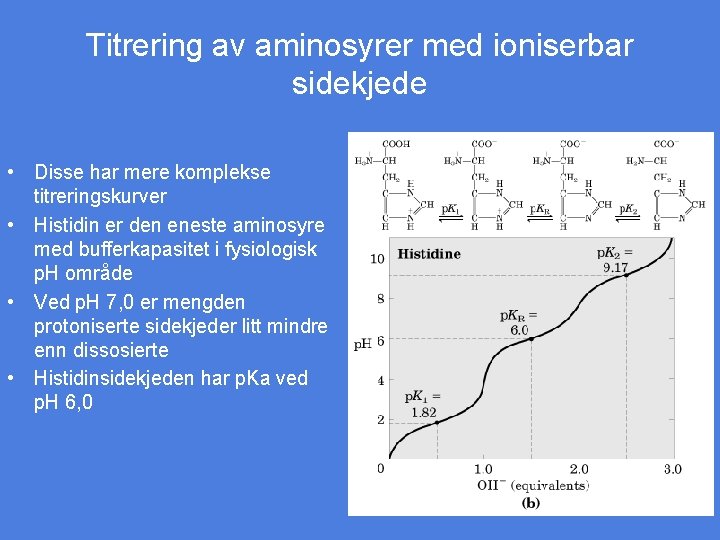
Titrering av aminosyrer med ioniserbar sidekjede • Disse har mere komplekse titreringskurver • Histidin er den eneste aminosyre med bufferkapasitet i fysiologisk p. H område • Ved p. H 7, 0 er mengden protoniserte sidekjeder litt mindre enn dissosierte • Histidinsidekjeden har p. Ka ved p. H 6, 0 Figur 5 -12

Polypeptider/proteiner • • • Aminosyrer koples sammen til liniære polymerer Minste polymerer kalles oligopeptider Små polymerer (< 10 k. D) kalles polypeptider Store polymerer kalles proteiner Proteinene er den gruppe makromolekyler med størst variasjon i egenskaper og funksjoner • Proteiners kjemiske egneskaper er summen av aminosyrenes egenskaper
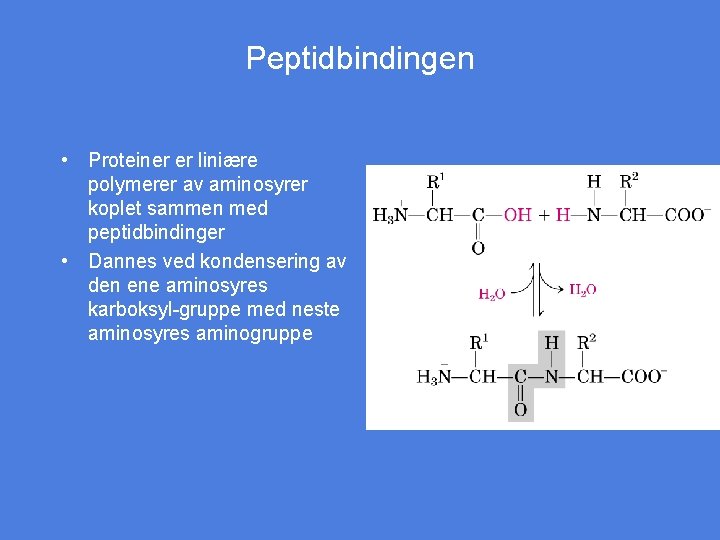
Peptidbindingen • Proteiner er liniære polymerer av aminosyrer koplet sammen med peptidbindinger • Dannes ved kondensering av den ene aminosyres karboksyl-gruppe med neste aminosyres aminogruppe
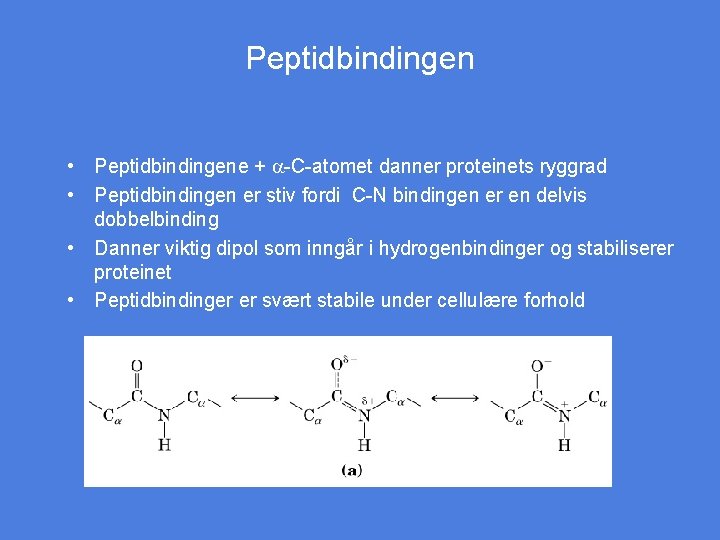
Peptidbindingen • Peptidbindingene + a-C-atomet danner proteinets ryggrad • Peptidbindingen er stiv fordi C-N bindingen er en delvis dobbelbinding • Danner viktig dipol som inngår i hydrogenbindinger og stabiliserer proteinet • Peptidbindinger er svært stabile under cellulære forhold
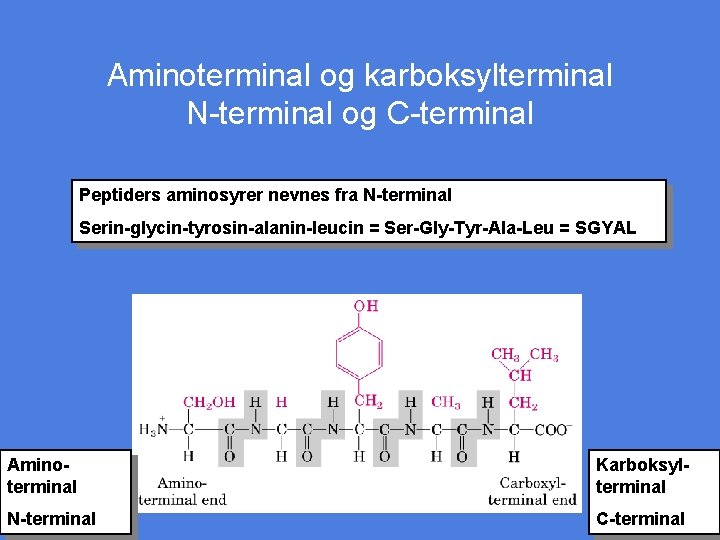
Aminoterminal og karboksylterminal N-terminal og C-terminal Peptiders aminosyrer nevnes fra N-terminal Serin-glycin-tyrosin-alanin-leucin = Ser-Gly-Tyr-Ala-Leu = SGYAL Aminoterminal Karboksylterminal N-terminal C-terminal

Proteiners nettoladning • I proteiner er både amino- og karbosylgruppen bundet opp i peptidbindingen og bidrar ikke til nettoladning, bortsett fra første og siste aminosyre • Aminosyrenes sidekjeder bestemmer da nettoladningen • I praksis er dette Asp, Glu, Lys, Arg og tildels His • I tilleg har Cys (p. Kr 8, 18) og Tyr (p. Kr 10, 07) potensielt ioniserbare sidekjeder, men ved fysiologisk p. H bidrar disse ikke
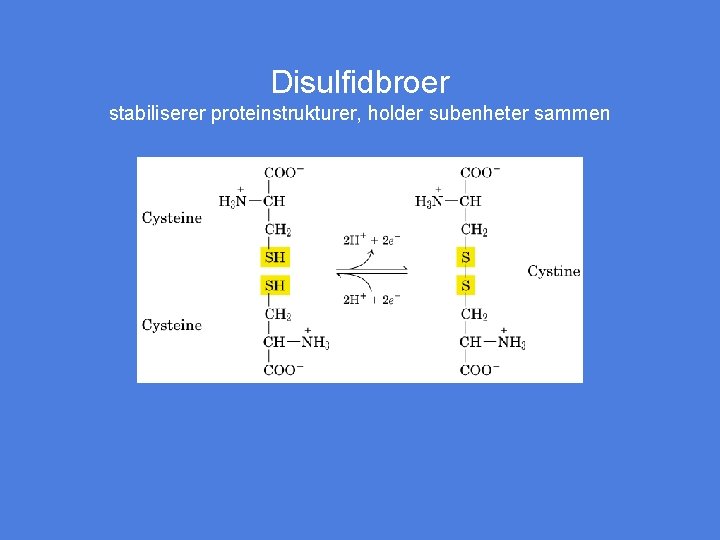
Disulfidbroer stabiliserer proteinstrukturer, holder subenheter sammen Figur 5 -7

Disulfidbroer • Kovalente bindinger mellom forskjellige områder av samme polypeptidkjede • Kovalente bindinger mellom uavhengige polypeptidkjeder Insulin
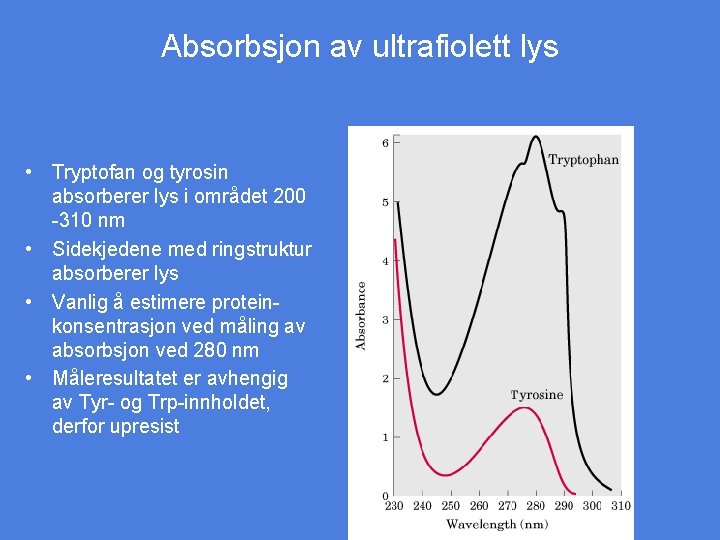
Absorbsjon av ultrafiolett lys • Tryptofan og tyrosin absorberer lys i området 200 -310 nm • Sidekjedene med ringstruktur absorberer lys • Vanlig å estimere proteinkonsentrasjon ved måling av absorbsjon ved 280 nm • Måleresultatet er avhengig av Tyr- og Trp-innholdet, derfor upresist Figur 5 -6
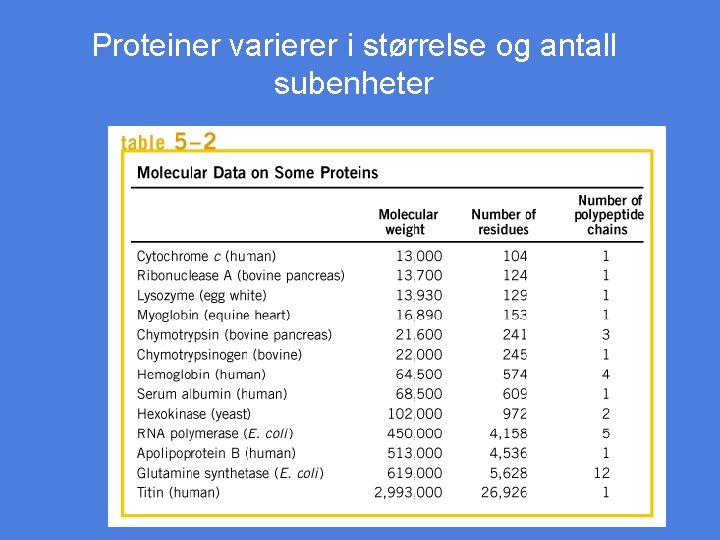
Proteiner varierer i størrelse og antall subenheter Tablee 5 -2

Proteiners aminosyresammensetning varierer Tabell 5 -3
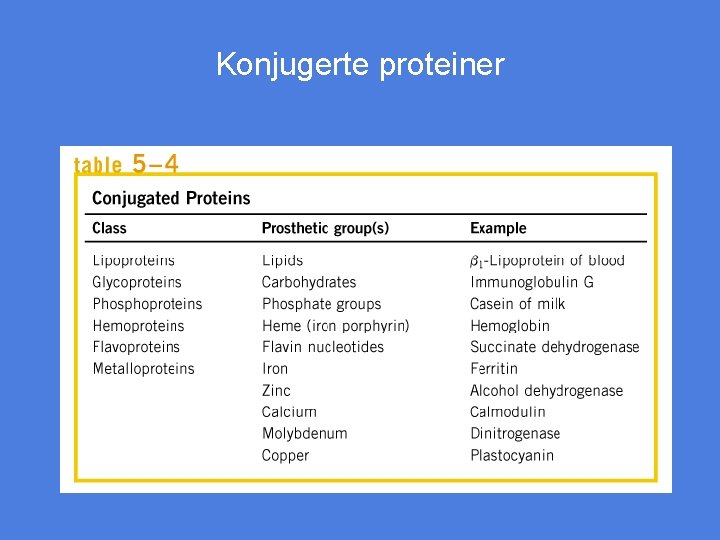
Konjugerte proteiner Tabell 5 -4
- Slides: 35