AMINOACIDOS Y PROTEINAS Aminoacidos Unidades estructurales bsicas que

AMINOACIDOS Y PROTEINAS

Aminoacidos � Unidades estructurales básicas que forman las proteínas. � Mas de 100 aa descritos. � Solo 22 participan en la síntesis de proteínas eucariotas.
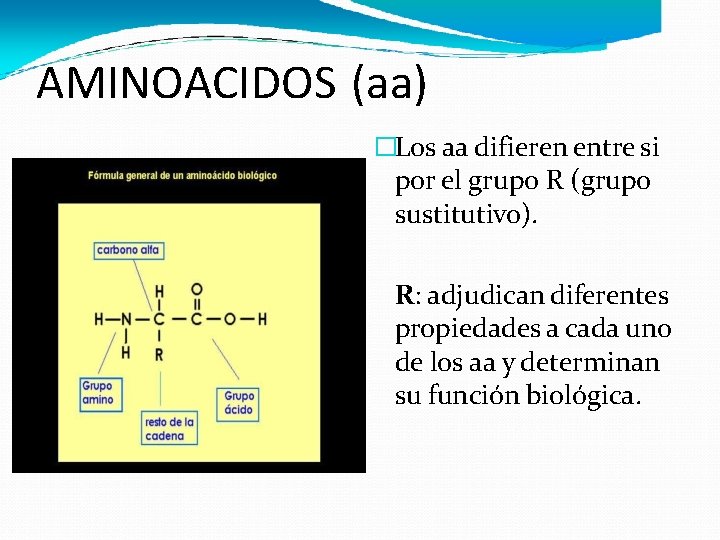
AMINOACIDOS (aa) �Los aa difieren entre si por el grupo R (grupo sustitutivo). R: adjudican diferentes propiedades a cada uno de los aa y determinan su función biológica.

Carbono Aminoacidos estructura Carbono Alfa Hidrogeno

Carbono Aminoacidos estructura CLASIFICACION Atendiendo a la naturaleza del grupo -R los aas pueden clasificarse en: · Neutros o apolares · Polares sin carga · Polares con carga negativa · Polares con carga positiva

alanina, valina, leucina e isoleucina. Ejmp Clasificación de los aa En función de la naturaleza de su cadena lateral: � Aa alifáticos cuyo R no es polar: Son muy poco reactivos, y fuertemente hidrofóbicos (excepto la Gly, cuya cadena lateral es un átomo de hidrógeno). Eje: Alanina, valina, leucina e isoleucina, metionina � Aa alifáticos cuyo R es polar pero no tiene carga: serina, treonina, cisteina, prolina asparragina y glutamina. Aminoácidos alifáticos. se encuetran los aminoácidos cuya cadena lateral es alifática, es decir una cadena hidrocarbonada

Clasificación de los aa En función de la naturaleza de su cadena lateral: � Aa alifáticos cuyo R es polar y se encuentra en estado de ion positivo: lisina, arginina e histidina. � Aa alifáticos cuyo R es polar y se encuentra en estado de ion negativo: aspartato y glutamato. � Aminoácidos aromáticos: Fenilalanina, tirosina, triptofano Aminoacidos aromáticos; aminoácidos cuya cadena lateral posee un anillo aromático (grupo fenil ) formado por 6 átomos de carbono y 5 átomos de hidrógeno.

Estructura de los aminoácidos �Por su estructura, los aa se ionizan en solucion acuosa de manera que pueden funcionar como ácidos y �como bases (anfoliticos). �Los aa que poseen un g. amino y un g. carboxilo (Gly, Leu, Ile) se convierten en iones dipolares � (Zwitteriones). � Estos net iones en slns acuosas son eléctricamente neutros y no emigran ni se someten a campos a eléctricos.
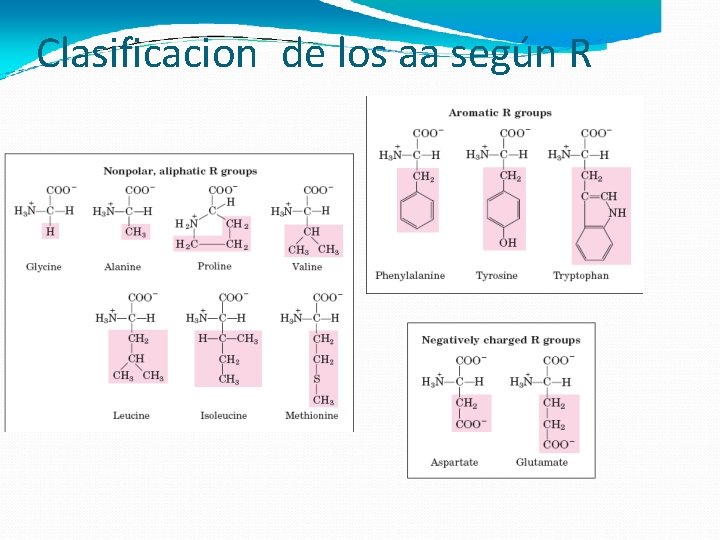
Clasificacion de los aa según R

Clasificacion de los aa según R
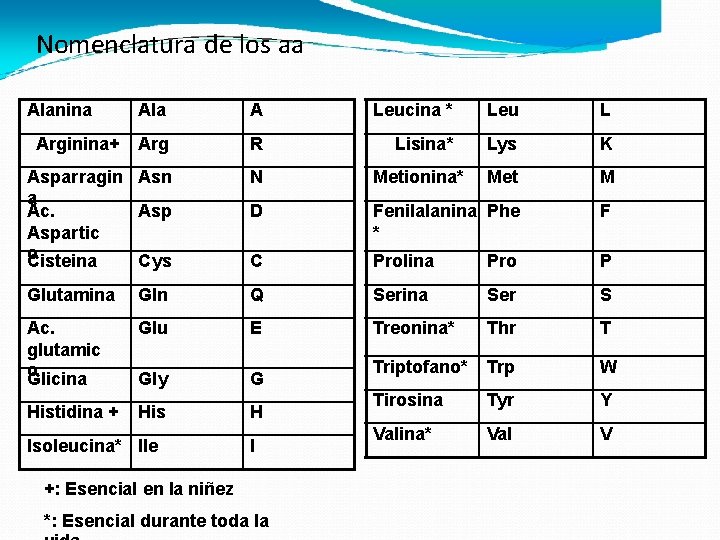
Nomenclatura de los aa Alanina Ala A Leucina * Leu L Arg R Lisina* Lys K Asparragin Asn a Ac. Aspartic o Cisteina Cys N Metionina* Met M D Fenilalanina Phe * F C Prolina Pro P Glutamina Gln Q Serina Ser S Ac. glutamic o Glicina Glu E Treonina* Thr T Gly G Triptofano* Trp W Histidina + His H Tirosina Tyr Y Valina* Val V Arginina+ Isoleucina* Ile I +: Esencial en la niñez *: Esencial durante toda la
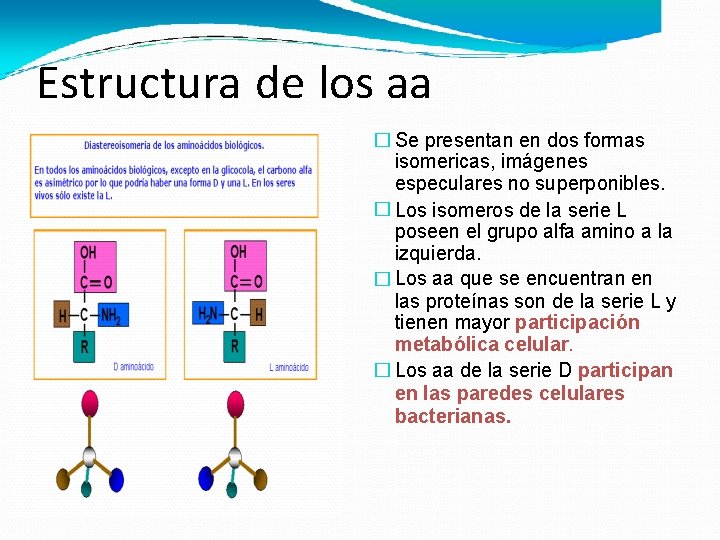
Estructura de los aa � Se presentan en dos formas isomericas, imágenes especulares no superponibles. � Los isomeros de la serie L poseen el grupo alfa amino a la izquierda. � Los aa que se encuentran en las proteínas son de la serie L y tienen mayor participación metabólica celular. � Los aa de la serie D participan en las paredes celulares bacterianas.

FORMACION DE PEPTIDOS Y POLIPEPTIDOS � Los aa se unen o polimerizan por medio de enlaces peptídicos: la unión química entre el grupo carboxil de un aa con el grupo amino de otro aa, con la liberación de una molécula de agua. � La rx + importante de los aa es la formación de un enlace peptídico ya que este enlace carece de carga a cualquier p. H de interés fisiológico.
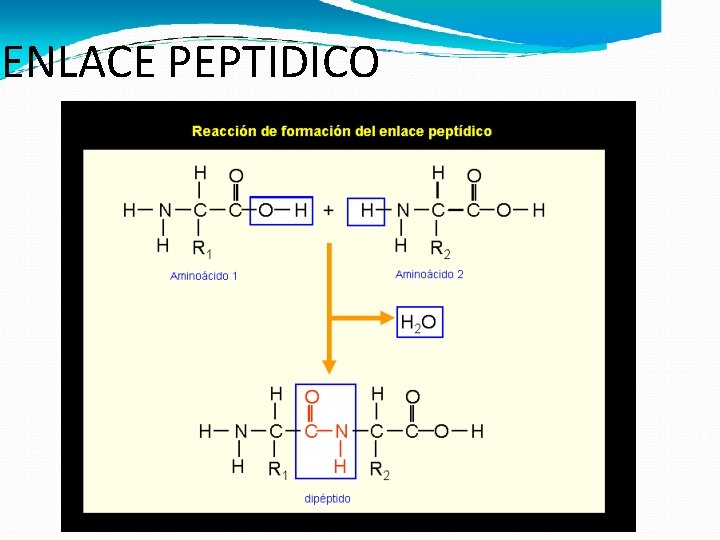
ENLACE PEPTIDICO

PEPTIDOS Y POLIPEPTIDOS La unión de dos o más aa hasta un máximo de 100 mediante enlaces peptídicos da lugar a los péptidos: � 2 aa = dipéptido � 3 aa =tripeptido, ……. . �Menos de 10 aa ………………Oligopeptido �Mas de 10 hasta 100 aa…………. . Polipéptido �Mas de 100 aa………………. . Proteína


PROTEINAS Son moléculas formadas por cadenas lineales de mas de 100 aminoácidos unidos por enlaces peptidicos.

PROTEINAS �Son cadenas de aa, su peso molecular va de 5, 000 a 400, 000 daltons, pudiendo llegar hasta un millon de daltons. �El enlace peptídico es un enlace covalente se requiere de ácidos fuertes para romperlo, en el organismo solamente se rompe por enzimas �proteasas Eje peptídico: a lo largo de este eje de grupos carboxilos se acomodan las cadenas laterales de los aa que conforman la proteína.

Clasificación de las proteínas Desde un punto de vista químico, existen dos grandes grupos de proteínas: 1. proteínas simples: formadas exclusivamente por a-aminoácidos, como es el caso de la albumina, es una protéina formada 1. proteínas por 585 AA. conjugadas: que contienen además de la cadena polipeptídica un que puede ser azúcar, un lípido, ungrupo ácido componente noun aminoacídico llamado nucleico o simplemente un ión inorgánico. prostético,

Clasificación de las proteínas �La proteína en ausencia de su grupo prostético no es funcional, y se llama �La proteína unida a su grupo apoproteína. prostético es funcional, y se llama holoproteína (holoproteína apoproteína + �Son proteínas =conjugadas; grupo (Heteroproteinas) la hemoglobina, prostético). la mioglobina, los citocromos, etc.

Clasificación Encuanto a su forma molecular, podemos distinguir: proteínas globulares: la cadena polipeptídica 1. aparece enrollada sobre sí misma dando lugar a una estructura más o menos esférica y compacta. Ejm: Mioglobina y Hemoglobina 2. proteínas fibrosas: si hay una dimensión que predomina sobre las demás, se dice que la proteína es fibrosa. � Las proteínas fibrosas, por lo general, tienen funciones estructurales. � Prot de la piel, el pelo, la � seda. Son siempre alargadas Son menos abundantes que las globulares

Por niveles de organización de la proteínas Estructura primaria Estructura secudaria Estructura terciaria Estructra Cuaternaria
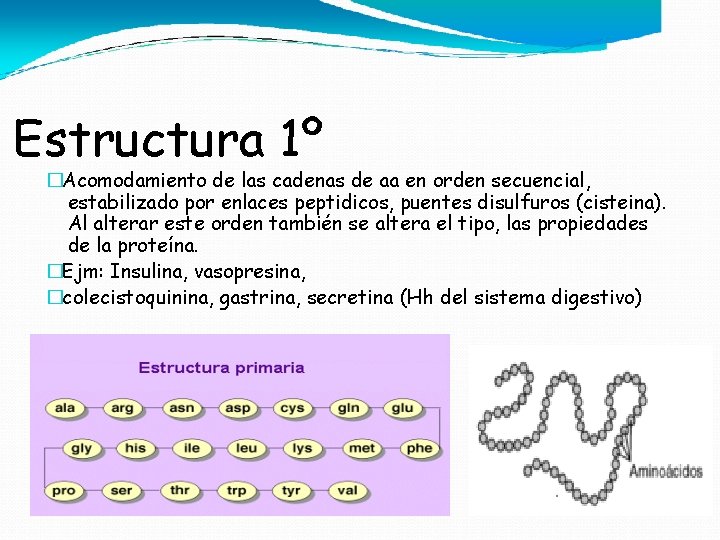
Estructura 1º �Acomodamiento de las cadenas de aa en orden secuencial, estabilizado por enlaces peptidicos, puentes disulfuros (cisteina). Al alterar este orden también se altera el tipo, las propiedades de la proteína. �Ejm: Insulina, vasopresina, �colecistoquinina, gastrina, secretina (Hh del sistema digestivo)
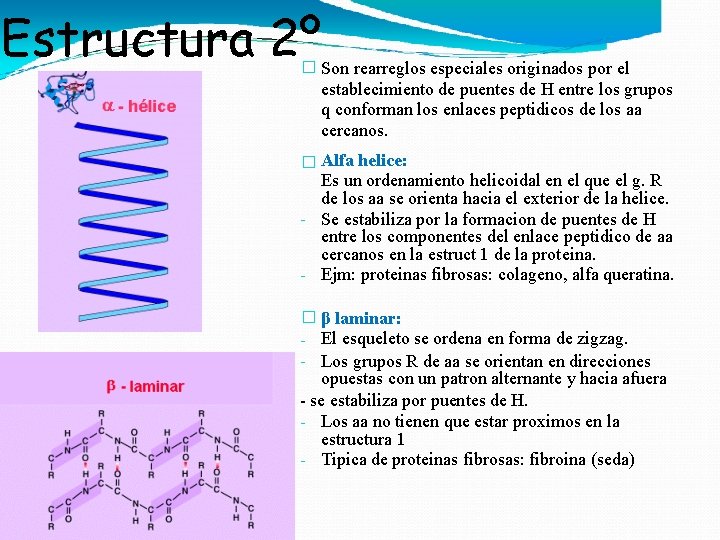
Estructura 2º � Son rearreglos especiales originados por el establecimiento de puentes de H entre los grupos q conforman los enlaces peptidicos de los aa cercanos. � Αlfa helice: Es un ordenamiento helicoidal en el que el g. R de los aa se orienta hacia el exterior de la helice. - Se estabiliza por la formacion de puentes de H entre los componentes del enlace peptidico de aa cercanos en la estruct 1 de la proteina. - Ejm: proteinas fibrosas: colageno, alfa queratina. � β laminar: - El esqueleto se ordena en forma de zigzag. - Los grupos R de aa se orientan en direcciones opuestas con un patron alternante y hacia afuera - se estabiliza por puentes de H. - Los aa no tienen que estar proximos en la estructura 1 - Tipica de proteinas fibrosas: fibroina (seda)

Estructura 3º �Es una modificación en el espacio, es el plegamiento tridimensional total de la cadena de una proteína o sea que se forma una proteína tridimensional, en la estructura terciaria se encuentran segmentos de estructura 2º y 1º. �Esta conformación facilita la solubilidad en agua y así realizar funciones de transporte, enzimáticas, hormonales, etc. �Ejm: mioglobina

Estructura 4º �Nivel mas complejo de organización. �Interacciones no covalentes que unen varias cadenas polipeptidicas en una sola molécula. �Cada cadena polipeptídica recibe el nombre de protómero. �El número de protómeros (cadenas) varía: 2 en la hexoquinasa (enzima tipo transferasa de P) 4 en la hemoglobina 60 en cápside del virus de la poliomielitis,

Estructura 4º Esta conformación se mantiene estable gracias la existencia de enlaces entre los radicales R de los aminoácidos. Aparecen varios tipos de enlaces: � los puentes de hidrógeno los puentes eléctricos entre aa de carga �diferente llamados tambien “atracciones electrostáticas” �las interacciones hidrófobas formación de un núcleo hidrofobito o interface hidrofobico �el puente disulfuro a
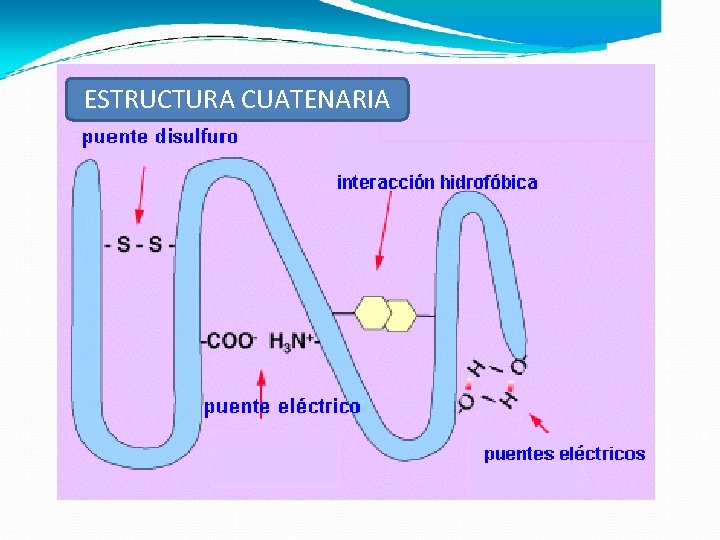
ESTRUCTURA CUATENARIA
- Slides: 28