AMINAS SEMANA 23 2015 Licda Isabel Fratti de

AMINAS SEMANA 23 ---- 2015 Licda: Isabel Fratti de del Cid Diapositivas con cuadros e imágenes, y estructuras proporcionadas por la Licda: Lilian Guzmán.

AMINAS 2 Compuestos nitrogenados que se pueden considerar como derivados del amoniaco ( NH 3), donde 1, 2, o 3 de sus hidrógenos, son sustituidos por radicales alifáticos ó aromáticos, ó ambos. . - NLas aminas poseen carácter básico debido a la presencia del Nitrógeno en el grupo AMINO. ; pues éste Nitrógeno posee , un par de electrones no compartidos( recordar concepto de base según Lewis)

Clasificación, en base al número de radicales unidos al Nitrógeno 3 Se dividen en 3 clases según el número de grupos alquilo ó arilo unidos al nitrógeno.

Nomenclatura 4 Común Identifique los radicales unidos al nitrógeno, nómbrelos alfabéticamente y a continuación coloque la palabra amina. Si el mismo grupo está presente dos ó tres veces use prefijos “di” ó “tri” UIQPA : se nombran como derivados del alcano, haciendo terminar su nombre en amina, la posición del grupo amino se da por un número.

Algunos ejemplos de aminas primarias: CH 3 CH 2 CH 2 -NH 2 Común : n-butilamina UIQPA: 1 -Butanamina CH 3 CH 2 CHCH 3 NH 2 Común: sec-butilamina UIQPA : 2 -Butanamina. Escriba la estructura de la terbutilamina y de nombre UIQPA
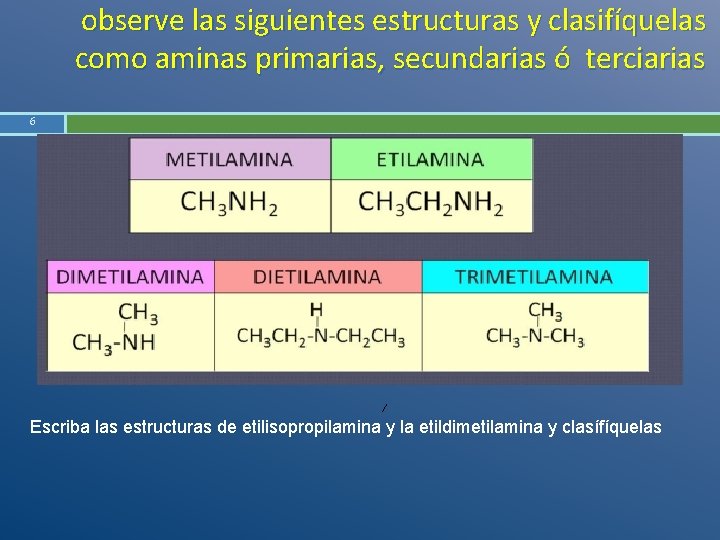
observe las siguientes estructuras y clasifíquelas como aminas primarias, secundarias ó terciarias 6 Escriba las estructuras de etilisopropilamina y la etildimetilamina y clasífíquelas

Las aminas aromáticas pueden nombrarse como derivadas de la anilina, o bien usarse los nombres de los radicales presentes incluyendo al radical fenil y usando la palabra amina, en el siguiente cuadro, se ven los ejemplos.
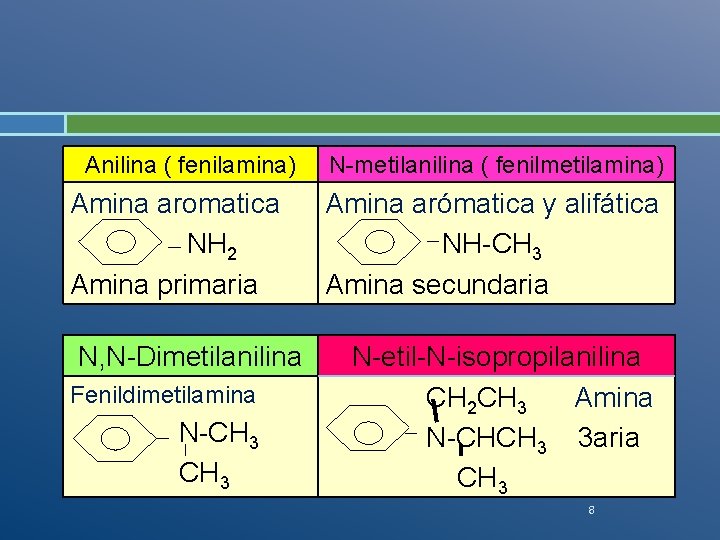
Anilina ( fenilamina) Amina aromatica NH 2 Amina primaria N, N-Dimetilanilina Fenildimetilamina N-CH 3 N-metilanilina ( fenilmetilamina) Amina arómatica y alifática NH-CH 3 Amina secundaria N-etil-N-isopropilanilina CH 2 CH 3 Amina N-CHCH 3 3 aria CH 3 8
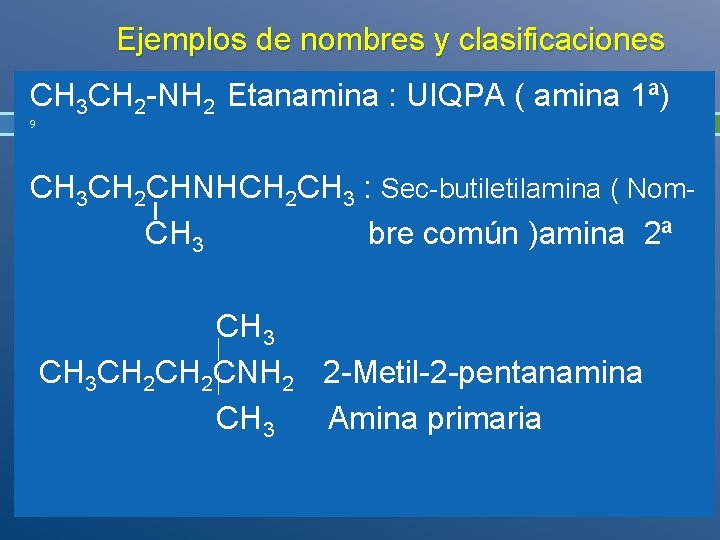
Ejemplos de nombres y clasificaciones CH 3 CH 2 -NH 2 Etanamina : UIQPA ( amina 1ª) 9 CH 3 CH 2 CHNHCH 2 CH 3 : Sec-butiletilamina ( Nom. CH 3 bre común )amina 2ª CH 3 CH 2 CNH 2 2 -Metil-2 -pentanamina CH 3 Amina primaria

Propiedades Físicas 10 - - - Los miembros inferiores de la serie son gases incoloros, solubles en agua y poseen olores penetrantes, algunos veces parecidos al amoniaco. Si poseen radicales pequeños, poseen olor a pescado Ej: dimetilamina, trimetilamina). La putrescina y cadaverina son responsables del olor a carne descompuesta: animal muerto y cadáver humano. H 2 NCH 2 CH 2 NH 2 Putrescina 1, 4 -butanodiamina H 2 NCH 2 CH 2 CH 2 NH 2 Cadaverina 1, 5 -pentanodiamina

Las aminas primarias y secundarias, pueden formar puentes de hidrógeno entre ellas mismas ó bien entre ellas y el agua. A ésto se debe que posean puntos de ebullición superiores a los alcanos de peso molecular semejante, las terciarias no poseen hidrogeno unido al nitrógeno y no forman puentes de hidrogeno entre sus moléculas. Las aminas de 1 -6 carbonos son solubles en agua, incluso las terciarias.
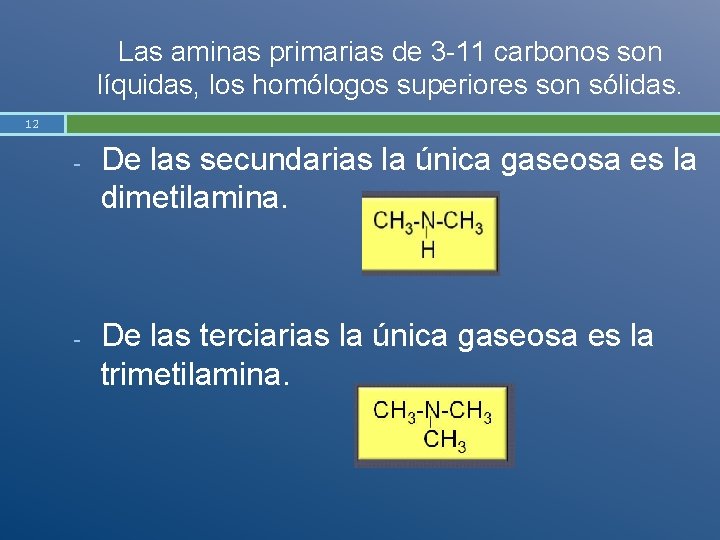
Las aminas primarias de 3 -11 carbonos son líquidas, los homólogos superiores son sólidas. 12 - - De las secundarias la única gaseosa es la dimetilamina. De las terciarias la única gaseosa es la trimetilamina.

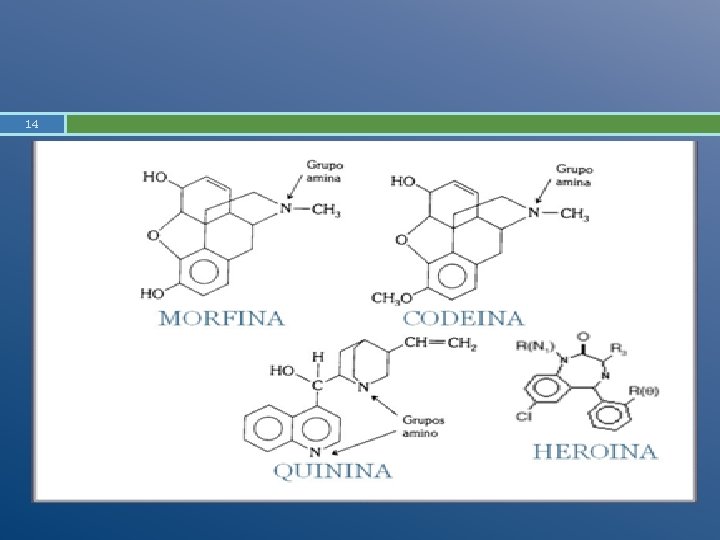
13 Gran cantidad de aminas se obtienen de la corteza, raíces, hojas, flores o frutos de varias plantas. Estas aminas con actividad fisiológica que se presentan en forma natural se denominan alcaloides Algunos ejemplos son: Codeína, Morfina, quinina, Heroína, que es una modificación quimica de un alcaloide natural. Como lo indica su nombre son alcalinas de ahí la palabra alcaloides.
14
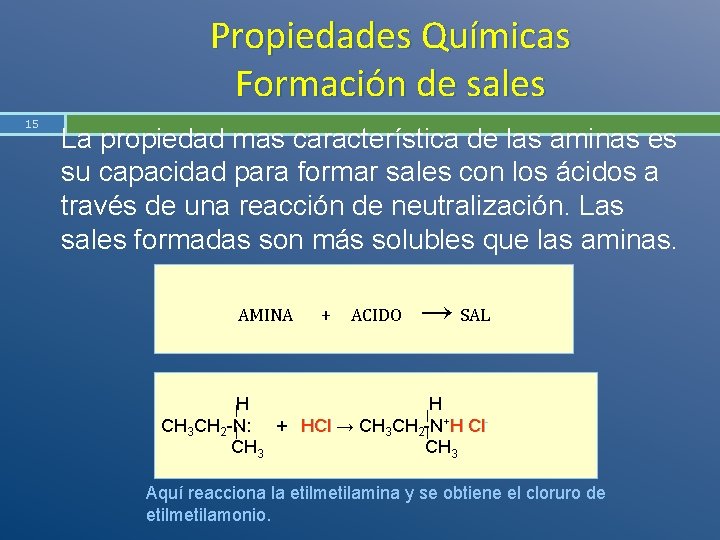
Propiedades Químicas Formación de sales 15 La propiedad mas característica de las aminas es su capacidad para formar sales con los ácidos a través de una reacción de neutralización. Las sales formadas son más solubles que las aminas. AMINA + ACIDO → SAL H H CH 3 CH 2 -N: + HCl → CH 3 CH 2 -N+H Cl. CH 3 Aquí reacciona la etilmetilamina y se obtiene el cloruro de etilmetilamonio.

Importancia de la formación de sales de amonio cuaternarias Al igual que la mayoría de sales, éstas sales de amonio cuaternarias, son iónicas muy solubles en agua y líquidos corporales, por ésta razón muchas aminas con acción farmacológica, son moléculas grandes, insolubles en agua y al convertirlas en sales de amonio cuaternaria se hacen más solubles en agua y líquidos corporales, por lo tanto la acción farmacológica es más rápida.

Ejemplos de formación de sales CH 3 CH 2 NH 2 + HCl CH 3 CH 2 NH 3+Cl. Etilamina Cloruro de etilamonio Estas sales son más solubles en agua y líquidos corporales que las aminas respectivas. 1 -Escriba la reacción y de nombre del producto de: Etilmetilamina y HBr. 2 - Escriba la reacción que muestra la formación del cloruro de Dimetilamonio

Aminas Heterocíclicas Son compuestos orgánicos cíclicos que consisten en un anillo de cinco a seis átomos, de los cuales uno ó dos son átomos de Nitrógeno, los demás son átomos de carbono. Entre algunos ejemplos tenemos la piperidina, que es parte del sabor y la sensación picante de la pimienta. Algunas forman parte de las bases nitrogenadas de los ácidos nucleicos, son parte del grupo Hem de la hemoglobina y los citocromos y de la clorofila.
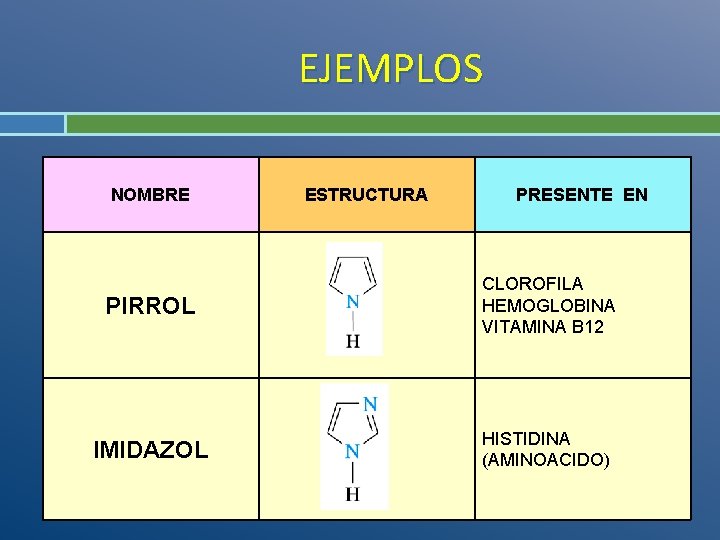
EJEMPLOS NOMBRE ESTRUCTURA PRESENTE EN PIRROL CLOROFILA HEMOGLOBINA VITAMINA B 12 IMIDAZOL HISTIDINA (AMINOACIDO)
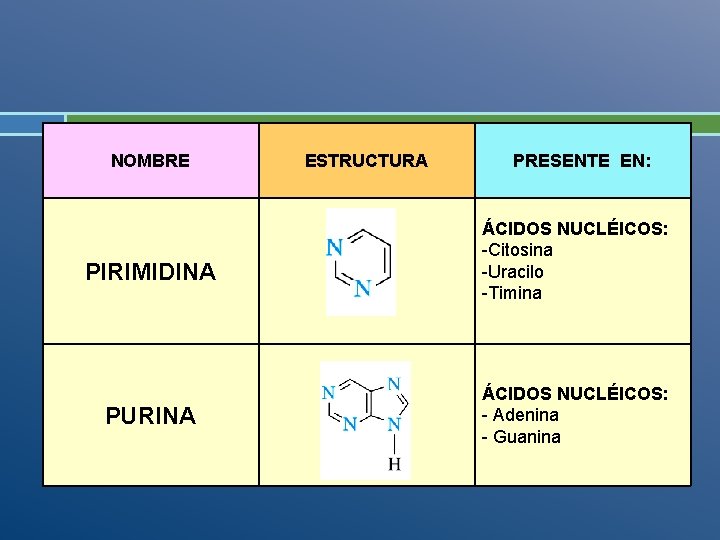
NOMBRE PIRIMIDINA PURINA ESTRUCTURA PRESENTE EN: ÁCIDOS NUCLÉICOS: -Citosina -Uracilo -Timina ÁCIDOS NUCLÉICOS: - Adenina - Guanina

Ejercicios Escriba la estructura de las siguientes aminas y clasifiquelas ( 1 as, 2 as, 3 as): a)3 -Hexanamina b) trietilamina C) 1 -Pentanamina d) Etilfenilmetilamina

Lea Química y salud; SINTESIS DE MEDICAMENTOS pág: 653 y coméntelas.
- Slides: 22