ALUMINIJUM https www shtreber comaluminijumbakariostalimetali http www wikiwand
ALUMINIJUM https: //www. shtreber. com/aluminijum-bakar-i-ostali-metali http: //www. wikiwand. com/bs/Aluminij

OTKRIĆE ALUMINIJUMA Naučnik Dejvi je 1808. opisao aluminijum. Zahvaljujući naučniku Fridrihu Veleru aluminijum je izolovan 1827. godine. Hans Christian Ørsted (1777 - 1851) Sir Humphry Davy (1778 - 1829)

STIPSA Naziv aluminijum je nastao od latinske reči alaun, što znači stipsa.
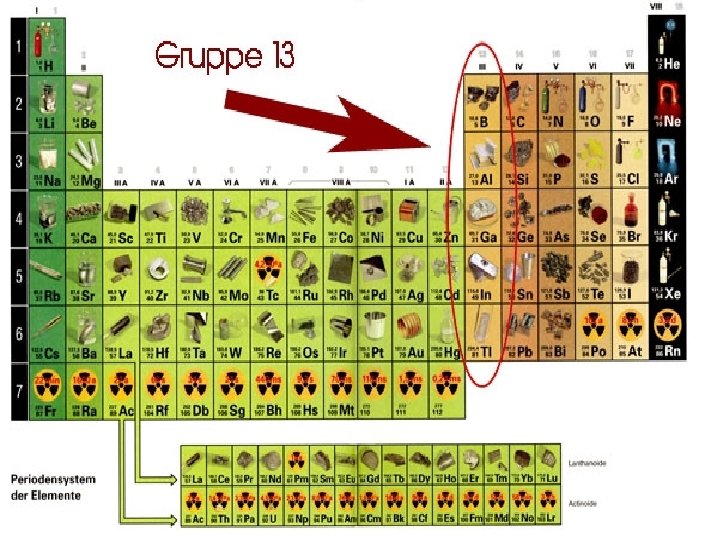
NALAŽENJE ALUMINIJUMA U TABLICI PSE Aluminijum se u Tablici PSE nalazi u IIIa (13) grupi i 3. periodi.

NALAŽENJE ALUMINIJUMA U PRIRODI - NEMA GA U SLOBODNOM STANJU: Aluminijum je najzastupljeniji metal u zemljinoj kori (oko 8%). - JEDINJENJA – RUDE: Alumijium-oksid se nalazi u obliku korunda, koji, u zavisnosti od primesa, može da bude raznih boja, kao drago kamenje: ljubičast – ametist crven – rubin safir – plav smaragd – zelen topaz - žut Al 2 O 3 x H 2 O – boksit koji se dobija iz glinice

MINERALI ALUMINIJUMA • Najpoznatiji alumosilikati su glinenci i liskumi. raspadanjem glineraca nastaje glina. • Od minerala aluminijuma najznačajniji su: Korund - Al 2 O 3 Boksit - Al 2 O 3 x H 2 O Kriolit - 3 Na. F x Al. F 3

OBLICI POSTOJANJA ALUMINIJUMA Levo su neobrađeni kristali korunda, a desno: safir, smaragd i rubin.

KRIOLIT BOKSIT KORUND
IZOTOPI ALUMINIJUMA • Jedini stabilni izotop mu je 27 Al http: //www. planeta. rs/15/12 hemija. htm https: //sh. wikipedia. org/wiki/Aluminijum

DOBIJANJE ALUMINIJUMA U vremenu kada je živeo Mendeljejev, aluminijum je bio skuplji od zlata, zbog skupog postupka za njegovo dobijanje. http: //www. slideshare. net/vvli/aluminijum? next_slideshow=1

FIZIČKA SVOJSTVA ALUMINIJUMA • Aluminijum je metal male tvrdoće, a velike rastegljivosti i savitljivosti, pa se lako izvlači u žice i tanke listove. • Dobar je provodnik struje (ima tek 62% provodljivosti koju ima bakar) • Lagan provodnik (gustina tek 30% gustine bakra). VALENCA ALUMINIJUMA: III http: //afrodita. rcub. bg. ac. rs/~rzoran/Obojeni metali i legure. pdf

HEMIJSKA SVOJSTVA ALUMINIJUMA

• Gori blještavom svetlošću: 4 Al + 3 O 2 → 2 Al 2 O 3 + Q • Aluminijum je amfoteran – ponaša se i kao baza i kao kiselina: 2 Al + 6 HCl → 2 Al. Cl 3 + 2 H 2 O 2 Al + 6 H 3 O+ + 6 H 2 O → 2(Al(H 2 O)6)3+ + 3 H 2 O 2 Al + 2 Na. OH + 2 H 2 O → 2 Na. Al. O 2 + 3 H 2 O(Al. O 2) 2 Al + 2 OH- + 6 H 2 O → 2(Al(OH 4)) + 3 H 2 tetrahidroksianjon • Aluminijum je na vazduhu otporan, jer se na njegovoj površini gradi zaštitni sloj, koji ga štiti od daljih delovanja. • Hidroksidi tehnički važnih metala ne rastvaraju se u vodi i ne mogu se dobiti reakcijom metala i vode ili oksida i vode.

JEDINJENJA ALUMINIJUMA Al 2 O 3 – aluminijum – oksid (bele boje) Al(OH)3 – aluminijum – hidroksid (bele boje)

• KAl(SO 4)2 x 12 H 2 O - kalijum-aluminijum-hidroksid • KAl(SO 4)2 - alaun (stipsa) • Alauni ili stipse su dvostruke soli između jednovalentnog i trovalentnog elektrona. • KAl(SO 4)2 steže površinu služokože pa služi za zaustavljanje krvarenja i kao dezinfekcijsko sredstvo. Upotrebljava se za povezivanje tekstilnih vlakana i u industriji drveta. • Al(SO 4)3 x 18 H 2 O - aluminijum- sulfat -hidroksid • 2 Al(OH)3 +3 H 2 SO 4+12 H 2 OAl(SO 4)3 x 18 H 2 O • Služi za prečišćavanje vode, jer pri hidrolizi gradi beli vakumilozni talog Al(OH)3, koji, kada pada na tlo, povlači za sobom i nečistoće.

LEGURE ALUMINIJUMA

UPOTREBA ALUMINIJUMA Alumijum je, posle Fe, drugi po redu metal koji se koristi u savremenoj mašinskoj tehnici. Upotrebljava se kao čist metal u elektrotehnici, metaloprerađivačkoj, prehrambenoj i hemijskoj industriji, ali mu je mnogo značajnija primena u vidu različitih višekomponentnih legura, koje se široko upotrebljavaju u mašinskoj industriji. Aluminijum se koristi za pravljenje limenki, folija. Al se koristi u tehnici i domaćinstvu za izradu posuđa, u vojnioj industriji, u građevinarstvu, autoindustriji, brodogradnji, avio-industriji itd.

Mnogobrojne legure aluminijuma su dobro redukciono sredstvo. • Upotrebljava se za proizvodnju oksida hroma. Cr 2 O 3 + 2 Al → Al 2 O 3 + 2 Cr Poznat je aluminijum-hidroksid: Al(OH)3, koji se koristi za neutralizaciju viška želudačne kiseline, zajedno sa magnezijum-hidroksidom i magnezijum -karbonatom.
UPOTREBA KORUNDA Al 2 O 3 • Korund je velike tvrdoće, pa se koristi kao šmirgla, odnosno za brušenje. Sloj korunda se koristi i kao kresivo za šibice. Zbog lepih boja, prilične otpornosti i retkosti, korund se koristi i kao drago kamenje.
- Slides: 21