ALKIL HALIDA PRESENTED BY Prof Dr Suyatno M

ALKIL HALIDA PRESENTED BY Prof. Dr. Suyatno, M. Si. DEPARTMENT OF CHEMISTRY STATE UNIVERSITY OF SURABAYA 2020
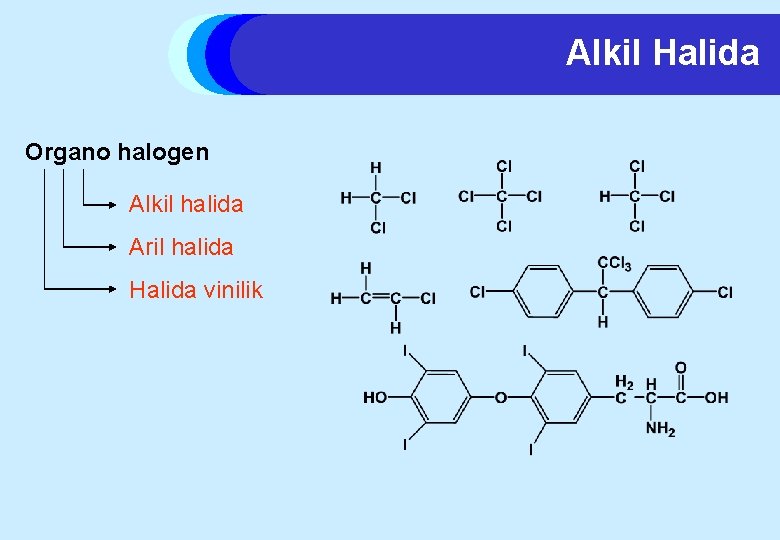
Alkil Halida Organo halogen Alkil halida Aril halida Halida vinilik
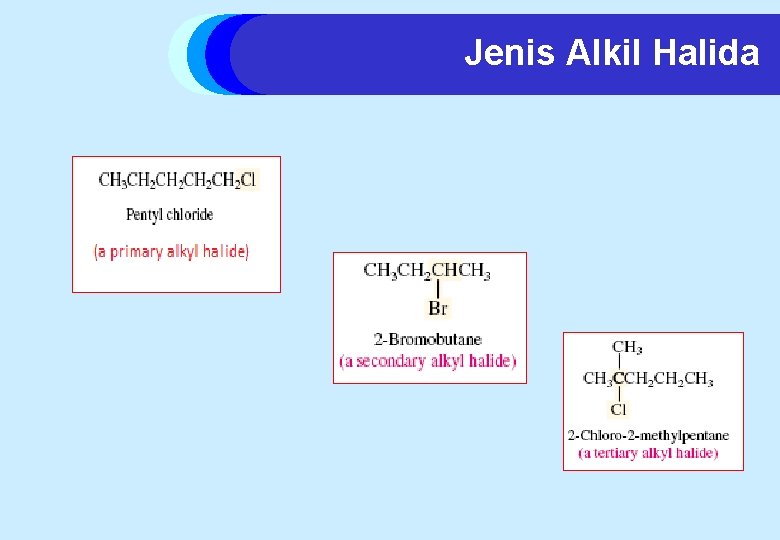
Jenis Alkil Halida
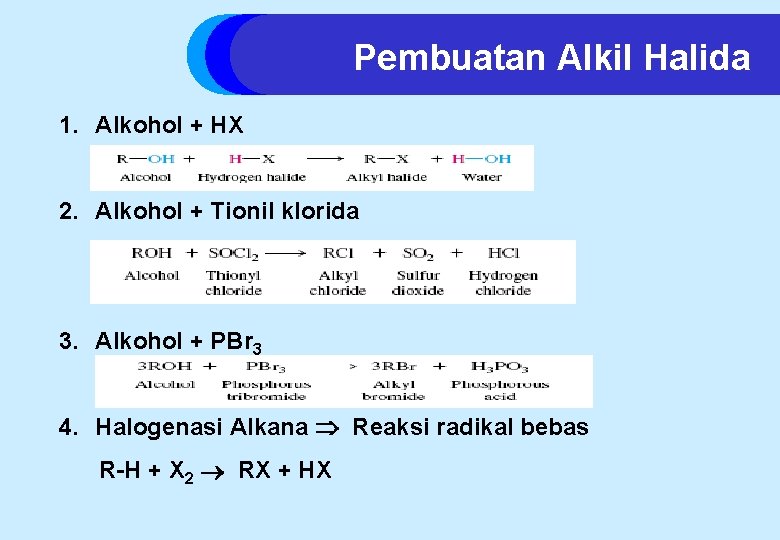
Pembuatan Alkil Halida 1. Alkohol + HX 2. Alkohol + Tionil klorida 3. Alkohol + PBr 3 4. Halogenasi Alkana Reaksi radikal bebas R-H + X 2 RX + HX

Reaksi Alkil Halida 1. Reaksi subtitusi : SN 1 dan SN 2 2. Reaksi eliminasi : E 1 dan E 2
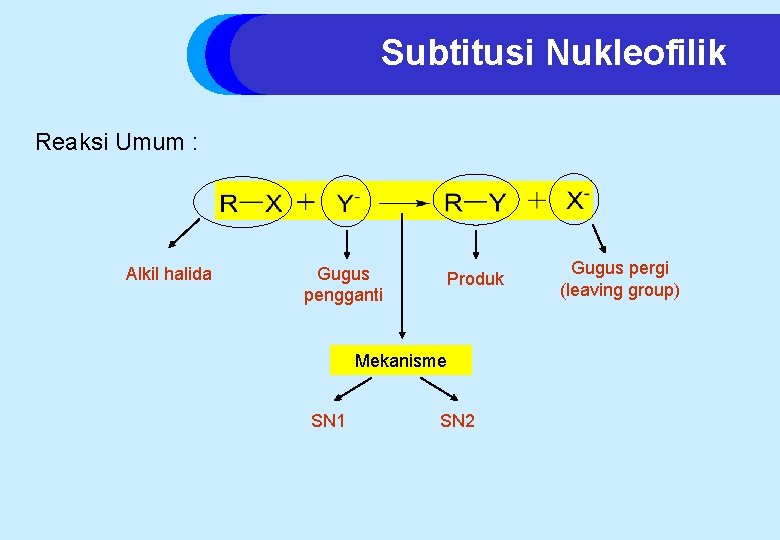
Subtitusi Nukleofilik Reaksi Umum : Alkil halida Gugus pengganti Produk Mekanisme SN 1 SN 2 Gugus pergi (leaving group)
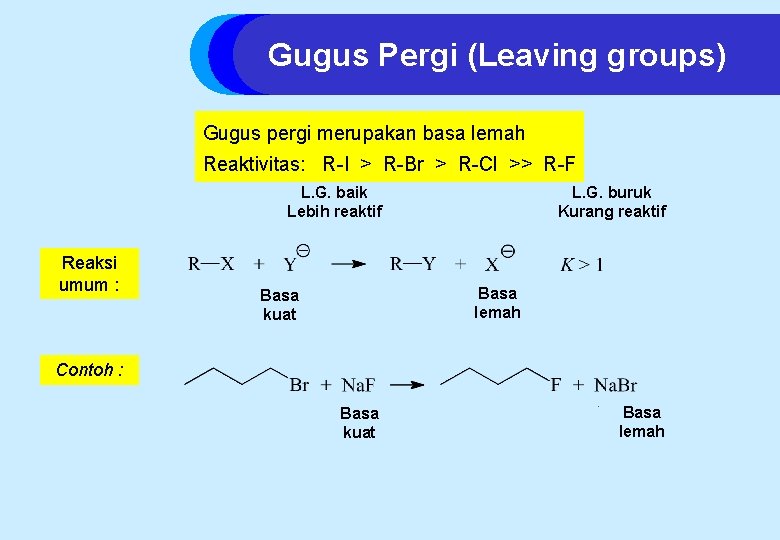
Gugus Pergi (Leaving groups) Gugus pergi merupakan basa lemah Reaktivitas: R-I > R-Br > R-Cl >> R-F L. G. buruk Kurang reaktif L. G. baik Lebih reaktif Reaksi umum : Basa lemah Basa kuat Contoh : Basa kuat Basa lemah
![Mekanisme SN Rumus umum laju reaksi : V = k 1[RX] + k 2[RX][Y–] Mekanisme SN Rumus umum laju reaksi : V = k 1[RX] + k 2[RX][Y–]](http://slidetodoc.com/presentation_image_h2/7b4b8770de119e1474b58275112268b9/image-8.jpg)
Mekanisme SN Rumus umum laju reaksi : V = k 1[RX] + k 2[RX][Y–] k 1 meningkat RX = CH 3 X 1º 2º 3º k 2 meningkat k 1 ~ 0 k 2 ~ 0 V = k 2[RX][Y–] (bimolekular) V = k 1[RX] (unimolekular) SN 2 SN 1
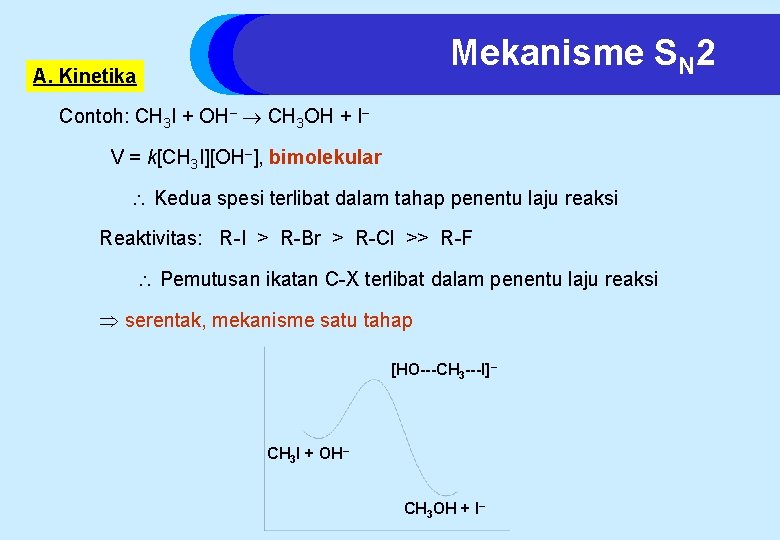
Mekanisme SN 2 A. Kinetika Contoh: CH 3 I + OH– CH 3 OH + I– V = k[CH 3 I][OH–], bimolekular Kedua spesi terlibat dalam tahap penentu laju reaksi Reaktivitas: R-I > R-Br > R-Cl >> R-F Pemutusan ikatan C-X terlibat dalam penentu laju reaksi serentak, mekanisme satu tahap [HO---CH 3 ---I]– CH 3 I + OH– CH 3 OH + I–
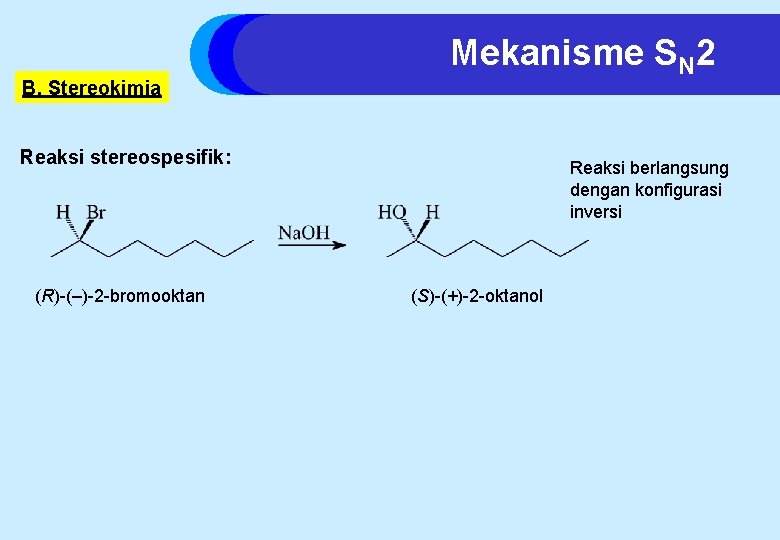
B. Stereokimia Mekanisme SN 2 Reaksi stereospesifik: (R)-(–)-2 -bromooktan Reaksi berlangsung dengan konfigurasi inversi (S)-(+)-2 -oktanol
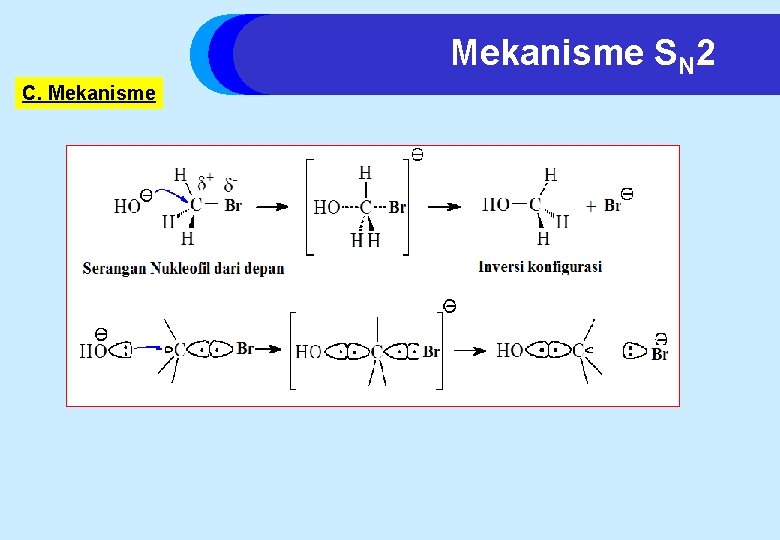
Mekanisme SN 2 C. Mekanisme
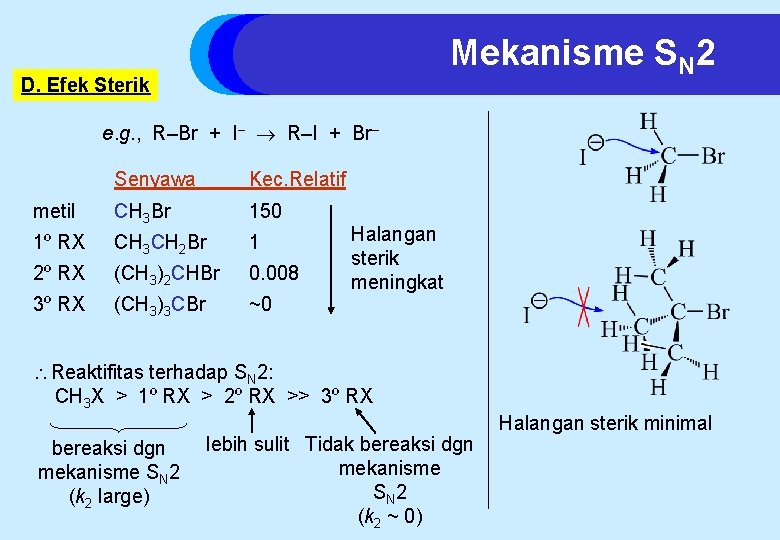
Mekanisme SN 2 Halangan sterik minimal D. Efek Sterik e. g. , R–Br + I– R–I + Br– Senyawa Kec. Relatif metil CH 3 Br 150 1º RX CH 3 CH 2 Br 1 2º RX (CH 3)2 CHBr 0. 008 3º RX (CH 3)3 CBr ~0 Halangan sterik meningkat Reaktifitas terhadap SN 2: CH 3 X > 1º RX > 2º RX >> 3º RX bereaksi dgn mekanisme SN 2 (k 2 large) lebih sulit Tidak bereaksi dgn mekanisme SN 2 (k 2 ~ 0) Halangan sterik minimal
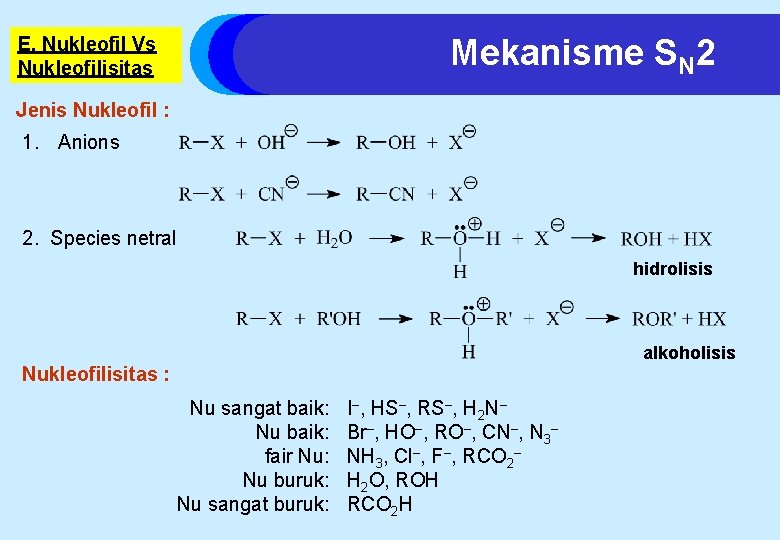
Mekanisme SN 2 E. Nukleofil Vs Nukleofilisitas Jenis Nukleofil : 1. Anions 2. Species netral hidrolisis alkoholisis Nukleofilisitas : Nu sangat baik: Nu baik: fair Nu: Nu buruk: Nu sangat buruk: I–, HS–, RS–, H 2 N– Br–, HO–, RO–, CN–, N 3– NH 3, Cl–, F–, RCO 2– H 2 O, ROH RCO 2 H
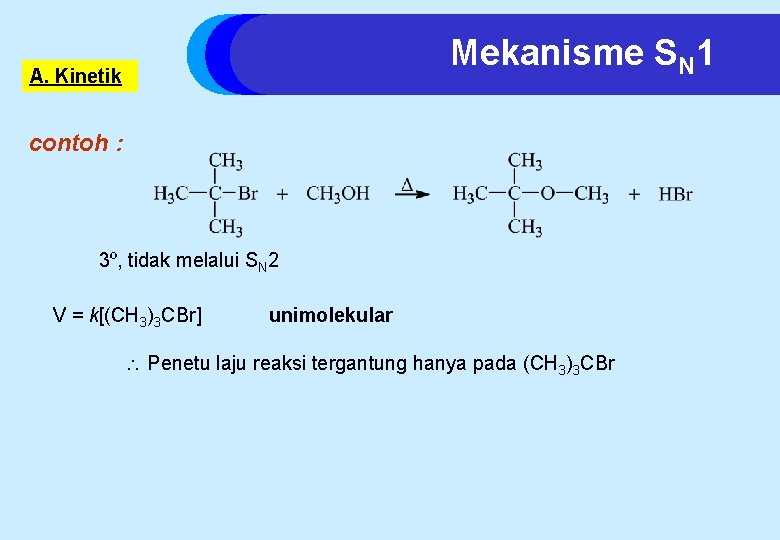
Mekanisme SN 1 A. Kinetik contoh : 3º, tidak melalui SN 2 V = k[(CH 3)3 CBr] unimolekular Penetu laju reaksi tergantung hanya pada (CH 3)3 CBr
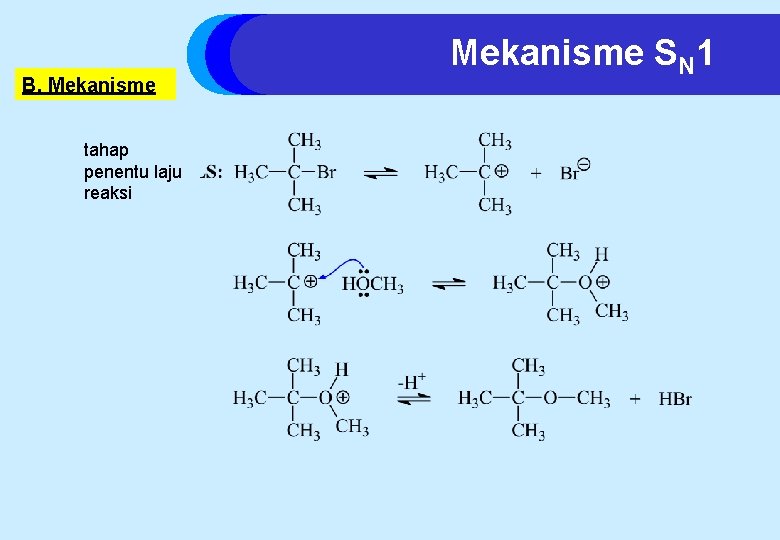
B. Mekanisme tahap penentu laju reaksi Mekanisme SN 1
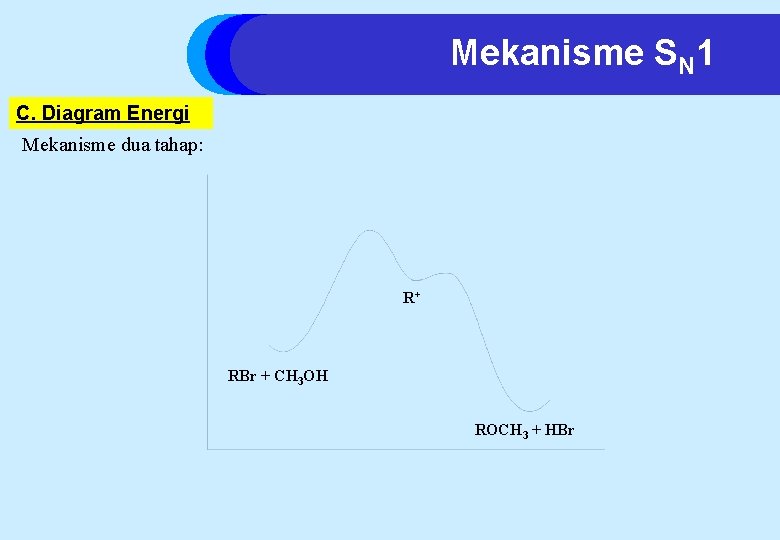
Mekanisme SN 1 C. Diagram Energi Mekanisme dua tahap: R+ RBr + CH 3 OH ROCH 3 + HBr
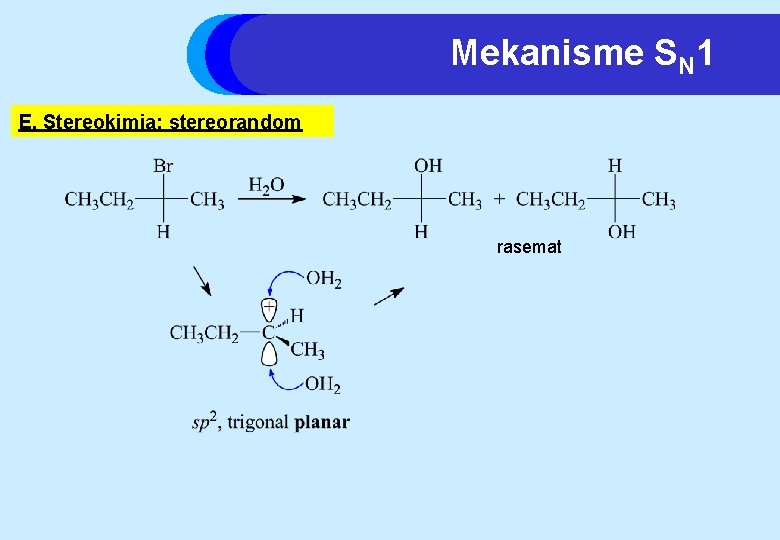
Mekanisme SN 1 E. Stereokimia: stereorandom rasemat
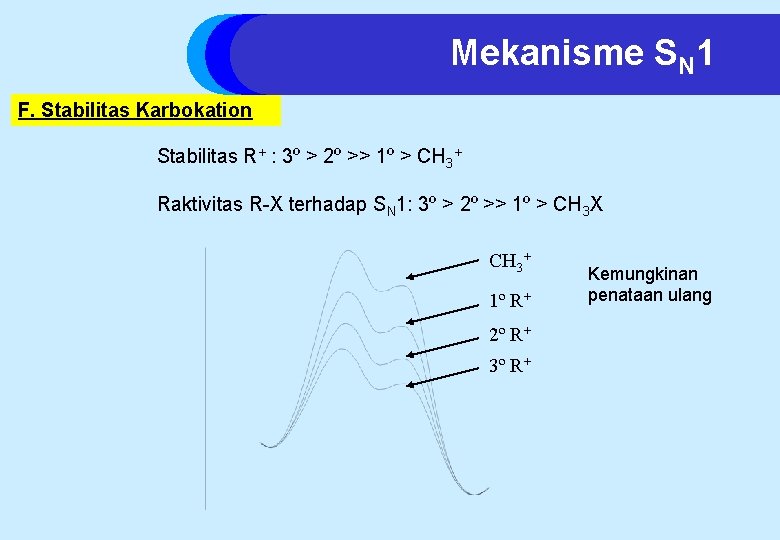
Mekanisme SN 1 F. Stabilitas Karbokation Stabilitas R+ : 3º > 2º >> 1º > CH 3+ Raktivitas R-X terhadap SN 1: 3º > 2º >> 1º > CH 3 X CH 3+ 1º R+ 2º R+ 3º R+ Kemungkinan penataan ulang
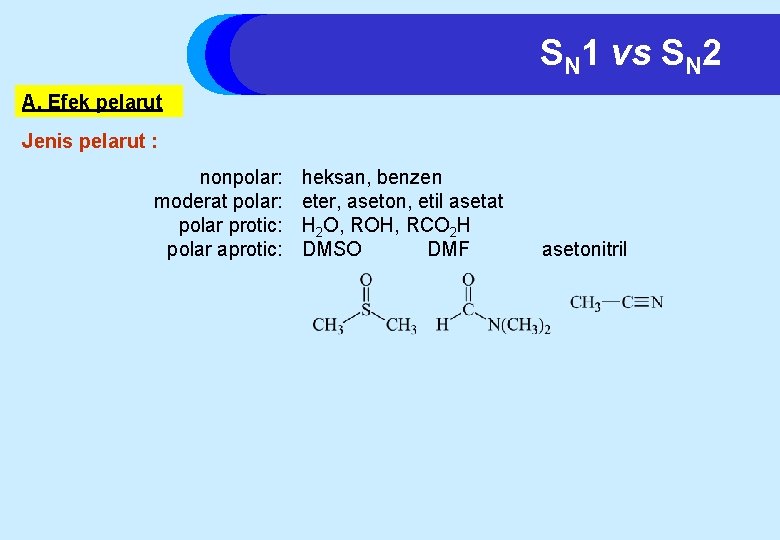
SN 1 vs SN 2 A. Efek pelarut Jenis pelarut : nonpolar: moderat polar: polar protic: polar aprotic: heksan, benzen eter, aseton, etil asetat H 2 O, ROH, RCO 2 H DMSO DMF asetonitril
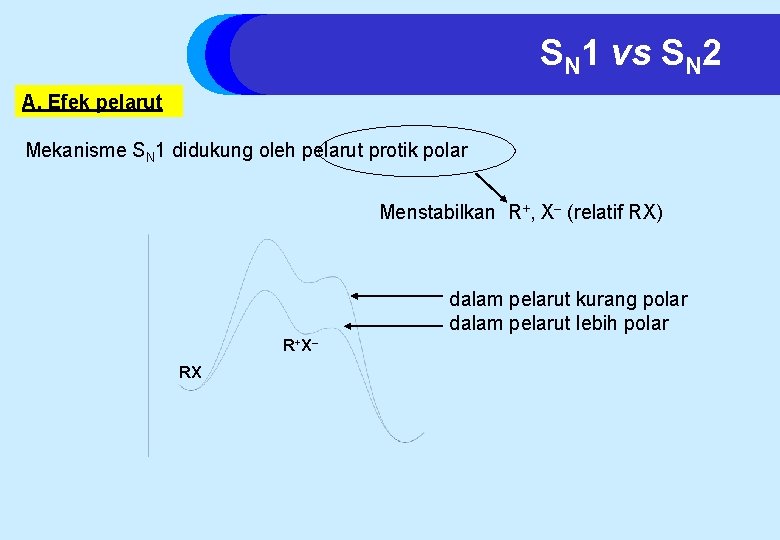
SN 1 vs SN 2 A. Efek pelarut Mekanisme SN 1 didukung oleh pelarut protik polar Menstabilkan R+, X– (relatif RX) dalam pelarut kurang polar dalam pelarut lebih polar R+X– RX
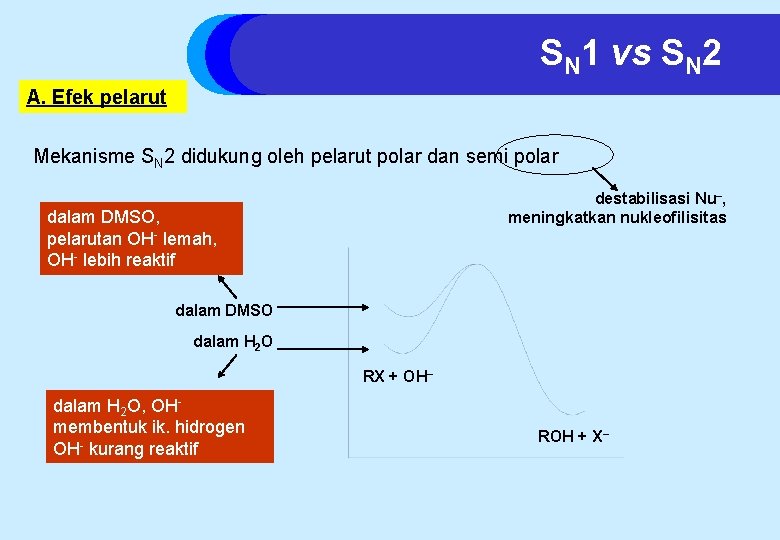
SN 1 vs SN 2 A. Efek pelarut Mekanisme SN 2 didukung oleh pelarut polar dan semi polar destabilisasi Nu–, meningkatkan nukleofilisitas dalam DMSO, pelarutan OH- lemah, OH- lebih reaktif dalam DMSO dalam H 2 O RX + OH– dalam H 2 O, OHmembentuk ik. hidrogen OH- kurang reaktif ROH + X–
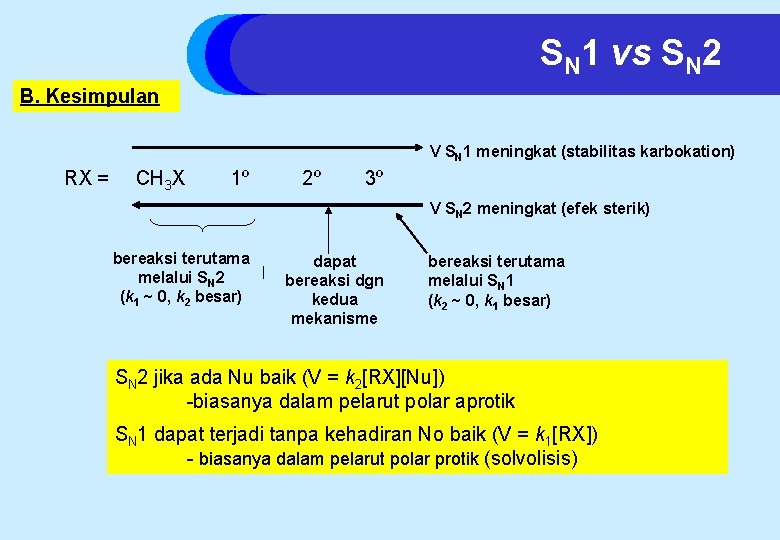
SN 1 vs SN 2 B. Kesimpulan V SN 1 meningkat (stabilitas karbokation) RX = CH 3 X 1º 2º 3º V SN 2 meningkat (efek sterik) bereaksi terutama melalui SN 2 (k 1 ~ 0, k 2 besar) dapat bereaksi dgn kedua mekanisme bereaksi terutama melalui SN 1 (k 2 ~ 0, k 1 besar) SN 2 jika ada Nu baik (V = k 2[RX][Nu]) -biasanya dalam pelarut polar aprotik SN 1 dapat terjadi tanpa kehadiran No baik (V = k 1[RX]) - biasanya dalam pelarut polar protik (solvolisis)
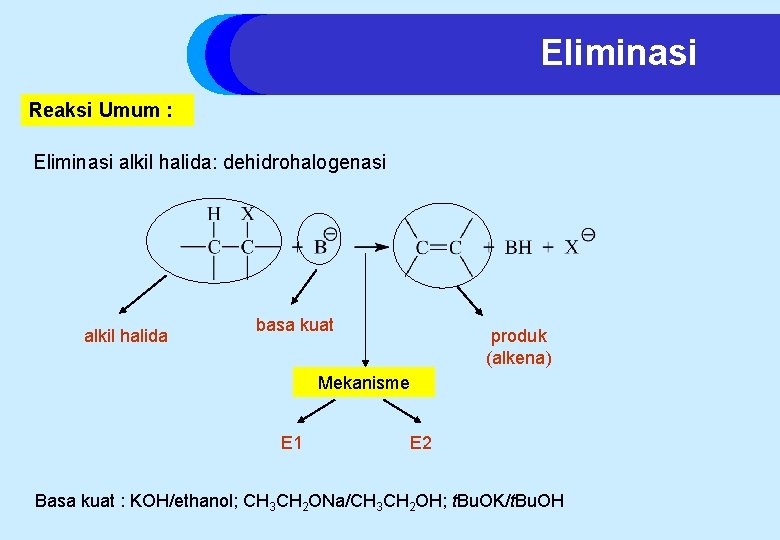
Eliminasi Reaksi Umum : Eliminasi alkil halida: dehidrohalogenasi alkil halida basa kuat produk (alkena) Mekanisme E 1 E 2 Basa kuat : KOH/ethanol; CH 3 CH 2 ONa/CH 3 CH 2 OH; t. Bu. OK/t. Bu. OH
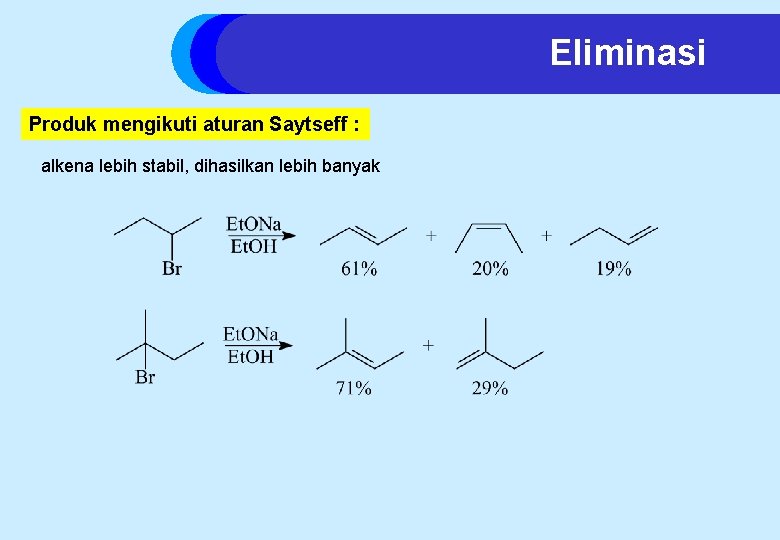
Eliminasi Produk mengikuti aturan Saytseff : alkena lebih stabil, dihasilkan lebih banyak

Mekanisme E 2 : eliminasi bimolekuler • Reaksi adalah bimolekul, V tergantung pada konsentrasi RX dan B– V = k[RX][B–] Tahap penentu laju reaksi melibatkan konsentrasi B– • reactivity: RI > RBr > RCl > RF kekuatan ikatan R—X meningkat Tahap penentu laju reaksi melibatkan pemutusan ikatan R—X (Reaksi tidak tergantung pada jenis RX apakah 1º, 2º, atau 3º)
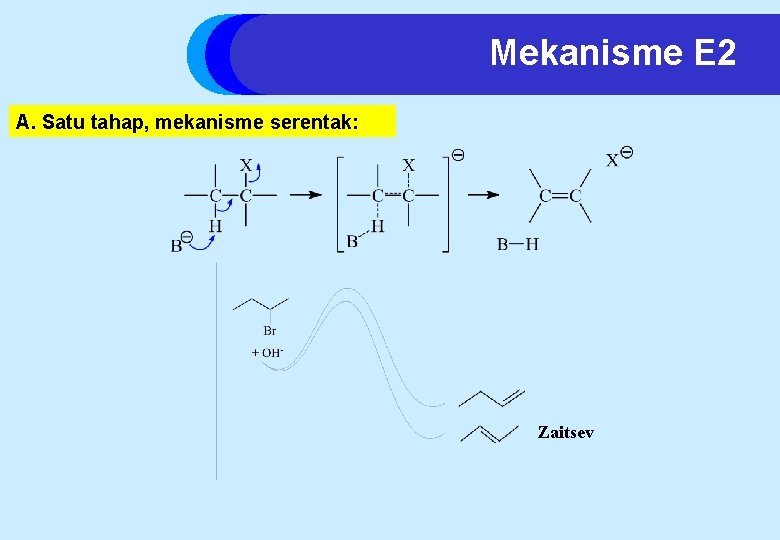
Mekanisme E 2 A. Satu tahap, mekanisme serentak: Zaitsev
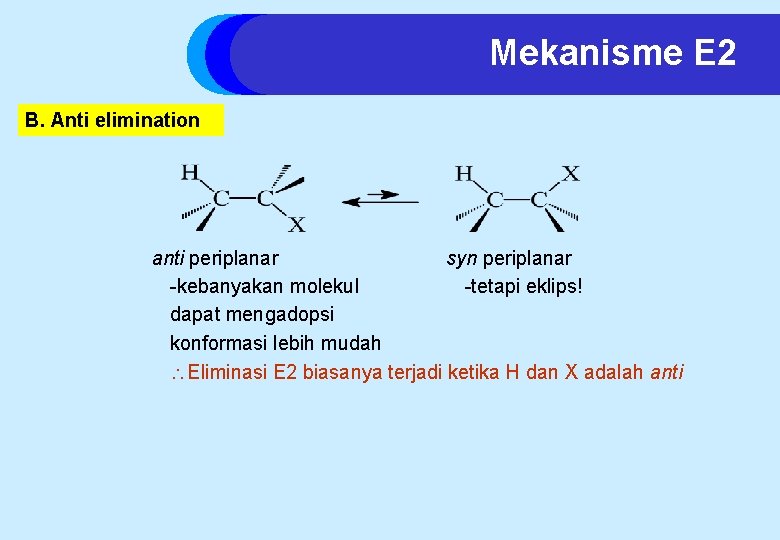
Mekanisme E 2 B. Anti elimination anti periplanar syn periplanar -kebanyakan molekul -tetapi eklips! dapat mengadopsi konformasi lebih mudah Eliminasi E 2 biasanya terjadi ketika H dan X adalah anti
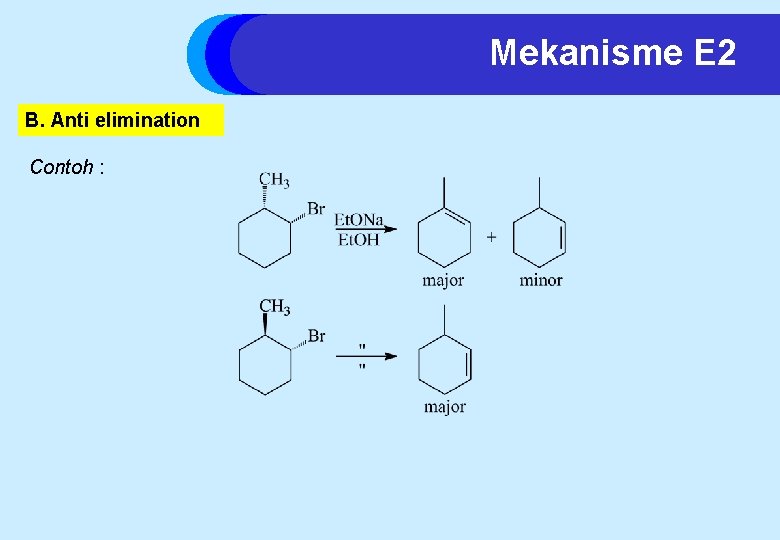
Mekanisme E 2 B. Anti elimination Contoh :
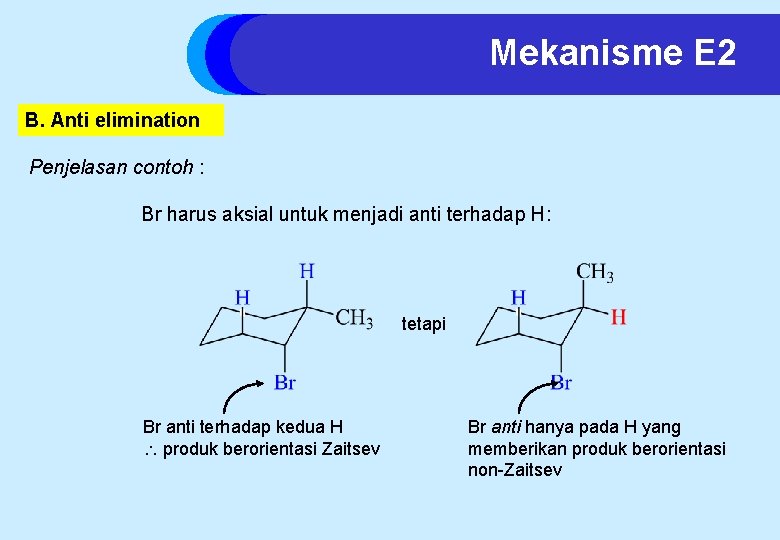
Mekanisme E 2 B. Anti elimination Penjelasan contoh : Br harus aksial untuk menjadi anti terhadap H: tetapi Br anti terhadap kedua H produk berorientasi Zaitsev Br anti hanya pada H yang memberikan produk berorientasi non-Zaitsev
![Mekanisme E 1 A. Mekanisme E 1 Mekanisme E 2: V = k[RBr][B–] Reaktivitas: Mekanisme E 1 A. Mekanisme E 1 Mekanisme E 2: V = k[RBr][B–] Reaktivitas:](http://slidetodoc.com/presentation_image_h2/7b4b8770de119e1474b58275112268b9/image-30.jpg)
Mekanisme E 1 A. Mekanisme E 1 Mekanisme E 2: V = k[RBr][B–] Reaktivitas: RI > RBr > RCl > RF (tidak ada efek 1º, 2º, 3º) Namun jika: Maka : V = k[RBr] E 1 Reaktivitas: RI > RBr > RCl > RF dan: 3º > 2º > 1º (melibatkan pemutusan R–X) (melibatkan R+)
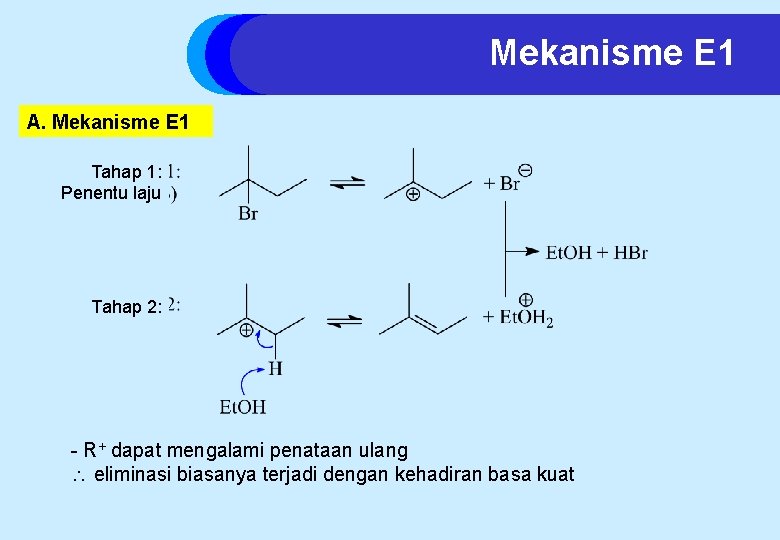
Mekanisme E 1 A. Mekanisme E 1 Tahap 1: Penentu laju Tahap 2: - R+ dapat mengalami penataan ulang eliminasi biasanya terjadi dengan kehadiran basa kuat

Subtitusi Vs Eliminasi A. Reaksi unimolekuler (SN 1, E 1) atau bimolekuler (SN 2, E 2)? V = k 1[RX] + k 2[RX][Nu / B] • faktor ini akan membesar jika konsentrasi Nu atau B meningkat Reaksi bimolekular (SN 2, E 2) didukung oleh konsentrasi Nu baik atau B kuat yang tinggi • faktor ini akan bernilai nol jika konsentrasi Nu atau B juga nol reaksi unimolekular (SN 1, E 1) terjadi pada ketidak hadiran Nu baik atau B kuat
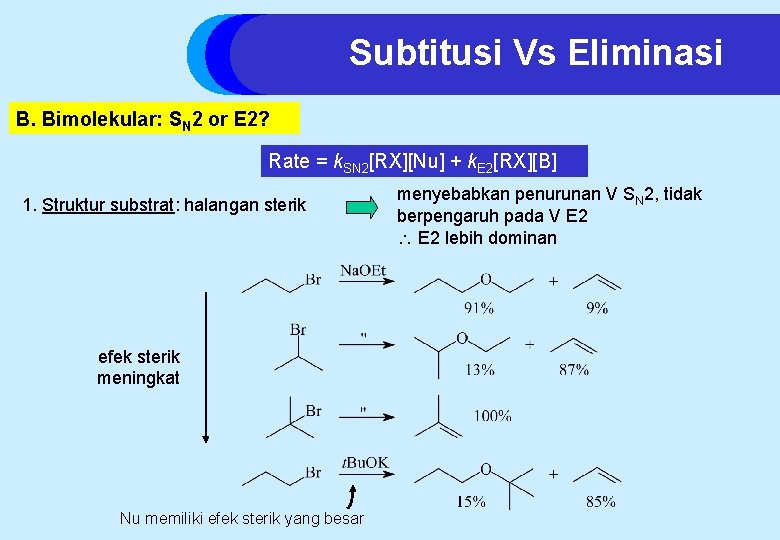
Subtitusi Vs Eliminasi B. Bimolekular: SN 2 or E 2? Rate = k. SN 2[RX][Nu] + k. E 2[RX][B] 1. Struktur substrat: halangan sterik efek sterik meningkat Nu memiliki efek sterik yang besar menyebabkan penurunan V SN 2, tidak berpengaruh pada V E 2 lebih dominan

Subtitusi Vs Eliminasi B. Bimolekular: SN 2 or E 2? 2. Basa Vs Nukleofil • basa yang lebih kuat mendukung E 2 • nukleofil yang baik mendukung SN 2 good Nu weak B good Nu strong B poor Nu strong B
![Subtitusi Vs Eliminasi C. Unimolekular: SN 1 or E 1? V = k[R+][H 2 Subtitusi Vs Eliminasi C. Unimolekular: SN 1 or E 1? V = k[R+][H 2](http://slidetodoc.com/presentation_image_h2/7b4b8770de119e1474b58275112268b9/image-35.jpg)
Subtitusi Vs Eliminasi C. Unimolekular: SN 1 or E 1? V = k[R+][H 2 O] tidak ada kontrol terhadap rasio SN 1 dan E 1

Subtitusi Vs Eliminasi D. Kesimpulan 1. bimolekular: SN 2 & E 2 Didukung oleh konsentrasi tinggi dari Nu baik atau B kuat Nu baik, B lemah : I–, Br–, HS–, RS–, NH 3, PH 3 mendukung SN 2 Nu baik, B kuat : HO–, RO–, H 2 N– SN 2 & E 2 Nu buruk, B kuat : t. Bu. O– (sterically hindered) mendukung E 2 Substrat: 1º RX 2º RX 3º RX lebih sering SN 2 (kecuali dengan t. Bu. O–) bisa SN 2 dan E 2 (tetapi lebih sering E 2) hanya E 2

Subtitusi Vs Eliminasi D. Kesimpulan 2. unimolekular: SN 1 & E 1 Terjadi pada ketidakhadiran dari Nu baik atau B kuat Nu buruk, B lemah: H 2 O, ROH, RCO 2 H Substrat: 1º RX 2º RX 3º RX SN 1 and E 1 (hanya dengan penataan ulang) SN 1 and E 1 (dapat terjadi penataan ulang) tidak dapat mengontrol rasio SN 1 to E 1
- Slides: 37