Alkane Kohlenstoffatom Alkane besitzen vier Bindungspartner an jedem
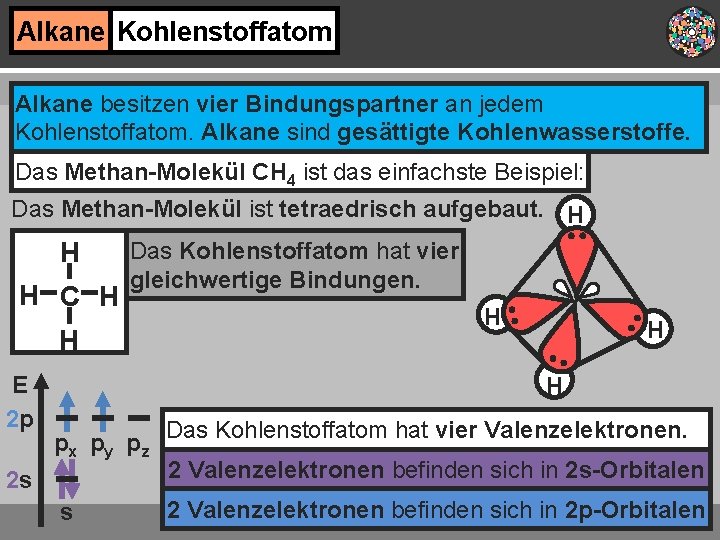
Alkane Kohlenstoffatom Alkane besitzen vier Bindungspartner an jedem Kohlenstoffatom. Alkane sind gesättigte Kohlenwasserstoffe. Das Methan-Molekül CH 4 ist das einfachste Beispiel: Das Methan-Molekül ist tetraedrisch aufgebaut. H H H C H Das Kohlenstoffatom hat vier gleichwertige Bindungen. H E 2 p H H H px py pz 2 s s Das Kohlenstoffatom hat vier Valenzelektronen. 2 Valenzelektronen befinden sich in 2 s-Orbitalen 2 Valenzelektronen befinden sich in 2 p-Orbitalen
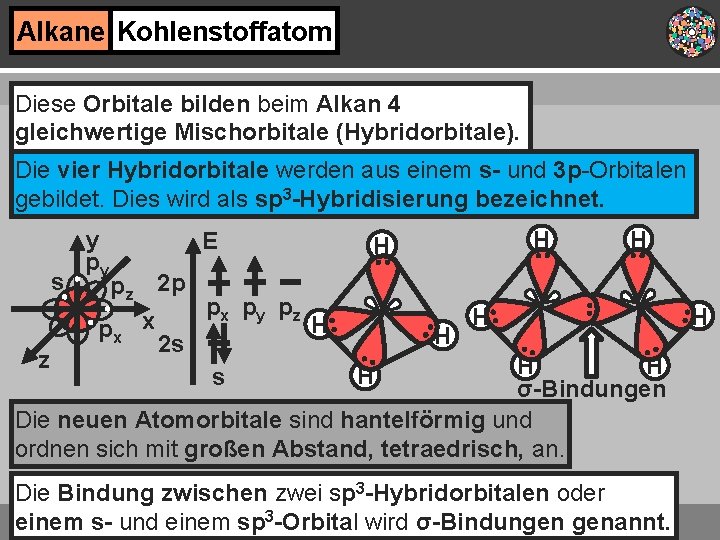
Alkane Kohlenstoffatom Diese Orbitale bilden beim Alkan 4 gleichwertige Mischorbitale (Hybridorbitale). Die vier Hybridorbitale werden aus einem s- und 3 p-Orbitalen gebildet. Dies wird als sp 3 -Hybridisierung bezeichnet. s z y py E pz px x 2 p px py pz 2 s H H H H σ-Bindungen Die neuen Atomorbitale sind hantelförmig und ordnen sich mit großen Abstand, tetraedrisch, an. s H Die Bindung zwischen zwei sp 3 -Hybridorbitalen oder einem s- und einem sp 3 -Orbital wird σ-Bindungen genannt. H
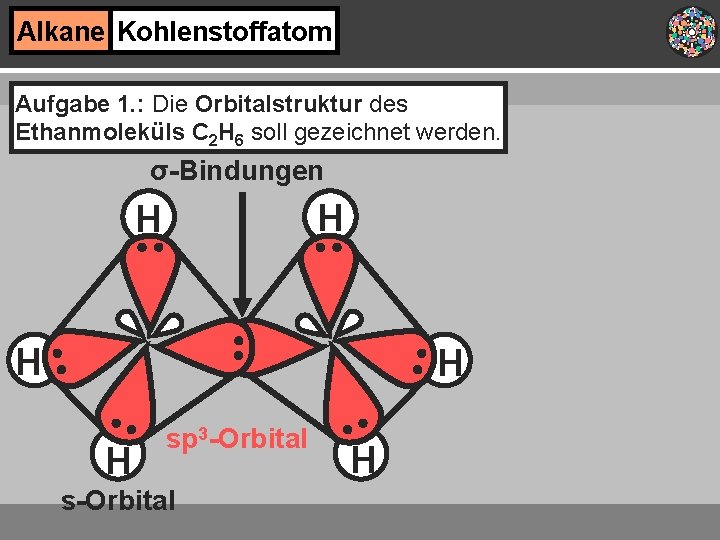
Alkane Kohlenstoffatom Aufgabe 1. : Die Orbitalstruktur des Ethanmoleküls C 2 H 6 soll gezeichnet werden. σ-Bindungen H H H sp 3 -Orbital s-Orbital H

Alkane Kohlenstoffatom Aufgabe 2. : Für die Verbrennung von Methan und Butan C 4 H 10 soll die Reaktionsgleichung formuliert werden. Was fällt beim Sauerstoffverbrauch der unterschiedlichen Gase auf? Verbrennung von Methan: CH 4 + 2 O 2 → CO 2 + 2 H 2 O Verbrennung von Butan: 2 C 4 H 10 + 13 O 2 → 8 CO 2 + 10 H 2 O Bei der Verbrennung von Butan (1: 2, 5) wird weniger Sauerstoff verbraucht als bei der Verbrennung von Methan (1: 4). Man erwartet eigentlich bei vier Kohlenstoffatome einen vierfach erhöhten Sauerstoffverbrauch.
- Slides: 4