ALGORITM DE TESTARE GENETIC N CANCERE RARE Prof


















- Slides: 38

ALGORITM DE TESTARE GENETICĂ ÎN CANCERE RARE Prof. Dr. Eusebiu Vlad Gorduza Disciplina de Genetică Medicală Departamentul de Oncogenetică UMF “Grigore T. Popa” Iaşi 1

U. M. F IAŞI GENETICA CANCERULUI v CANCER = grup de maladii (carcinoame; sarcoame; leucemii şi limfoame) caracterizate prin proliferare celulară necontrolată → TUMORĂ (neoplazie): § benignă → limitată la ţesutul de origine; § malignă → penetrează ţesuturile vecine şi se propagă la distanţă (metastaze) v CAUZE: § Factori de mediu (75%) → modificări la nivelul aparatului genetic; § Predispoziţie genetică → mutaţii genice; § Vârsta → erori de replicare şi de corecţie a modificărilor ADN v cancer – maladie genetică a celulelor somatice → apariţia de MUTAŢII MULTIPLE, în gene care controlează : proliferarea celulară , ciclul mitotic, repararea ADN, apoptoză. 2

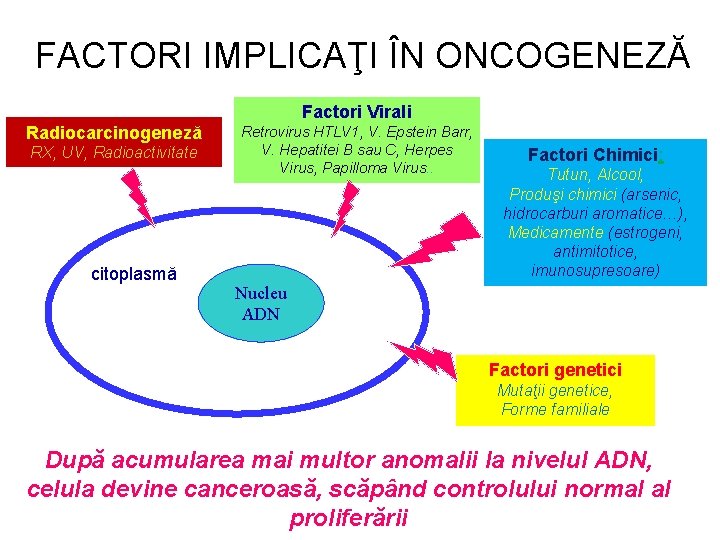
FACTORI IMPLICAŢI ÎN ONCOGENEZĂ Factori Virali Radiocarcinogeneză RX, UV, Radioactivitate citoplasmă Retrovirus HTLV 1, V. Epstein Barr, V. Hepatitei B sau C, Herpes Virus, Papilloma Virus. . Factori Chimici: Tutun, Alcool, Produşi chimici (arsenic, hidrocarburi aromatice…), Medicamente (estrogeni, antimitotice, imunosupresoare) Nucleu ADN Factori genetici Mutaţii genetice, Forme familiale După acumularea mai multor anomalii la nivelul ADN, celula devine canceroasă, scăpând controlului normal al proliferării

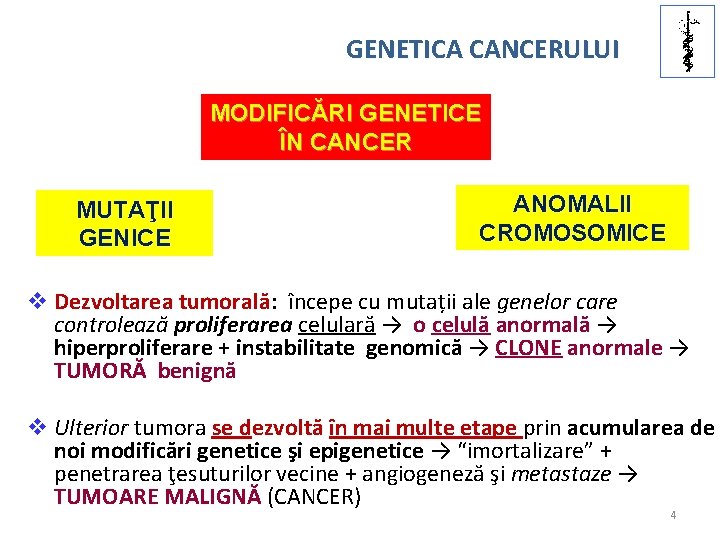
U. M. F IAŞI GENETICA CANCERULUI MODIFICĂRI GENETICE ÎN CANCER MUTAŢII GENICE ANOMALII CROMOSOMICE v Dezvoltarea tumorală: începe cu mutații ale genelor care controlează proliferarea celulară → o celulă anormală → hiperproliferare + instabilitate genomică → CLONE anormale → TUMORĂ benignă v Ulterior tumora se dezvoltă în mai multe etape prin acumularea de noi modificări genetice şi epigenetice → “imortalizare” + penetrarea ţesuturilor vecine + angiogeneză şi metastaze → TUMOARE MALIGNĂ (CANCER) 4

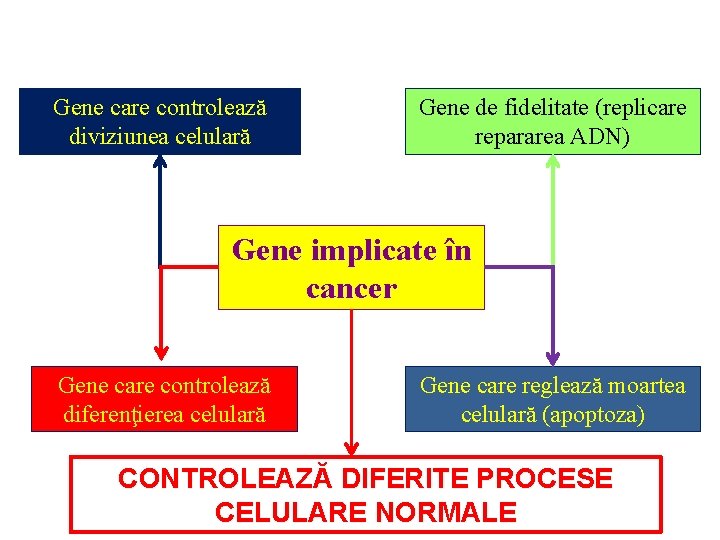
Gene care controlează diviziunea celulară Gene de fidelitate (replicare repararea ADN) Gene implicate în cancer Gene care controlează diferenţierea celulară Gene care reglează moartea celulară (apoptoza) CONTROLEAZĂ DIFERITE PROCESE CELULARE NORMALE

U. M. F IAŞI Oncogene ACTIVAREA PROTOONCOGENELOR în celulele somatice: vmutaţii punctiforme (← ≠ cancerigeni → ex. , gena RAS); v. Translocații cromosomice (transferul proto-onc în proximitatea unei gene active) (ex. , t(9 q; 22 q) în Leucemia mieloidă cronică); v. Inserții virale; v. Amplificare genică. Activarea oncogenelor = câștig de funcție → ONCOGENELE AU EFECT DOMINANT LA NIVEL CELULAR → o singură alelă mutantă (An) modifică fenotipul celular 6

U. M. F IAŞI GENE SUPRESOARE ALE CREȘTERII TUMORALE (GST) v GST (→ receptori; proteine citoplasmatice / nucleare) → inhibare proliferării celulare (“tumor-suppressor genes”). v Mutațiile GST → “pierderea funcției” de supresie → proliferare celulară necontrolată. v Au efect RECESIV (aa) la nivel celular Ø Transformarea unei celule normale într-o celulă tumorală → necesită două mutaţii în GST (ipoteza "two hits", Knudson, 1971): § prima mutaţie poate fi moştenită (în cancere ereditare) sau dobândită postnatal → (Na) status heterozigot. § A doua mutaţie → pierderea heterozigoţiei (“loss of heterozygosity” - LOH) → (aa). 7

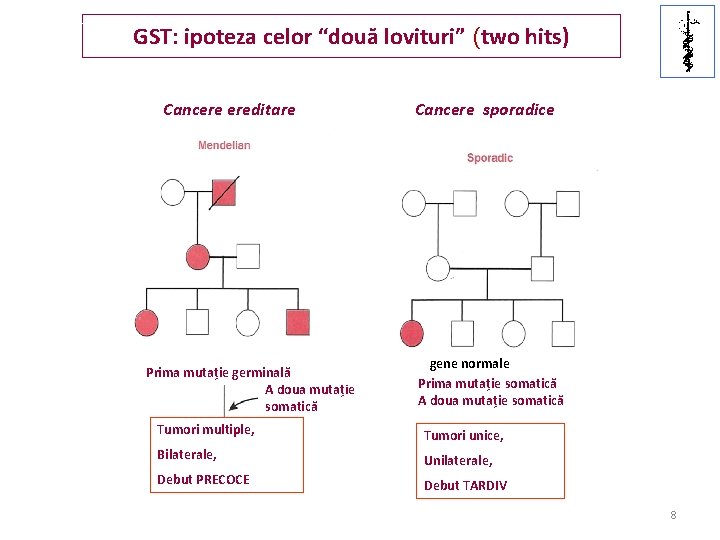
U. M. F IAŞI GST: ipoteza celor “două lovituri” (two hits) Cancere ereditare Prima mutație germinală A doua mutație somatică Cancere sporadice gene normale Prima mutație somatică A doua mutație somatică Tumori multiple, Tumori unice, Bilaterale, Unilaterale, Debut PRECOCE Debut TARDIV 8

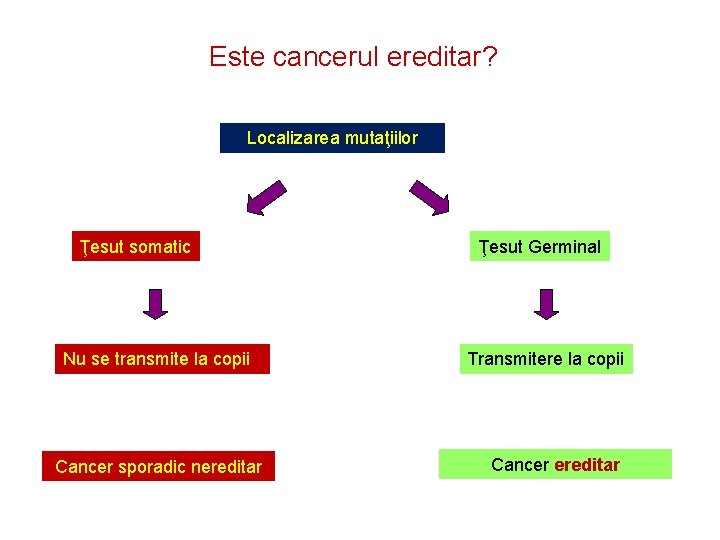
Este cancerul ereditar? Localizarea mutaţiilor Ţesut somatic Nu se transmite la copii Cancer sporadic nereditar Ţesut Germinal Transmitere la copii Cancer ereditar

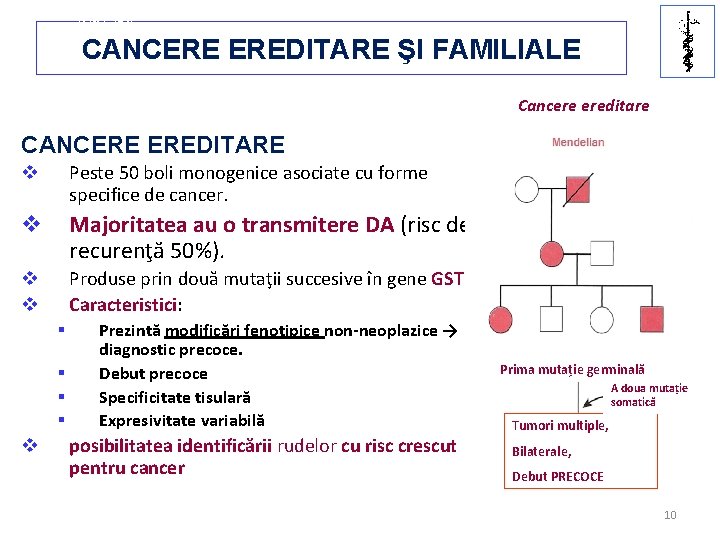
U. M. F IAŞI CANCERE EREDITARE ŞI FAMILIALE Cancere ereditare CANCERE EREDITARE v Peste 50 boli monogenice asociate cu forme specifice de cancer. v Majoritatea au o transmitere DA (risc de recurenţă 50%). v v Produse prin două mutaţii succesive în gene GST Caracteristici: § § v Prezintă modificări fenotipice non-neoplazice → diagnostic precoce. Debut precoce Specificitate tisulară Expresivitate variabilă posibilitatea identificării rudelor cu risc crescut pentru cancer Prima mutație germinală A doua mutație somatică Tumori multiple, Bilaterale, Debut PRECOCE 10

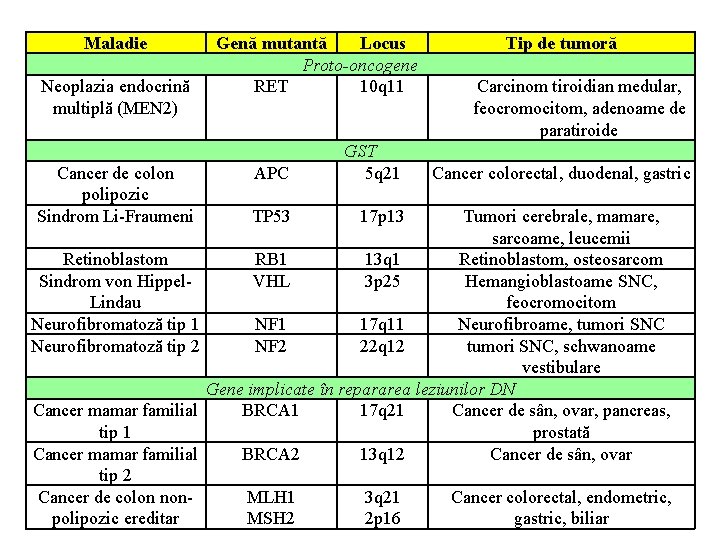
Maladie Neoplazia endocrină multiplă (MEN 2) Cancer de colon polipozic Sindrom Li-Fraumeni Retinoblastom Sindrom von Hippel. Lindau Neurofibromatoză tip 1 Neurofibromatoză tip 2 Cancer mamar familial tip 1 Cancer mamar familial tip 2 Cancer de colon nonpolipozic ereditar Genă mutantă Locus Proto-oncogene RET 10 q 11 APC GST 5 q 21 TP 53 17 p 13 MLH 1 MSH 2 3 q 21 2 p 16 Tip de tumoră Carcinom tiroidian medular, feocromocitom, adenoame de paratiroide Cancer colorectal, duodenal, gastric Tumori cerebrale, mamare, sarcoame, leucemii RB 1 13 q 1 Retinoblastom, osteosarcom VHL 3 p 25 Hemangioblastoame SNC, feocromocitom NF 1 17 q 11 Neurofibroame, tumori SNC NF 2 22 q 12 tumori SNC, schwanoame vestibulare Gene implicate în repararea leziunilor DN BRCA 1 17 q 21 Cancer de sân, ovar, pancreas, prostată BRCA 2 13 q 12 Cancer de sân, ovar Cancer colorectal, endometric, gastric, biliar

U. M. F IAŞI CANCERE FAMILIALE v Majoritatea sunt cancere ginecologice sau digestive v Au agregare familială, dar fără transmitere monogenică → importanţa anamnezei familiale corecte. v Debut relativ precoce v Sunt produse de variante alelice ale genelor implicate şi în cancerele ereditare v Risc de recurenţă : mediu DETERMINISM MULTIFACTORIAL 12


CANCERE EREDITARE (GENETICE)

Testarea genetică în cancerele ereditare Este utilă doar în cazurile cu istoric familial pozitiv Anamneză familială obligatorie – consult genetic pretestare Avantaje: • Poate schimba stilul de viaţă. • Limitarea anxietăţii în absenţa mutaţiei. • Permite aplicarea de măsuri profilactice. • Permite testarea şi a altor membri cu risc din familie Dezavantaje: • Nu reduce riscul de a dezvolta o tumoare • Există riscul de desecretizare a informaţiei. • Poate apărea o discriminare din partea asiguratorilor sau angajatorului. • Poate da un fals sentiment de siguranţă legat de absenţa riscului tumoral • Este scumpă şi de regulă preţul nu este acoperit de asigurările medicale Impune obligatoriu sfat genetic posttestare

Testarea genetică în cancerele ereditare • Testarea genetică se face din sânge • Testarea se bazează în majoritatea cazurilor pe secvenţiere genică şi necesită perioade mari de timp până la câteva luni sau un an • Testarea se începe de la cazul index, iar ulterior, dacă s-a probat un anumit tip de mutaţie se aplică şi la alţi membri ai familiei care au risc crescut de a fi moştenit mutaţia • Există o probabilitate de aproximativ 20% de a nu putea certifica nici un fel de mutație • Depistarea mutației și la alți membri ai familiei nu înseamnă că aceștia vor dezvolta obligatoriu una din tumorile tipice pentru respectiva formă de cancer Testarea genetică şi cunoaşterea tipului de mutaţie oferă avantajul identificării persoanelor cu risc crescut de a dezvolta un anumit tip de cancer şi de a aplica măsurile profilactice adecvate

EXEMPLE DE CANCERE EREDITARE ŞI FAMILIALE

CANCERE ENDOCRINE

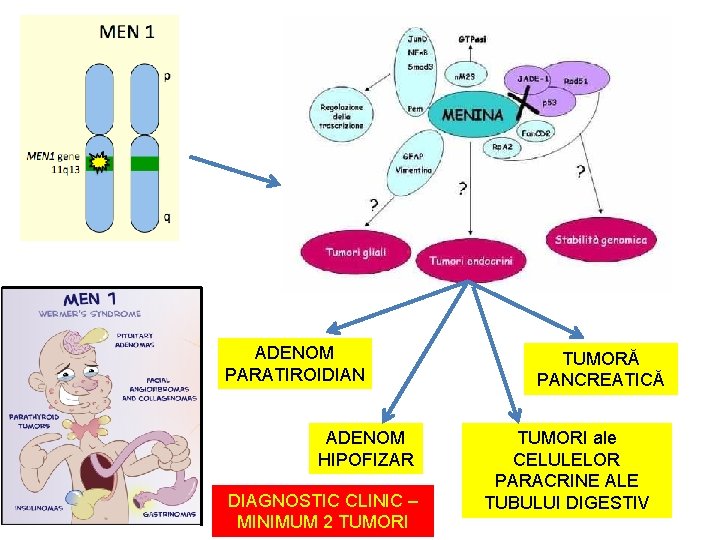
Neoplazia endocrină multiplă tip 1 (MEN 1) • diferite combinaţii a peste 20 tumori endocrine şi non-endocrine • 1/35. 000 de persoane • Este produs de mutaţia genei MEN 1 o genă cu structură înalt conservată pe parcursul evoluţiei • Gena este activă în numeroase celule (la nivelul cărora apar şi tumorile) dar prezintă o matisare alternativă ce permite sinteza a diferite forme de menină în ţesuturi diferite • Mutaţiile sunt prezente la 75 -90% din pacienţii cu MEN 1 • Transmitere dominant autosomală • Mecanism patogenic bazat pe ipoteza “two hits” existând o primă mutaţie moştenită (în cazuri familiale) sau produsă precoce în embriogeneză (cazuri sporadice) urmată de o a doua mutaţie somatică în celulele endocrine cu pierderea heterozigoţiei şi risc crescut de tumorigeneză • Speranţă de viaţă limitată corelată cu prezenţa de tumori maligne.

ADENOM PARATIROIDIAN ADENOM HIPOFIZAR DIAGNOSTIC CLINIC – MINIMUM 2 TUMORI TUMORĂ PANCREATICĂ TUMORI ale CELULELOR PARACRINE ALE TUBULUI DIGESTIV

CANCER DE COLON

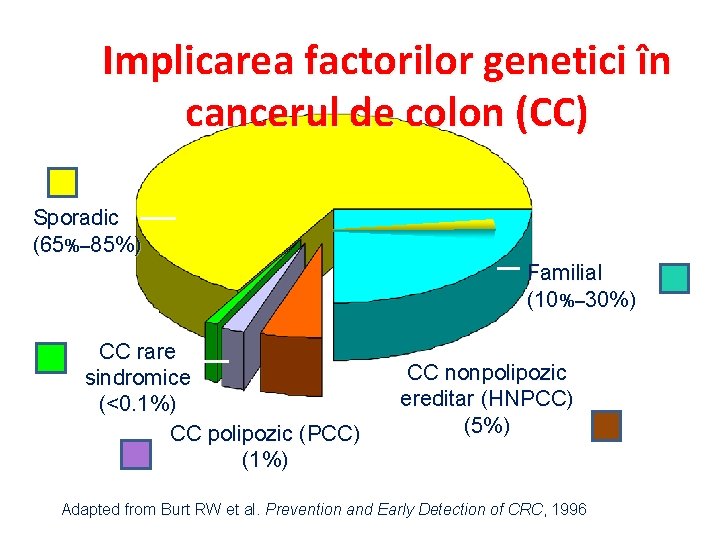
Implicarea factorilor genetici în cancerul de colon (CC) Sporadic (65%– 85%) Familial (10%– 30%) CC rare sindromice (<0. 1%) CC polipozic (PCC) (1%) CC nonpolipozic ereditar (HNPCC) (5%) Adapted from Burt RW et al. Prevention and Early Detection of CRC, 1996

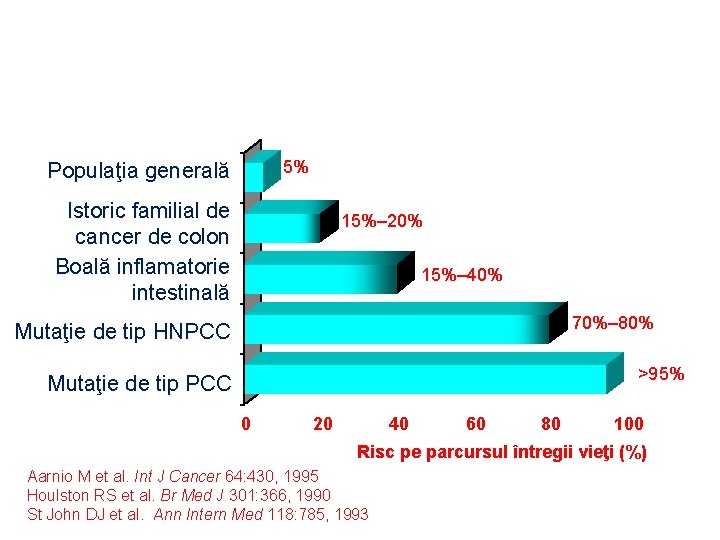
5% Populaţia generală Istoric familial de cancer de colon Boală inflamatorie intestinală 15%– 20% 15%– 40% 70%– 80% Mutaţie de tip HNPCC >95% Mutaţie de tip PCC 0 20 40 60 80 100 Risc pe parcursul întregii vieţi (%) Aarnio M et al. Int J Cancer 64: 430, 1995 Houlston RS et al. Br Med J 301: 366, 1990 St John DJ et al. Ann Intern Med 118: 785, 1993

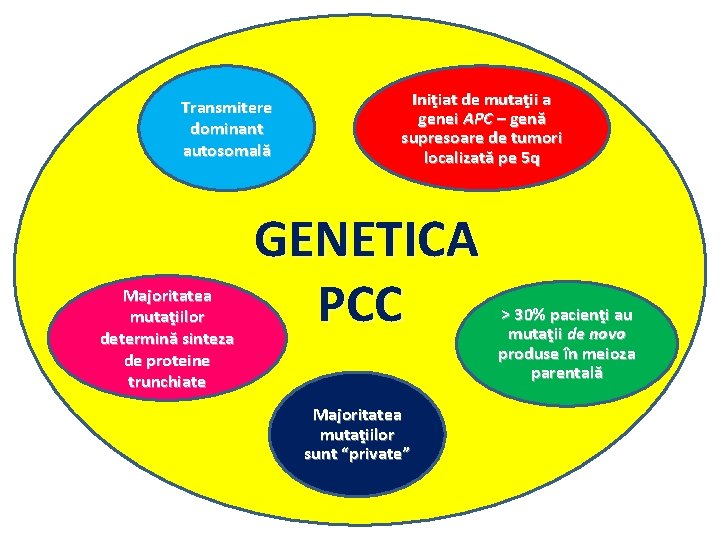
Transmitere dominant autosomală Majoritatea mutaţiilor determină sinteza de proteine trunchiate Iniţiat de mutaţii a genei APC – genă supresoare de tumori localizată pe 5 q GENETICA PCC Majoritatea mutaţiilor sunt “private” > 30% pacienţi au mutaţii de novo produse în meioza parentală

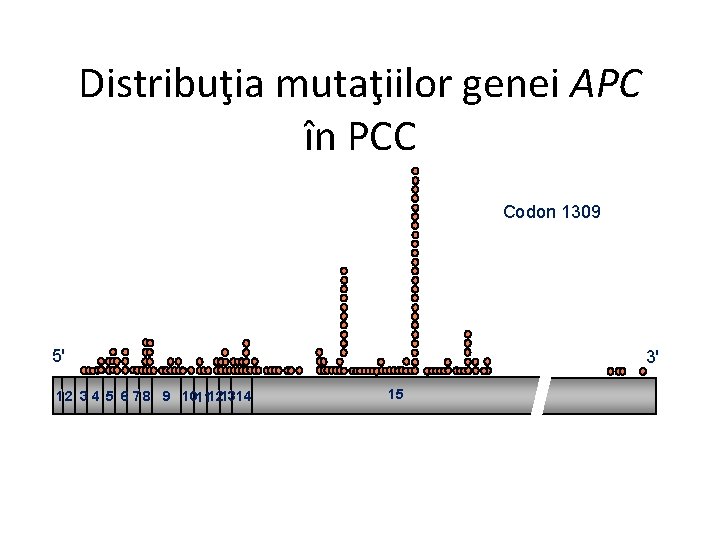
Distribuţia mutaţiilor genei APC în PCC Codon 1309 5' 1 2 3 4 5 6 7 8 9 1011121314 3' 15

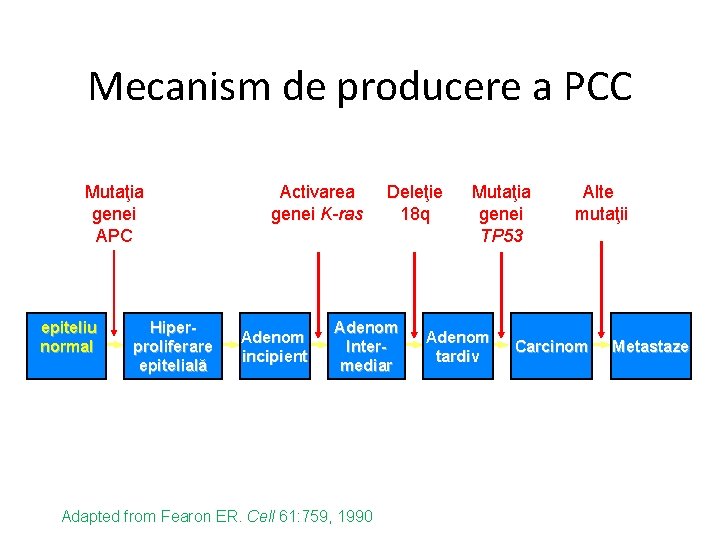
Mecanism de producere a PCC Mutaţia genei APC epiteliu normal Hiperproliferare epitelială Activarea genei K-ras Adenom incipient Deleţie 18 q Adenom Intermediar Adapted from Fearon ER. Cell 61: 759, 1990 Mutaţia genei TP 53 Adenom tardiv Alte mutaţii Carcinom Metastaze

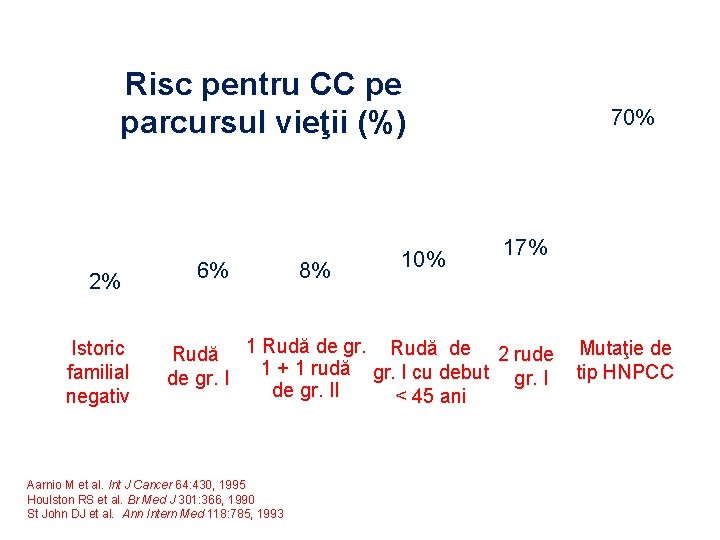
Risc pentru CC pe parcursul vieţii (%) 2% Istoric familial negativ 6% 8% 10% 70% 17% Rudă 1 Rudă de gr. Rudă de 2 rude 1 + 1 rudă gr. I cu debut gr. I de gr. II < 45 ani Aarnio M et al. Int J Cancer 64: 430, 1995 Houlston RS et al. Br Med J 301: 366, 1990 St John DJ et al. Ann Intern Med 118: 785, 1993 Mutaţie de tip HNPCC

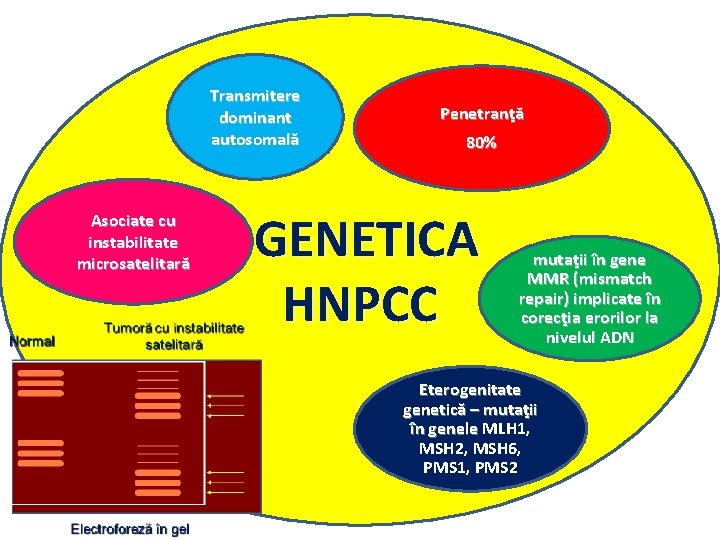
Transmitere dominant autosomală Asociate cu instabilitate microsatelitară Penetranţă 80% GENETICA HNPCC mutaţii în gene MMR (mismatch repair) implicate în corecţia erorilor la nivelul ADN Eterogenitate genetică – mutaţii în genele MLH 1, MSH 2, MSH 6, PMS 1, PMS 2

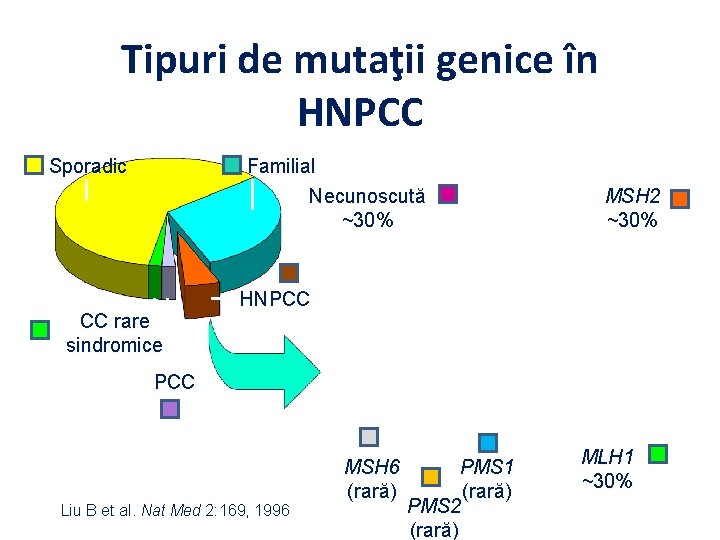
Tipuri de mutaţii genice în HNPCC Sporadic Familial Necunoscută ~30% CC rare sindromice MSH 2 ~30% HNPCC Liu B et al. Nat Med 2: 169, 1996 MSH 6 (rară) PMS 1 (rară) PMS 2 (rară) MLH 1 ~30%

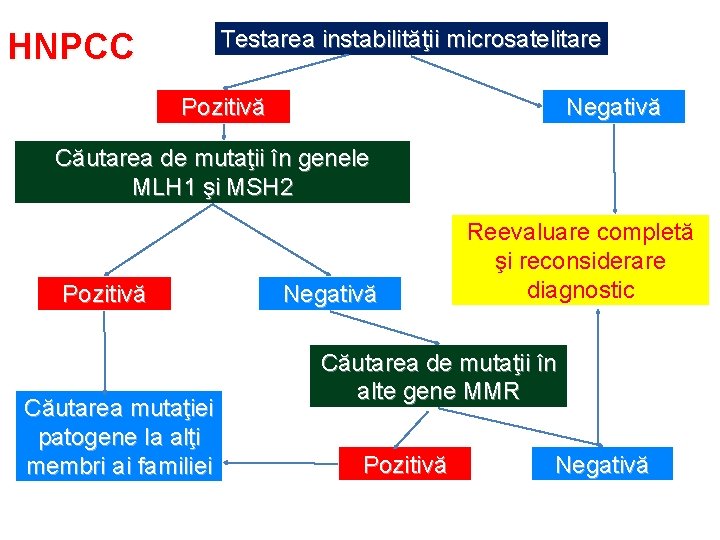
Testarea instabilităţii microsatelitare HNPCC Pozitivă Negativă Căutarea de mutaţii în genele MLH 1 şi MSH 2 Pozitivă Căutarea mutaţiei patogene la alţi membri ai familiei Negativă Reevaluare completă şi reconsiderare diagnostic Căutarea de mutaţii în alte gene MMR Pozitivă Negativă

CANCER DE S N ŞI DE OVAR

CANCER EREDITAR DE S N ŞI OVAR 5 – 10 % din cancerele de sân Un purtător de mutaţie are un risc de 40 -70% de a face cancer de sân pe parcursul vieţii Un purtător de mutaţie are un risc de 10 -45% de a face cancer de ovar pe parcursul vieţii Risc crescut pentru cancer de prostată la bărbaţii cu mutaţie Testarea genetică posibilă, dar scumpă şi laborioasă La persoanele cu risc se poate face profilaxie

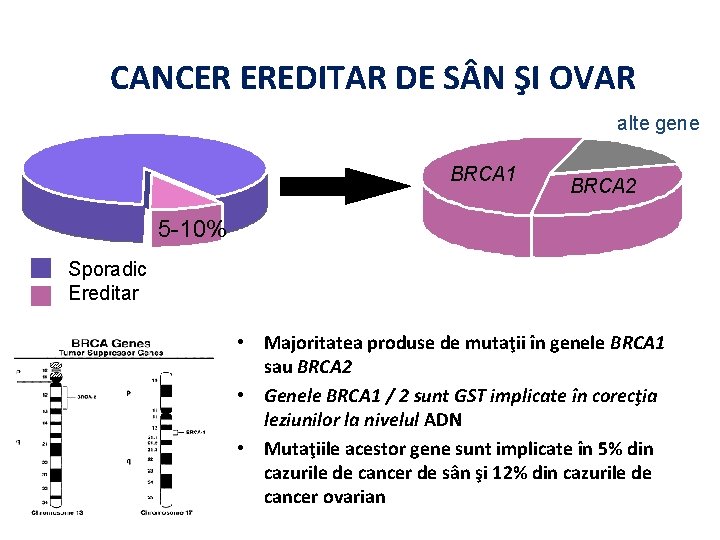
CANCER EREDITAR DE S N ŞI OVAR alte gene BRCA 1 BRCA 2 5 -10% Sporadic Ereditar • Majoritatea produse de mutaţii în genele BRCA 1 sau BRCA 2 • Genele BRCA 1 / 2 sunt GST implicate în corecţia leziunilor la nivelul ADN • Mutaţiile acestor gene sunt implicate în 5% din cazurile de cancer de sân şi 12% din cazurile de cancer ovarian

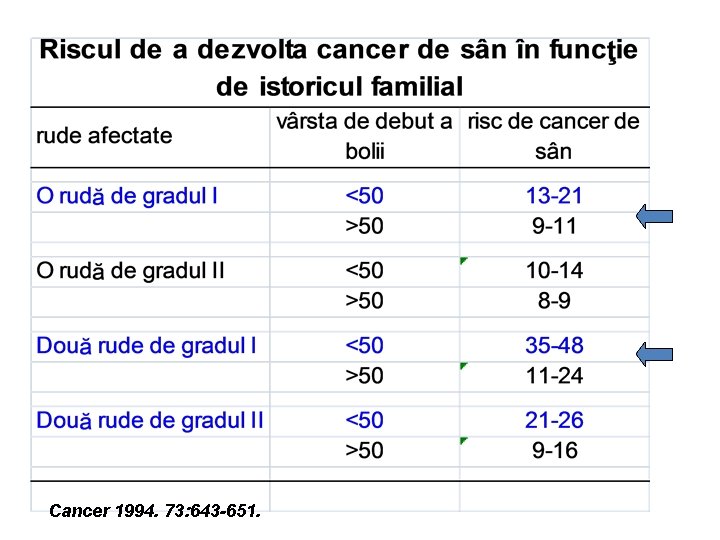
Cancer 1994. 73: 643 -651.

Riscul de a dezvolta un cancer la purtătorii de mutaţie BRCA 1 Cancer de sân 56%-87% (de obicei cu debut precoce) Cancer de sân secundar 64% Cancer ovarian 16%-44% Risc crescut pentru alte forme de cancer, de exemplu de pancreas sau de prostată

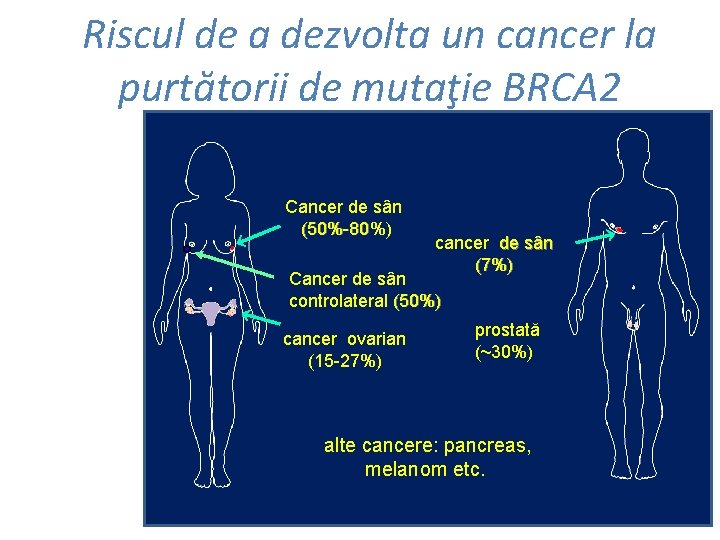
Riscul de a dezvolta un cancer la purtătorii de mutaţie BRCA 2 Cancer de sân (50%-80%) cancer de sân (7%) Cancer de sân controlateral (50%) cancer ovarian (15 -27%) prostată (~30%) alte cancere: pancreas, melanom etc.

Opţiuni pentru purtătorii de mutaţii ale genelor BRCA 1/2 • Screeningul tumoral – Mamografie şi/sau RMN – Evaluare radiologică a ovarului • Mastectomie bilaterală profilactică – Reduce cu ~90% riscul de a dezvolta o tumoră • Ovariectomie şi anexectomie bilaterală profilactică – Reduce cu 96 -98% riscul de cancer ovarian – Reduce cu ~50% riscul de cancer de sân • Posibilă chemoprevenţie în viitor cu medicamente ţintite

Cancer Boală a genomului somatic • Majoritatea cazurilor sunt sporadice, dar există o serie de forme rare cu caracter ereditar sau familial • În cancerele ereditare există posibilitatea testării genetice care oferă avantaje şi dezavantaje • Testarea genetică trebuie avizată de genetician pe baza istoricului familial • Interpretarea rezultatelor şi comunicarea acestora impune de asemenea intervenţia geneticianului.