ALDEHID DAN KETON Tim Dosen Kimia Dasar II









![1) Oksidasi dengan Oksidator Kuat [O] R-CO-H → R- CO-OH Aldehida Asam karboksilat Catatan: 1) Oksidasi dengan Oksidator Kuat [O] R-CO-H → R- CO-OH Aldehida Asam karboksilat Catatan:](https://slidetodoc.com/presentation_image_h/9d56f2572e3489b30d28a4cb019ff274/image-28.jpg)





- Slides: 35

ALDEHID DAN KETON Tim Dosen Kimia Dasar II/ Kimia Organik


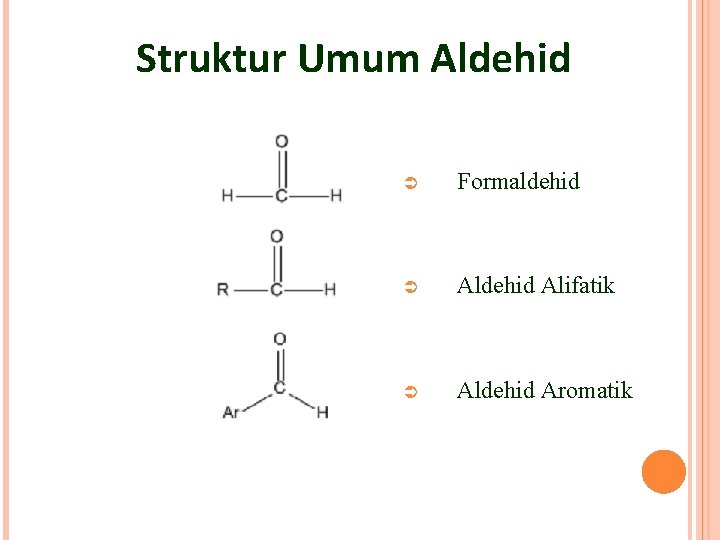
Struktur Umum Aldehid Ü Formaldehid Ü Aldehid Alifatik Ü Aldehid Aromatik

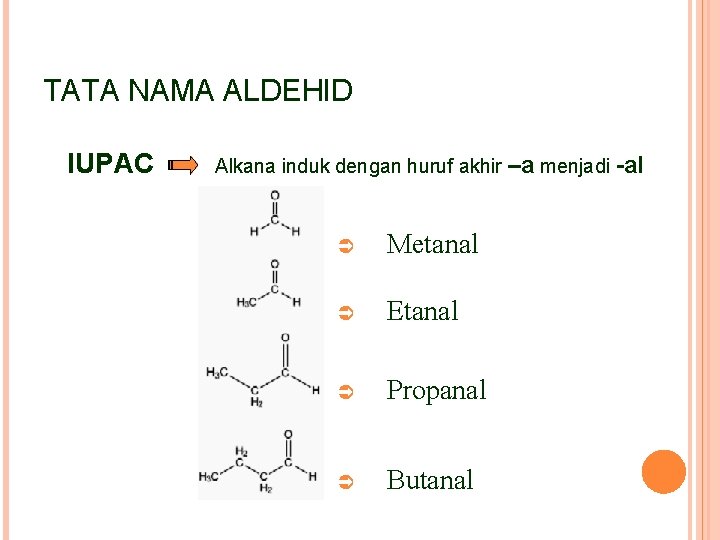
TATA NAMA ALDEHID IUPAC Alkana induk dengan huruf akhir –a menjadi -al Ü Metanal Ü Etanal Ü Propanal Ü Butanal

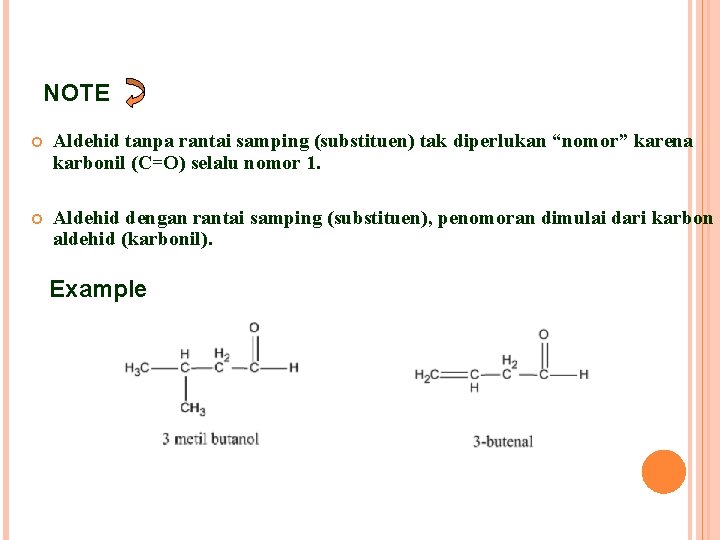
NOTE Aldehid tanpa rantai samping (substituen) tak diperlukan “nomor” karena karbonil (C=O) selalu nomor 1. Aldehid dengan rantai samping (substituen), penomoran dimulai dari karbon aldehid (karbonil). Example 3 metil butanal 3 -butenal

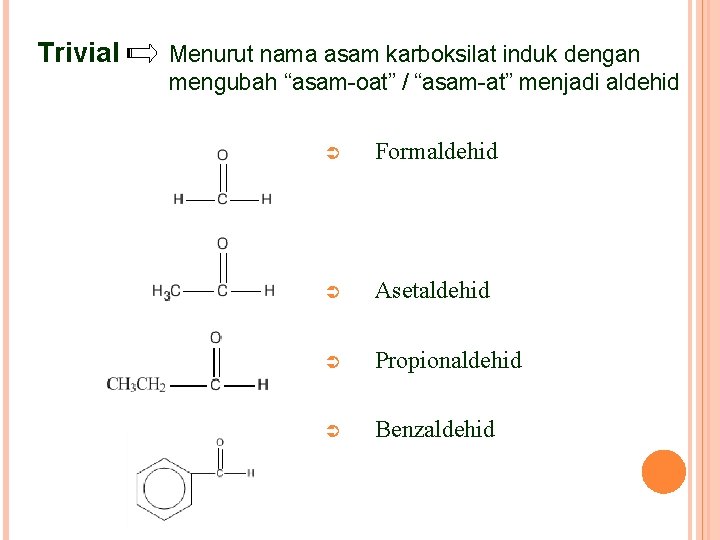
Trivial Menurut nama asam karboksilat induk dengan mengubah “asam-oat” / “asam-at” menjadi aldehid Ü Formaldehid Ü Asetaldehid Ü Propionaldehid Ü Benzaldehid

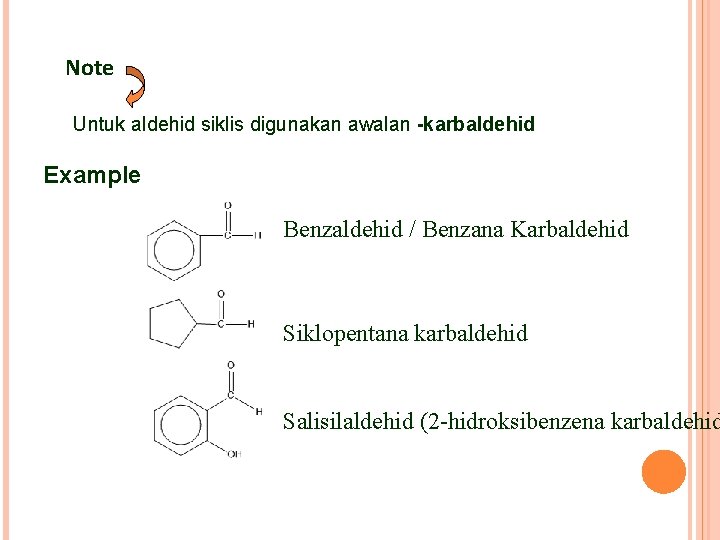
Note Untuk aldehid siklis digunakan awalan -karbaldehid Example Benzaldehid / Benzana Karbaldehid Siklopentana karbaldehid Salisilaldehid (2 -hidroksibenzena karbaldehid


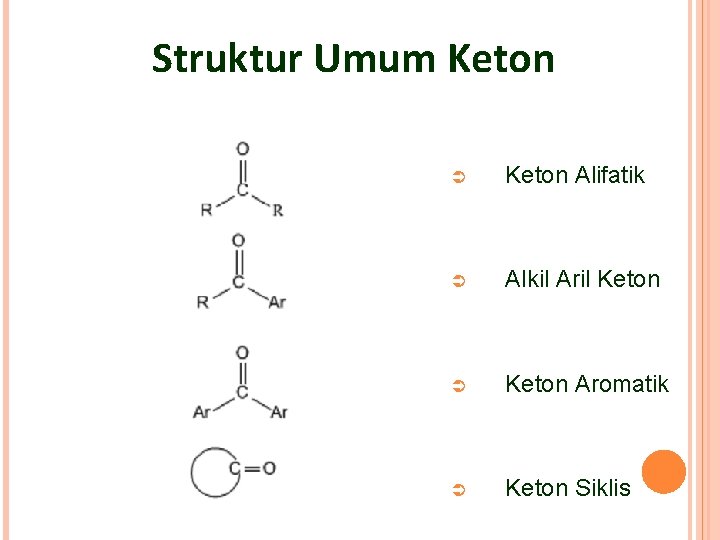
Struktur Umum Keton Ü Keton Alifatik Ü Alkil Aril Keton Ü Keton Aromatik Ü Keton Siklis

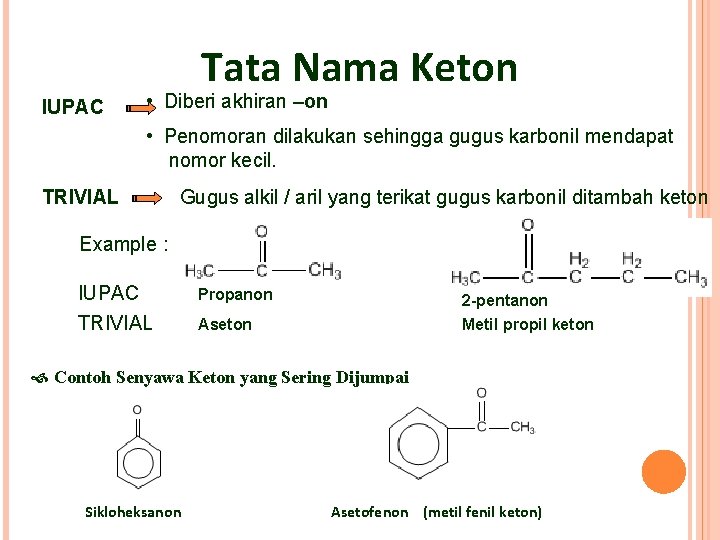
Tata Nama Keton IUPAC • Diberi akhiran –on • Penomoran dilakukan sehingga gugus karbonil mendapat nomor kecil. TRIVIAL Gugus alkil / aril yang terikat gugus karbonil ditambah keton Example : IUPAC TRIVIAL Propanon 2 -pentanon Metil propil keton Aseton Contoh Senyawa Keton yang Sering Dijumpai Sikloheksanon Asetofenon (metil fenil keton)

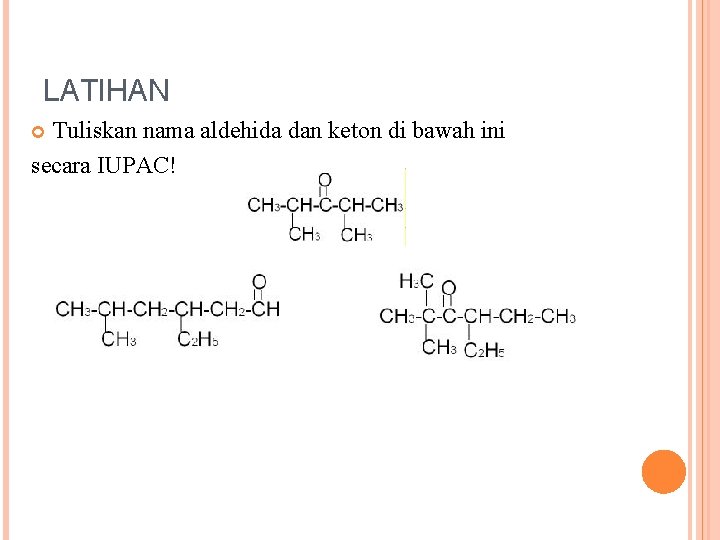
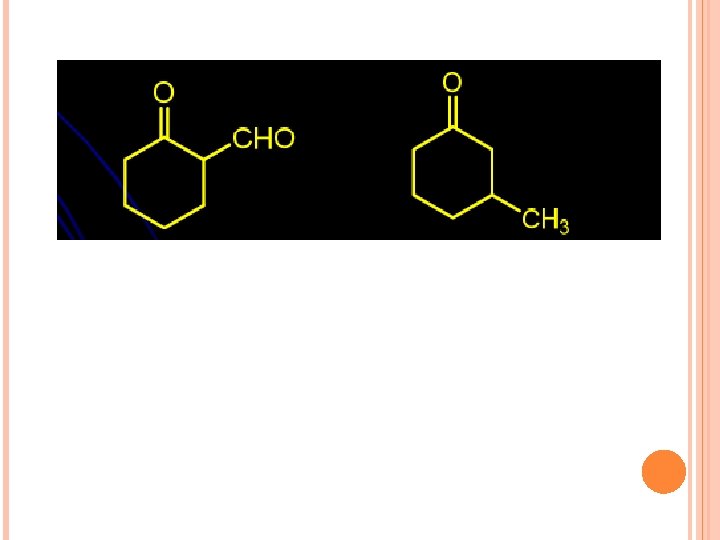
LATIHAN Tuliskan nama aldehida dan keton di bawah ini secara IUPAC!


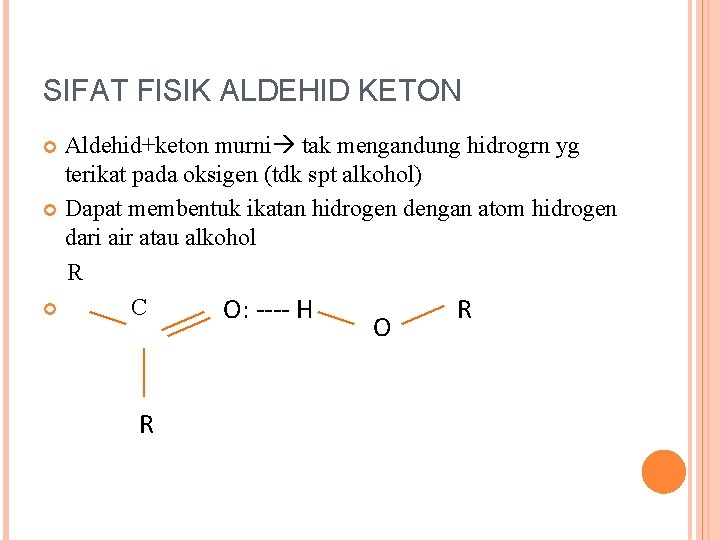
SIFAT FISIK ALDEHID KETON Aldehid+keton murni tak mengandung hidrogrn yg terikat pada oksigen (tdk spt alkohol) Dapat membentuk ikatan hidrogen dengan atom hidrogen dari air atau alkohol R C O: ---- H R O R

KONSEKUENSI KEPOLARAN GUGUS KARBONIL: Terjadi asosiasi yang lemah diantara molekul-molekul aldehida dan keton titik didih lebih tinggi daripada alkana yang setara. Tetapi aldehida dan keton tidak dapat membentuk ikatan hidrogen dengan sesamanya titik didih lebih rendah dibanding alkohol yang setara. 16

KONSEKUENSI KEPOLARAN GUGUS KARBONIL: Aldehida dan keton dapat berikatan hidrogen dengan molekul lain Aldehida dan keton BM rendah larut dalam air. Secara terbatas aldehida dan keton dapat mensolvasi ion. Contoh: Na. I larut dalam aseton. 17

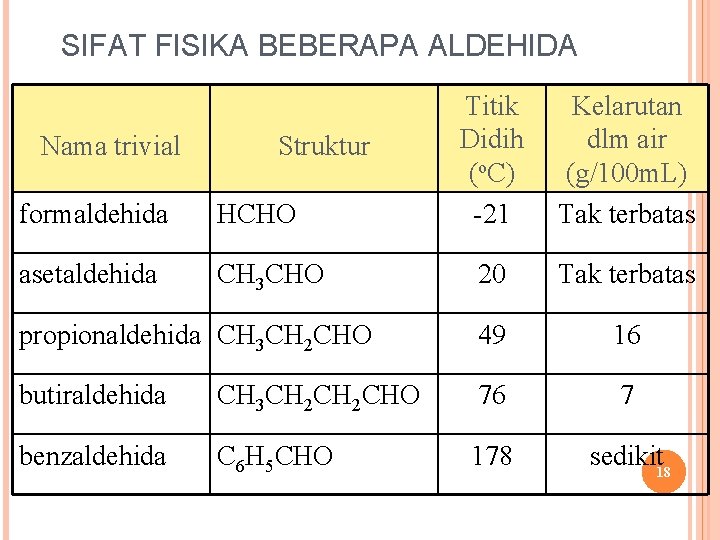
SIFAT FISIKA BEBERAPA ALDEHIDA Titik Didih (o. C) -21 Kelarutan dlm air (g/100 m. L) Tak terbatas 20 Tak terbatas propionaldehida CH 3 CH 2 CHO 49 16 butiraldehida CH 3 CH 2 CHO 76 7 benzaldehida C 6 H 5 CHO 178 sedikit 18 Nama trivial Struktur formaldehida HCHO asetaldehida CH 3 CHO

SIFAT FISIKA BEBERAPA KETON Nama trivial aseton Struktur CH 3 COCH 3 Titik Kelarutan Didih dlm air (o. C) (g/100 m. L) 56 Tak terbatas metil keton CH 3 COCH 2 CH 3 80 26 asetofenon C 6 H 5 COCH 3 202 Tak larut benzofenon C 6 H 5 COC 6 H 5 306 Tak larut 19


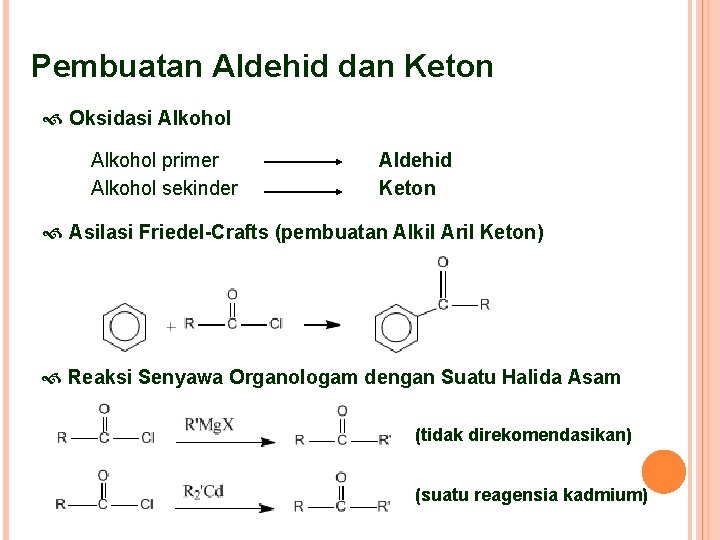
Pembuatan Aldehid dan Keton Oksidasi Alkohol primer Alkohol sekinder Aldehid Keton Asilasi Friedel-Crafts (pembuatan Alkil Aril Keton) Reaksi Senyawa Organologam dengan Suatu Halida Asam (tidak direkomendasikan) (suatu reagensia kadmium)

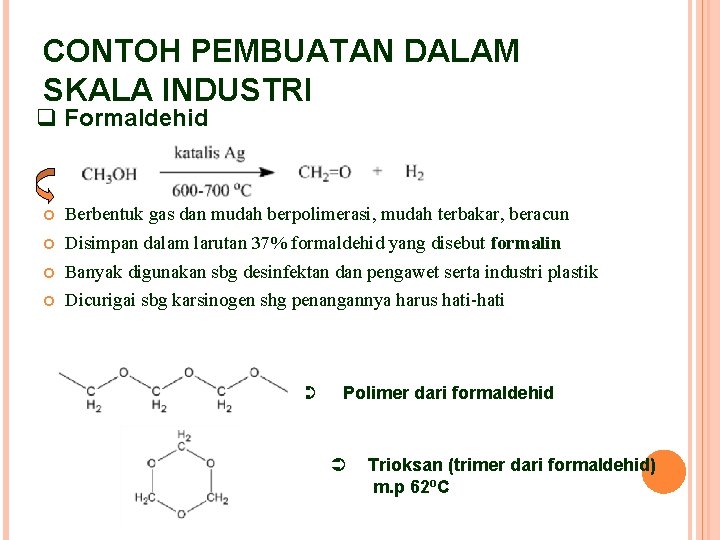
CONTOH PEMBUATAN DALAM SKALA INDUSTRI q Formaldehid Berbentuk gas dan mudah berpolimerasi, mudah terbakar, beracun Disimpan dalam larutan 37% formaldehid yang disebut formalin Banyak digunakan sbg desinfektan dan pengawet serta industri plastik Dicurigai sbg karsinogen shg penangannya harus hati-hati Ü Polimer dari formaldehid Ü Trioksan (trimer dari formaldehid) m. p 62 o. C

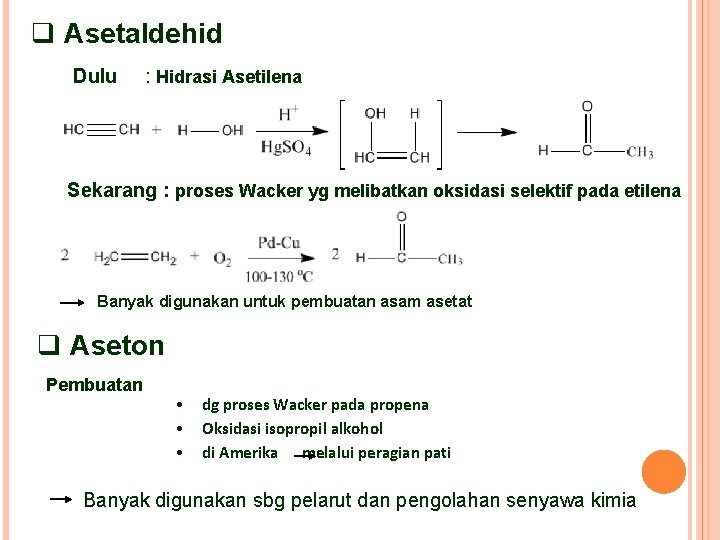
q Asetaldehid Dulu : Hidrasi Asetilena Sekarang : proses Wacker yg melibatkan oksidasi selektif pada etilena Banyak digunakan untuk pembuatan asam asetat q Aseton Pembuatan • • • dg proses Wacker pada propena Oksidasi isopropil alkohol di Amerika melalui peragian pati Banyak digunakan sbg pelarut dan pengolahan senyawa kimia

TUGAS !!

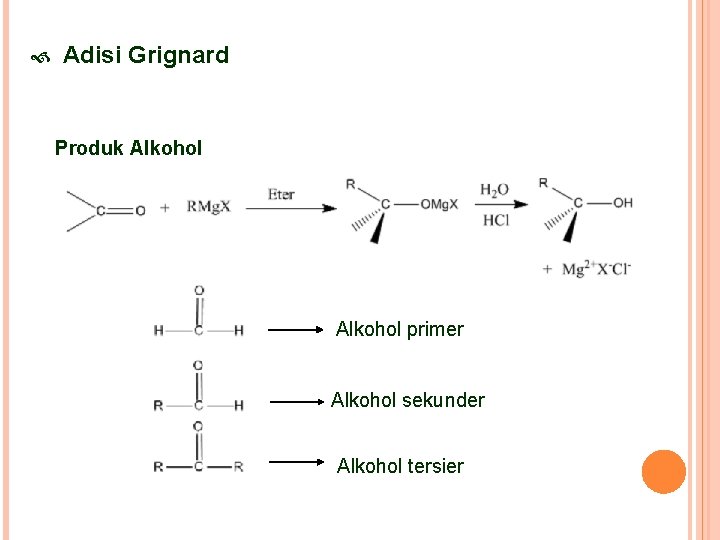
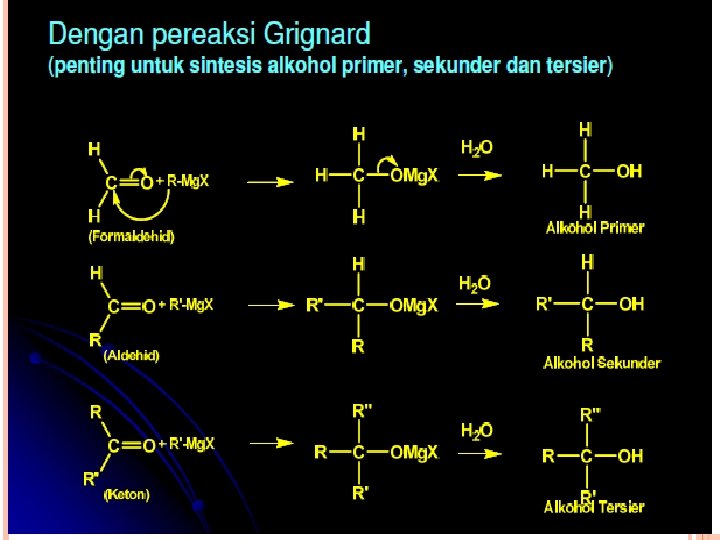
Adisi Grignard Produk Alkohol primer Alkohol sekunder Alkohol tersier


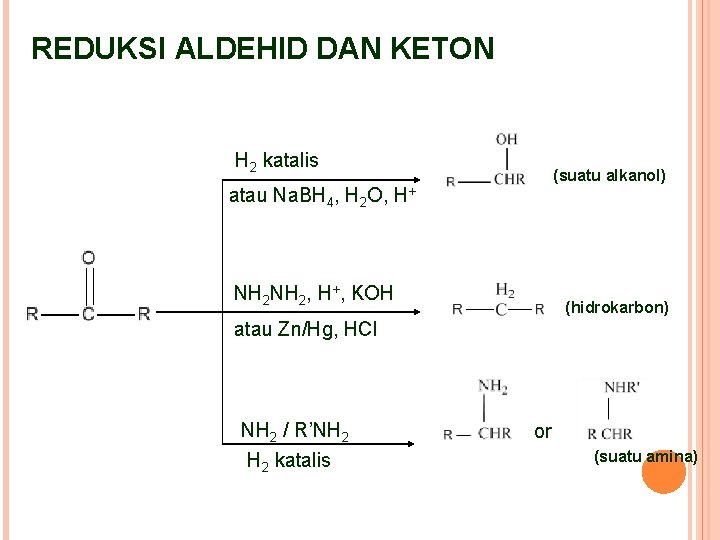
REDUKSI ALDEHID DAN KETON H 2 katalis atau Na. BH 4, H 2 O, (suatu alkanol) H+ NH 2, H+, KOH (hidrokarbon) atau Zn/Hg, HCl NH 2 / R’NH 2 katalis or (suatu amina)

q Hidrogenasi Keton H 2 katalitik Alkohol Sekunder Aldehid H 2 katalitik Alkohol Primer Jika suatu senyawa mengandung ikatan rangkap dan karbonil, maka : Ü C=C tereduksi, tetapi C=O tidak dilakukan pd P, T kamar Ü C=C tereduksi, tetapi C=O tereduksi dilakukan dengan penambahan P, T Ü C=C tidak, tetapi C=O tereduksi dilakukan dengan hidrida logam q Hidrida Logam Ü Li. Al. H 4 (LAH) dibuat dari 4 Li. H dan Al. Cl 3 merupakan pereduksi kuat Ü Na. BH 44 dibuat dari 4 Na. H + B (OMe)3 Merupakan pereduksi lembut Li. Al. H 4 + 3 Li. Cl Na. BH 4 + 3 Me. O-Na+

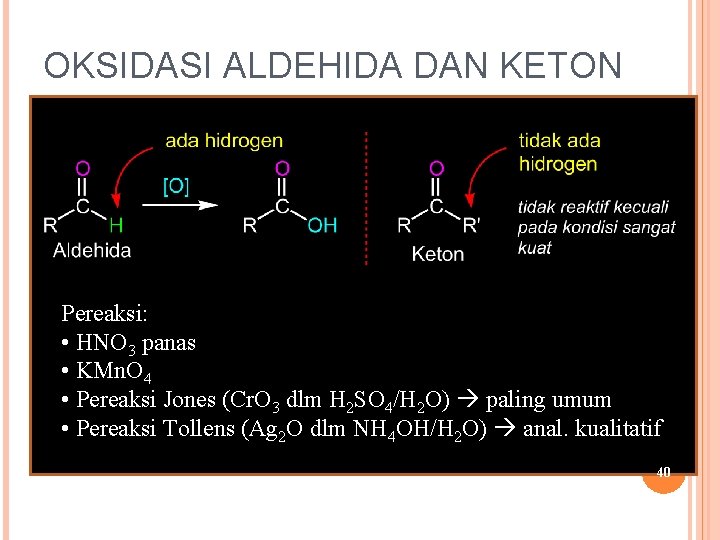
OKSIDASI ALDEHIDA DAN KETON Pereaksi: • HNO 3 panas • KMn. O 4 • Pereaksi Jones (Cr. O 3 dlm H 2 SO 4/H 2 O) paling umum • Pereaksi Tollens (Ag 2 O dlm NH 4 OH/H 2 O) anal. kualitatif 40
![1 Oksidasi dengan Oksidator Kuat O RCOH R COOH Aldehida Asam karboksilat Catatan 1) Oksidasi dengan Oksidator Kuat [O] R-CO-H → R- CO-OH Aldehida Asam karboksilat Catatan:](https://slidetodoc.com/presentation_image_h/9d56f2572e3489b30d28a4cb019ff274/image-28.jpg)
1) Oksidasi dengan Oksidator Kuat [O] R-CO-H → R- CO-OH Aldehida Asam karboksilat Catatan: Keton tidak dapat dioksidasi dengan oksidator lemah seperti pereaksi. Fehling dan pereaksi Tollens. Jika keton dioksidasi paksa, maka keton akan pecah menjadi 2 macam asam karboksilat yang jumlah atom C-nya masing-masing lebih sedikit daripada keton semula. 2) Oksidasi dengan Pereaksi Tollens (Oksidator Lemah) R-CO-H + Ag 2 O (aq) → R- CO-OH + 2 Ag (s) Aldehida Pereaksi Tollens Asam karboksilat Cermin perak Contoh: CH 3 -CH 2 -CO-CH 2 -CH 3 [O] 3) Oksidasi dengan Pereaksi Fehling R-CO-H + 2 Cu. O (aq) → R- CO-OH + Cu 2 O (s) Aldehida Pereaksi Fehling Asam karboksilat Tembaga oksida (merah bata) 4) Oksidasi oleh oksigen di udara pada suhu kamar R-CO-H + O 2 → R- CO-OH Aldehida Asam karboksilat CH 3 -COOH + CH 3 -CH 2 -COOH

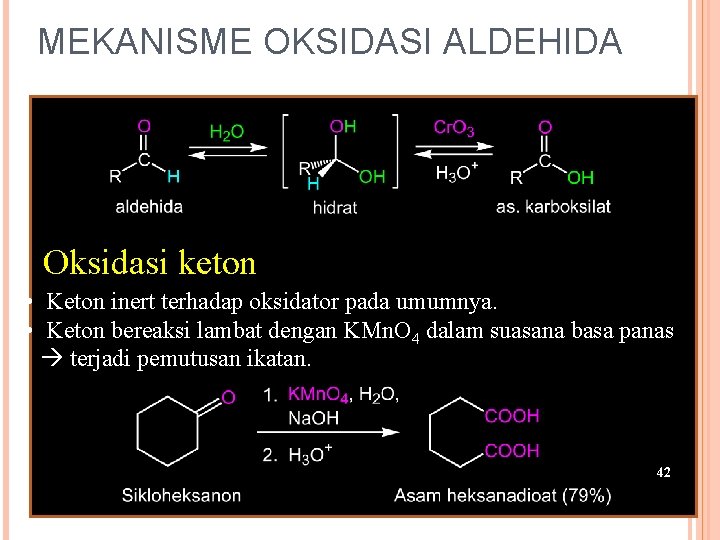
MEKANISME OKSIDASI ALDEHIDA • Oksidasi berlangsung melalui intermediat 1, 1 -diol. Oksidasi keton • Keton inert terhadap oksidator pada umumnya. • Keton bereaksi lambat dengan KMn. O 4 dalam suasana basa panas terjadi pemutusan ikatan. 42

ISOMER PADA ALDEHIDA DAN KETON a. Isomer Posisi Isomer rantai pada aldehida dimulai dari suku keempat, yaitu aldehid yang memiliki empat atom karbon (C 4 H 8 O). : 2 -metilpropanal (isobutanal) butanal Isomer heksanon (keton) 2 -heksanon (metil butil keton) 3 -metil-2 -pentanon (metil sec-butil keton) 3 -heksanon (etil propil keton)

b. Isomer Fungsi Senyawa yang mempunyai rumus molekul sama tetapi mengandung gugus fungsi berbeda.

KEGUNAAN Yang paling umum penggunaannya adalah propanon, dalam kehidupan sehari-hari dikenal dengan aseton. Kegunaan utama sebagi pelarut, khususnya untuk zat-zat yang kurang polar dan non polar.

TERIMA KASIH

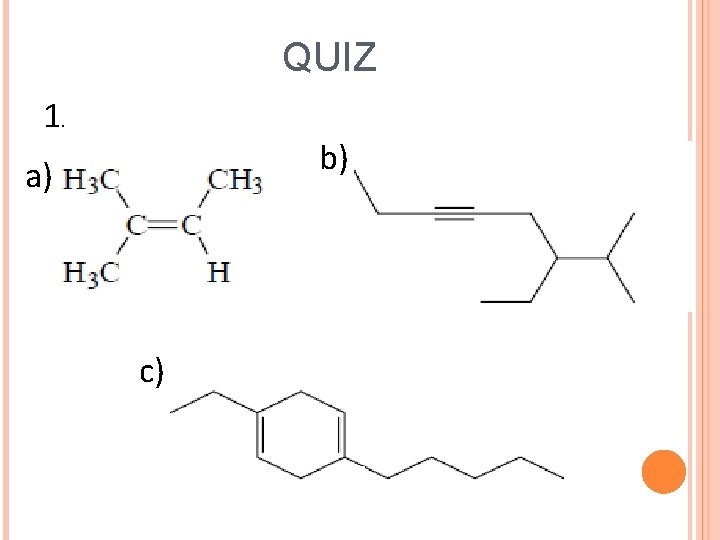
QUIZ 1. b) a) c)

2. Tuliskan isomer fungsi untuk C 5 H 10 sebagai aldehid dan keton