Alberts Johnson Lewis Morgan Raff Roberts Walter Biologie

Alberts • Johnson • Lewis • Morgan • Raff • Roberts • Walter Biologie moléculaire de la cellule Sixième Édition Chapitre 17 Le cycle cellulaire Copyright © Garland Science 2015

Le cycle cellulaire I. Vue d'ensemble du cycle cellulaire II. Le système de contrôle du cycle cellulaire III. La phase S IV. La mitose V. La cytocinèse VI. Méiose VII. Contrôle de la division et de la croissance cellulaire

Définition • Dernière étape du cycle cellulaire • Division du cytoplasme • Dans une cellule type, la cytocinèse accompagne chaque mitose

Mitose sans cytocinèse • Embryons précoces de Drosophila (abordé plus loin) • Certains hépatocytes et cellules de muscle cardiaque de mammifères • Subissent la mitose sans cytocinèse • acquisition de multiples noyaux • Dans la plupart des cellules animales, la cytocinèse commence à l'anaphase et se termine peu après l'achèvement de la mitose pendant la télophase

Sillon de division • La première modification visible de la cytocinèse dans une cellule animale est l'apparition soudaine d'une ride, ou sillon de division, à la surface de la cellule • Le sillon s'approfondit rapidement et se propage autour de la cellule jusqu'à ce qu'il divise complètement la cellule en deux

Anneau contractile • Structure qui sous-tend ce phénomène • Assemblage dynamique composé de filaments d'actine, de filaments de myosine II, et de nombreuses protéines de structure et de régulation • Au cours de l'anaphase, l'anneau s'assemble juste sous la membrane plasmique • Figure 17 -41, voir aussi Planche 17 -1
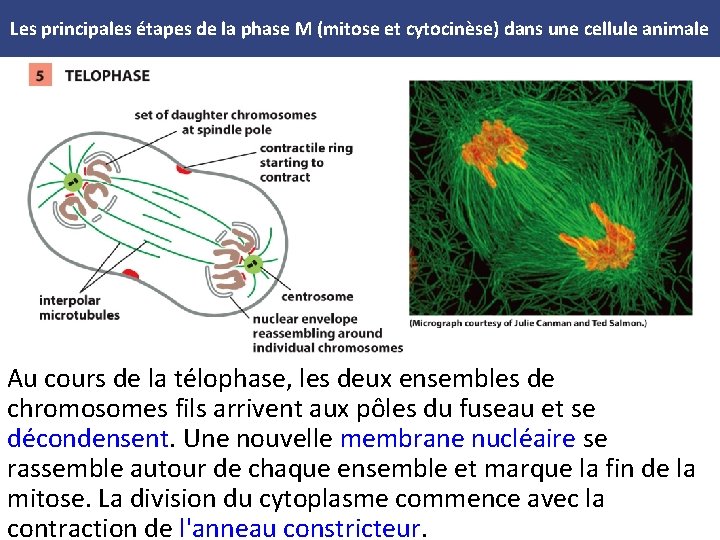
Les principales étapes de la phase M (mitose et cytocinèse) dans une cellule animale Au cours de la télophase, les deux ensembles de chromosomes fils arrivent aux pôles du fuseau et se décondensent. Une nouvelle membrane nucléaire se rassemble autour de chaque ensemble et marque la fin de la mitose. La division du cytoplasme commence avec la contraction de l'anneau constricteur.
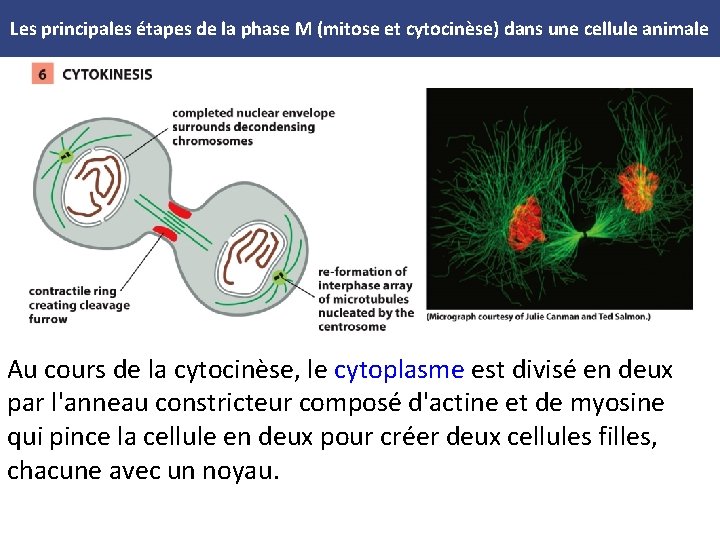
Les principales étapes de la phase M (mitose et cytocinèse) dans une cellule animale Au cours de la cytocinèse, le cytoplasme est divisé en deux par l'anneau constricteur composé d'actine et de myosine qui pince la cellule en deux pour créer deux cellules filles, chacune avec un noyau.

Cytocinèse (A) Les faisceaux d'actine-myosine des anneaux contractiles sont orientés comme indiqué sur le schéma, de telle sorte que leurs contractions tirent la membrane vers l'intérieur. (B) Dans cette photographie en microscopie électronique à balayage à faible grossissement d'un œuf de grenouille en train de se scinder, le sillon de division est bien défini et particulièrement bien dessiné car la cellule est particulièrement grosse. La formation du sillon dans la membrane cellulaire est causée par l'activité de l'anneau contractile situé juste dessous. (C) La surface du sillon à plus fort grossissement
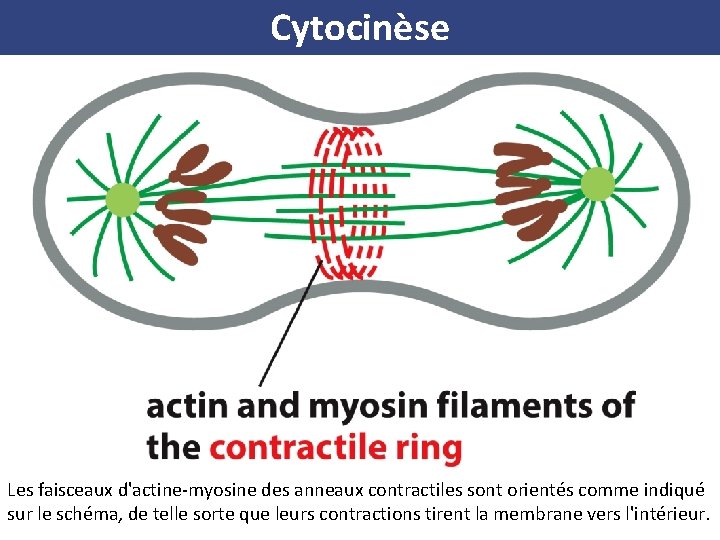
Cytocinèse Les faisceaux d'actine-myosine des anneaux contractiles sont orientés comme indiqué sur le schéma, de telle sorte que leurs contractions tirent la membrane vers l'intérieur.
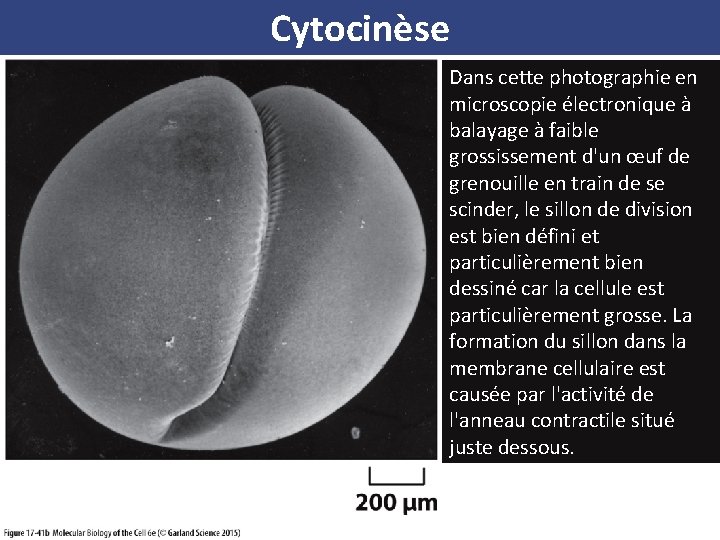
Cytocinèse Dans cette photographie en microscopie électronique à balayage à faible grossissement d'un œuf de grenouille en train de se scinder, le sillon de division est bien défini et particulièrement bien dessiné car la cellule est particulièrement grosse. La formation du sillon dans la membrane cellulaire est causée par l'activité de l'anneau contractile situé juste dessous.

Cytocinèse La surface du sillon à plus fort grossissement

La membrane plasmique • L'anneau se contracte progressivement, et en même temps, la fusion de vésicules intracellulaire avec la membrane plasmique insère une nouvelle membrane, proche de l'anneau • Cette addition de membrane compense l'augmentation de surface qui accompagne la division du cytoplasme • Quand la contraction de l'anneau est terminée, l'insertion de membrane et la fusion scellent l'espace vide entre les deux cellules filles

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

L'anneau contractile • À l'interphase, les filaments d'actine et de myosine II forment un réseau cortical qui double la membrane plasmique des cellules • Dans certaines cellules, ils forment aussi de gros faisceaux cytoplasmiques appelés fibres du stress • Alors que la cellule entre en mitose, ces rangées d'actine et de myosine se relâchent ; une grande partie de l'actine se réorganise et les filaments de myosine II sont libérés • Quand les chromatides sœurs se séparent à l'anaphase, l'actine et la myosine II commencent à s'accumuler dans l'anneau contractile qui s'assemble rapidement avec de nombreuses autres protéines qui apportent une structure de support ou aident à l'assemblage de l'anneau • Figure 17 -42
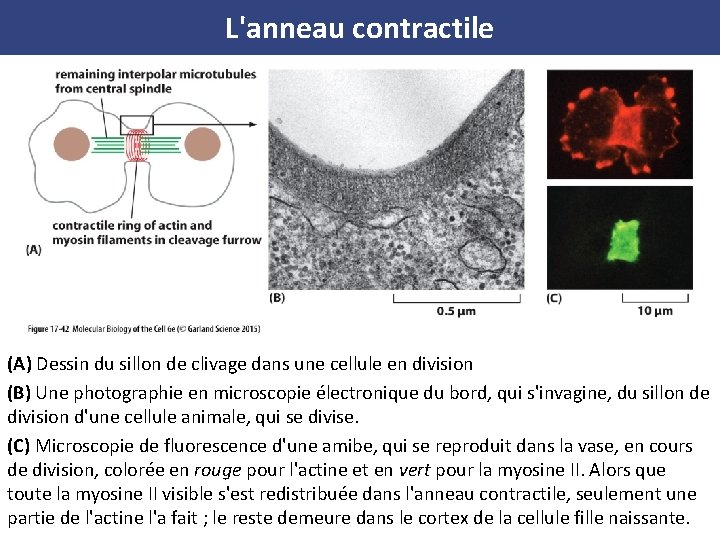
L'anneau contractile (A) Dessin du sillon de clivage dans une cellule en division (B) Une photographie en microscopie électronique du bord, qui s'invagine, du sillon de division d'une cellule animale, qui se divise. (C) Microscopie de fluorescence d'une amibe, qui se reproduit dans la vase, en cours de division, colorée en rouge pour l'actine et en vert pour la myosine II. Alors que toute la myosine II visible s'est redistribuée dans l'anneau contractile, seulement une partie de l'actine l'a fait ; le reste demeure dans le cortex de la cellule fille naissante.
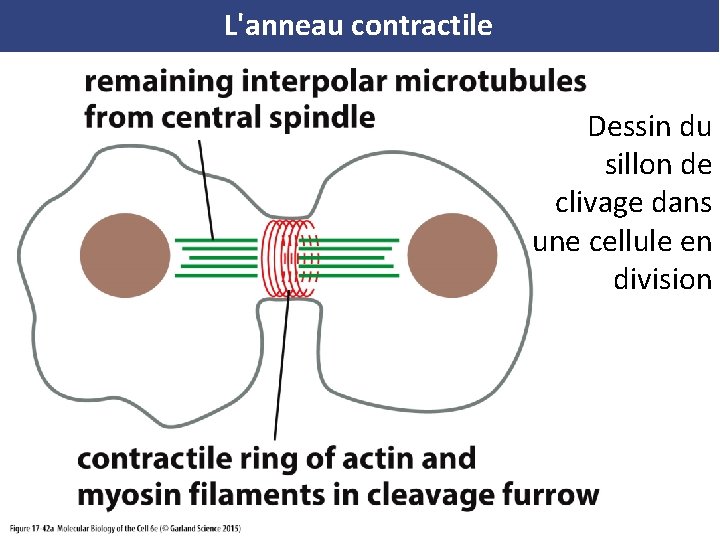
L'anneau contractile Dessin du sillon de clivage dans une cellule en division
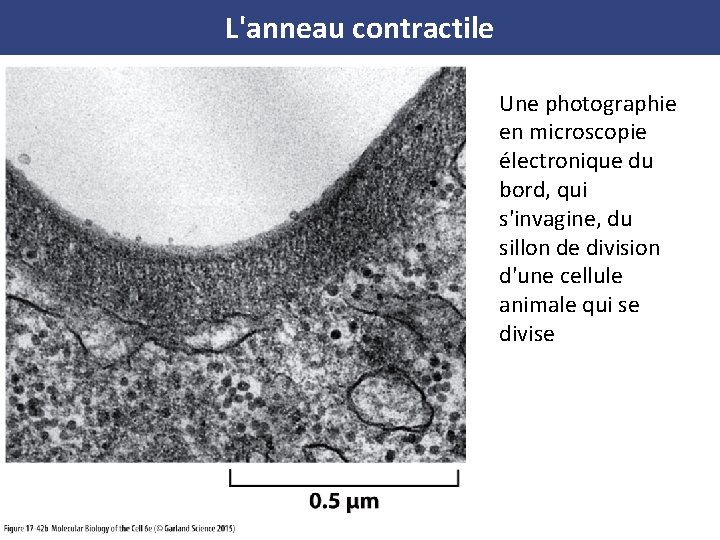
L'anneau contractile Une photographie en microscopie électronique du bord, qui s'invagine, du sillon de division d'une cellule animale qui se divise
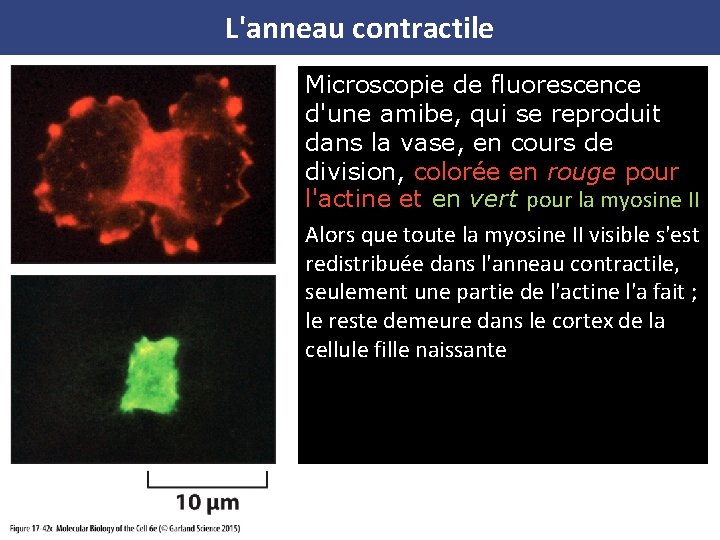
L'anneau contractile Microscopie de fluorescence d'une amibe, qui se reproduit dans la vase, en cours de division, colorée en rouge pour l'actine et en vert pour la myosine II Alors que toute la myosine II visible s'est redistribuée dans l'anneau contractile, seulement une partie de l'actine l'a fait ; le reste demeure dans le cortex de la cellule fille naissante

L'assemblage de l'anneau contractile • Résulte en partie de la formation locale de nouveaux filaments d'actine, qui dépendent des molécules des protéines formines qui permettent – la nucléation de filaments d'actine linéaires, – parallèles non branchés

Force • Après l'anaphase, les rangées chevauchantes de filaments d'actine et de myosine II se contractent pour produire la force nécessaire à la division du cytoplasme en deux • Une fois que la contraction a commencé, l'anneau exerce une force si grande qu'elle serait capable de briser une aiguille de verre insérée sur son chemin

Épaisseur de l'anneau • Au cours de sa contraction, l'anneau conserve la même épaisseur, suggérant que son volume total et le nombre de filaments qu'il contient diminuent régulièrement • De plus, contrairement à l'actine des muscles, les filaments d'actine de l'anneau sont très dynamiques et leur organisation se modifie continuellement pendant la cytocinèse

Corps central (= midbody) • L'anneau contractile est finalement rendu superflu quand la séparation se termine et que la membrane plasmique du sillon de division se rétrécit pour former le corps central (midbody) • Le corps central persiste en tant que lien entre les deux cellules filles et – renferme les restes du fuseau central, une grande structure protéique issue des microtubules interpolaires antiparallèles de la région centrale du fuseau, – avec, compressés à l'intérieur, des matériaux denses de la matrice • Figure 17 -43
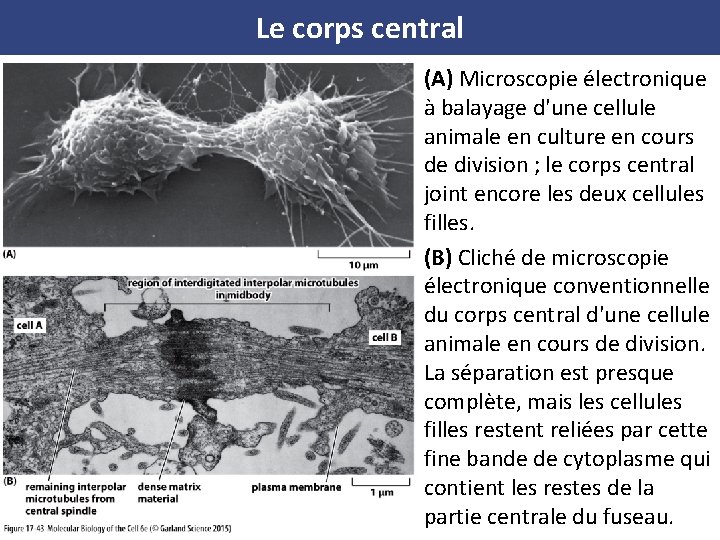
Le corps central (A) Microscopie électronique à balayage d'une cellule animale en culture en cours de division ; le corps central joint encore les deux cellules filles. (B) Cliché de microscopie électronique conventionnelle du corps central d'une cellule animale en cours de division. La séparation est presque complète, mais les cellules filles restent reliées par cette fine bande de cytoplasme qui contient les restes de la partie centrale du fuseau.
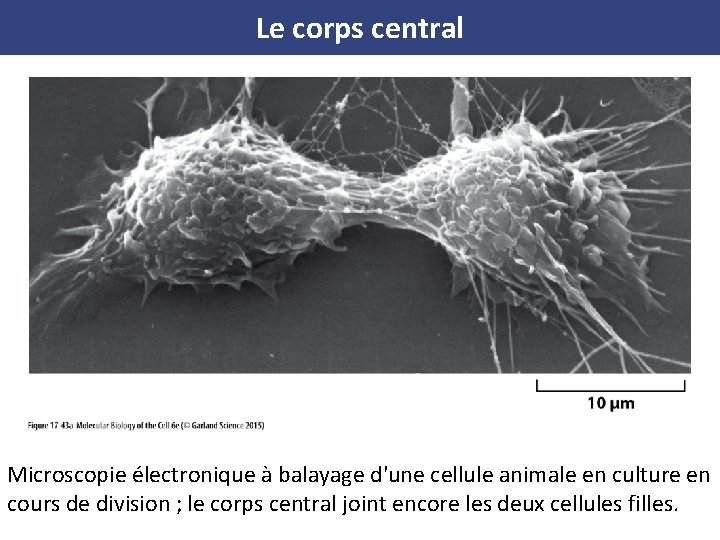
Le corps central Microscopie électronique à balayage d'une cellule animale en culture en cours de division ; le corps central joint encore les deux cellules filles.
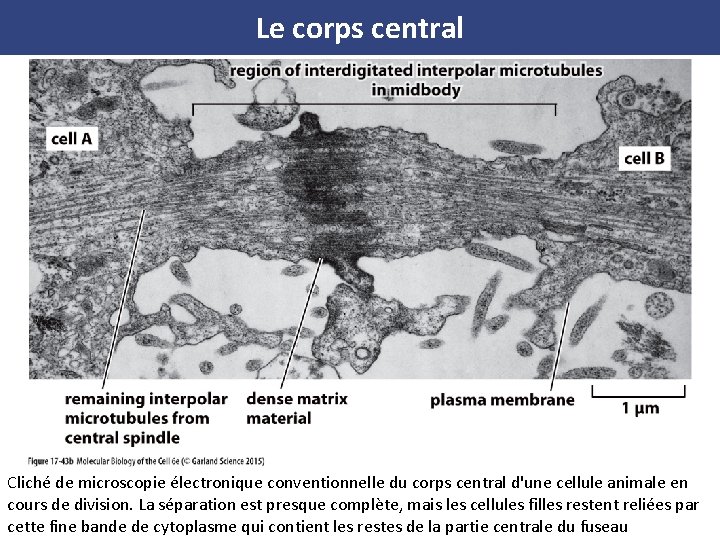
Le corps central Cliché de microscopie électronique conventionnelle du corps central d'une cellule animale en cours de division. La séparation est presque complète, mais les cellules filles restent reliées par cette fine bande de cytoplasme qui contient les restes de la partie centrale du fuseau

À la fin de la cytocinèse • Une fois que les cellules filles sont effectivement séparées, certaines des composantes du corps central résiduel restent souvent à l'intérieur de la membrane plasmique de chaque cellule, • où elles peuvent servir de marquage sur le cortex, aidant à orienter le fuseau dans la division cellulaire suivante

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

Rho. A • Rho. A, une petite GTPase de la superfamille de Ras contrôle l'assemblage et le fonctionnement de l'anneau contractile au site de clivage • Rho. A est activée au niveau du cortex cellulaire du site de la future division, où elle favorise – la formation du filament d'actine, – l'assemblage de la myosine II – et la contraction de l'anneau • Elle favorise la formation du filament d'actine par activation des formines, et elle favorise l'assemblage de la myosine II et les contractions en activant de multiples protéines kinases, dont la kinase Rhock activée par Rho • Figure 17 -44

rho-Associated Kinases • A group of intracellular-signaling serine threonine kinases that bind to RHO GTP-BINDING PROTEINS. • They were originally found to mediate the effects of rho. A GTPBINDING PROTEIN on the formation of STRESS FIBERS and FOCAL ADHESIONS. • Rho-associated kinases have specificity for a variety of substrates including MYOSIN-LIGHT-CHAIN PHOSPHATASE and LIM KINASES. • Year introduced: 2008

Rho Guanine Nucleotide Exchange Factors • Signaling proteins which function as master molecular switches by activating Rho GTPases through conversion of guanine nucleotides. • Rho GTPases in turn control many aspects of cell behavior through the regulation of multiple downstream signal transduction pathways. • Year introduced: 2014

rho. A GTP-Binding Protein • A RHO GTP-BINDING PROTEIN involved in regulating signal transduction pathways that control assembly of focal adhesions and actin stress fibers. • This enzyme was formerly listed as EC 3. 6. 1. 47. • Year introduced: 2000
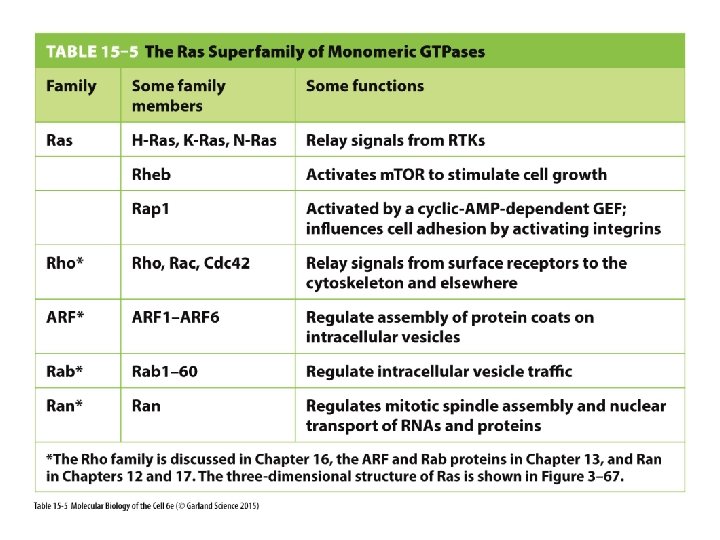
Tableau 15 -5

The Ras Superfamily of Monomeric GTPases Some family members Some functions Rheb Activates m. TOR to stimulate cell growth Rap 1 Activated by a cyclic-AMP-dependent GEF; influences cell adhesion by activating integrins Rho* Rho, Rac, Cdc 42 Relay signals from surface receptors to the cytoskeieton and elsewhere ARF* ARF 1 -ARF 6 Regulate assembly of protein coats on intracellular vesicies Rab* Rab 1 -60 Regulate intracellular vesicle traffic Ran* Ran Regulates mitotic spindie assembly and nuclear transport of RNAs and proteins Family Ras Tableau 15 -5 H-Ras, K-Ras, N-Ras Relay signais from RTKs *The Rho family is discussed in Chapter 16, the ARF and Rab proteins in Chapter 13, and Ran in Chapters 12 and 17. The three-dimensional structure of Ras is shown in Figure 3 -67.
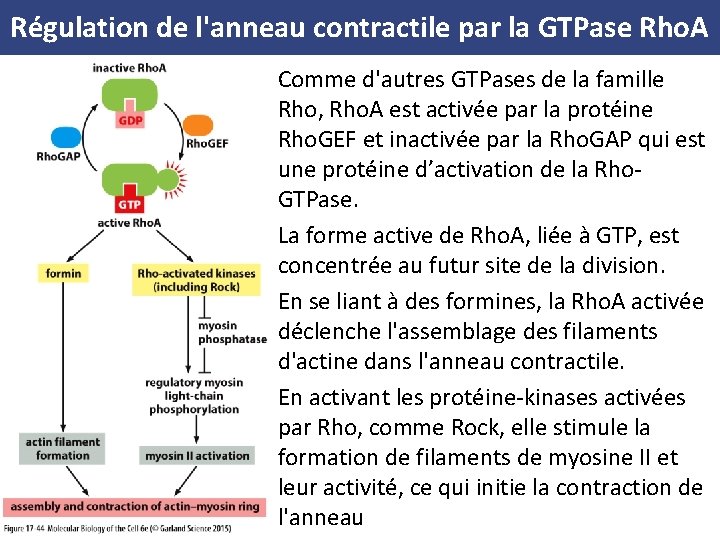
Régulation de l'anneau contractile par la GTPase Rho. A Comme d'autres GTPases de la famille Rho, Rho. A est activée par la protéine Rho. GEF et inactivée par la Rho. GAP qui est une protéine d’activation de la Rho. GTPase. La forme active de Rho. A, liée à GTP, est concentrée au futur site de la division. En se liant à des formines, la Rho. A activée déclenche l'assemblage des filaments d'actine dans l'anneau contractile. En activant les protéine-kinases activées par Rho, comme Rock, elle stimule la formation de filaments de myosine II et leur activité, ce qui initie la contraction de l'anneau

RMLC, (regulatory myosin light chain) • Ces kinases phosphorylent la chaîne légère régulatrice de la myosine (RMLC, regulatory myosin light chain), qui est une des sous-unités de la myosine II • RMLC phosphorylée stimule la formation de filaments de myosine II bipolaires et l'activité motrice

Rho-GEF • On pense que Rho. A est activé par un facteur d'échange entre Rho et un nucléotide à guanine Guanine nucléotide Exchange Factor (Rho-GEF) • Se trouve au niveau du cortex cellulaire du futur site de division, où il stimule la libération de GDP et la liaison de GTP sur Rho. A • Figure 17 -44
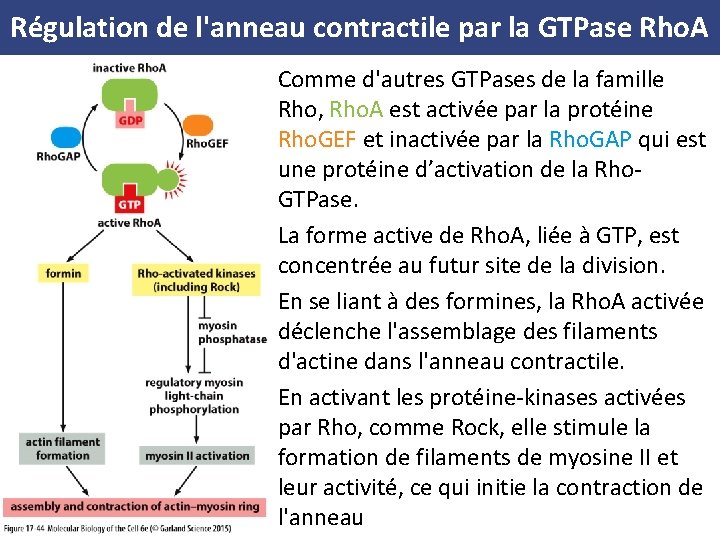
Régulation de l'anneau contractile par la GTPase Rho. A Comme d'autres GTPases de la famille Rho, Rho. A est activée par la protéine Rho. GEF et inactivée par la Rho. GAP qui est une protéine d’activation de la Rho. GTPase. La forme active de Rho. A, liée à GTP, est concentrée au futur site de la division. En se liant à des formines, la Rho. A activée déclenche l'assemblage des filaments d'actine dans l'anneau contractile. En activant les protéine-kinases activées par Rho, comme Rock, elle stimule la formation de filaments de myosine II et leur activité, ce qui initie la contraction de l'anneau

Localisation de Rho. GEF • On sait très peu de choses sur la localisation de Rho. GEF ou sur son activation au site de division • bien que les microtubules du fuseau d'anaphase semblent être impliqués dans son fonctionnement, (comme nous allons le voir maintenant)

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

Problème fondamental de la cytocinèse • S'assurer que la division a lieu au bon moment et au bon endroit • La cytocinèse doit avoir lieu seulement – après que les deux ensembles de chromosomes se sont complètement séparés, – et le lieu de la division doit se situer entre les deux ensembles de chromosomes fils, pour être sûr que chaque cellule fille en reçoive un jeu complet • Le moment et la position corrects de la cytocinèse dans les cellules animales sont atteints par des mécanismes qui dépendent du fuseau mitotique

Au bon endroit • Au cours de l'anaphase, le fuseau produit des signaux qui déclenchent la formation du sillon sur une position située à mi-chemin entre les pôles du fuseau, s'assurant ainsi que la division aura bien lieu entre les deux jeux de chromosomes qui viennent d'être séparés

Au bon moment • Comme ces signaux ont leur origine dans le fuseau d'anaphase, ce mécanisme contribue aussi à déterminer le moment correct pour la cytocinèse en fin de mitose • La cytocinèse a aussi lieu au bon moment car la déphosphorylation des substrats de Cdk, qui dépend de la destruction des cyclines en cours de métaphase et d'anaphase, déclenche la cytocinèse

Nous décrirons maintenant ces mécanismes régulateurs avec plus de détails et en nous appuyant surtout sur la cytocinèse des cellules animales

Le fuseau induit la formation du sillon • Des études sur les œufs fécondés d'invertébrés marins furent les premières à révéler l'importance des microtubules du fuseau pour déterminer la place de l'anneau contractile • Après la fécondation, ces embryons se scindent rapidement sans l'intervention d'une période intermédiaire de croissance • De cette façon l'œuf est progressivement divisé en cellules de plus en plus petites • Comme leur cytoplasme est très clair ces divisions peuvent être suivies en temps réel au microscope • Si au cours de l'anaphase précoce, on pousse un peu le fuseau avec une fine aiguille de verre, le sillon, qui commençait à se faire, disparaît, et un nouveau sillon se forme en rapport avec la nouvelle place du fuseau — ce qui est en accord avec l'idée que ce sont des signaux produits par le fuseau qui induisent la formation du sillon

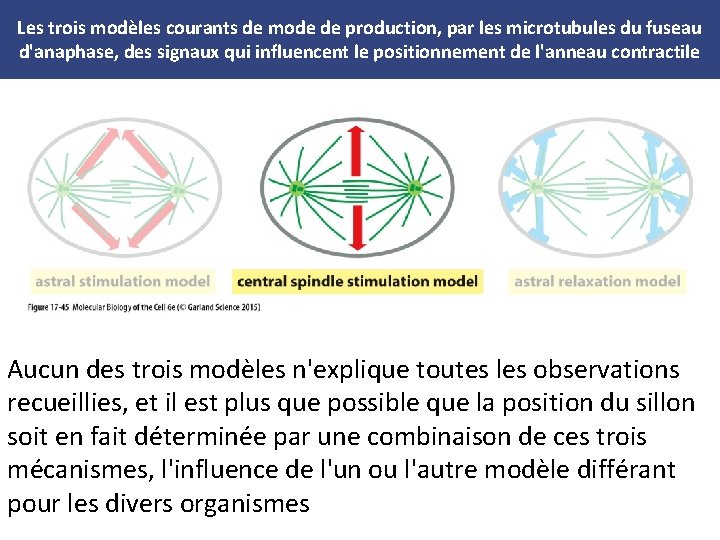
Comment le fuseau mitotique choisit-il le site de la future division ? • Trois mécanismes généraux ont été proposés et la plupart des cellules semblent en combiner plusieurs • (Figure 17 -45)
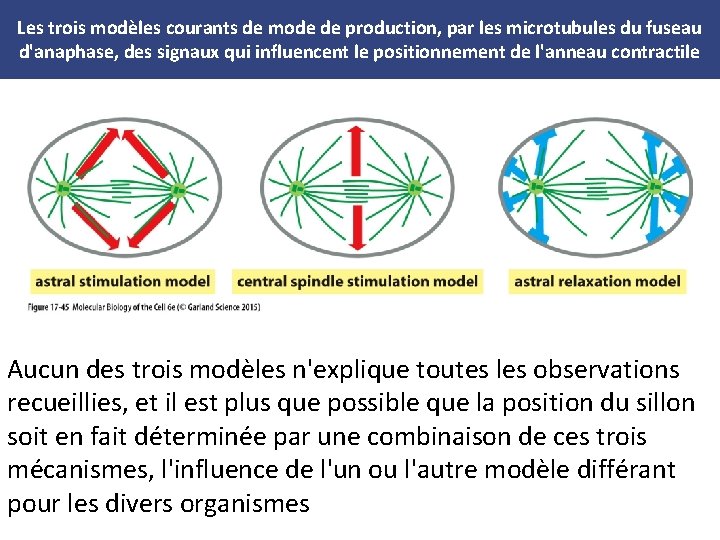
Les trois modèles courants de mode de production, par les microtubules du fuseau d'anaphase, des signaux qui influencent le positionnement de l'anneau contractile Aucun des trois modèles n'explique toutes les observations recueillies, et il est plus que possible que la position du sillon soit en fait déterminée par une combinaison de ces trois mécanismes, l'influence de l'un ou l'autre modèle différant pour les divers organismes

i - Modèle de la stimulation astrale • Les microtubules astraux portent des signaux déclenchant la formation du sillon jusqu'au cortex cellulaire, où ils se rassemblent finalement pour former un anneau à mi-chemin entre les deux pôles du fuseau • Des preuves en faveur de ce modèle viennent d'expériences ingénieuses sur des grosses cellules embryonnaires, démontrant qu'un sillon de division se forme à mi-chemin entre deux asters, même quand les deux centrosomes à l'origine de la nucléation des asters ne sont pas connectés entre eux par le fuseau mitotique • (Figure 17 -46)
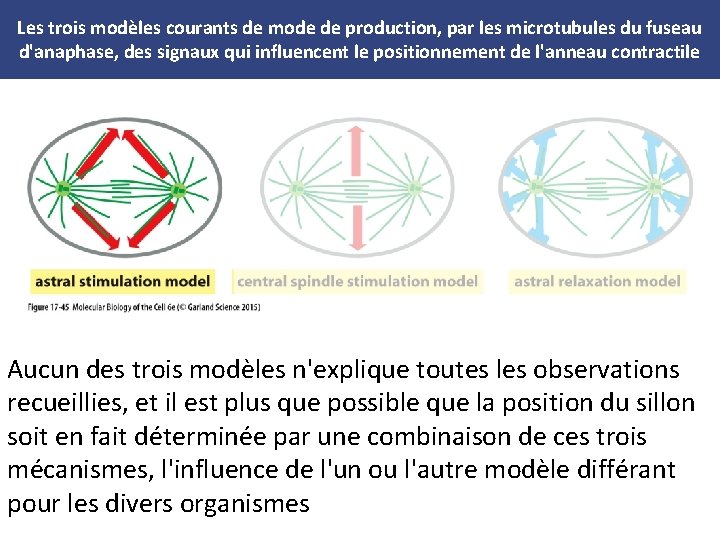
Les trois modèles courants de mode de production, par les microtubules du fuseau d'anaphase, des signaux qui influencent le positionnement de l'anneau contractile Aucun des trois modèles n'explique toutes les observations recueillies, et il est plus que possible que la position du sillon soit en fait déterminée par une combinaison de ces trois mécanismes, l'influence de l'un ou l'autre modèle différant pour les divers organismes
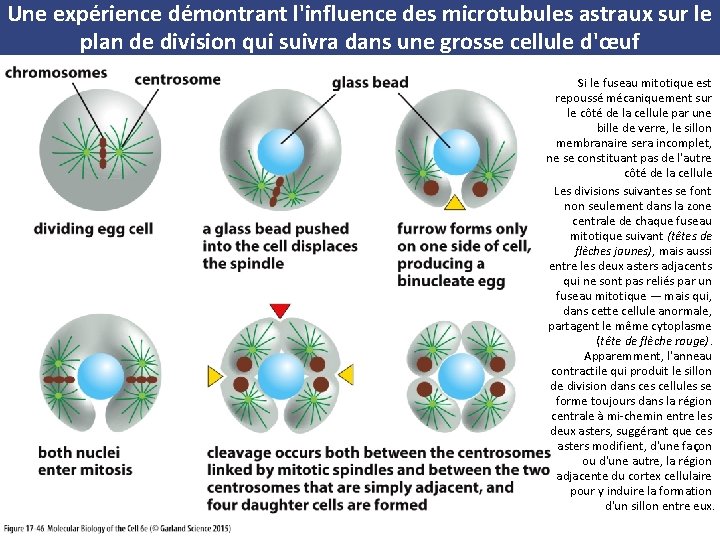
Une expérience démontrant l'influence des microtubules astraux sur le plan de division qui suivra dans une grosse cellule d'œuf Si le fuseau mitotique est repoussé mécaniquement sur le côté de la cellule par une bille de verre, le sillon membranaire sera incomplet, ne se constituant pas de l'autre côté de la cellule Les divisions suivantes se font non seulement dans la zone centrale de chaque fuseau mitotique suivant (têtes de flèches jaunes), mais aussi entre les deux asters adjacents qui ne sont pas reliés par un fuseau mitotique — mais qui, dans cette cellule anormale, partagent le même cytoplasme (tête de flèche rouge). Apparemment, l'anneau contractile qui produit le sillon de division dans cellules se forme toujours dans la région centrale à mi-chemin entre les deux asters, suggérant que ces asters modifient, d'une façon ou d'une autre, la région adjacente du cortex cellulaire pour y induire la formation d'un sillon entre eux.

ii - Modèle de stimulation par le fuseau central • La région centrale du fuseau produit un signal déclenchant la formation du sillon qui spécifie aussi le site sur lequel le sillon se formera sur le cortex cellulaire • Figure 17 -45
Les trois modèles courants de mode de production, par les microtubules du fuseau d'anaphase, des signaux qui influencent le positionnement de l'anneau contractile Aucun des trois modèles n'explique toutes les observations recueillies, et il est plus que possible que la position du sillon soit en fait déterminée par une combinaison de ces trois mécanismes, l'influence de l'un ou l'autre modèle différant pour les divers organismes

Stimulation par le fuseau central • Les microtubules interpolaires qui se chevauchent s'associent avec de nombreuses protéines de signalisation, y compris des protéines qui pourraient stimuler Rho. A • Des défauts dans le fonctionnement de ces protéines (chez des mutants de Drosophila par exemple) provoquent un échec de la cytocinèse. • (Figure 17 -47)
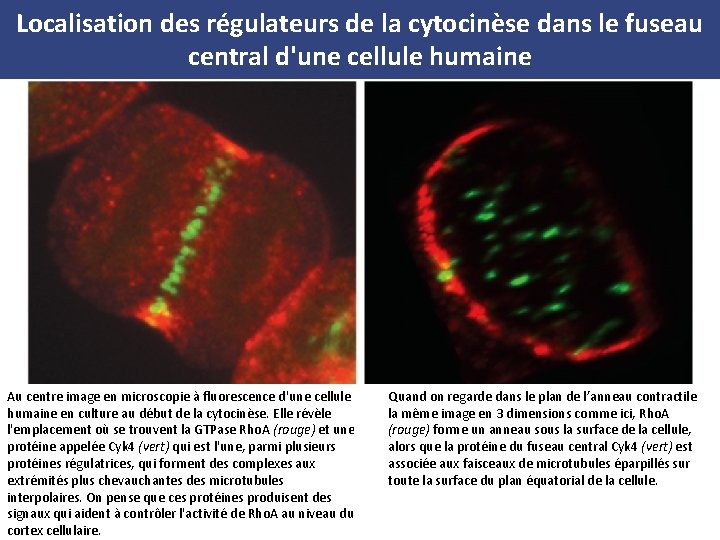
Localisation des régulateurs de la cytocinèse dans le fuseau central d'une cellule humaine Au centre image en microscopie à fluorescence d'une cellule humaine en culture au début de la cytocinèse. Elle révèle l'emplacement où se trouvent la GTPase Rho. A (rouge) et une protéine appelée Cyk 4 (vert) qui est l'une, parmi plusieurs protéines régulatrices, qui forment des complexes aux extrémités plus chevauchantes des microtubules interpolaires. On pense que ces protéines produisent des signaux qui aident à contrôler l'activité de Rho. A au niveau du cortex cellulaire. Quand on regarde dans le plan de l’anneau contractile la même image en 3 dimensions comme ici, Rho. A (rouge) forme un anneau sous la surface de la cellule, alors que la protéine du fuseau central Cyk 4 (vert) est associée aux faisceaux de microtubules éparpillés sur toute la surface du plan équatorial de la cellule.

iii - Modèle de relaxation astrale • Dans certains types cellulaires, les microtubules astraux déclenchent la relaxation locale des faisceaux d'actine et de myosine au niveau du cortex cellulaire • Suivant ce modèle de relaxation astrale, la relaxation corticale est minimum à l'équateur du fuseau, ce qui déclenche une contraction du cortex en cet endroit • (voir Figure 17 -45) • Dans les embryons précoces de C. elegans, par exemple, les traitements qui entraînent la perte des microtubules astraux conduisent à une activité contractile à travers tout le cortex, en accord avec ce modèle
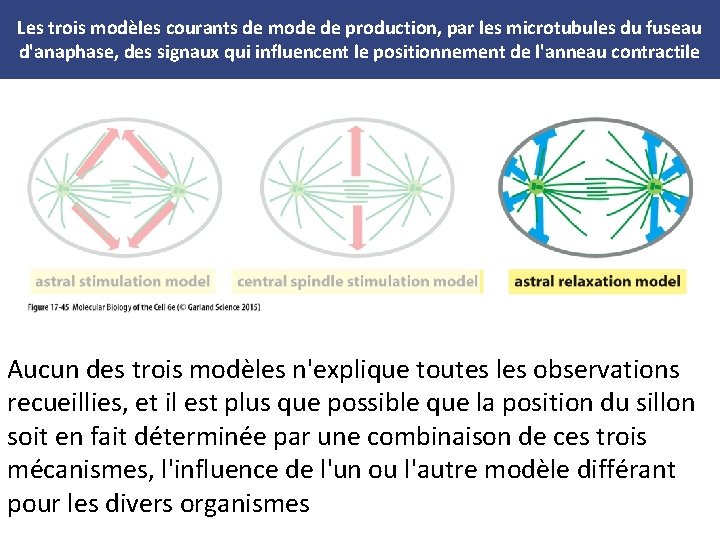
Les trois modèles courants de mode de production, par les microtubules du fuseau d'anaphase, des signaux qui influencent le positionnement de l'anneau contractile Aucun des trois modèles n'explique toutes les observations recueillies, et il est plus que possible que la position du sillon soit en fait déterminée par une combinaison de ces trois mécanismes, l'influence de l'un ou l'autre modèle différant pour les divers organismes

Site d'assemblage de l'anneau choisi avant la mitose • Dans certains types cellulaires, le site d'assemblage de l'anneau est choisi avant la mitose • Chez les levures bourgeonnantes par exemple, – un anneau de protéines appelées septines s'assemble pendant la phase G 1 tardive au futur site de division – On pense que les septines forment un échafaudage sur lequel d'autres composantes de l'anneau contractile, y compris la myosine II, s'assemblent • Dans les cellules végétales, – une bande organisée de microtubules et de filaments d'actine, appelée la bande de pré-prophase, s'assemble juste avant la mitose et marque le site où le mur s'assemblera pour diviser la cellule en deux

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

Végétaux supérieurs • Dans la plupart des cellules animales, – les mouvements du sillon de division dirigés vers l'intérieur dépendent d'une augmentation de la surface de la membrane plasmique – De nouvelles membranes sont ajoutées aux bords internes du sillon de division, généralement apportées par de petites vésicules transportées le long des microtubules de l'appareil de Golgi jusqu'au sillon • Le dépôt de membrane supplémentaire est particulièrement important pour la cytocinèse des cellules des végétaux supérieurs – Ces cellules sont entourées de parois cellulaires semi-rigides – Plutôt qu'un anneau contractile divisant le cytoplasme de l'extérieur vers l'intérieur, le cytoplasme des plantes est compartimenté de l'intérieur vers l'extérieur par la construction d'une nouvelle paroi cellulaire, la plaque cellulaire, entre les deux noyaux fils • Figure 17 -48
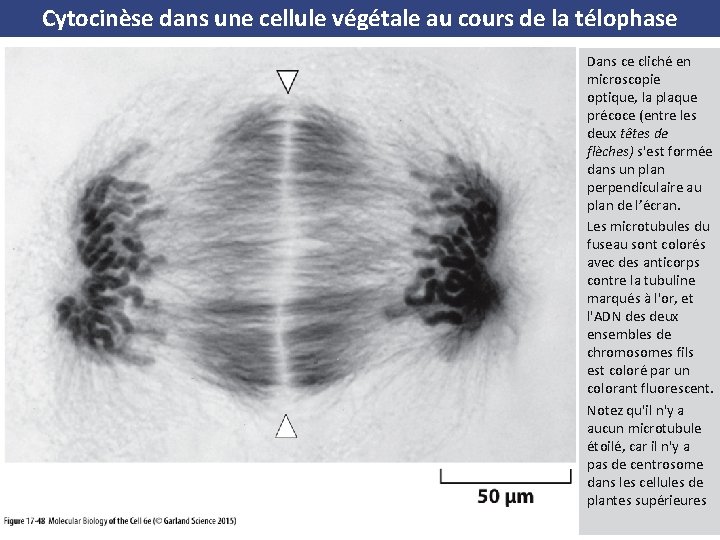
Cytocinèse dans une cellule végétale au cours de la télophase Dans ce cliché en microscopie optique, la plaque précoce (entre les deux têtes de flèches) s'est formée dans un plan perpendiculaire au plan de l’écran. Les microtubules du fuseau sont colorés avec des anticorps contre la tubuline marqués à l'or, et l'ADN des deux ensembles de chromosomes fils est coloré par un colorant fluorescent. Notez qu'il n'y a aucun microtubule étoilé, car il n'y a pas de centrosome dans les cellules de plantes supérieures

Le phragmoplaste • L'assemblage de la plaque cellulaire commence à la fin de l'anaphase et est guidé par une structure appelée phragmoplaste, qui contient des microtubules en provenance du fuseau mitotique • Phragmoplaste = microtubules • Fuseau = microtubules

Plaque cellulaire et paroi cellulaire • Des protéines motrices transportent les petites vésicules le long de ces microtubules depuis l'appareil de Golgi jusqu'au centre de la cellule • Ces vésicules, remplies de polysaccharides et de glycoprotéines, matériaux nécessaires à la synthèse d'une nouvelle paroi cellulaire, fusionnent pour former une sorte de structure entourée de membrane en forme de disque appelée la plaque cellulaire précoce • Cette plaque s'agrandit vers l'extérieur par des fusions de vésicules supplémentaires jusqu'à ce qu'elle atteigne la membrane plasmique et la paroi cellulaire originale et divise la cellule en deux • Plus tard, des microfibrilles de cellulose sont déposées dans la matrice de la plaque cellulaire, complétant la construction de la nouvelle paroi cellulaire • Figure 17 -49
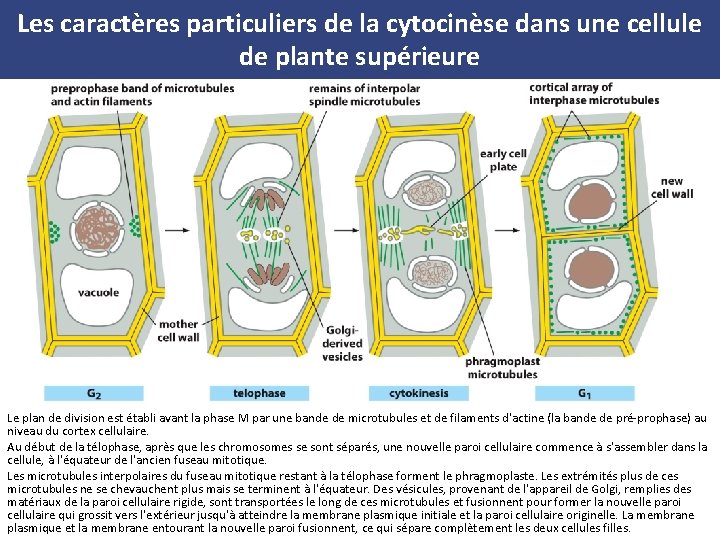
Les caractères particuliers de la cytocinèse dans une cellule de plante supérieure Le plan de division est établi avant la phase M par une bande de microtubules et de filaments d'actine (la bande de pré-prophase) au niveau du cortex cellulaire. Au début de la télophase, après que les chromosomes se sont séparés, une nouvelle paroi cellulaire commence à s'assembler dans la cellule, à l'équateur de l'ancien fuseau mitotique. Les microtubules interpolaires du fuseau mitotique restant à la télophase forment le phragmoplaste. Les extrémités plus de ces microtubules ne se chevauchent plus mais se terminent à l'équateur. Des vésicules, provenant de l'appareil de Golgi, remplies des matériaux de la paroi cellulaire rigide, sont transportées le long de ces microtubules et fusionnent pour former la nouvelle paroi cellulaire qui grossit vers l'extérieur jusqu'à atteindre la membrane plasmique initiale et la paroi cellulaire originelle. La membrane plasmique et la membrane entourant la nouvelle paroi fusionnent, ce qui sépare complètement les deux cellules filles.

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

Mitose cytocinèse • Les processus de la mitose s'assurent que chaque cellule fille reçoit un jeu complet de chromosomes • Quand une cellule eucaryote se divise, cependant, chaque cellule fille doit aussi hériter de toutes les autres composantes essentielles de la cellule, y compris les organites entourés de membranes

Répartition des organites entourés de membranes • Les mitochondries et les chloroplastes ne peuvent être assemblés de novo à partir de leurs composantes proviennent toujours de la croissance et de la division d'organites préexistants • De même, les cellules ne peuvent pas construire un nouveau réticulum endoplasmique (RE) à moins que certaines de ses parties ne soient présentes

Comment les divers organites entourés de membranes se répartissent-ils lorsque la cellule se divise ? • Les organites comme mitochondries et chloroplastes – sont habituellement présents en nombre suffisant pour être transmis sans danger si, en moyenne, leur nombre double une fois à chaque cycle • Le réticulum endoplasmique – dans les cellules en interphase est continu avec la membrane nucléaire et est organisé par les microtubules du cytosquelette – À l'entrée en phase M, la réorganisation des microtubules et la rupture de l'enveloppe nucléaire libèrent le RE – Dans la plupart des cellules, le réticulum endoplasmique reste tel quel et est coupé en deux au cours de la cytocinèse • L'appareil de Golgi – est réorganisé et fragmenté au cours de la mitose – Des fragments de Golgi s'associent aux deux pôles du fuseau et sont ainsi distribués aux deux extrémités du fuseau, s'assurant ainsi que chaque cellule fille héritera du matériel nécessaire pour reconstruire un appareil de Golgi pendant la télophase

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

En general… • La plupart des cellules animales se divisent de façon symétrique : l'anneau contractile qui se forme autour de l'équateur de la cellule mère, produit deux cellules filles de tailles égales et avec les mêmes composantes • Cette symétrie résulte du placement du fuseau mitotique, qui, dans la plupart des cas tend à se centrer dans le cytoplasme • Les microtubules astraux et les protéines motrices qui poussent ou tirent sur ces microtubules contribuent à ce processus de centrage

Cependant… • Nombreuses circonstances au cours du développement dans lesquelles la cellule se divise de façon asymétrique et produit deux cellules différant – par la taille – le contenu cytoplasmique dont elles héritent – ou les deux • Habituellement, les deux cellules filles différentes sont destinées à se développer selon des voies différentes • Pour créer des cellules filles aux destinées différentes de cette façon, la cellule mère doit – d'abord répartir certaines composantes (appelées déterminants du destin de la cellule) d'un côté de la cellule, – puis positionner le plan de la division de façon que la cellule fille appropriée reçoive bien ces composantes • Figure 17 -50
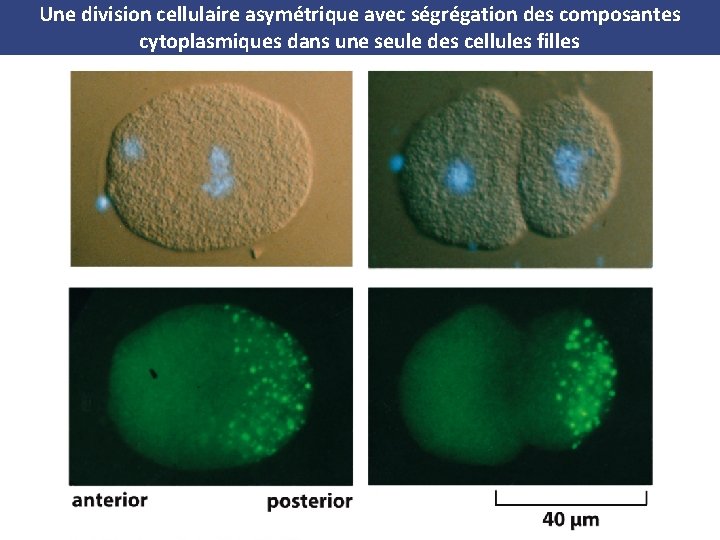
Une division cellulaire asymétrique avec ségrégation des composantes cytoplasmiques dans une seule des cellules filles

Division asymétrique • Pour positionner ainsi, de façon asymétrique, le plan de division, le fuseau doit être déplacé de façon contrôlée à l'intérieur de la cellule en division • Il semble probable que des modifications locales du cortex cellulaire dirigent les mouvements du fuseau et que les protéines motrices localisées là tirent l'un des pôles du fuseau, via ses microtubules astraux, vers la région appropriée • L'analyse génétique chez C. elegans et Drosophila a permis d'identifier certaines des protéines nécessaires pour créer une telle asymétrie, et certaines de ces protéines semblent avoir un rôle identique chez les vertébrés

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

Embryon précoce de Drosophila • La division cellulaire est généralement suivie de la division du cytoplasme • Il existe des exceptions • Certaines cellules subissent de multiples tours de division nucléaire sans qu'il y ait de division du cytoplasme

Formation d’un syncytium • Dans l'embryon précoce de Drosophila, par exemple, les 13 premiers tours de division nucléaire se font sans division du cytoplasme ce qui résulte en la formation d'une seule très grosse cellule, comportant plusieurs milliers de noyaux, organisés en une monocouche située près de la surface • Une cellule qui comporte plusieurs noyaux partageant le même cytoplasme est appelée un syncytium • Cette organisation accélère énormément le développement précoce, car les cellules n'ont pas besoin de prendre le temps de traverser les étapes de la cytocinèse à chaque division

Cellularisation • Après ces divisions nucléaires rapides, des membranes sont créées autour de chaque noyau en une seule étape de cytocinèse coordonnée : la cellularisation • La membrane plasmique se prolonge vers l'intérieur et, avec l'aide d'un anneau d'actine et de myosine, se pince pour entourer chaque noyau • Figure 17 -51
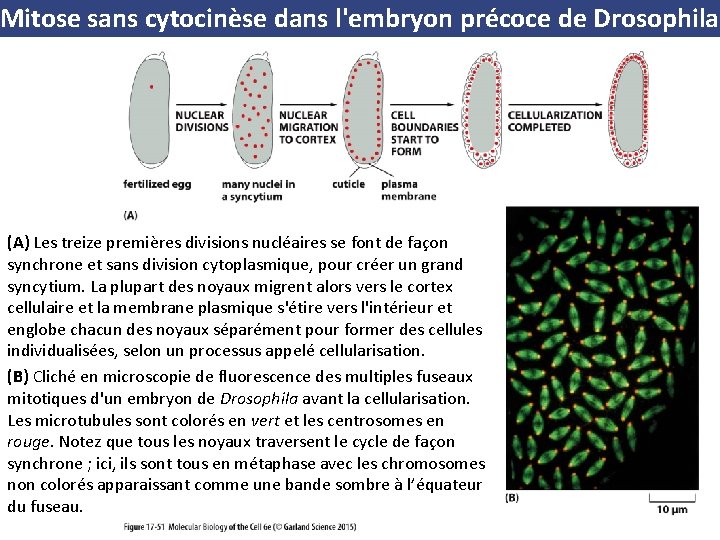
Mitose sans cytocinèse dans l'embryon précoce de Drosophila (A) Les treize premières divisions nucléaires se font de façon synchrone et sans division cytoplasmique, pour créer un grand syncytium. La plupart des noyaux migrent alors vers le cortex cellulaire et la membrane plasmique s'étire vers l'intérieur et englobe chacun des noyaux séparément pour former des cellules individualisées, selon un processus appelé cellularisation. (B) Cliché en microscopie de fluorescence des multiples fuseaux mitotiques d'un embryon de Drosophila avant la cellularisation. Les microtubules sont colorés en vert et les centrosomes en rouge. Notez que tous les noyaux traversent le cycle de façon synchrone ; ici, ils sont tous en métaphase avec les chromosomes non colorés apparaissant comme une bande sombre à l’équateur du fuseau.
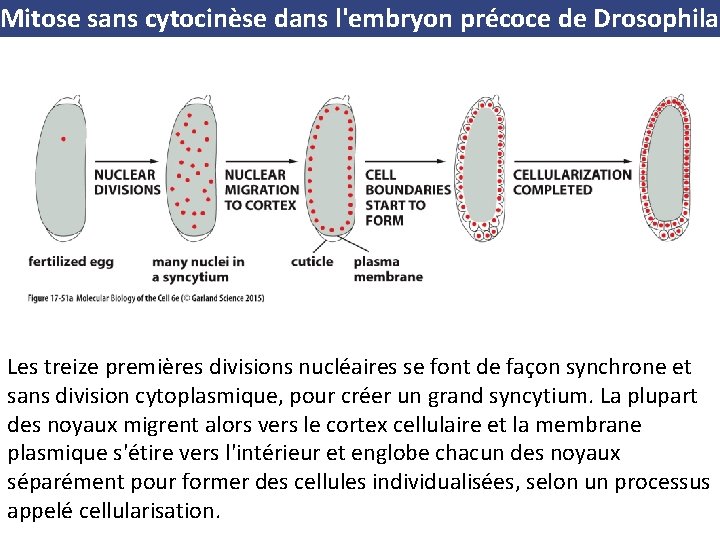
Mitose sans cytocinèse dans l'embryon précoce de Drosophila Les treize premières divisions nucléaires se font de façon synchrone et sans division cytoplasmique, pour créer un grand syncytium. La plupart des noyaux migrent alors vers le cortex cellulaire et la membrane plasmique s'étire vers l'intérieur et englobe chacun des noyaux séparément pour former des cellules individualisées, selon un processus appelé cellularisation.
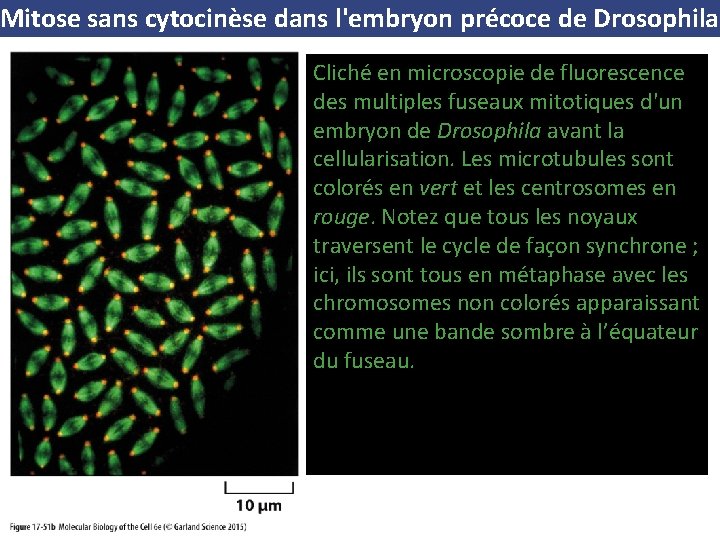
Mitose sans cytocinèse dans l'embryon précoce de Drosophila Cliché en microscopie de fluorescence des multiples fuseaux mitotiques d'un embryon de Drosophila avant la cellularisation. Les microtubules sont colorés en vert et les centrosomes en rouge. Notez que tous les noyaux traversent le cycle de façon synchrone ; ici, ils sont tous en métaphase avec les chromosomes non colorés apparaissant comme une bande sombre à l’équateur du fuseau.

CYTOKINESIS • Une division nucléaire sans cytocinèse existe aussi dans certains types de cellules de mammifères – Les mégacaryocytes, qui produisent les plaquettes sanguines, – certains hépatocytes – et certaines cellules musculaires cardiaques, par exemple, deviennent multinucléés de cette façon • Après la cytocinèse, la plupart des cellules entrent en phase G 1, dans laquelle les Cdk sont pour la plupart inactives

Comment cet état est-il obtenu à la fin de la phase M ?

V. La cytocinèse 1. L'actine et la myosine II de l'anneau contractile produisent la force nécessaire à la cytocinèse 2. L'activation locale de Rho. A déclenche l'assemblage et la contraction de l'anneau contractile 3. Les microtubules du fuseau mitotique déterminent le plan de division de la cellule animale 4. Le phragmoplaste guide la cytocinèse des végétaux supérieurs 5. Les organites entourés de membranes doivent être distribués aux cellules filles pendant la cytocinèse 6. Certaines cellules repositionnent leur fuseau pour se diviser asymétriquement 7. La mitose peut avoir lieu sans cytocinèse 8. La phase G 1 est un état stable d'inactivité des Cdk

2 mécanismes qui suppriment l'activité Cdk pendant G 1 i. Inactivation des Cdk ii. Augmentation de la production de CKI

i - Inactivation des Cdk

Conséquences de l'inactivation des Cdk • L'événement régulateur clé de la fin de la phase M est l'inactivation des Cdk, entraînée essentiellement par la destruction des cyclines APC/C dépendante • Comme nous l'avons déjà décrit supra, l'inactivation des Cdk à la fin de la phase M a plusieurs fonctions : – elle déclenche les événements de la fin de la mitose, – elle prépare la cytocinèse – et permet la synthèse des complexes pré-réplicatifs aux origines de réplication de l'ADN. – Elle fournit aussi un mécanisme permettant de remettre à jour le système de contrôle du cycle cellulaire vers un état d'inactivation de Cdk, alors que la cellule se prépare à entrer dans un nouveau cycle cellulaire • Dans la plupart des cellules, cet état d'inactivité des Cdk produit une phase transitoire G 1, durant laquelle la cellule grossit et contrôle son environnement avant de s'engager dans une nouvelle division cellulaire

Rappel • Chez les embryons précoces d'animaux, l'inactivation de M-Cdk à la fin de la mitose est due presque entièrement à l'action du complexe Cdc 20 -APC/C, discuté supra • Rappelons, cependant, que M-Cdk stimule l'activité de Cdc 20 APC/C • Ainsi, la destruction de la cycline M à la fin de la mitose conduit rapidement à l'inactivation de toute activité APC/C dans une cellule embryonnaire • Cette inactivation d'APC/C immédiatement après la mitose est surtout utile dans les cycles embryonnaires rapides, car elle permet à la cellule de commencer rapidement à accumuler de nouvelles molécules de cycline M pour le cycle suivant • Figure 17 -52 A
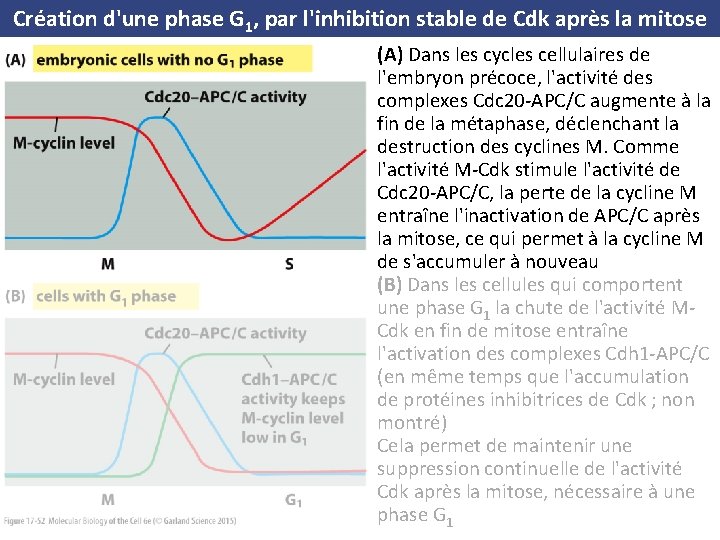
Création d'une phase G 1, par l'inhibition stable de Cdk après la mitose (A) Dans les cycles cellulaires de l'embryon précoce, l'activité des complexes Cdc 20 -APC/C augmente à la fin de la métaphase, déclenchant la destruction des cyclines M. Comme l'activité M-Cdk stimule l'activité de Cdc 20 -APC/C, la perte de la cycline M entraîne l'inactivation de APC/C après la mitose, ce qui permet à la cycline M de s'accumuler à nouveau (B) Dans les cellules qui comportent une phase G 1 la chute de l'activité MCdk en fin de mitose entraîne l'activation des complexes Cdh 1 -APC/C (en même temps que l'accumulation de protéines inhibitrices de Cdk ; non montré) Cela permet de maintenir une suppression continuelle de l'activité Cdk après la mitose, nécessaire à une phase G 1
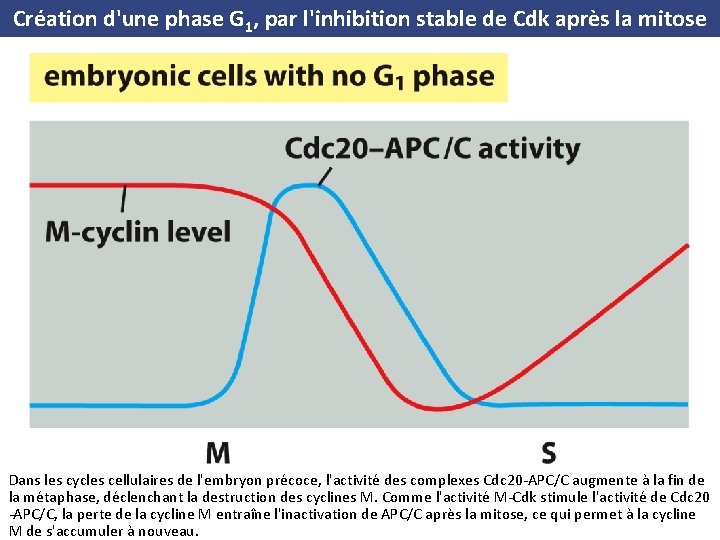
Création d'une phase G 1, par l'inhibition stable de Cdk après la mitose Dans les cycles cellulaires de l'embryon précoce, l'activité des complexes Cdc 20 -APC/C augmente à la fin de la métaphase, déclenchant la destruction des cyclines M. Comme l'activité M-Cdk stimule l'activité de Cdc 20 -APC/C, la perte de la cycline M entraîne l'inactivation de APC/C après la mitose, ce qui permet à la cycline M de s'accumuler à nouveau.
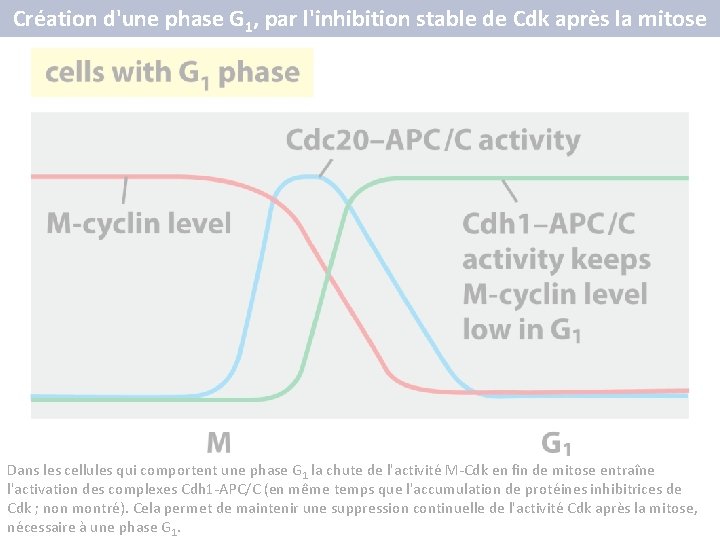
Création d'une phase G 1, par l'inhibition stable de Cdk après la mitose Dans les cellules qui comportent une phase G 1 la chute de l'activité M-Cdk en fin de mitose entraîne l'activation des complexes Cdh 1 -APC/C (en même temps que l'accumulation de protéines inhibitrices de Cdk ; non montré). Cela permet de maintenir une suppression continuelle de l'activité Cdk après la mitose, nécessaire à une phase G 1.

Cellules ayant un cycle cellulaire comprenant une phase G 1 • Cependant, l'accumulation rapide de cyclines immédiatement après la mitose n'est pas utile pour les cellules ayant un cycle cellulaire comprenant une phase G 1 • Ces cellules utilisent plusieurs mécanismes pour empêcher la réactivation de Cdk après la mitose

Un des mécanismes pour empêcher la réactivation de Cdk après la mitose • Emploie Cdh 1 • Autre protéine d'activation d'APC/C (déjà mentionnée plus haut) • Apparentée à Cdc 20 • voir Tableau suivant (rappel)

Récapitulatif des principales protéines régulatrices du cycle cellulaire (RAPPEL) Functions and comments Tableau 17 -2 Récapitulatif des Protein kinases and protein phosphatases that modify Cdks principales protéines régulatrices du cycle cellulaire General name Cdk-activating kinase (CAK) Phosphorylates an activating site in Cdks Wee 1 kinase Phosphorylates inhibitory sites in Cdks; primarily involved in suppressing Cdk 1 activity before mitosis Cdc 25 phosphatase Removes inhibitory phosphates from Cdks; three family members (Cdc 25 A, B, C) in mammals; primarily involved in controlling Cdkî activation at the onset of mitosis Cdk inhibitor proteins (CKIs) Sic 1 (budding yeast) Suppresses Cdk. I activity in G 1; phosphorylation by Cdk 1 at the end of G 1 triggers its destruction p 27 (mammals) Suppresses G 1/S-Cdk and S-Cdk activities in G 1; helps cells withdraw from cell cycle when they terminally differentiate; phosphorylation by Cdk 2 triggers its ubiquitylation by SCF p 21 (mammals) Suppresses G 1/S-Cdk and S-Cdk activities following DNA damage p 16 (mammals) Suppresses G 1 -Cdk activity in G 1; frequently inactivated in cancer Ubiquitin ligases and their activators APC/C Catalyzes ubiquitylation of regulatory proteins involved primarily in exit from mitosis, including securin and S-and M-cyclins; regulated by association with activating subunits Cdc 20 or Cdh 1 Cdc 20 APC/C-activating subunit in ail cells; triggers initial activation of APC/C at metaphase-ta-anaphase transition; stimulated by M-Cdk activity Cdh 1 APC/C-activating subunit that maintains APC/C activity after anaphase and throughout G 1; inhibited by Cdk activity SCF Catalyzes ubiquitylation of regulatory proteins involved in G 1 control, including some CKIs (Sic 1 in budding yeast, p 27 in mammals); phosphorylation of target protein usually required for this activity

Cdh 1 et Cdc 20 sur APC/C • Bien que toutes deux (Cdh 1 et Cdc 20) se lient et activent APC/C, Cdh 1 et Cdc 20 diffèrent l'une de l'autre par un point important – Alors que M-Cdk active le complexe Cdc 20 -APC/C, – elle inhibe le complexe Cdh 1 -APC/C par phosphorylation directe de Cdh 1 • Il résulte de ces liens que l'activité du complexe Cdh 1 -APC/C augmente en fin de mitose, après que le complexe Cdc 20 -APC/C a initié la destruction de la cycline M • La destruction de la cycline M continue donc après la mitose : bien que l'activité Cdc 20 -APC/C ait diminué, l'activité Cdh 1 APC/C est très élevée • Figure 17 -52 B

Création d'une phase G 1, par l'inhibition stable de Cdk après la mitose Dans les cellules qui comportent une phase G 1 la chute de l'activité M-Cdk en fin de mitose entraîne l'activation des complexes Cdh 1 -APC/C (en même temps que l'accumulation de protéines inhibitrices de Cdk ; non montré). Cela permet de maintenir une suppression continuelle de l'activité Cdk après la mitose, nécessaire à une phase G 1.

ii - Augmentation de la production de CKI

ii - Augmentation de la production de CKI • Second mécanisme, qui supprime l'activité Cdk pendant G 1 • Dépend de l'augmentation de la production de CKI, la protéine inhibitrice de Cdk, déjà vue • Les cellules de levure bourgeonnante, dans lesquelles ce mécanisme est très bien compris, contiennent une protéine inhibitrice de type CKI appelée Sic 1, qui se lie et active M-Cdk en fin de mitose et en G 1 • voir Tableau 17 -2
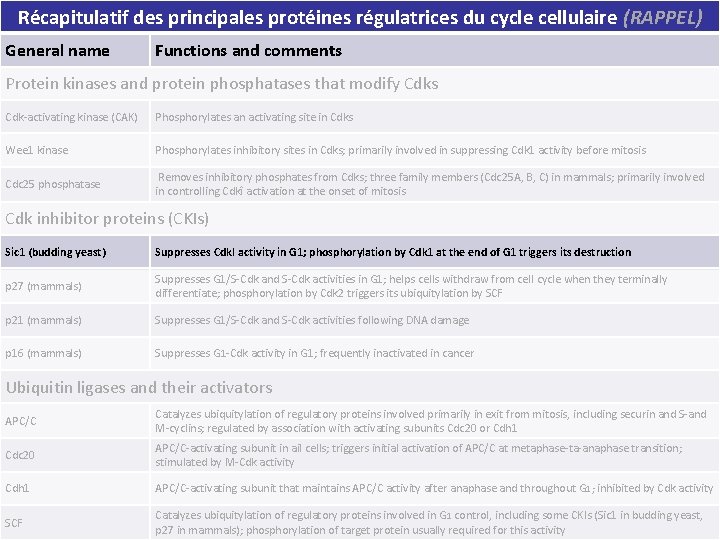
Récapitulatif des principales protéines régulatrices du cycle cellulaire (RAPPEL) Functions and comments Tableau 17 -2 Récapitulatif des Protein kinases and protein phosphatases that modify Cdks principales protéines régulatrices du cycle cellulaire General name Cdk-activating kinase (CAK) Phosphorylates an activating site in Cdks Wee 1 kinase Phosphorylates inhibitory sites in Cdks; primarily involved in suppressing Cdk 1 activity before mitosis Cdc 25 phosphatase Removes inhibitory phosphates from Cdks; three family members (Cdc 25 A, B, C) in mammals; primarily involved in controlling Cdkî activation at the onset of mitosis Cdk inhibitor proteins (CKIs) Sic 1 (budding yeast) Suppresses Cdk. I activity in G 1; phosphorylation by Cdk 1 at the end of G 1 triggers its destruction p 27 (mammals) Suppresses G 1/S-Cdk and S-Cdk activities in G 1; helps cells withdraw from cell cycle when they terminally differentiate; phosphorylation by Cdk 2 triggers its ubiquitylation by SCF p 21 (mammals) Suppresses G 1/S-Cdk and S-Cdk activities following DNA damage p 16 (mammals) Suppresses G 1 -Cdk activity in G 1; frequently inactivated in cancer Ubiquitin ligases and their activators APC/C Catalyzes ubiquitylation of regulatory proteins involved primarily in exit from mitosis, including securin and S-and M-cyclins; regulated by association with activating subunits Cdc 20 or Cdh 1 Cdc 20 APC/C-activating subunit in ail cells; triggers initial activation of APC/C at metaphase-ta-anaphase transition; stimulated by M-Cdk activity Cdh 1 APC/C-activating subunit that maintains APC/C activity after anaphase and throughout G 1; inhibited by Cdk activity SCF Catalyzes ubiquitylation of regulatory proteins involved in G 1 control, including some CKIs (Sic 1 in budding yeast, p 27 in mammals); phosphorylation of target protein usually required for this activity

Cdh 1 et Sic 1 • Comme Cdh 1, Sic 1 est inhibée par M-Cdk, qui phosphoryle Sic 1 au cours de la mitose et déclenche alors son ubiquitinylation par SCF – Ainsi, Sic 1 et M-Cdk, – comme Cdh 1 et M-Cdk s'inhibent l'une l'autre • Le résultat est que le déclin d'activité de M-Cdk qui a lieu en fin de mitose cause l'accumulation de la protéine Sic 1, et cette CKI aide à garder l'activité de M-Cdk basse après la mitose • Une protéine inhibitrice de type CKI appelée p 27 pourrait avoir les mêmes fonctions dans les cellules animales • voir Figure 17 -14
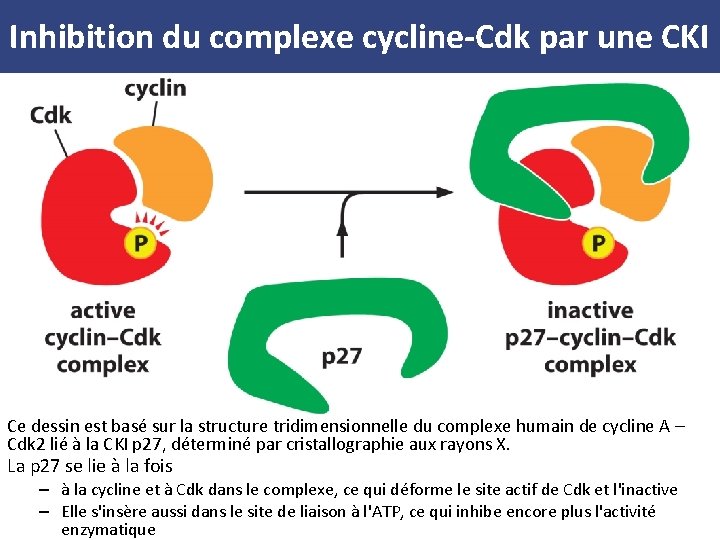
Inhibition du complexe cycline-Cdk par une CKI Ce dessin est basé sur la structure tridimensionnelle du complexe humain de cycline A – Cdk 2 lié à la CKI p 27, déterminé par cristallographie aux rayons X. La p 27 se lie à la fois – à la cycline et à Cdk dans le complexe, ce qui déforme le site actif de Cdk et l'inactive – Elle s'insère aussi dans le site de liaison à l'ATP, ce qui inhibe encore plus l'activité enzymatique

Sortie de mitose • Dans la plupart des cellules, la diminution de transcription des gènes des cyclines M inactive aussi M-Cdk en fin de mitose • Chez la levure bourgeonnante, par exemple, M-Cdk déclenche l'expression de ces gènes, avec pour résultat une boucle de rétrocontrôle positif • Cette boucle s'arrête lorsque les cellules sortent de la mitose : l'inactivation de M-Cdk par Cdh 1 et Sic 1 conduit à une diminution de la transcription du gène de la cycline M et donc à une baisse de la synthèse de cycline M • Les protéines régulatrices de gènes qui déclenchent l'expression de G 1/S et des cyclines S sont aussi inhibées au cours de G 1

Suppression de toute activité Cdk – Ainsi, l'activation de Cdh 1 -APC/C, – l'accumulation de CKI – et la diminution de l'expression du gène de la cycline • agissent ensemble pour assurer que le début de la phase G 1 soit un temps où toute activité Cdk est supprimée • Comme dans beaucoup d'autres aspects du contrôle du cycle cellulaire, l'utilisation de multiples mécanismes régulateurs rend le système suppresseur robuste, opérant avec une efficacité raisonnable même si l'un des mécanismes vient à lâcher

Alors, comment la cellule échappe-t-elle à cet état G 1 stable pour initier un nouveau cycle cellulaire ? • La réponse est que l'activité G 1/S-Cdk, qui augmente en fin de G 1 libère tous les mécanismes de freinage qui supprimaient l'activité Cdk • Cf. VII

Résumé • Après que la mitose a achevé la formation d'une paire de noyaux fils, la cytocinèse termine le cycle en divisant la cellule elle-même • La cytocinèse dépend d'un anneau de filaments d'actine et de myosine qui se contracte en fin de mitose, sur un site qui se trouve à mi chemin entre les chromosomes séparés • Dans les cellules animales, le positionnement de l'anneau contractile est déterminé par des signaux émanant des microtubules du fuseau d'anaphase • La déphosphorylation des cibles de Cdk, qui résulte de l'inactivation de Cdk pendant l'anaphase, déclenche la cytocinèse au bon moment après l'anaphase • Après la cytocinèse, la cellule entre en phase G 1 stable, où l'activité Cdk est basse et où elle attend des signaux pour un nouveau cycle cellulaire

Le cycle cellulaire I. Vue d'ensemble du cycle cellulaire II. Le système de contrôle du cycle cellulaire III. La phase S IV. La mitose V. La cytocinèse VI. Méiose VII. Contrôle de la division et de la croissance cellulaire

Fin
- Slides: 106