Alberts Johnson Lewis Morgan Raff Roberts Walter Biologie

Alberts • Johnson • Lewis • Morgan • Raff • Roberts • Walter Biologie Moléculaire de la cellule Sixième Édition Chapitre 16 Le cytosquelette Copyright © Garland Science 2015

LE CYTOSQUELETTE I. Fonction et origine du cytosquelette II. Actine et protéines de liaison à l’actine III. Myosine et actine IV. Microtubules V. Filaments intermédiaires et septine VI. Polarisation cellulaire et migration cellulaire

PLAN I. III. IV. V. VI. Fonction et origine du cytosquelette Actine et protéines de liaison à l’actine Myosine et actine Microtubules Filaments intermédiaires et septine Polarisation cellulaire et migration cellulaire 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Introduction • Un des défis communs à tous les domaines de la biologie cellulaire est de comprendre comment se combinent les fonctions des nombreuses composantes moléculaires indi viduelles pour produire des comportements cellulaires complexes • La migration cellulaire que nous allons décrire dans cette section finale repose sur le déploiement coordonné des composants et processus que nous avons explorés dans les cinq premières parties de ce chapitre : – l'assemblage et le désassemblage dyna miques des polymères du cytosquelette, – la régulation et la modification de leur struc ture par les protéines qui leur sont associées, – et l'action des protéines motrices qui se déplacent sur eux ou bien exercent une tension opposée. • Comment toutes ces activités sont elles coordonnées pour définir sa polarité et lui permettre de migrer ?

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Importance de la migration des cellules • Beaucoup de cellules se déplacent en rampant sur des surfaces plutôt qu'en utilisant des cils ou des flagelles pour nager • Les amibes prédatrices rampent continuellement à la recherche de nourriture et on peut facilement les observer dans une goutte d'eau de mare, lorsqu'elles attaquent et dévorent de plus petits ciliés et flagellés • Movie 1. 4 • Chez les animaux, presque toute la locomotion des cellules se produit en rampant, si on excepte les spermatozoïdes qui nagent • Pendant l'embryogenèse, la structure d'un animal se crée par la migration de chaque cellule vers sa localisation cible spécifique, et par les mouvements coordonnés de feuillets épithéliaux entiers • Chez les vertébrés, les cellules de la crête neurale sont remarquables par leur migration sur de longues distances, depuis leur site d'origine dans le tube neural jusqu'à divers sites répartis dans tout l'embryon • Movie 21. 5 • Ces cellules ont destins variés et deviennent des cellules pigmentaires cutanées, des neurones sensoriels ou sympathiques, des cellules de la glie et diverses structures de la face • Cette possibilité de migrer sur de longues distances est fondamentale pour l'édification de la totalité du système nerveux : c'est de cette façon que les cônes de croissance, riches en actine, à l'extrémité conductrice des axones en développement, se déplacent vers leurs cibles synaptiques finales, guidés par l'association, tout le long du chemin, de signaux solubles et de signaux fixés sur les surfaces cellulaires et

Exemples de l’importance de la migration des cellules • • • Les animaux adultes aussi grouillent de cellules qui rampent Les macrophages et les neutrophiles rampent vers les sites d'infection et engloutissent les envahisseurs étrangers, ce qui constitue une partie fondamentale de la réponse immunitaire innée Les ostéoclastes forment des tunnels dans les os, et créent des canaux qui seront remplis par les ostéoblastes qui les suivent, selon un processus continu de remodelage et de renouvellement des os De même, les fibroblastes peuvent ramper à travers les tissus conjonctifs, les remodeler si nécessaire, et les aider à reconstruire les structures endommagées au niveau des sites de lésions Selon une procession ordonnée, les cellules de l'épithélium intestinal remontent le long des côtés des villosités intestinales, jusqu'à l'extrémité des villosités, et remplacent les cellules absorbantes perdues à ce niveau Malheureusement, cette migration des cellules joue aussi un rôle dans de nombreux cancers, lorsque les cellules d'une tumeur primaire envahissent les tissus voisins et rampent vers les vaisseaux sanguins ou les vaisseaux lymphatiques pour se transporter vers d'autres sites de l'organisme et former des métastases

Conditions de la migration des cellules • La migration des cellules est un processus complexe qui dépend du cortex, riche en actine, situé sous la membrane plasmique • Elle implique trois activités distinctes : – la protrusion, au cours de laquelle les structures riches en actine sont poussées à l'avant de la cellule – la fixation, au cours de laquelle le cytosquelette d'actine se connecte, à travers la membrane plasmique, au support – la traction, au cours de laquelle la masse restante du cytoplasme est tirée vers l'avant
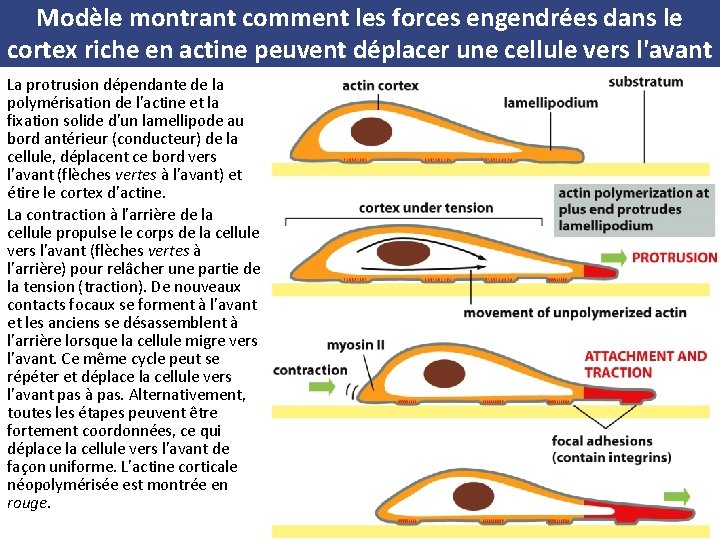
Modèle montrant comment les forces engendrées dans le cortex riche en actine peuvent déplacer une cellule vers l'avant La protrusion dépendante de la polymérisation de l'actine et la fixation solide d'un lamellipode au bord antérieur (conducteur) de la cellule, déplacent ce bord vers l'avant (flèches vertes à l'avant) et étire le cortex d'actine. La contraction à l'arrière de la cellule propulse le corps de la cellule vers l'avant (flèches vertes à l'arrière) pour relâcher une partie de la tension (traction). De nouveaux contacts focaux se forment à l'avant et les anciens se désassemblent à l'arrière lorsque la cellule migre vers l'avant. Ce même cycle peut se répéter et déplace la cellule vers l'avant pas à pas. Alternativement, toutes les étapes peuvent être fortement coordonnées, ce qui déplace la cellule vers l'avant de façon uniforme. L'actine corticale néopolymérisée est montrée en rouge.

Conséquences sur l’aspect de la migration • Dans certaines cellules rampantes, comme les kératocytes de l'épiderme des poissons, ces activités se font en même temps, et les cellules semblent glisser uniformément vers l'avant sans changer de forme • Dans d'autres cellules, comme les fibroblastes, ces activités sont plus indépendantes et la locomotion apparaît saccadée et irrégulière

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Protrusion • La première étape de la locomotion, la protrusion d'un bord conducteur, semble reposer principalement sur des forces engendrées par la polymérisation de l'actine qui repousse la membrane plasmique vers l'extérieur • Les différents types de cellules produisent des types différents de structures saillantes, parmi lesquelles filopodes (appelés aussi micropointes), les lamellipodes • Elles sont toutes remplies d'un cœur dense de filaments d'actine qui exclut les organites entourés d'une membrane • Ces trois structures diffèrent principalement dans le mode d'organisation de l'actine par la présence de différentes protéines de liaison croisée à l'actine
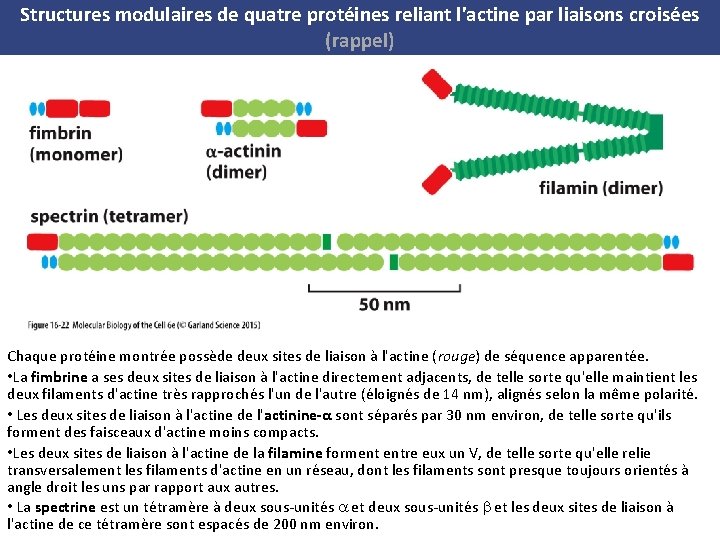
Structures modulaires de quatre protéines reliant l'actine par liaisons croisées (rappel) Chaque protéine montrée possède deux sites de liaison à l'actine (rouge) de séquence apparentée. • La fimbrine a ses deux sites de liaison à l'actine directement adjacents, de telle sorte qu'elle maintient les deux filaments d'actine très rapprochés l'un de l'autre (éloignés de 14 nm), alignés selon la même polarité. • Les deux sites de liaison à l'actine de l'actinine α sont séparés par 30 nm environ, de telle sorte qu'ils forment des faisceaux d'actine moins compacts. • Les deux sites de liaison à l'actine de la filamine forment entre eux un V, de telle sorte qu'elle relie transversalement les filaments d'actine en un réseau, dont les filaments sont presque toujours orientés à angle droit les uns par rapport aux autres. • La spectrine est un tétramère à deux sous unités et les deux sites de liaison à l'actine de ce tétramère sont espacés de 200 nm environ.

Filopodes • • Cônes de croissance des neurones qui se déplacent Certains types de fibroblastes Essentiellement unidimensionnels Contiennent un cœur de longs filaments d'actine en faisceau qui rappellent ceux des microvillosités, mais sont • Plus longs • Plus fins • Plus dynamiques

Lamellipodes • Cellules épithéliales • Fibroblastes • Certains neurones • Sont des structures bidimensionnelles, en feuillets • Contiennent un réseau orthogonal de liaisons croisées de filaments d'actine dont la plupart sont dans un plan parallèle au support solide

Invadopodes et structures apparentées Connus sous le nom de podosomes 3 e type de protrusion riche en actine En 3 dimensions Importants pour la traversée des barrières tissulaires par les cellules (envahissement de tissus environnants par des cellules métastatiques de cancer) • Contiennent beaucoup de composants régulateurs d’actine comme ceux des filopodes et des lamellipodes • Dégradent la matrice extracellulaire qui réclame la libération de vésicules contenant les protéases de dégradation de la matrice • •

The 'ins' and 'outs' of podosomes and invadopodia: characteristics, formation and function Danielle A. Murphy & Sara A. Courtneidge Nature Reviews Molecular Cell Biology 12, 413 426 (July 2011)
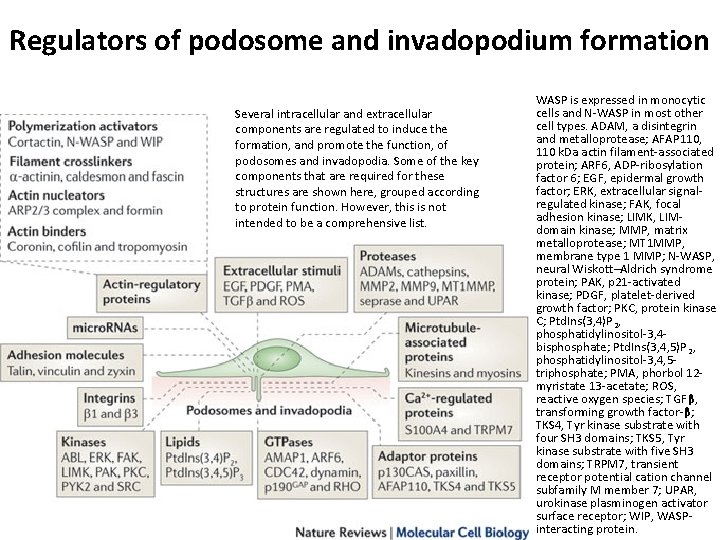
Regulators of podosome and invadopodium formation Several intracellular and extracellular components are regulated to induce the formation, and promote the function, of podosomes and invadopodia. Some of the key components that are required for these structures are shown here, grouped according to protein function. However, this is not intended to be a comprehensive list. WASP is expressed in monocytic cells and N WASP in most other cell types. ADAM, a disintegrin and metalloprotease; AFAP 110, 110 k. Da actin filament associated protein; ARF 6, ADP ribosylation factor 6; EGF, epidermal growth factor; ERK, extracellular signal regulated kinase; FAK, focal adhesion kinase; LIMK, LIM domain kinase; MMP, matrix metalloprotease; MT 1 MMP, membrane type 1 MMP; N WASP, neural Wiskott–Aldrich syndrome protein; PAK, p 21 activated kinase; PDGF, platelet derived growth factor; PKC, protein kinase C; Ptd. Ins(3, 4)P 2, phosphatidylinositol 3, 4 bisphosphate; Ptd. Ins(3, 4, 5)P 2, phosphatidylinositol 3, 4, 5 triphosphate; PMA, phorbol 12 myristate 13 acetate; ROS, reactive oxygen species; TGFβ, transforming growth factor β; TKS 4, Tyr kinase substrate with four SH 3 domains; TKS 5, Tyr kinase substrate with five SH 3 domains; TRPM 7, transient receptor potential cation channel subfamily M member 7; UPAR, urokinase plasminogen activator surface receptor; WIP, WASP interacting protein.
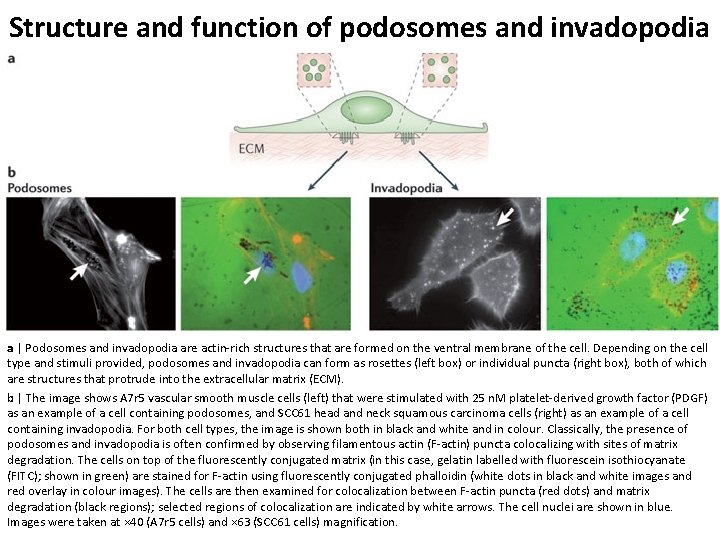
Structure and function of podosomes and invadopodia a | Podosomes and invadopodia are actin rich structures that are formed on the ventral membrane of the cell. Depending on the cell type and stimuli provided, podosomes and invadopodia can form as rosettes (left box) or individual puncta (right box), both of which are structures that protrude into the extracellular matrix (ECM). b | The image shows A 7 r 5 vascular smooth muscle cells (left) that were stimulated with 25 n. M platelet derived growth factor (PDGF) as an example of a cell containing podosomes, and SCC 61 head and neck squamous carcinoma cells (right) as an example of a cell containing invadopodia. For both cell types, the image is shown both in black and white and in colour. Classically, the presence of podosomes and invadopodia is often confirmed by observing filamentous actin (F actin) puncta colocalizing with sites of matrix degradation. The cells on top of the fluorescently conjugated matrix (in this case, gelatin labelled with fluorescein isothiocyanate (FITC); shown in green) are stained for F actin using fluorescently conjugated phalloidin (white dots in black and white images and red overlay in colour images). The cells are then examined for colocalization between F actin puncta (red dots) and matrix degradation (black regions); selected regions of colocalization are indicated by white arrows. The cell nuclei are shown in blue. Images were taken at × 40 (A 7 r 5 cells) and × 63 (SCC 61 cells) magnification.
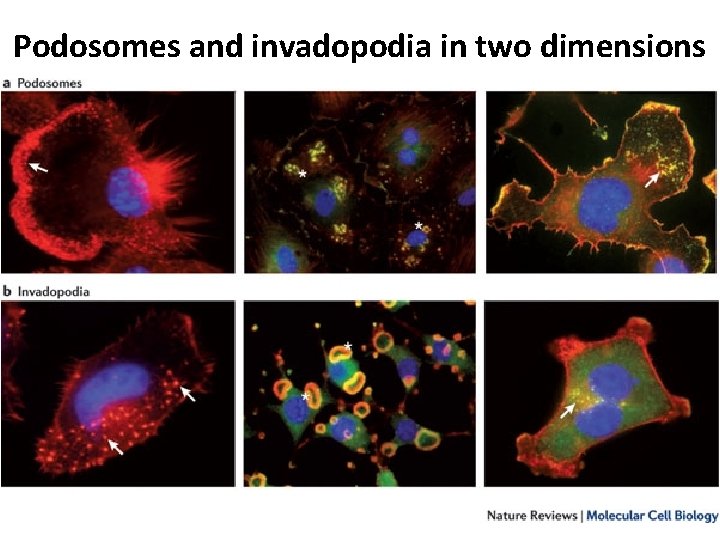
Podosomes and invadopodia in two dimensions
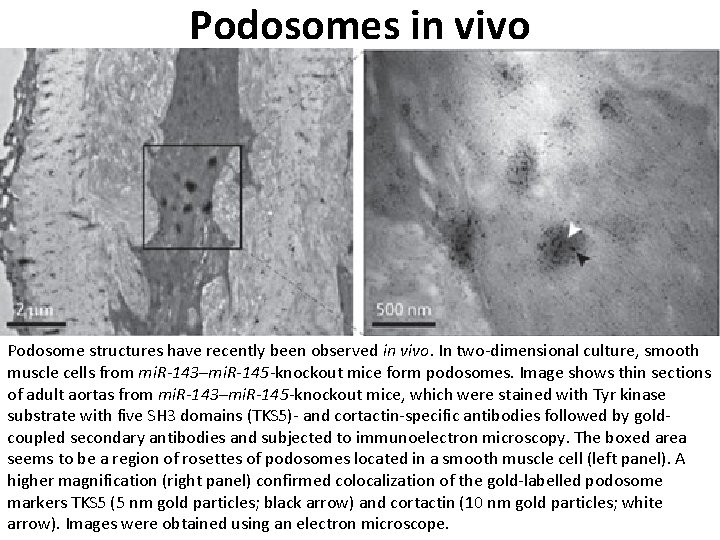
Podosomes in vivo Podosome structures have recently been observed in vivo. In two dimensional culture, smooth muscle cells from mi. R-143–mi. R-145 knockout mice form podosomes. Image shows thin sections of adult aortas from mi. R-143–mi. R-145 knockout mice, which were stained with Tyr kinase substrate with five SH 3 domains (TKS 5) and cortactin specific antibodies followed by gold coupled secondary antibodies and subjected to immunoelectron microscopy. The boxed area seems to be a region of rosettes of podosomes located in a smooth muscle cell (left panel). A higher magnification (right panel) confirmed colocalization of the gold labelled podosome markers TKS 5 (5 nm gold particles; black arrow) and cortactin (10 nm gold particles; white arrow). Images were obtained using an electron microscope.
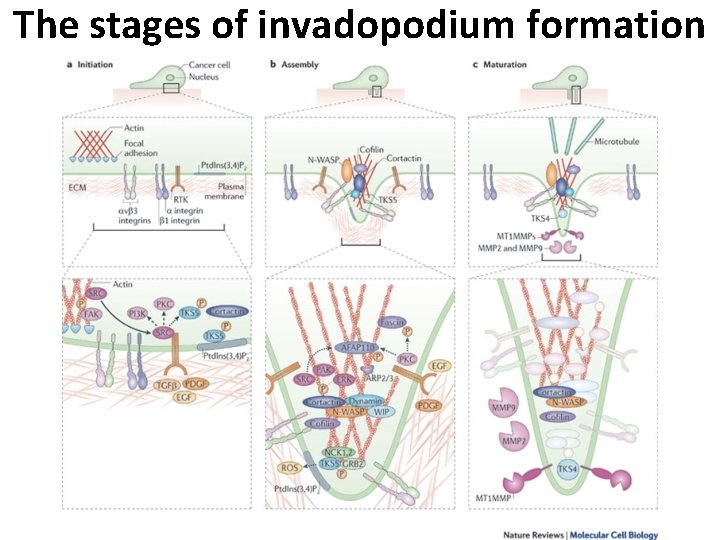
The stages of invadopodium formation
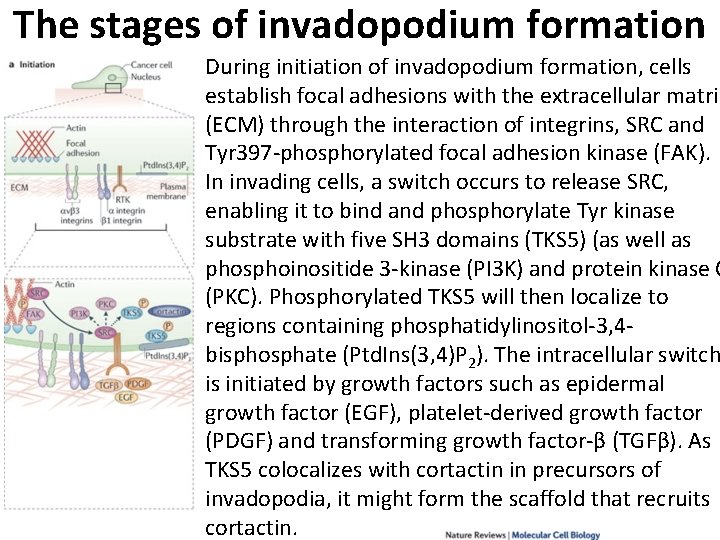
The stages of invadopodium formation During initiation of invadopodium formation, cells establish focal adhesions with the extracellular matrix (ECM) through the interaction of integrins, SRC and Tyr 397 phosphorylated focal adhesion kinase (FAK). In invading cells, a switch occurs to release SRC, enabling it to bind and phosphorylate Tyr kinase substrate with five SH 3 domains (TKS 5) (as well as phosphoinositide 3 kinase (PI 3 K) and protein kinase C (PKC). Phosphorylated TKS 5 will then localize to regions containing phosphatidylinositol 3, 4 bisphosphate (Ptd. Ins(3, 4)P 2). The intracellular switch is initiated by growth factors such as epidermal growth factor (EGF), platelet derived growth factor (PDGF) and transforming growth factor β (TGFβ). As TKS 5 colocalizes with cortactin in precursors of invadopodia, it might form the scaffold that recruits cortactin.
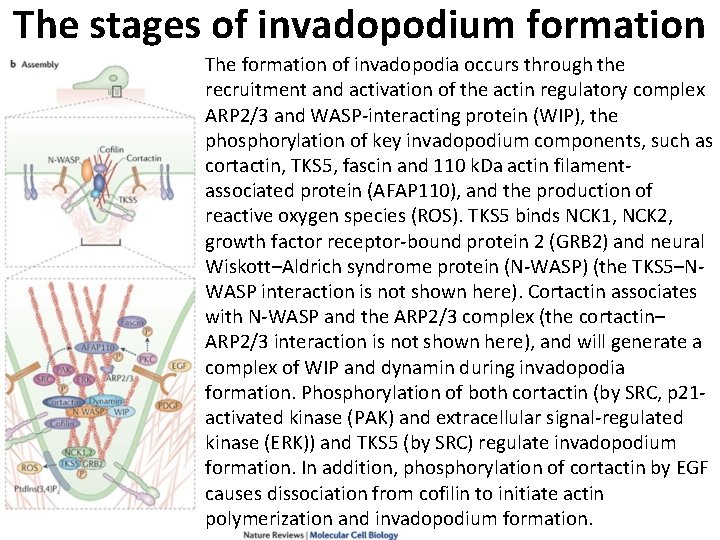
The stages of invadopodium formation The formation of invadopodia occurs through the recruitment and activation of the actin regulatory complex ARP 2/3 and WASP interacting protein (WIP), the phosphorylation of key invadopodium components, such as cortactin, TKS 5, fascin and 110 k. Da actin filament associated protein (AFAP 110), and the production of reactive oxygen species (ROS). TKS 5 binds NCK 1, NCK 2, growth factor receptor bound protein 2 (GRB 2) and neural Wiskott–Aldrich syndrome protein (N WASP) (the TKS 5–N WASP interaction is not shown here). Cortactin associates with N WASP and the ARP 2/3 complex (the cortactin– ARP 2/3 interaction is not shown here), and will generate a complex of WIP and dynamin during invadopodia formation. Phosphorylation of both cortactin (by SRC, p 21 activated kinase (PAK) and extracellular signal regulated kinase (ERK)) and TKS 5 (by SRC) regulate invadopodium formation. In addition, phosphorylation of cortactin by EGF causes dissociation from cofilin to initiate actin polymerization and invadopodium formation.
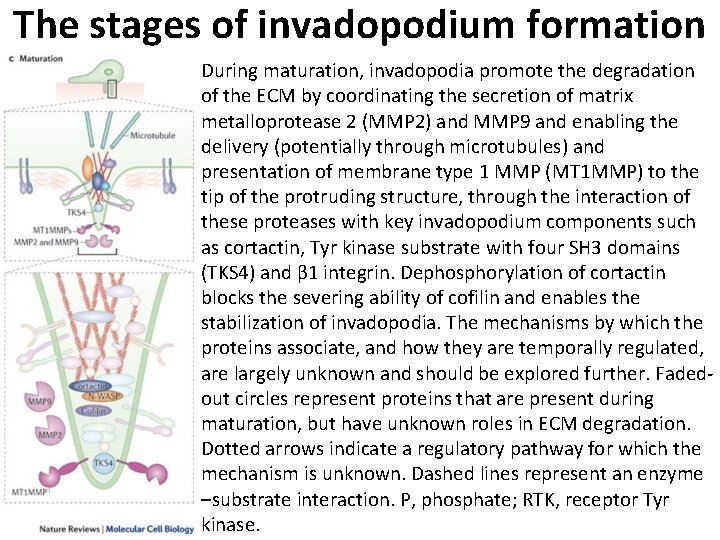
The stages of invadopodium formation During maturation, invadopodia promote the degradation of the ECM by coordinating the secretion of matrix metalloprotease 2 (MMP 2) and MMP 9 and enabling the delivery (potentially through microtubules) and presentation of membrane type 1 MMP (MT 1 MMP) to the tip of the protruding structure, through the interaction of these proteases with key invadopodium components such as cortactin, Tyr kinase substrate with four SH 3 domains (TKS 4) and β 1 integrin. Dephosphorylation of cortactin blocks the severing ability of cofilin and enables the stabilization of invadopodia. The mechanisms by which the proteins associate, and how they are temporally regulated, are largely unknown and should be explored further. Faded out circles represent proteins that are present during maturation, but have unknown roles in ECM degradation. Dotted arrows indicate a regulatory pathway for which the mechanism is unknown. Dashed lines represent an enzyme –substrate interaction. P, phosphate; RTK, receptor Tyr kinase.

The 'ins' and 'outs' of podosomes and invadopodia: characteristics, formation and function Podosomes and invadopodia are actin based dynamic protrusions of the plasma membrane. They act as sites of attachment to — and degradation of — the extracellular matrix. These structures contain actin regulators such as cortactin and neural Wiskott–Aldrich syndrome protein (N WASP), adaptor proteins such as Tyr kinase substrate with four SH 3 domains (TKS 4) and Tyr kinase substrate with five SH 3 domains (TKS 5), and several pericellular proteases. Podosomes are found in vascular smooth muscle and endothelial cells, as well as in cells derived from monocyte lineages. Their presence correlates with migratory ability. Invadopodia are found in invasive human cancer cells. In two dimensional culture, their presence correlates with invasive behaviour. However, in three dimensional culture and in vivo, invadopodium associated proteins are also required for cell growth. Podosome associated proteins have been implicated in human developmental and immune disorders, and dysregulation of podosome formation is associated with atherosclerosis. Small molecule regulation of podosomes and invadopodia might represent a new therapeutic strategy to treat several diseases.

Bourgeonnement membranaire • Forme distincte de protrusion membranaire • Souvent observée in vivo • Ou quand les cellules sont cultivées sur un support de matrice extra cellulaire • Les bourgeons se forment quand la membrane se détache localement du cortex d’actine sous jacent et que le flux cytoplasmique pousse alors la membrane vers l’extérieur
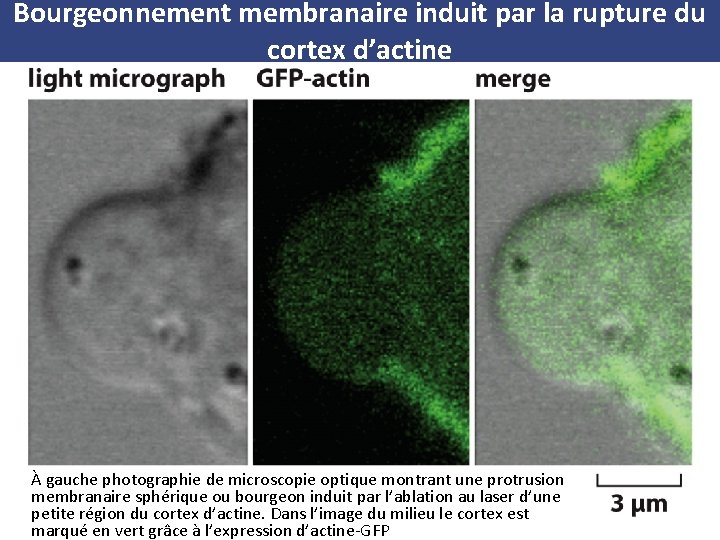
Bourgeonnement membranaire induit par la rupture du cortex d’actine À gauche photographie de microscopie optique montrant une protrusion membranaire sphérique ou bourgeon induit par l’ablation au laser d’une petite région du cortex d’actine. Dans l’image du milieu le cortex est marqué en vert grâce à l’expression d’actine GFP

Bourgeonnement membranaire • Le bourgeonnement membranaire dépend aussi de la pression hydrostatique générée par la contraction d’assemblage d’actine et de myosine dans la cellule • Une fois le bourgeonnement formé, les filaments d’actine se réassemblent sur la membrane du bourgeon pour former un nouveau cortex d’actine • Le recrutement de la myosine II et la contraction actine myosine rétractent la membrane du bourgeon • Sinon la formation de nouveaux bourgeons à partir d’anciens permet la migration de la cellule

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Kératocytes • Ils ont été particulièrement bien étudiés dans les cellules épithéliales de l'épiderme des poissons et des grenouilles • On les nomme ainsi à cause de l'abondance des filaments de kératine qu'ils contiennent • Ces cellules recouvrent normalement l'animal en formant un feuillet épithélial et sont spécialisées dans la fermeture très rapide des blessures, se déplaçant à des vitesses pouvant atteindre 30 µm/min • Lorsqu'ils sont dissociés et mis en culture, les kératocytes prennent une forme par ticulière, composée d'un très gros lamellipode traînant un petit corps cellulaire qui n'est pas fixé sur le support
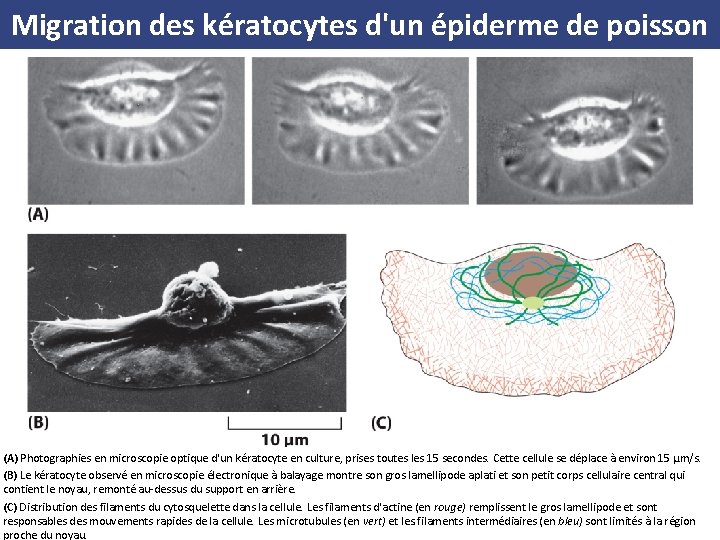
Migration des kératocytes d'un épiderme de poisson (A) Photographies en microscopie optique d'un kératocyte en culture, prises toutes les 15 secondes. Cette cellule se déplace à environ 15 µm/s. (B) Le kératocyte observé en microscopie électronique à balayage montre son gros lamellipode aplati et son petit corps cellulaire central qui contient le noyau, remonté au dessus du support en arrière. (C) Distribution des filaments du cytosquelette dans la cellule. Les filaments d'actine (en rouge) remplissent le gros lamellipode et sont responsables des mouvements rapides de la cellule. Les microtubules (en vert) et les. filaments intermédiaires (en bleu) sont limités à la région proche du noyau.
Migration des kératocytes d'un épiderme de poisson Photographies en microscopie optique d'un kératocyte en culture, prises toutes les 15 secondes. Cette cellule se déplace à environ 15 µm/s
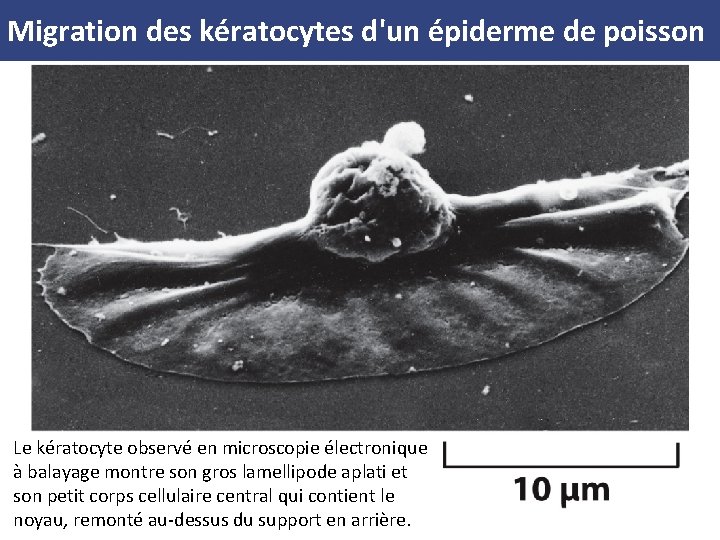
Migration des kératocytes d'un épiderme de poisson Le kératocyte observé en microscopie électronique à balayage montre son gros lamellipode aplati et son petit corps cellulaire central qui contient le noyau, remonté au dessus du support en arrière.
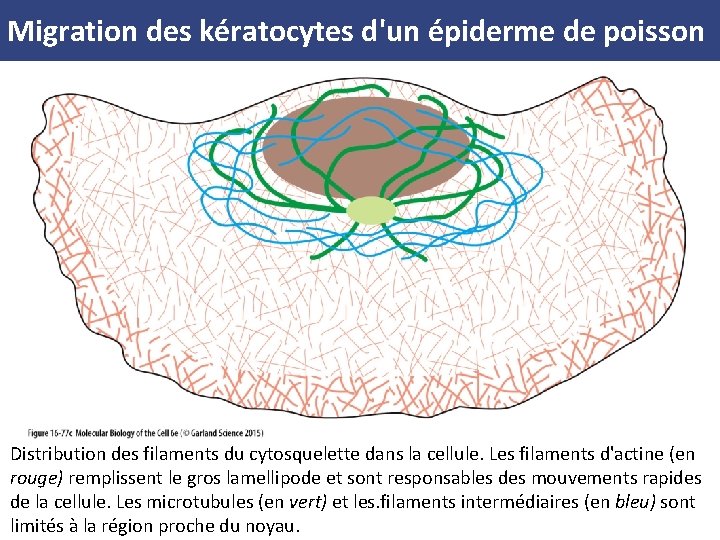
Migration des kératocytes d'un épiderme de poisson Distribution des filaments du cytosquelette dans la cellule. Les filaments d'actine (en rouge) remplissent le gros lamellipode et sont responsables des mouvements rapides de la cellule. Les microtubules (en vert) et les. filaments intermédiaires (en bleu) sont limités à la région proche du noyau.

Lamellipode • Des fragments de ce lamellipode peuvent être détachés avec une micropipette • Bien que ces fragments soient généralement dépourvus de microtubules et d'organites entourés d'une membrane, ils poursuivent normalement leur migration, et ressemblent à de minuscules kératocytes

Lamellipode • On peut étudier le comportement dynamique des filaments d'actine dans les lamellipodes kératocytes en marquant une petite région d'actine, et en suivant son destin • On constate que, tandis que le lamellipode rampe vers l'avant, les filaments d'actine restent stationnaires par rapport au support • Les filaments d'actine du réseau sont surtout orientés avec leurs extrémités plus vers l'avant • Les extrémités moins sont souvent attachées sur les côtés d'autres filaments d'actine par des complexes ARP 2/3 • ce qui facilite la formation du réseau bidimensionnel • Figure 16 78
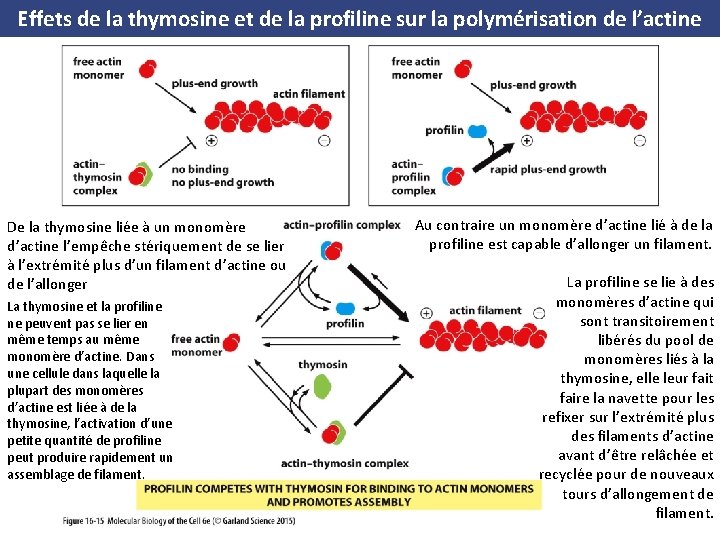
Effets de la thymosine et de la profiline sur la polymérisation de l’actine De la thymosine liée à un monomère d’actine l’empêche stériquement de se lier à l’extrémité plus d’un filament d’actine ou de l’allonger La thymosine et la profiline ne peuvent pas se lier en même temps au même monomère d’actine. Dans une cellule dans laquelle la plupart des monomères d’actine est liée à de la thymosine, l’activation d’une petite quantité de profiline peut produire rapidement un assemblage de filament. Au contraire un monomère d’actine lié à de la profiline est capable d’allonger un filament. La profiline se lie à des monomères d’actine qui sont transitoirement libérés du pool de monomères liés à la thymosine, elle leur fait faire la navette pour les refixer sur l’extrémité plus des filaments d’actine avant d’être relâchée et recyclée pour de nouveaux tours d’allongement de filament.

Nucléation des filaments d'actine et formation d'un réseau par le complexe ARP dans les lamellipodes (A) Kératocyte avec des filaments d'actine marqués en rouge par la phalloïdine fluorescente et un complexe ARP marqué en vert par un anticorps dirigé contre une de ses composantes protéiques. Les régions où les deux se chevauchent apparaissent en jaune. Le complexe ARP est hautement concentré à l'avant du lamellipode, où la nucléation d'actine est la plus active. (B) Photographie en microscopie électronique d'une réplique ombrée au platine du bord antérieur d'un kératocyte, montrant le réseau dense de filament d'actine. Les marques délimitent des zones agrandies en C. (C) Agrandissement des régions marquées du réseau d'actine sur le bord avant, montrées en B. De nombreux filaments ramifiés peuvent être observés avec l'angle de 70° caractéristique qui se forme lorsque le complexe ARP nuclée un nouveau filament d'actine, sur le côté d'un filament d'actine préexistant
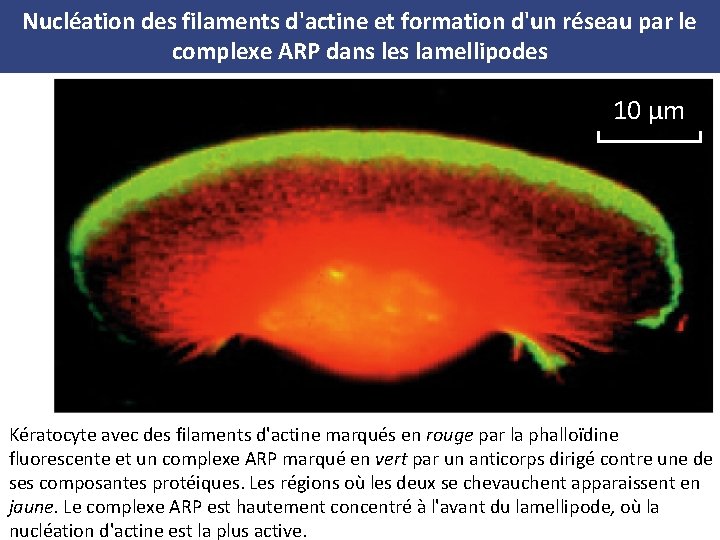
Nucléation des filaments d'actine et formation d'un réseau par le complexe ARP dans les lamellipodes 10 µm Kératocyte avec des filaments d'actine marqués en rouge par la phalloïdine fluorescente et un complexe ARP marqué en vert par un anticorps dirigé contre une de ses composantes protéiques. Les régions où les deux se chevauchent apparaissent en jaune. Le complexe ARP est hautement concentré à l'avant du lamellipode, où la nucléation d'actine est la plus active.

Nucléation des filaments d'actine et formation d'un réseau par le complexe ARP dans les lamellipodes Les marques délimitent des zones agrandies sur la dia suivante Agrandissement des régions marquées du réseau d'actine sur le bord avant, montrées en B. De nombreux filaments ramifiés peuvent être observés avec l'angle de 70° caractéristique qui se forme lorsque le complexe ARP nuclée un nouveau filament d'actine, sur le côté d'un filament d'actine préexistant Photographie en microscopie électronique d'une réplique ombrée au platine du bord antérieur d'un kératocyte, montrant le réseau dense de filament d'actine.

Nucléation des filaments d'actine et formation d'un réseau par le complexe ARP dans les lamellipodes Agrandissement des régions marquées du réseau d'actine sur le bord avant, montrées en B. De nombreux filaments ramifiés peuvent être observés avec l'angle de 70° caractéristique qui se forme lorsque le complexe ARP nuclée un nouveau filament d'actine, sur le côté d'un filament d'actine préexistant (voir Figure 16 14).

« Treadmilling » • Le réseau dans son ensemble subir un treadmilling, s'assemblant par devant et se désassemblant par derrière, ce qui rappelle le treadmilling qui se produit dans les filaments d'actine et les microtubules individuels et dont nous avons déjà parlé • voir rappels…
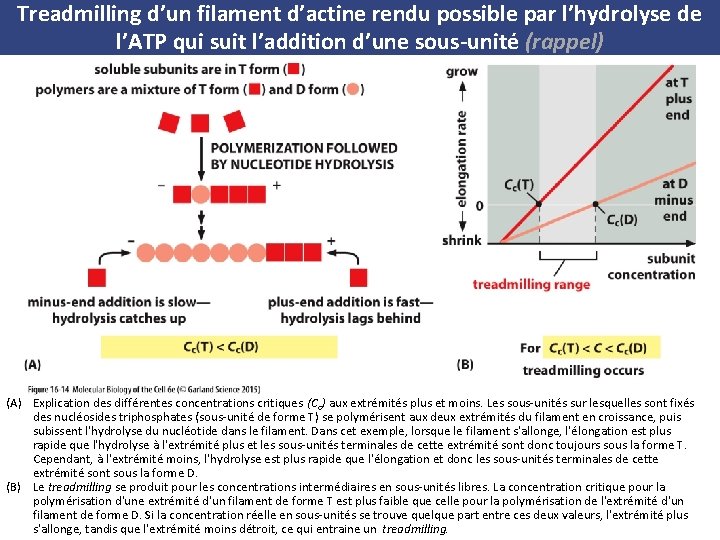
Treadmilling d’un filament d’actine rendu possible par l’hydrolyse de l’ATP qui suit l’addition d’une sous unité (rappel) (A) Explication des différentes concentrations critiques (Cc) aux extrémités plus et moins. Les sous unités sur lesquelles sont fixés des nucléosides triphosphates (sous unité de forme T) se polymérisent aux deux extrémités du filament en croissance, puis subissent l'hydrolyse du nucléotide dans le filament. Dans cet exemple, lorsque le filament s'allonge, l'élongation est plus rapide que l'hydrolyse à l'extrémité plus et les sous unités terminales de cette extrémité sont donc toujours sous la forme T. Cependant, à l'extrémité moins, l'hydrolyse est plus rapide que l'élongation et donc les sous unités terminales de cette extrémité sont sous la forme D. (B) Le treadmilling se produit pour les concentrations intermédiaires en sous unités libres. La concentration critique pour la polymérisation d'une extrémité d'un filament de forme T est plus faible que celle pour la polymérisation de l'extrémité d'un filament de forme D. Si la concentration réelle en sous unités se trouve quelque part entre ces deux valeurs, l'extrémité plus s'allonge, tandis que l'extrémité moins détroit, ce qui entraine un treadmilling.
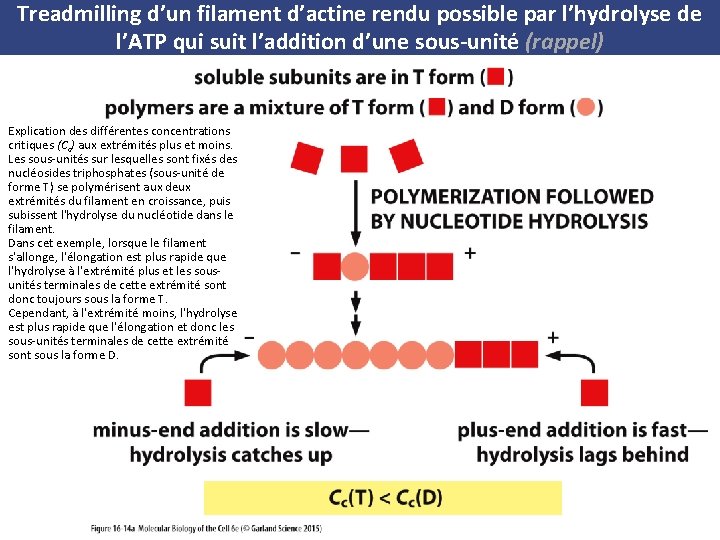
Treadmilling d’un filament d’actine rendu possible par l’hydrolyse de l’ATP qui suit l’addition d’une sous unité (rappel) Explication des différentes concentrations critiques (Cc) aux extrémités plus et moins. Les sous unités sur lesquelles sont fixés des nucléosides triphosphates (sous unité de forme T) se polymérisent aux deux extrémités du filament en croissance, puis subissent l'hydrolyse du nucléotide dans le filament. Dans cet exemple, lorsque le filament s'allonge, l'élongation est plus rapide que l'hydrolyse à l'extrémité plus et les sous unités terminales de cette extrémité sont donc toujours sous la forme T. Cependant, à l'extrémité moins, l'hydrolyse est plus rapide que l'élongation et donc les sous unités terminales de cette extrémité sont sous la forme D.
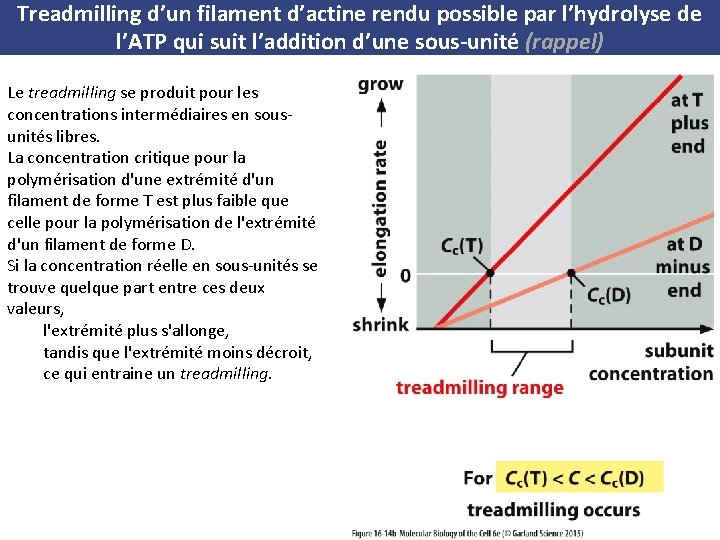
Treadmilling d’un filament d’actine rendu possible par l’hydrolyse de l’ATP qui suit l’addition d’une sous unité (rappel) Le treadmilling se produit pour les concentrations intermédiaires en sous unités libres. La concentration critique pour la polymérisation d'une extrémité d'un filament de forme T est plus faible que celle pour la polymérisation de l'extrémité d'un filament de forme D. Si la concentration réelle en sous unités se trouve quelque part entre ces deux valeurs, l'extrémité plus s'allonge, tandis que l'extrémité moins décroit, ce qui entraine un treadmilling.

Bord conducteur • On pense que le maintien unidirectionnel des mouvements par les lamellipodes nécessite la coopération et l'intégration mécanique de plusieurs facteurs • La nucléation des filaments s'effectue sur le bord conducteur, et la croissance des nouveaux filaments d'actine se produit surtout à cet endroit, ce qui repousse la membrane plas mique vers l'avant • La plus grande partie de la dépolymérisation des filaments se produit sur des sites localisés bien en arrière du bord conducteur.
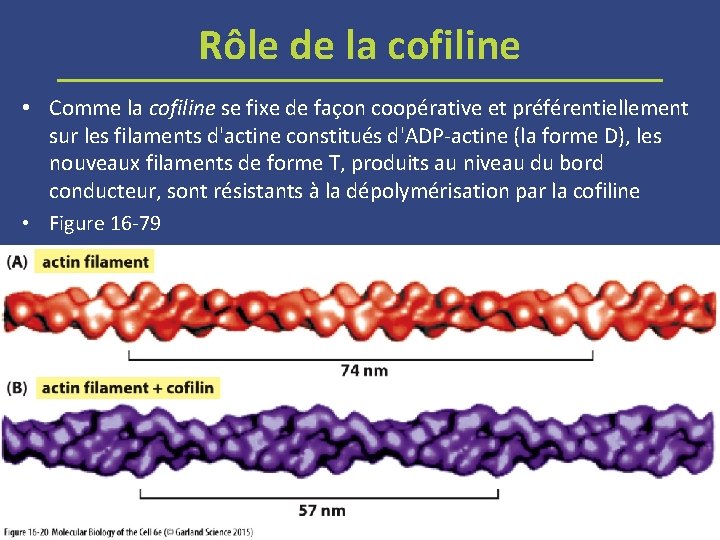
Rôle de la cofiline • Comme la cofiline se fixe de façon coopérative et préférentiellement sur les filaments d'actine constitués d'ADP actine (la forme D), les nouveaux filaments de forme T, produits au niveau du bord conducteur, sont résistants à la dépolymérisation par la cofiline • Figure 16 79

Enroulement d'un filament d'actine induit par la cofiline (Rappel) A. B. Reconstruction tridimensionnelle à partir de photographies en microscopie cryoélectronique de filaments constitués d'actine pure. Les crochets montrent la longueur de deux tours d'hélice d'actine. Reconstruction d'un filament d'actine recouvert de cofiline, qui se fixe avec une stœchiométrie de 1: 1 aux sous unités d'actine tout le long du filament. La cofiline est une petite protéine (14 kilodaltons) comparée à l'actine (43 kilodaltons) et par conséquent le filament ne semble que légèrement plus épais. L'énergie de la liaison de la cofiline sert à déformer le réseau de filaments d'actine, resserrant l'enroulement pour réduire la distance entre deux tours d'hélice.
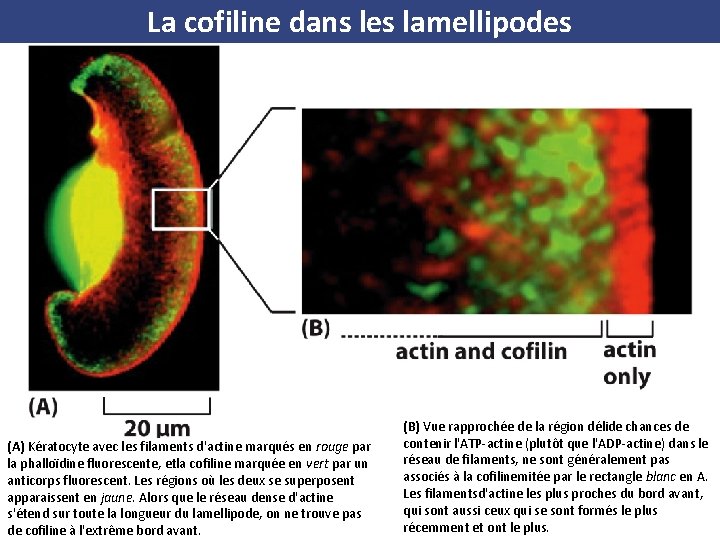
La cofiline dans les lamellipodes (A) Kératocyte avec les filaments d'actine marqués en rouge par la phalloïdine fluorescente, etla cofiline marquée en vert par un anticorps fluorescent. Les régions où les deux se superposent apparaissent en jaune. Alors que le réseau dense d'actine s'étend sur toute la longueur du lamellipode, on ne trouve pas de cofiline à l'extrême bord avant. (B) Vue rapprochée de la région délide chances de contenir l'ATP actine (plutôt que l'ADP actine) dans le réseau de filaments, ne sont généralement pas associés à la cofilinemitée par le rectangle blanc en A. Les filamentsd'actine les plus proches du bord avant, qui sont aussi ceux qui se sont formés le plus récemment et ont le plus.

Treadmilling unidirectionnel dans les lamelli podes • Lorsque le filament vieillit et que l'hydrolyse de l'ATP s'ef fectue, la cofiline dissocie efficacement les plus vieux filaments • On pense donc que l'hydrolyse retardée de l'ATP par l'actine filamenteuse est à la base d'un mécanisme qui maintient un processus de treadmilling unidirectionnel efficace dans les lamelli podes
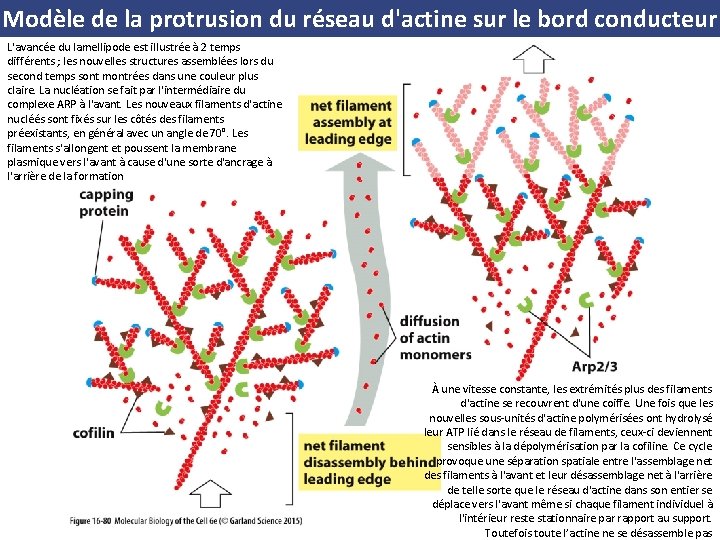
Modèle de la protrusion du réseau d'actine sur le bord conducteur L'avancée du lamellipode est illustrée à 2 temps différents ; les nouvelles structures assemblées lors du second temps sont montrées dans une couleur plus claire. La nucléation se fait par l'intermédiaire du complexe ARP à l'avant. Les nouveaux filaments d'actine nucléés sont fixés sur les côtés des filaments préexistants, en général avec un angle de 70°. Les filaments s'allongent et poussent la membrane plasmique vers l'avant à cause d'une sorte d'ancrage à l'arrière de la formation À une vitesse constante, les extrémités plus des filaments d'actine se recouvrent d'une coiffe. Une fois que les nouvelles sous unités d'actine polymérisées ont hydrolysé leur ATP lié dans le réseau de filaments, ceux ci deviennent sensibles à la dépolymérisation par la cofiline. Ce cycle provoque une séparation spatiale entre l'assemblage net des filaments à l'avant et leur désassemblage net à l'arrière de telle sorte que le réseau d'actine dans son entier se déplace vers l'avant même si chaque filament individuel à l'intérieur reste stationnaire par rapport au support. Toutefois toute l’actine ne se désassemble pas

Explique également le mouvement intracellulaire de bactéries pathogènes comme Listeria …
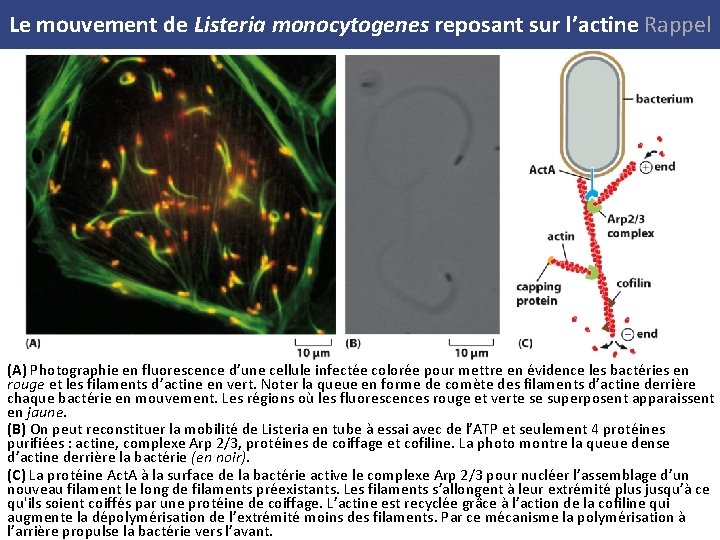
Le mouvement de Listeria monocytogenes reposant sur l’actine Rappel (A) Photographie en fluorescence d’une cellule infectée colorée pour mettre en évidence les bactéries en rouge et les filaments d’actine en vert. Noter la queue en forme de comète des filaments d’actine derrière chaque bactérie en mouvement. Les régions où les fluorescences rouge et verte se superposent apparaissent en jaune. (B) On peut reconstituer la mobilité de Listeria en tube à essai avec de l’ATP et seulement 4 protéines purifiées : actine, complexe Arp 2/3, protéines de coiffage et cofiline. La photo montre la queue dense d’actine derrière la bactérie (en noir). (C) La protéine Act. A à la surface de la bactérie active le complexe Arp 2/3 pour nucléer l’assemblage d’un nouveau filament le long de filaments préexistants. Les filaments s’allongent à leur extrémité plus jusqu’à ce qu'ils soient coiffés par une protéine de coiffage. L’actine est recyclée grâce à l’action de la cofiline qui augmente la dépolymérisation de l’extrémité moins des filaments. Par ce mécanisme la polymérisation à l’arrière propulse la bactérie vers l’avant.
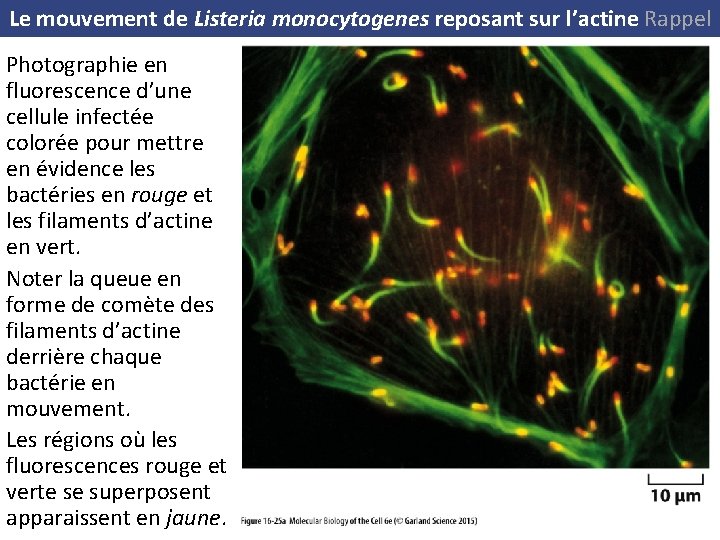
Le mouvement de Listeria monocytogenes reposant sur l’actine Rappel Photographie en fluorescence d’une cellule infectée colorée pour mettre en évidence les bactéries en rouge et les filaments d’actine en vert. Noter la queue en forme de comète des filaments d’actine derrière chaque bactérie en mouvement. Les régions où les fluorescences rouge et verte se superposent apparaissent en jaune.

Le mouvement de Listeria monocytogenes reposant sur l’actine Rappel On peut reconstituer la mobilité de Listeria en tube à essai avec de l’ATP et seulement 4 protéines purifiées : 1. actine, 2. complexe Arp 2/3, 3. protéines de coiffage et 4. cofiline. La photo montre la queue dense d’actine derrière la bactérie (en noir).
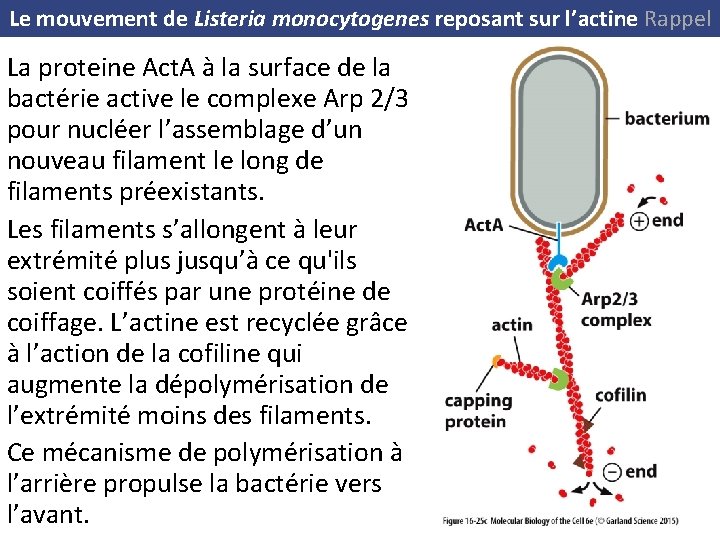
Le mouvement de Listeria monocytogenes reposant sur l’actine Rappel La proteine Act. A à la surface de la bactérie active le complexe Arp 2/3 pour nucléer l’assemblage d’un nouveau filament le long de filaments préexistants. Les filaments s’allongent à leur extrémité plus jusqu’à ce qu'ils soient coiffés par une protéine de coiffage. L’actine est recyclée grâce à l’action de la cofiline qui augmente la dépolymérisation de l’extrémité moins des filaments. Ce mécanisme de polymérisation à l’arrière propulse la bactérie vers l’avant.

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Coordination des mouvements • Les forces générées par la polymérisation des filaments d’actine en avant d’une cellule en migration sont transmises au support sous jacent pour conduire la locomotion de la cellule • Pour que le bord conducteur d’une cellule puisse avancer, il faut que la protrusion de la membrane soit suivie d’une adhésion au support en avant • Au contraire pour que le corps cellulaire suive, la contraction doit être couplée à une dés adhésion de l’arrière de la cellule • Les processus qui contribuent à la migration doivent donc être étroitement régulés dans le temps et dans l’espace • Avec la polymérisation de l’actine • Des adhésions dynamiques • Et la contraction de myosine • Utilisés pour coordonner le mouvement

• La myosine II aide la migration cellulaire par au moins deux moyens I. Contacts focaux II. Bipolarité du filament de myosine II

i Contacts focaux • Aident à connecter le cytosquelette d’actine au support grâce à des adhésions à intégrine • Des forces sont générées au site d’attachement par à la fois – la polymérisation de l’actine – L’activité de la myosine • Pour créer une tension aux sites d’attachement leur permettant de maturer en contacts focaux

Contacts focaux (rappel) • Assemblages dynamiques de protéines de structure et de signalisation qui font la liaison entre la cellule en migration et la matrice extracellulaire • Figure 19 59
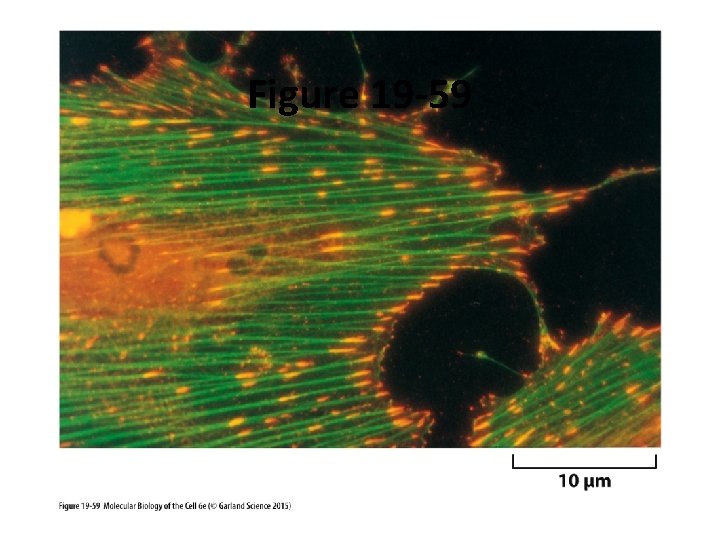
Figure 19 59

ii Bipolarité du filament de myosine II • Filament de myosine II bipolaire s’associe aux filaments d’actine à l’arrière du lamellipode et les réoriente • Depuis perpendiculaire au bord conducteur • Jusqu'à presque parallèle au bord conducteur • Cette contraction qui se rapproche de celle du sarcomère empêche la protrusion et elle aboutit à un pincement sur les côtés du lamellipode en déplacement en aidant à récupérer sur les côtés de la cellule quand elle avance • Figure 16 81
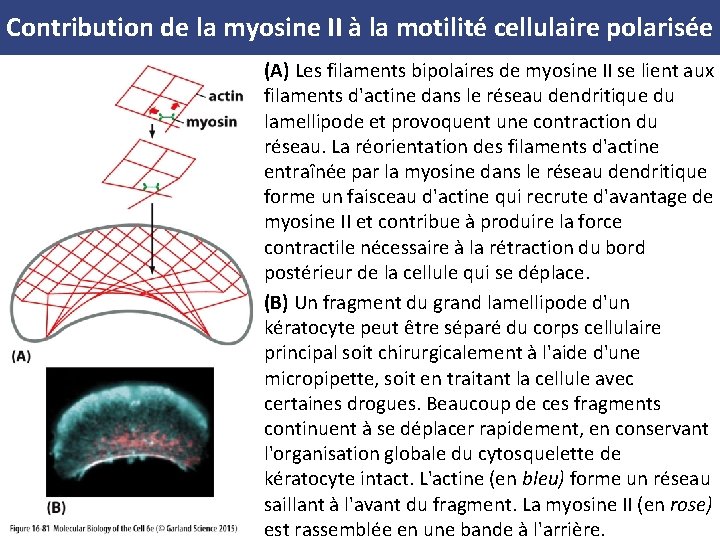
Contribution de la myosine II à la motilité cellulaire polarisée (A) Les filaments bipolaires de myosine II se lient aux filaments d'actine dans le réseau dendritique du lamellipode et provoquent une contraction du réseau. La réorientation des filaments d'actine entraînée par la myosine dans le réseau dendritique forme un faisceau d'actine qui recrute d'avantage de myosine II et contribue à produire la force contractile nécessaire à la rétraction du bord postérieur de la cellule qui se déplace. (B) Un fragment du grand lamellipode d'un kératocyte peut être séparé du corps cellulaire principal soit chirurgicalement à l'aide d'une micropipette, soit en traitant la cellule avec certaines drogues. Beaucoup de ces fragments continuent à se déplacer rapidement, en conservant l'organisation globale du cytosquelette de kératocyte intact. L'actine (en bleu) forme un réseau saillant à l'avant du fragment. La myosine II (en rose) est rassemblée en une bande à l'arrière.
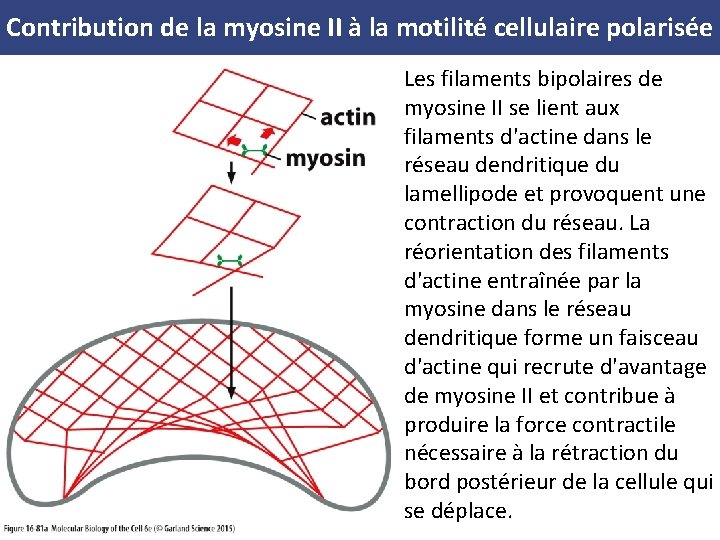
Contribution de la myosine II à la motilité cellulaire polarisée Les filaments bipolaires de myosine II se lient aux filaments d'actine dans le réseau dendritique du lamellipode et provoquent une contraction du réseau. La réorientation des filaments d'actine entraînée par la myosine dans le réseau dendritique forme un faisceau d'actine qui recrute d'avantage de myosine II et contribue à produire la force contractile nécessaire à la rétraction du bord postérieur de la cellule qui se déplace.
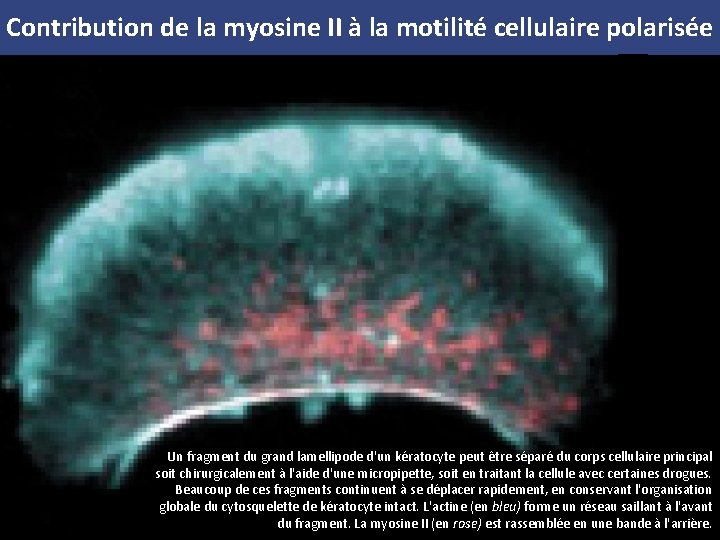
Contribution de la myosine II à la motilité cellulaire polarisée Un fragment du grand lamellipode d'un kératocyte peut être séparé du corps cellulaire principal soit chirurgicalement à l'aide d'une micropipette, soit en traitant la cellule avec certaines drogues. Beaucoup de ces fragments continuent à se déplacer rapidement, en conservant l'organisation globale du cytosquelette de kératocyte intact. L'actine (en bleu) forme un réseau saillant à l'avant du fragment. La myosine II (en rose) est rassemblée en une bande à l'arrière.

Interactions entre le réseau d’actine et les contacts focaux • Les protrusions transmises par l’actine ne peuvent pousser le bord conducteur de la cellule en avant que si il y a de fortes interactions entre le réseau d’actine et les contacts focaux qui relient la cellule à son support • Quand il y a désengagement de ces interactions, • la pression de la polymérisation au bord conducteur • Et la contraction myosine dépendante • Fait retomber le réseau d’actine aboutissant à un phénomène appelé flux rétrograde
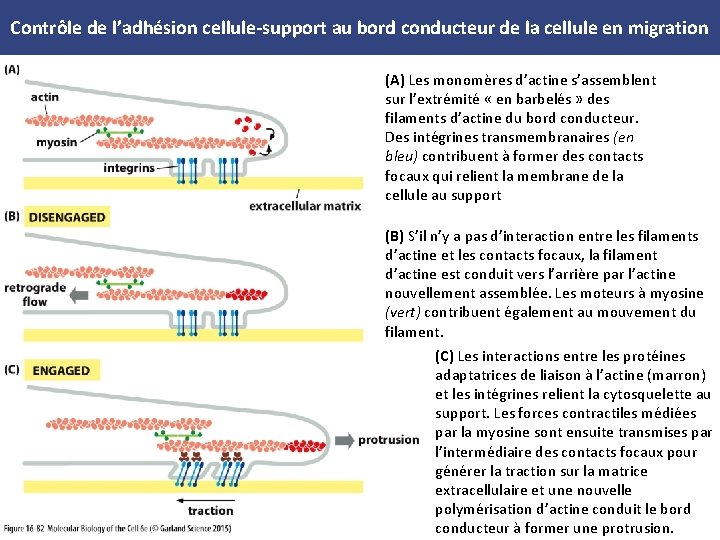
Contrôle de l’adhésion cellule support au bord conducteur de la cellule en migration (A) Les monomères d’actine s’assemblent sur l’extrémité « en barbelés » des filaments d’actine du bord conducteur. Des intégrines transmembranaires (en bleu) contribuent à former des contacts focaux qui relient la membrane de la cellule au support (B) S’il n’y a pas d’interaction entre les filaments d’actine et les contacts focaux, la filament d’actine est conduit vers l’arrière par l’actine nouvellement assemblée. Les moteurs à myosine (vert) contribuent également au mouvement du filament. (C) Les interactions entre les protéines adaptatrices de liaison à l’actine (marron) et les intégrines relient la cytosquelette au support. Les forces contractiles médiées par la myosine sont ensuite transmises par l’intermédiaire des contacts focaux pour générer la traction sur la matrice extracellulaire et une nouvelle polymérisation d’actine conduit le bord conducteur à former une protrusion.

Force de la cellule sur le support • Les forces de traction engendrées par les cellules qui migrent, exercent une traction significative sur le support • En faisant pousser des cellules sur une surface recouvertes de minuscules petits spicules flexibles, on peut calculer la force exercée sur le support en mesurant la déviation de chaque spicule par rapport à la verticale

Forces de traction exercées par une cellule mobile (A) De minuscules colonnes flexibles fixées sur le support se courbent sous l’effet des forces de traction. (B) Photographie de microscopie à balayage d’une cellule sur un support recouvert de picots de 6, 1 µm de haut. On calcule la force correspondant aux forces de traction internes exercées sur le support sous jacent à partir de la déviation des picots.
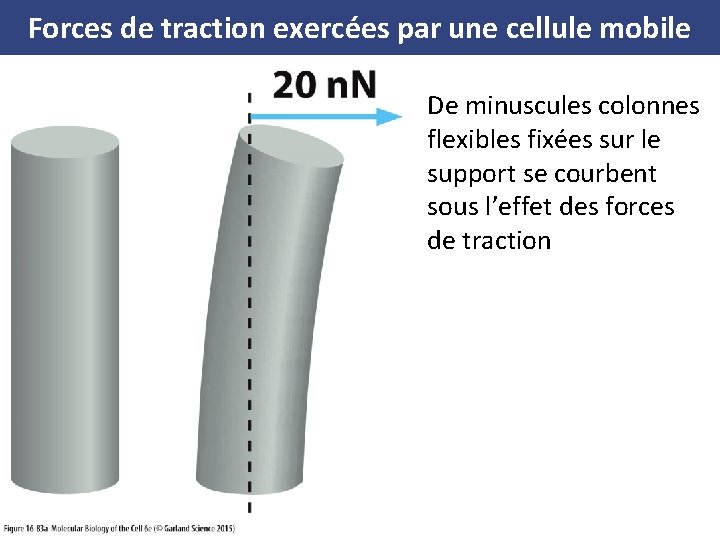
Forces de traction exercées par une cellule mobile De minuscules colonnes flexibles fixées sur le support se courbent sous l’effet des forces de traction
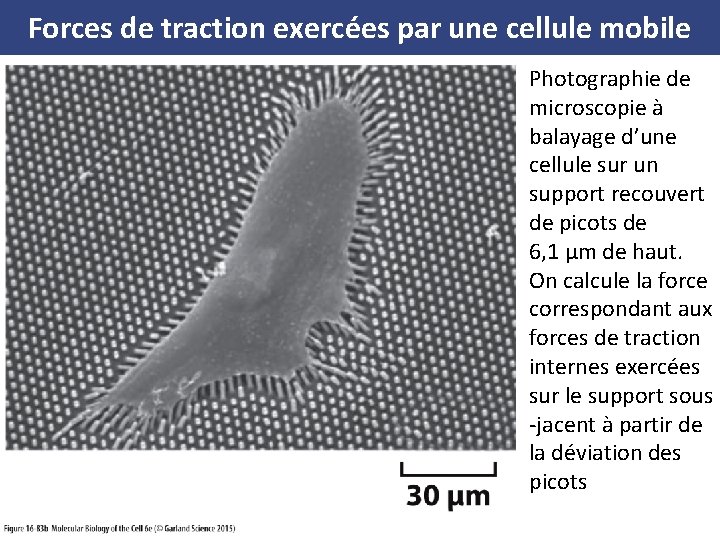
Forces de traction exercées par une cellule mobile Photographie de microscopie à balayage d’une cellule sur un support recouvert de picots de 6, 1 µm de haut. On calcule la force correspondant aux forces de traction internes exercées sur le support sous jacent à partir de la déviation des picots
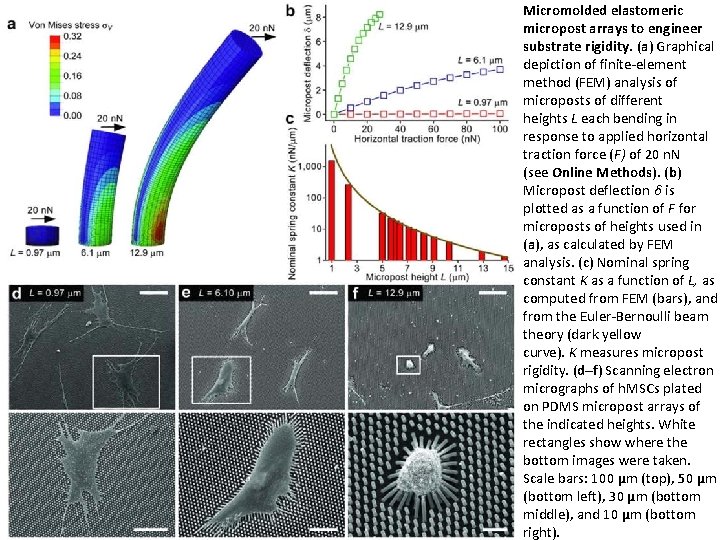
Mechanical regulation of cell function with geometrically modulated elastomeric substrates Jianping Fu, Yang Kao, Wang, Michael T. , Yang, Ravi A. Desai, Xiang Yu, Zhijun Liu, and Christopher S. Chen Nat Methods. 2010 Sep; 7(9): 733– 736. Fig 1 Micromolded elastomeric micropost arrays to engineer substrate rigidity. (a) Graphical depiction of finite element method (FEM) analysis of microposts of different heights L each bending in response to applied horizontal traction force (F) of 20 n. N (see Online Methods). (b) Micropost deflection δ is plotted as a function of F for microposts of heights used in (a), as calculated by FEM analysis. (c) Nominal spring constant K as a function of L, as computed from FEM (bars), and from the Euler Bernoulli beam theory (dark yellow curve). K measures micropost rigidity. (d–f) Scanning electron micrographs of h. MSCs plated on PDMS micropost arrays of the indicated heights. White rectangles show where the bottom images were taken. Scale bars: 100 μm (top), 50 μm (bottom left), 30 μm (bottom middle), and 10 μm (bottom right).
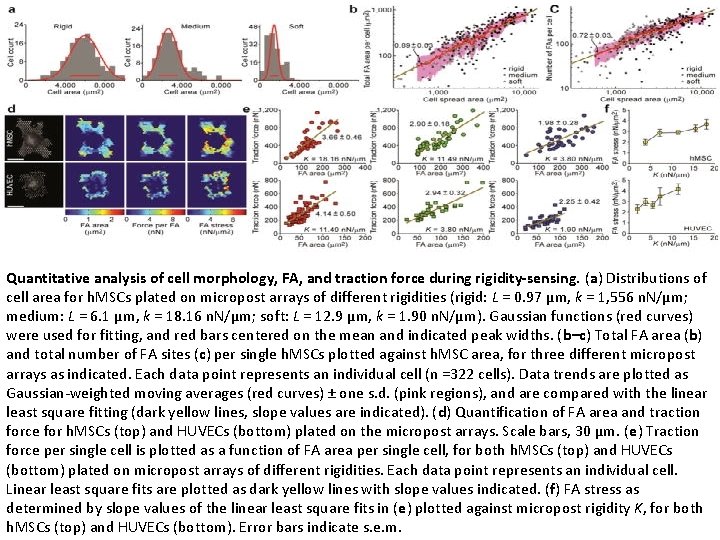
Mechanical regulation of cell function with geometrically modulated elastomeric substrates Jianping Fu, Yang Kao, Wang, Michael T. , Yang, Ravi A. Desai, Xiang Yu, Zhijun Liu, and Christopher S. Chen Nat Methods. 2010 Sep; 7(9): 733– 736. Fig 2 Quantitative analysis of cell morphology, FA, and traction force during rigidity sensing. (a) Distributions of cell area for h. MSCs plated on micropost arrays of different rigidities (rigid: L = 0. 97 μm, k = 1, 556 n. N/μm; medium: L = 6. 1 μm, k = 18. 16 n. N/μm; soft: L = 12. 9 μm, k = 1. 90 n. N/μm). Gaussian functions (red curves) were used for fitting, and red bars centered on the mean and indicated peak widths. (b–c) Total FA area (b) and total number of FA sites (c) per single h. MSCs plotted against h. MSC area, for three different micropost arrays as indicated. Each data point represents an individual cell (n =322 cells). Data trends are plotted as Gaussian weighted moving averages (red curves) ± one s. d. (pink regions), and are compared with the linear least square fitting (dark yellow lines, slope values are indicated). (d) Quantification of FA area and traction force for h. MSCs (top) and HUVECs (bottom) plated on the micropost arrays. Scale bars, 30 μm. (e) Traction force per single cell is plotted as a function of FA area per single cell, for both h. MSCs (top) and HUVECs (bottom) plated on micropost arrays of different rigidities. Each data point represents an individual cell. Linear least square fits are plotted as dark yellow lines with slope values indicated. (f) FA stress as determined by slope values of the linear least square fits in (e) plotted against micropost rigidity K, for both h. MSCs (top) and HUVECs (bottom). Error bars indicate s. e. m.
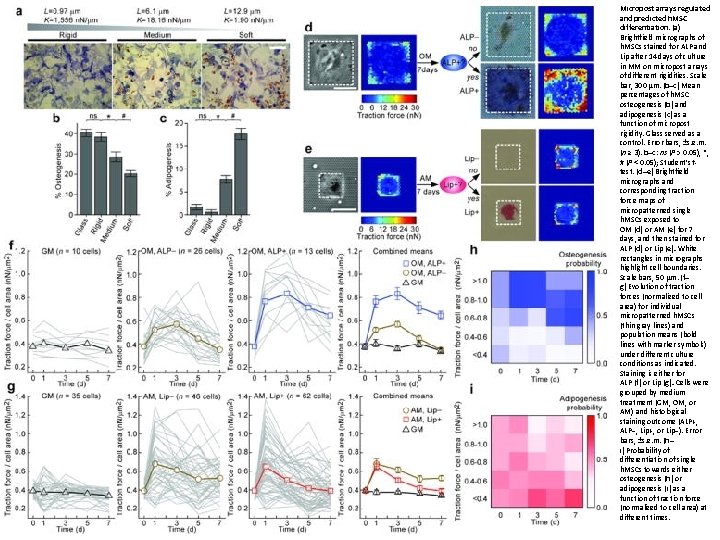
Mechanical regulation of cell function with geometrically modulated elastomeric substrates Jianping Fu, Yang Kao, Wang, Michael T. , Yang, Ravi A. Desai, Xiang Yu, Zhijun Liu, and Christopher S. Chen Nat Methods. 2010 Sep; 7(9): 733– 736. Fig 3 Micropost arrays regulated and predicted h. MSC differentiation. (a) Brightfield micrographs of h. MSCs stained for ALP and Lip after 14 days of culture in MM on micropost arrays of different rigidities. Scale bar, 300 μm. (b–c) Mean percentages of h. MSC osteogenesis (b) and adipogenesis (c) as a function of micropost rigidity. Glass served as a control. Error bars, ±s. e. m. (n ≥ 3). b–c: ns (P > 0. 05), *, # (P < 0. 05); Student’s t test. (d–e) Brightfield micrographs and corresponding traction force maps of micropatterned single h. MSCs exposed to OM (d) or AM (e) for 7 days, and then stained for ALP (d) or Lip (e). White rectangles in micrographs highlight cell boundaries. Scale bars, 50 μm. (f– g) Evolution of traction forces (normalized to cell area) for individual micropatterned h. MSCs (thin gray lines) and population means (bold lines with marker symbols) under different culture conditions as indicated. Staining is either for ALP (f) or Lip (g). Cells were grouped by medium treatment (GM, OM, or AM) and histological staining outcome (ALP+, ALP−, Lip+, or Lip−). Error bars, ±s. e. m. (h– i) Probability of differentiation of single h. MSCs towards either osteogenesis (h) or adipogenesis (i) as a function of traction force (normalized to cell area) at different times.

Cellule ↔ support • Chez les animaux vivants, la plupart des cellules qui se déplacent, migrent sur un support semi flexible, formé par la matrice extracellulaire, et qui peut être déformé et réarrangé par ces forces cellulaires. • À l'inverse, une cellule sur laquelle est appliqué, de l'extérieur, une tension mécanique ou un étirement, va développer des fibres de stress et des adhésions focales, et devenir plus contractile • Bien que mal comprise, cette interaction mécanique, dans les deux sens, entre les cellules et leur environnement physique représente un des principaux modes par lesquels les tissus des vertébrés s'auto organisent

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Coordination entre les extrémités d'une cellule • La migration cellulaire nécessite une communication sur de longues distances et une coordination entre les extrémités d'une cellule • Pendant la migration dirigée, il est important que l'extrémité avant de la cellule reste structurellement et fonctionnellement distincte de l'extrémité arrière • Le cytosquelette est responsable, non seulement de la conduction de processus mécaniques locaux tels que la protrusion à l'avant et la rétraction à l'arrière de la cellule, mais aussi de • la coordination de la forme cellulaire, • de son organisation, • et des propriétés mécaniques • d'une extrémité à l'autre de la cellule, • une distance qui est généralement de plusieurs dixièmes de micromètres dans les cellules animales

Rôle de la polarisation cellulaire • Très souvent, et la migration cellulaire n'en est qu'un exemple, cette coordination à grande échelle du cytosquelette prend la forme d'une polarisation cellulaire, où la cellule construit des structures différentes, avec des composants différents – entre l'avant et l'arrière, – ou entre le haut et le bas • Pour que la locomotion cellulaire puisse démarrer dans une direction précise, il faut que la cellule soit initialement polarisée • Des processus soigneusement contrôlés de polarisation cellulaire sont aussi nécessaires à une division cellulaire orientée dans les tissus, et à la formation d'une structure multicellulaire cohérente et organisée

Rôle de la polarité cellulaire • Les études génétiques chez les levures, les mouches et les vers ont fourni la plus grande partie de nos connaissances sur les bases moléculaires de la polarité cellulaire • L'exploration des mécanismes qui créent la polarité cellulaire chez les vertébrés n'est qu'à son début • Dans tous les cas cependant, le cytosquelette joue un rôle central et de nombreux composants moléculaires ont été conservés au cours de l'évolution

Rôle de la polarité cellulaire • De nombreuses sortes de polarité cellulaire dépendent de la régulation locale du cytosquelette d'actine par des récepteurs membranaires différents en réponse à des signaux externes • Mais, à l'intérieur de la cellule, tous ces signaux semblent converger vers un groupe de GTPases monomériques étroitement apparentées qui sont membres de la famille de protéines Rho – Cdc 42 – Rac – Rho • Comme d'autres GTPases monomériques, ces protéines Rho sont des commutateurs moléculaires qui contrôlent les processus cellulaires en passant d'un état actif lié au GTP, à un état inactif lié au GDP et réciproquement (voir Figure 3 66 ex 71
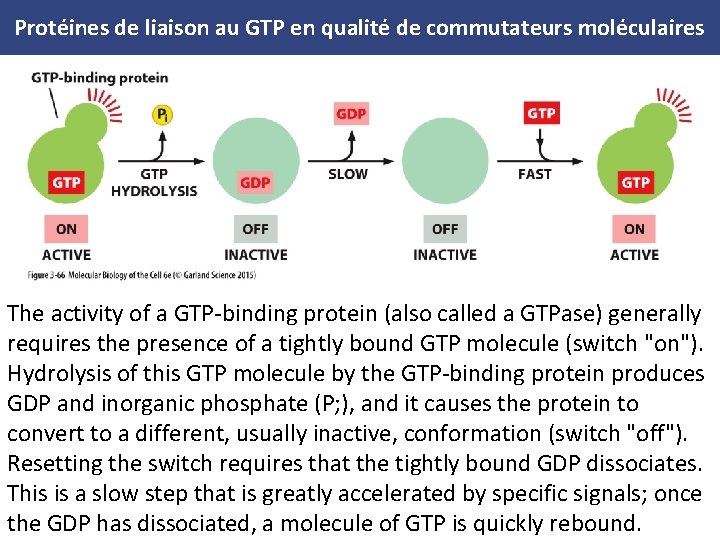
Protéines de liaison au GTP en qualité de commutateurs moléculaires The activity of a GTP binding protein (also called a GTPase) generally requires the presence of a tightly bound GTP molecule (switch "on"). Hydrolysis of this GTP molecule by the GTP binding protein produces GDP and inorganic phosphate (P; ), and it causes the protein to convert to a different, usually inactive, conformation (switch "off"). Resetting the switch requires that the tightly bound GDP dissociates. This is a slow step that is greatly accelerated by specific signals; once the GDP has dissociated, a molecule of GTP is quickly rebound.

Cdc 42, Rac, Rho • L'activation de Cdc 42 sur la membrane plasmique déclenche la polymérisation de l'actine et la formation de faisceaux pour former des filopodes • L'activation de Rac entraîne la polymérisation de l'actine à la périphérie cellulaire, ce qui conduit à la formation d'extension en feuillets de type lamellipode • L'activation de Rho provoque – l'association en faisceaux de filaments d'actine et de myosine II pour former des fibres de stress – et l'agrégation des intégrines et de protéines associées, pour former des contacts en foyers • Figure 16 84
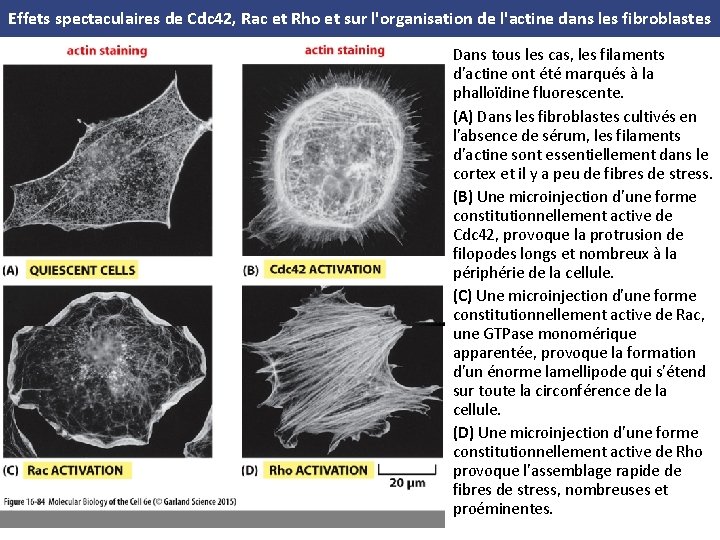
Effets spectaculaires de Cdc 42, Rac et Rho et sur l'organisation de l'actine dans les fibroblastes Dans tous les cas, les filaments d'actine ont été marqués à la phalloïdine fluorescente. (A) Dans les fibroblastes cultivés en l'absence de sérum, les filaments d'actine sont essentiellement dans le cortex et il y a peu de fibres de stress. (B) Une microinjection d'une forme constitutionnellement active de Cdc 42, provoque la protrusion de filopodes longs et nombreux à la périphérie de la cellule. (C) Une microinjection d'une forme constitutionnellement active de Rac, une GTPase monomérique apparentée, provoque la formation d'un énorme lamellipode qui s'étend sur toute la circonférence de la cellule. (D) Une microinjection d'une forme constitutionnellement active de Rho provoque l'assemblage rapide de fibres de stress, nombreuses et proéminentes.

Les cibles de ces 3 molécules • Ces changements de structure, spectaculaires et complexes, se produisent parce que chacune des trois molécules qui les déclenchent agissent en aval sur de nombreuses protéines cibles qui affectent l'organisation et la dynamique de l'actine • Protéines cibles • Membres de la famille de protéines WASp

Membres de la famille de protéines WASp • Principales cibles de Cdc 42 activée • Les patients déficients en WASp souffrent du syndrome de Wiskott Aldrich, – Forme sévère de déficit immunitaire – dans laquelle la mobilité, dépendante de l'actine, des cellules du système immunitaire est anormale, – et les plaquettes ne se forment pas normalement • Bien que WASp elle même ne soit exprimée que dans les cellules sanguines et les cellules du système immunitaire, d'autres membres de la famille sont exprimés de façon ubiquitaire dans beaucoup d’autres types de cellules et permettent à Cdc 42 d'activer la polymérisation de l'actine

Membres de la famille de protéines WASp • Les protéines WASp peuvent exister – sous une forme inactive repliée – et une forme active à conformation ouverte • L'association à Cdc 42 GTP stabilise la conformation ouverte de WASp, lui permettant de se lier au complexe ARP 2/3 et d'augmenter fortement l'activité de nucléation de l'actine de ce complexe (voir Figure 16 34) • De cette manière, l'activation de Cdc 42 augmente la nucléation de l'actine
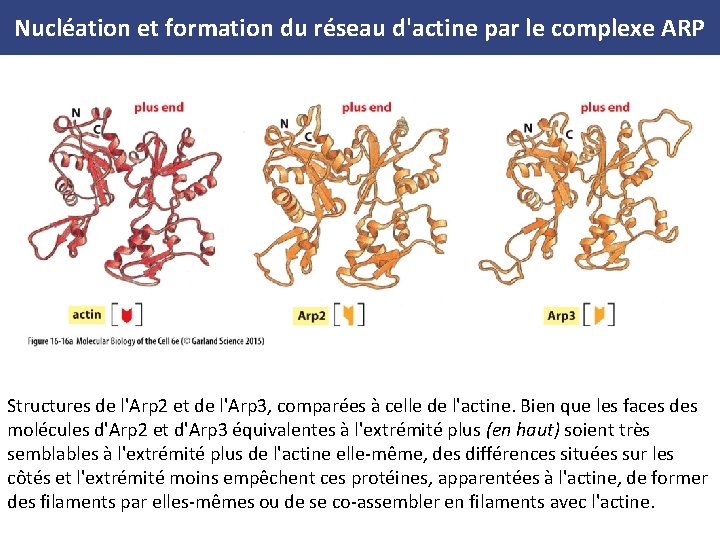
Nucléation et formation du réseau d'actine par le complexe ARP Structures de l'Arp 2 et de l'Arp 3, comparées à celle de l'actine. Bien que les faces des molécules d'Arp 2 et d'Arp 3 équivalentes à l'extrémité plus (en haut) soient très semblables à l'extrémité plus de l'actine elle même, des différences situées sur les côtés et l'extrémité moins empêchent ces protéines, apparentées à l'actine, de former des filaments par elles mêmes ou de se co assembler en filaments avec l'actine.

Rac GTP • Rac GTP active aussi les membres de la famille WASp • De plus active la formation de liaisons croisées par la filamine, une protéine qui forme des gels • Et inhibe l'activité contractile de la protéine motrice myosine II • Stabilise ainsi les lamellipodes, et inhibe la formation de fibres de stress contractiles • Figure 16 85 A
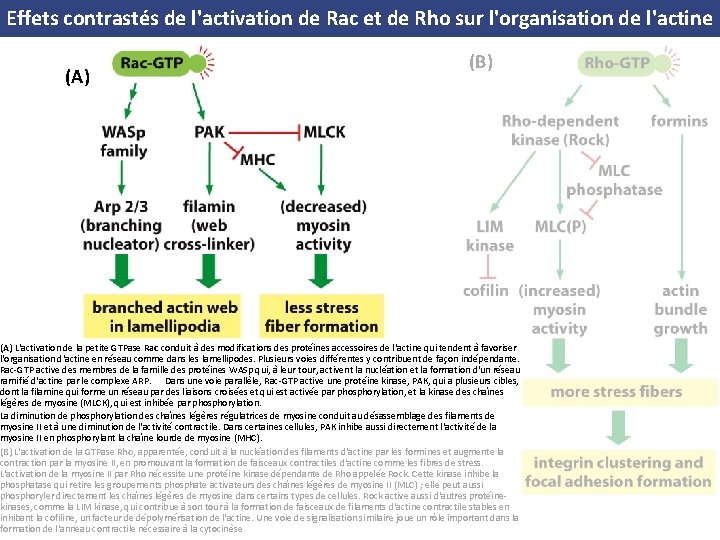
Effets contrastés de l'activation de Rac et de Rho sur l'organisation de l'actine (A) (B) (A) L'activation de la petite GTPase Rac conduit à des modifications des protéines accessoires de l'actine qui tendent à favoriser l'organisation d'actine en réseau comme dans les lamellipodes. Plusieurs voies différentes y contribuent de façon indépendante. Rac GTP active des membres de la famille des protéines WASp qui, à leur tour, activent la nucléation et la formation d'un réseau ramifié d'actine par le complexe ARP. Dans une voie parallèle, Rac GTP active une protéine kinase, PAK, qui a plusieurs cibles, dont la filamine qui forme un réseau par des liaisons croisées et qui est activée par phosphorylation, et la kinase des chaînes légères de myosine (MLCK), qui est inhibée par phosphorylation. La diminution de phosphorylation des chaînes légères régulatrices de myosine conduit au désassemblage des filaments de myosine II et à une diminution de l'activité contractile. Dans certaines cellules, PAK inhibe aussi directement l'activité de la myosine II en phosphorylant la chaîne lourde de myosine (MHC). (B) L'activation de la GTPase Rho, apparentée, conduit à la nucléation des filaments d'actine par les formines et augmente la contraction par la myosine II, en promouvant la formation de faisceaux contractiles d'actine comme les fibres de stress. L'activation de la myosine II par Rho nécessite une protéine kinase dépendante de Rho appelée Rock. Cette kinase inhibe la phosphatase qui retire les groupements phosphate activateurs des chaînes légères de myosine II (MLC) ; elle peut aussi phosphoryler directement les chaînes légères de myosine dans certains types de cellules. Rock active aussi d'autres protéine kinases, comme la LIM kinase, qui contribue à son tour à la formation de faisceaux de filaments d'actine contractile stables en inhibant la cofiline, un facteur de dépolymérisation de l'actine. Une voie de signalisation similaire joue un rôle important dans la formation de l'anneau contractile nécessaire à la cytocinèse
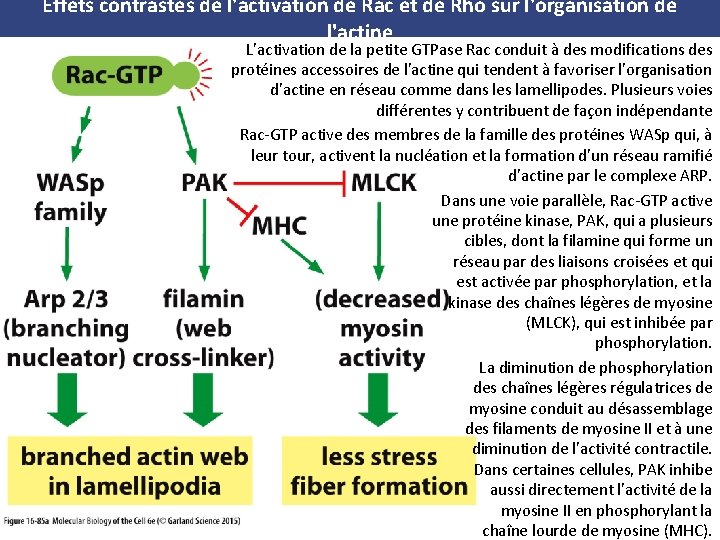
Effets contrastés de l'activation de Rac et de Rho sur l'organisation de l'actine L'activation de la petite GTPase Rac conduit à des modifications des protéines accessoires de l'actine qui tendent à favoriser l'organisation d'actine en réseau comme dans les lamellipodes. Plusieurs voies différentes y contribuent de façon indépendante Rac GTP active des membres de la famille des protéines WASp qui, à leur tour, activent la nucléation et la formation d'un réseau ramifié d'actine par le complexe ARP. Dans une voie parallèle, Rac GTP active une protéine kinase, PAK, qui a plusieurs cibles, dont la filamine qui forme un réseau par des liaisons croisées et qui est activée par phosphorylation, et la kinase des chaînes légères de myosine (MLCK), qui est inhibée par phosphorylation. La diminution de phosphorylation des chaînes légères régulatrices de myosine conduit au désassemblage des filaments de myosine II et à une diminution de l'activité contractile. Dans certaines cellules, PAK inhibe aussi directement l'activité de la myosine II en phosphorylant la chaîne lourde de myosine (MHC).

Rho GTP • Rho GTP a un groupe de cibles très différent • Au lieu d'activer le complexe ARP 2/3 pour qu'il construise un réseau d'actine, • Rho GTP stimule la formation, par les formines, de faisceaux d'actine parallèles • En même temps, Rho GTP active une protéine kinase qui inhibe indirectement l'activité de la cofiline, conduisant à la stabilisation des filaments d'actine • La même protéine kinase inhibe une phosphatase agissant sur les chaînes légères de la myosine • voir Figure 16 39
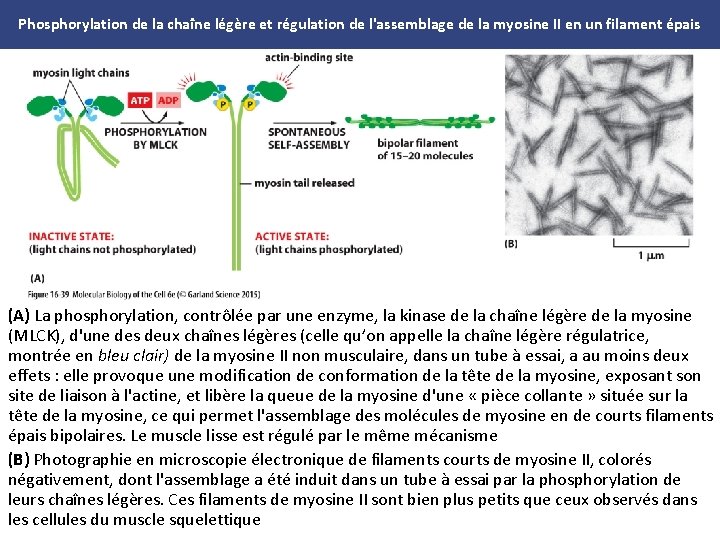
Phosphorylation de la chaîne légère et régulation de l'assemblage de la myosine II en un filament épais (A) La phosphorylation, contrôlée par une enzyme, la kinase de la chaîne légère de la myosine (MLCK), d'une des deux chaînes légères (celle qu’on appelle la chaîne légère régulatrice, montrée en bleu clair) de la myosine II non musculaire, dans un tube à essai, a au moins deux effets : elle provoque une modification de conformation de la tête de la myosine, exposant son site de liaison à l'actine, et libère la queue de la myosine d'une « pièce collante » située sur la tête de la myosine, ce qui permet l'assemblage des molécules de myosine en de courts filaments épais bipolaires. Le muscle lisse est régulé par le même mécanisme (B) Photographie en microscopie électronique de filaments courts de myosine II, colorés négativement, dont l'assemblage a été induit dans un tube à essai par la phosphorylation de leurs chaînes légères. Ces filaments de myosine II sont bien plus petits que ceux observés dans les cellules du muscle squelettique
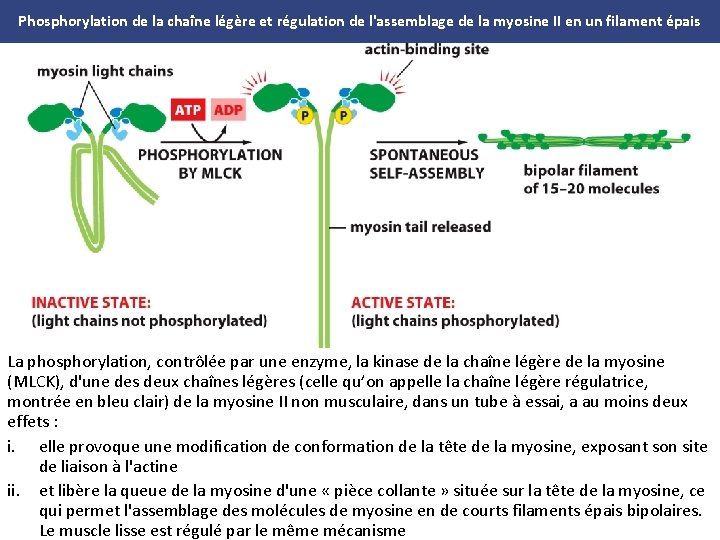
Phosphorylation de la chaîne légère et régulation de l'assemblage de la myosine II en un filament épais La phosphorylation, contrôlée par une enzyme, la kinase de la chaîne légère de la myosine (MLCK), d'une des deux chaînes légères (celle qu’on appelle la chaîne légère régulatrice, montrée en bleu clair) de la myosine II non musculaire, dans un tube à essai, a au moins deux effets : i. elle provoque une modification de conformation de la tête de la myosine, exposant son site de liaison à l'actine ii. et libère la queue de la myosine d'une « pièce collante » située sur la tête de la myosine, ce qui permet l'assemblage des molécules de myosine en de courts filaments épais bipolaires. Le muscle lisse est régulé par le même mécanisme

Phosphorylation de la chaîne légère et régulation de l'assemblage de la myosine II en un filament épais Photographie en microscopie électronique de filaments courts de myosine II, colorés négativement, dont l'assemblage a été induit dans un tube à essai par la phosphorylation de leurs chaînes légères. Ces filaments de myosine II sont bien plus petits que ceux observés dans les cellules du muscle squelettique

Rho GTP • L'augmentation de la quantité de chaînes légères phosphorylées qui en résulte augmente l'activité contractile de la myosine dans la cellule, augmentant ainsi la formation de structures dépendantes de la tension, comme les fibres de stress • voir Figure 16 85 B
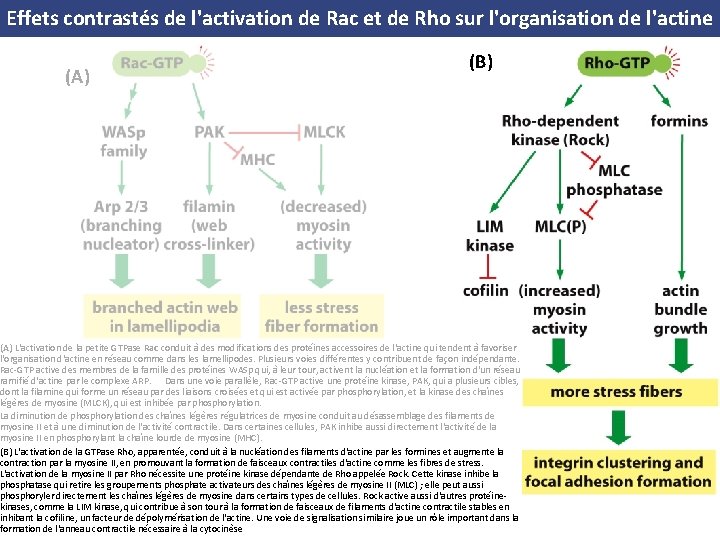
Effets contrastés de l'activation de Rac et de Rho sur l'organisation de l'actine (A) (B) (A) L'activation de la petite GTPase Rac conduit à des modifications des protéines accessoires de l'actine qui tendent à favoriser l'organisation d'actine en réseau comme dans les lamellipodes. Plusieurs voies différentes y contribuent de façon indépendante. Rac GTP active des membres de la famille des protéines WASp qui, à leur tour, activent la nucléation et la formation d'un réseau ramifié d'actine par le complexe ARP. Dans une voie parallèle, Rac GTP active une protéine kinase, PAK, qui a plusieurs cibles, dont la filamine qui forme un réseau par des liaisons croisées et qui est activée par phosphorylation, et la kinase des chaînes légères de myosine (MLCK), qui est inhibée par phosphorylation. La diminution de phosphorylation des chaînes légères régulatrices de myosine conduit au désassemblage des filaments de myosine II et à une diminution de l'activité contractile. Dans certaines cellules, PAK inhibe aussi directement l'activité de la myosine II en phosphorylant la chaîne lourde de myosine (MHC). (B) L'activation de la GTPase Rho, apparentée, conduit à la nucléation des filaments d'actine par les formines et augmente la contraction par la myosine II, en promouvant la formation de faisceaux contractiles d'actine comme les fibres de stress. L'activation de la myosine II par Rho nécessite une protéine kinase dépendante de Rho appelée Rock. Cette kinase inhibe la phosphatase qui retire les groupements phosphate activateurs des chaînes légères de myosine II (MLC) ; elle peut aussi phosphoryler directement les chaînes légères de myosine dans certains types de cellules. Rock active aussi d'autres protéine kinases, comme la LIM kinase, qui contribue à son tour à la formation de faisceaux de filaments d'actine contractile stables en inhibant la cofiline, un facteur de dépolymérisation de l'actine. Une voie de signalisation similaire joue un rôle important dans la formation de l'anneau contractile nécessaire à la cytocinèse
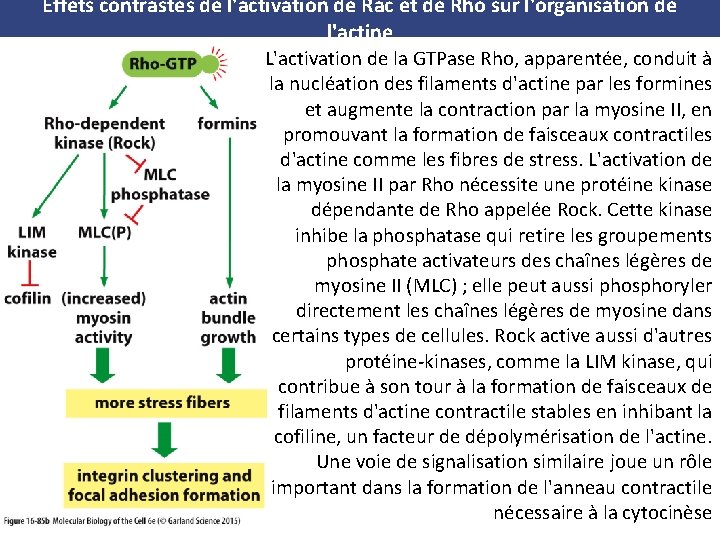
Effets contrastés de l'activation de Rac et de Rho sur l'organisation de l'actine L'activation de la GTPase Rho, apparentée, conduit à la nucléation des filaments d'actine par les formines et augmente la contraction par la myosine II, en promouvant la formation de faisceaux contractiles d'actine comme les fibres de stress. L'activation de la myosine II par Rho nécessite une protéine kinase dépendante de Rho appelée Rock. Cette kinase inhibe la phosphatase qui retire les groupements phosphate activateurs des chaînes légères de myosine II (MLC) ; elle peut aussi phosphoryler directement les chaînes légères de myosine dans certains types de cellules. Rock active aussi d'autres protéine kinases, comme la LIM kinase, qui contribue à son tour à la formation de faisceaux de filaments d'actine contractile stables en inhibant la cofiline, un facteur de dépolymérisation de l'actine. Une voie de signalisation similaire joue un rôle important dans la formation de l'anneau contractile nécessaire à la cytocinèse

Voies Rac et Rho • Dans certains types cellulaires, Rac GTP active Rho, habituellement avec une cinétique lente par rapport à l'activation des complexes ARP par Rac • Cela permet aux cellules d'utiliser la voie Rac pour construire une nouvelle structure d'actine, et d'activer ensuite la voie Rho pour induire la contractilité qui va entraîner une accumulation de tension dans cette structure • Ceci a lieu, par exemple, pendant la formation et la maturation des contacts intercellulaires • Comme nous allons le voir plus en détails ci dessous, la communication entre les voies Rac et Rho facilite aussi le maintien de grandes différences entre l'avant et l'arrière de la cellule pendant la migration

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

GEFs • • L'activation des GTPases monomériques Rho, Rac et Cdc 42 se fait par un échange entre GTP et une molécule de GDP étroitement liée, catalysé par les facteurs d'échange de nucléotides (GEF) Parmi les nombreuses (85 ? ) GEF qui ont été identifiés dans le génome humain, certaines sont spécifiques d'une GTPase particulière de la famille Rho, alors que d'autres semblent agir sur les trois membres de la famille Les différents GEFs sont limités à des tissus spécifiques, voire à des localisations subcellulaires spécifiques, et ils sont sensibles à des signaux différents Divers signaux extracellulaires activent les GEFs par l’intermédiaire de récepteurs membranaires o en réponse à des signaux intracellulaires Les GEFs peuvent également agir comme des voies qui dirigent les GTPases vers des effecteurs d’aval Il est intéressant de noter que plusieurs GEF de la famille Rho s'associent à la croissance des extrémités des microtubules en se liant à une des +TIPs Cela permet de relier la dynamique du cytosquelette de microtubules et l'organisation à grande échelle du cytosquelette d'actine, ce qui est important pour l'intégration globale de la forme et du mouvement cellulaire

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Chimiotaxie • Définie comme un mouvement cellulaire attractif ou répulsif contrôlé par un gradient d'une substance chimique diffusible • C'est un exemple particulièrement intéressant dans lequel un signal externe active les protéines de la famille Rho, pour qu'elles organisent la polarité cellulaire, en agissant sur l'organisation de l'appareil de mobilité cellulaire • Un des exemples bien étudié est le mouvement chimiotaxique d'une classe de leucocytes sanguins, les neutrophiles, vers une source d'infection bactérienne • Les récepteurs protéiques à la surface des neutrophiles leur permettent de détecter de très faibles concentrations en peptides N formylés, dérivés des protéines bactériennes (seuls les procaryotes commencent la synthèse protéique par la N formylméthionine) • L'utilisation de ces récepteurs permet de guider les neutrophiles vers les cibles bactériennes, du fait de leur capacité à détecter une différence de concentration en peptides diffusibles de seulement 1 p. 100 entre un côté de la cellule et l'autre • Figure 16 86 A
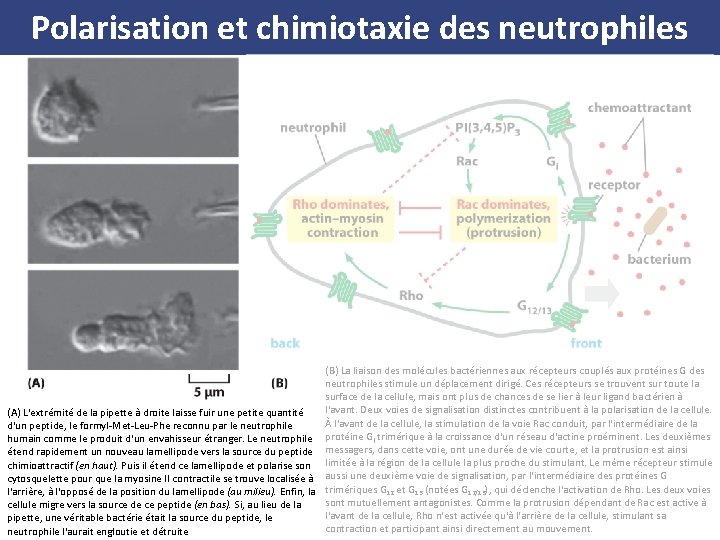
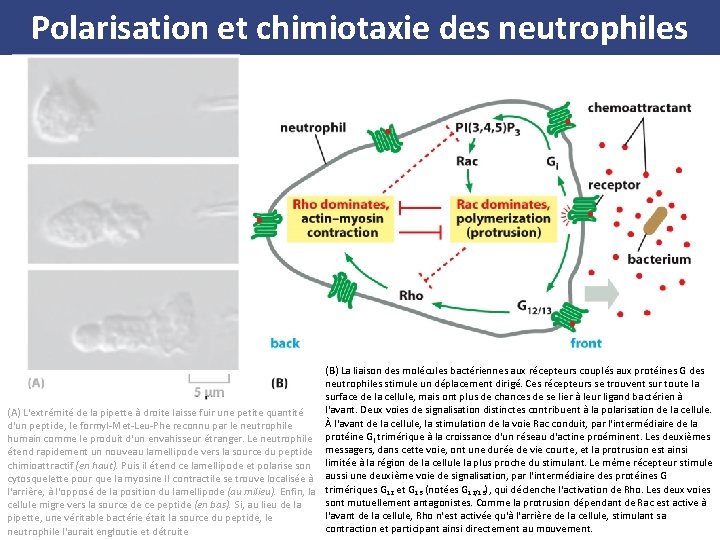
Polarisation et chimiotaxie des neutrophiles (B) La liaison des molécules bactériennes aux récepteurs couplés aux protéines G des neutrophiles stimule un déplacement dirigé. Ces récepteurs se trouvent sur toute la surface de la cellule, mais ont plus de chances de se lier à leur ligand bactérien à l'avant. Deux voies de signalisation distinctes contribuent à la polarisation de la cellule. (A) L'extrémité de la pipette à droite laisse fuir une petite quantité À l'avant de la cellule, la stimulation de la voie Rac conduit, par l'intermédiaire de la d'un peptide, le formyl Met Leu Phe reconnu par le neutrophile humain comme le produit d'un envahisseur étranger. Le neutrophile protéine Gi trimérique à la croissance d'un réseau d'actine proéminent. Les deuxièmes étend rapidement un nouveau lamellipode vers la source du peptide messagers, dans cette voie, ont une durée de vie courte, et la protrusion est ainsi chimioattractif (en haut). Puis il étend ce lamellipode et polarise son limitée à la région de la cellule la plus proche du stimulant. Le même récepteur stimule cytosquelette pour que la myosine II contractile se trouve localisée à aussi une deuxième voie de signalisation, par l'intermédiaire des protéines G l'arrière, à l'opposé de la position du lamellipode (au milieu). Enfin, la trimériques G 12 et G 13 (notées G 12/13), qui déclenche l'activation de Rho. Les deux voies sont mutuellement antagonistes. Comme la protrusion dépendant de Rac est active à cellule migre vers la source de ce peptide (en bas). Si, au lieu de la l'avant de la cellule, Rho n'est activée qu'à l'arrière de la cellule, stimulant sa pipette, une véritable bactérie était la source du peptide, le contraction et participant ainsi directement au mouvement. neutrophile l'aurait engloutie et détruite
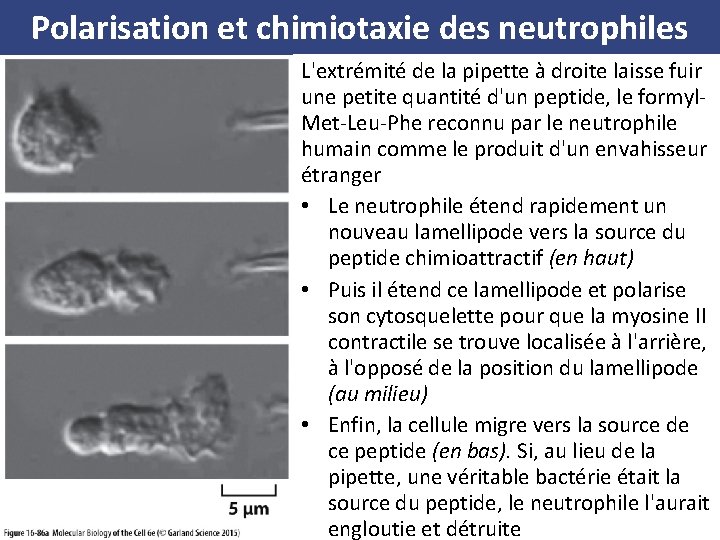
Polarisation et chimiotaxie des neutrophiles L'extrémité de la pipette à droite laisse fuir une petite quantité d'un peptide, le formyl Met Leu Phe reconnu par le neutrophile humain comme le produit d'un envahisseur étranger • Le neutrophile étend rapidement un nouveau lamellipode vers la source du peptide chimioattractif (en haut) • Puis il étend ce lamellipode et polarise son cytosquelette pour que la myosine II contractile se trouve localisée à l'arrière, à l'opposé de la position du lamellipode (au milieu) • Enfin, la cellule migre vers la source de ce peptide (en bas). Si, au lieu de la pipette, une véritable bactérie était la source du peptide, le neutrophile l'aurait engloutie et détruite

Intervention de PI 3 K • Dans ce cas, comme lors de la chimiotaxie similaire d'une amibe, Dictyostelium, vers une source d'AMP cyclique, la liaison du ligand chimioattractif à son récepteur couplé à une protéine G active les phosphoinositides 3 kinases (PI 3 K), • Voir Figure 15 52
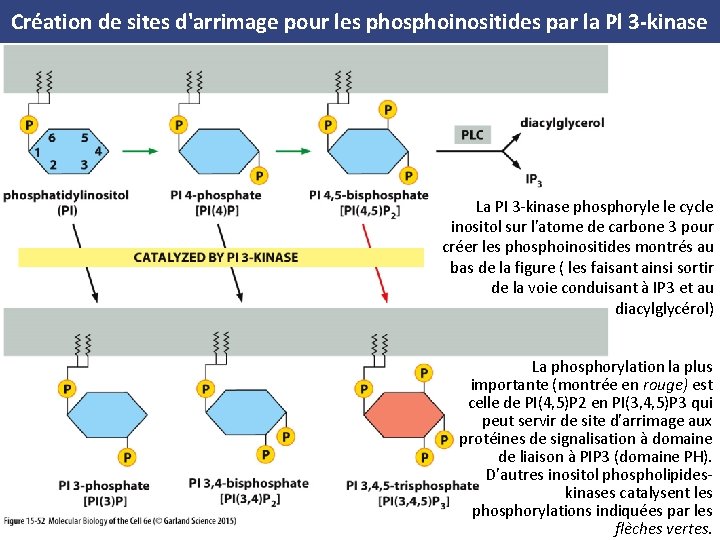
Création de sites d'arrimage pour les phosphoinositides par la Pl 3 kinase La PI 3 kinase phosphoryle le cycle inositol sur l'atome de carbone 3 pour créer les phosphoinositides montrés au bas de la figure ( les faisant ainsi sortir de la voie conduisant à IP 3 et au diacylglycérol) La phosphorylation la plus importante (montrée en rouge) est celle de PI(4, 5)P 2 en PI(3, 4, 5)P 3 qui peut servir de site d'arrimage aux protéines de signalisation à domaine de liaison à PIP 3 (domaine PH). D'autres inositol phospholipides kinases catalysent les phosphorylations indiquées par les flèches vertes.

• PI 3 K produit la molécule de signalisation lipidique [PI(3, 4, 5)P 3], qui active la GTPase Rac en retour • Rac active alors le complexe Arp 2/3 et des lamellipodes se forment • Par un mécanisme inconnu, l'accumulation d'un réseau d'actine polarisée au bord conducteur, augmente encore l'activité de PI 3 K en une boucle de rétrocontrôle positif, renforçant l'induction de la protrusion • PI(3, 4, 5)P 3 qui active Rac, ne peut pas diffuser loin de son site de synthèse, car il est rapidement converti en PI(4, 5)P 2 par une lipide phosphatase active constitutivement • En même temps, la liaison du ligand chimioattractif à son récepteur active une autre voie de signalisation, qui active Rho et augmente la contractilité basée sur la myosine • Ces deux procédés s'inhibent l'un l'autre directement, et le résultat est que – l'activation de Rac domine à l'avant de la cellule, – alors que l'activation de Rho domine à l'arrière • (Figure 16 86 B)
Polarisation et chimiotaxie des neutrophiles (B) La liaison des molécules bactériennes aux récepteurs couplés aux protéines G des neutrophiles stimule un déplacement dirigé. Ces récepteurs se trouvent sur toute la surface de la cellule, mais ont plus de chances de se lier à leur ligand bactérien à l'avant. Deux voies de signalisation distinctes contribuent à la polarisation de la cellule. (A) L'extrémité de la pipette à droite laisse fuir une petite quantité À l'avant de la cellule, la stimulation de la voie Rac conduit, par l'intermédiaire de la d'un peptide, le formyl Met Leu Phe reconnu par le neutrophile humain comme le produit d'un envahisseur étranger. Le neutrophile protéine Gi trimérique à la croissance d'un réseau d'actine proéminent. Les deuxièmes étend rapidement un nouveau lamellipode vers la source du peptide messagers, dans cette voie, ont une durée de vie courte, et la protrusion est ainsi chimioattractif (en haut). Puis il étend ce lamellipode et polarise son limitée à la région de la cellule la plus proche du stimulant. Le même récepteur stimule cytosquelette pour que la myosine II contractile se trouve localisée à aussi une deuxième voie de signalisation, par l'intermédiaire des protéines G l'arrière, à l'opposé de la position du lamellipode (au milieu). Enfin, la trimériques G 12 et G 13 (notées G 12/13), qui déclenche l'activation de Rho. Les deux voies sont mutuellement antagonistes. Comme la protrusion dépendant de Rac est active à cellule migre vers la source de ce peptide (en bas). Si, au lieu de la l'avant de la cellule, Rho n'est activée qu'à l'arrière de la cellule, stimulant sa pipette, une véritable bactérie était la source du peptide, le contraction et participant ainsi directement au mouvement. neutrophile l'aurait engloutie et détruite
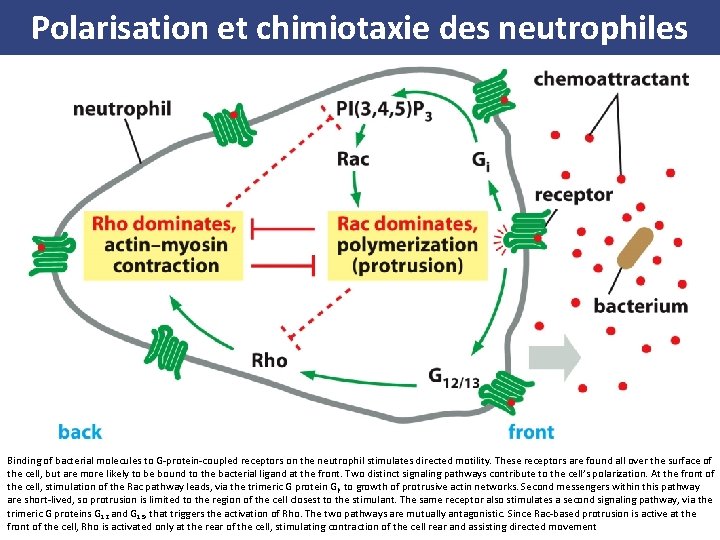
Polarisation et chimiotaxie des neutrophiles Binding of bacterial molecules to G protein coupled receptors on the neutrophil stimulates directed motility. These receptors are found all over the surface of the cell, but are more likely to be bound to the bacterial ligand at the front. Two distinct signaling pathways contribute to the cell’s polarization. At the front of the cell, stimulation of the Rac pathway leads, via the trimeric G protein Gi, to growth of protrusive actin networks. Second messengers within this pathway are short lived, so protrusion is limited to the region of the cell closest to the stimulant. The same receptor also stimulates a second signaling pathway, via the trimeric G proteins G 12 and G 13, that triggers the activation of Rho. The two pathways are mutually antagonistic. Since Rac based protrusion is active at the front of the cell, Rho is activated only at the rear of the cell, stimulating contraction of the cell rear and assisting directed movement

Signaux chimiques • Des signaux chimiques non diffusibles attachés à la matrice extracellulaire ou à la surface des cellules peuvent aussi influencer la direction de la migration cellulaire • Quand ces signaux activent des récepteurs, ils peuvent augmenter l'adhésion cellulaire et la polymérisation dirigée de l'actine • La plupart des migrations cellulaires de longue distance chez les animaux, entre autres la migration des cellules de la crête neurale et les déplacements de cônes de croissance des neurones, dépendent d'une association de signaux diffusibles et non diffusibles, pour diriger le déplacement de la cellule ou du cône de croissance vers leur destination appropriée

PLAN I. III. IV. V. VI. FONCTION ET ORIGINE DU CYTOSQUELETTE ACTINE ET PROTÉINES DE LIAISON À L’ACTINE MYOSINE ET ACTINE MICROTUBULES FILAMENTS INTERMÉDIAIRES ET SEPTINE POLARISATION CELLULAIRE ET MIGRATION CELLULAIRE 1. De nombreuses cellules peuvent ramper sur un support solide 2. La protrusion de la membrane plasmique est actionnée par la polymérisation de l'actine 3. Les lamellipodes contiennent tous les éléments de la machinerie nécessaires à la mobilité de la cellule 4. La contraction de la myosine et l’adhérence cellulaire permettent aux cellules d’avancer 5. Les membres de la famille des protéines Rho contrôlent la polarisation cellulaire 6. Des signaux extracellulaires activent les trois membres de la famille de protéines Rho 7. Des signaux externes peuvent dicter la direction de la migration cellulaire 8. La communication entre les éléments du cytosquelette coordonne la polarisation et la locomotion de la cellule entière

Interconnexion des éléments du cytosquelette • L ’interconnexion des éléments du cytosquelette est indispensable à la migration de la cellule • Bien que ce soit la polarisation de l’actine et la contractilité de la myosine qui soient responsables en premier du mouvement, les septines et les filaments intermédiaires interviennent aussi • Par exemple le réseau de filaments intermédiaires de vimentine s’associent avec les intégrines aux contacts focaux • Des fibroblastes déficients en vimentine présentent une diminution • de leur stabilité mécanique • de leur migration • et de leur capacités contractiles

Interconnexion des éléments du cytosquelette • De plus la perturbation des protéines de liaison qui relient les différents éléments du cytosquelette – Y compris plusieurs plakines – et les protéines KASH • Conduisent à des défauts de polarisation et migration cellulaire • Ainsi des conduites impliquant toute la cellule aussi complexes que la migration nécessitent – les interactions entre les différents systèmes de filaments cytoplasmique – De même que les liens mécaniques avec le noyau

Microtubules • Les cellules utilisent aussi les microtubules pour aider à l’organisation de mouvements permanents dans une direction donnée • Dans de nombreuses cellules en mouvement, la position du centrosome est influencée par la localisation de la polymérisation de l’actine protrusive • L’activation de récepteurs sur le bord conducteur protrusif d’une cellule peut activer localement des protéines motrices de dynéine qui peuvent déplacer le centrosome en tirant sur ses microtubules • Plusieurs effecteurs protéiques en aval de Rac et de Rho modulent directement la dynamique des microtubules • Par exemple, une protéine kinase activée par Rac peut phosphoryler (et ainsi inhiber) la stathmine qui est une protéine de liaison à la tubuline (voir Planche 16 4), stabilisant ainsi les microtubules

Microtubules ↔ actine • • • Mais la dynamique des microtubules agit à son tour sur la réorganisation de l'actine et l’adhérence cellulaire La nucléation d'un grand nombre de microtubules dynamiques se fait à partir du centrosome, et son repositionnement montre que beaucoup de ces microtubules étendent leurs extrémités plus du centrosome vers les régions protrusives de la cellule Des interactions directes avec les microtubules aident à la dynamique de l’adhérence focale des cellules en migration Il se pourrait aussi que les microtubules influencent la formation de filaments d’actine en en libérant Rac GEF qui est lié aux +TIP qui se déplacent sur les extrémités des microtubules en croissance Les microtubules transportent aussi des charges en direction et en provenance des contacts focaux modifiant ainsi leur signalisation et leur désassemblage Ainsi les microtubules renforcent l’information de polarité que le cytosquelette d’actine reçoit du monde extérieur permettant – une réponse fine aux signaux faibles et – au déplacement de persister longtemps dans la même direction

Résumé • Les mouvements des cellules entières, ainsi que la forme et la structure cellulaires à grande échelle, nécessitent l'activité coordonnée des trois systèmes de filaments fondamentaux, ainsi qu'un large éventail de protéines accessoires du cytosquelette, γ compris les protéines motrices • La migration par reptation des cellules — un comportement très répandu et important lors du développement embryonnaire, de la cicatrisation des blessures, de l'entretien des tissus et de la fonction du système immunitaire chez l'animal adulte — est un autre exemple important de cette action coordonnée si complexe du cytosquelette • Pour qu'une cellule migre, elle doit générer et entretenir une polarité structurelle globale qui est influencée par des signaux externes • De plus, la cellule doit coordonner – la protrusion du bord conducteur (par l'assemblage de nouveaux filaments d'actine), – l'adhésion au support de la partie issue de cette protrusion, – et les forces dues aux moteurs moléculaires qui permettent de déplacer le corps cellulaire vers l'avant

Ce que nous ne savons pas • Comment est régulé le cortex cellulaire localement et globalement pour coordonner ses activités aux différents endroits de la surface cellulaire ? • Qu’est ce qui détermine par exemple où doit se former le filopode ? • Comment sont régulées dans le cytoplasme les protéines régulatrices de l’actine pour générer dans la même cellule de nombreux types d’organisation du réseau d’actine différents ? • Se passent ils d’importants phénomènes biologiques à l’intérieur d’un microtubule ? • Comment peut on expliquer qu’il y aient dans le cytoplasme beaucoup de types différents de kinésine et de myosine mais une seule dynéine ? • Des mutations dans les protéines des lamines nucléaires sont à l’origine de nombreuses maladies appelées laminopathies. Qu’est ce qu’on ne comprend pas sur la lamina nucléaire qui serait à l’origine de ce fait ?

Fin

PROBLEMS
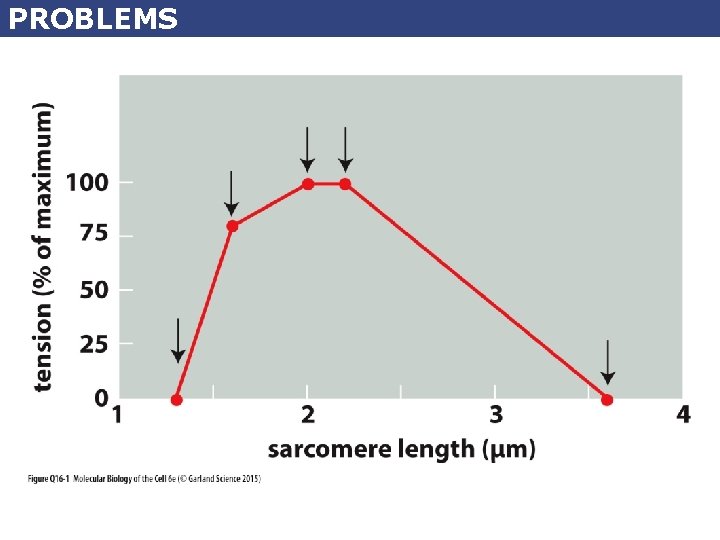
PROBLEMS
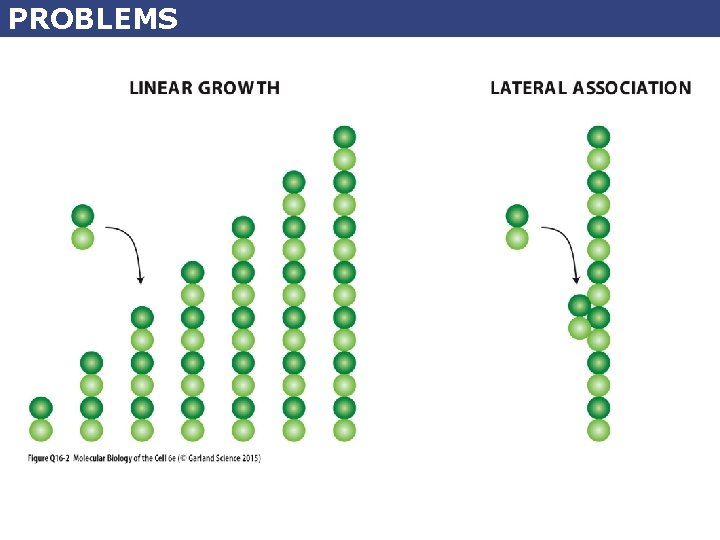
PROBLEMS
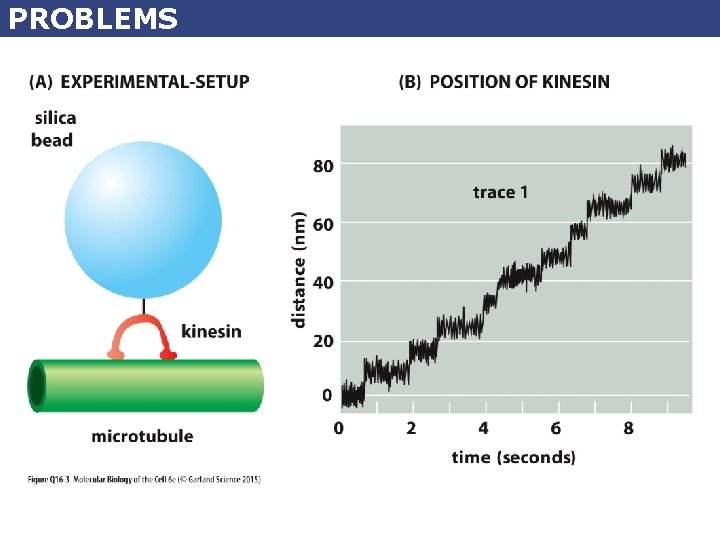
PROBLEMS
- Slides: 124