AKADEMIA TALENTW PRZYRODNICZYCH Przepyw energii sonecznej i obieg

AKADEMIA TALENTÓW PRZYRODNICZYCH Przepływ energii słonecznej i obieg wody w krajobrazie rolniczym. Przepływ wody przez system GRAK I produkcja pierwotna 1. WPŁYW ZASOLENIA GLEBY 2. CZY ROŚLINY GORĄCZKUJĄ? 3. CO TO ZNACZY, ŻE ROŚLINY WIĄŻĄ ENERGIĘ? Prof. Andrzej Kędziora, Dr Zdzisław Bernacki Instytut Środowiska Rolniczego i Leśnego PAN w Poznaniu Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

CEL EKSPERYMENTÓW: 1. Wykazanie znaczenia rozpuszczonych w wodzie glebowej soli dla procesu przepływu wody z gleby do rośliny (pojęcie suszy fizjologicznej) i dla stanu fizjologicznego rośliny Eksperyment: Wpływ zasolenia gleby. 2. Wyjaśnienie związku pomiędzy stanem fizjologicznym rośliny i strumieniem wody przez nią płynącej Eksperyment: Czy rośliny gorączkują?

WPROWADZENIE W całym cyklu obiegu wody w przyrodzie jest niezwykle ważny fragment, W którym istotną rolę odgrywa roślina. Jest to SYSTEM GRAK: GLEBA – ROŚLINA – ATMOSFERA KONTINUUM

Przepływ energii i wody przez system GRAK. Woda znajdująca się w glebie, roślinach i atmosferze jest poddana działaniu różnych sił: sile przyciągania przez cząstki gleby, włókna rośliny, substancje rozpuszczone w wodzie glebowej, siłę grawitacji i siłę ssącą atmosfery. Roślina, aby pobrać wodę z gleby musi wykonać pracę, tym większą im większe są siły utrzymujące wodę. Miarą tej pracy jest potencjał wody, który dla wody czystej nie poddanej działaniu żadnych sił wynosi 0. W każdym innym przypadku potencjał ten jest ujemny. Woda zawsze płynie z miejsc o wyższym potencjale do miejsc, w których ma mniejszy potencjał. Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Woda przez system GRAK płynie zawsze z miejsc o wyższym potencjale do miejsca o potencjale niższym. Ilość wody, która przepływa z gleby do atmosfery przez roślinę jest wprost proporcjonalna do różnicy pomiędzy potencjałem wody na wejściu do roślinny i potencjałem przy wyjściu, (czyli pomiędzy potencjałem wody w glebie, który zależy od wilgotności gleby i potencjałem wody, a właściwie pary wodnej w atmosferze, który zależy od temperatury i wilgotności powietrza) a odwrotnie proporcjonalna do oporów jakie spotyka strumień wody na swej drodze przez roślinę. Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
![Różnica potencjału wody (Δφ) [J kg-1] Gęstość strumienia wody [ kg m-2 s-1] = Różnica potencjału wody (Δφ) [J kg-1] Gęstość strumienia wody [ kg m-2 s-1] =](http://slidetodoc.com/presentation_image/3dfbafb17bbba2522ecd3d29c33f41dc/image-6.jpg)
Różnica potencjału wody (Δφ) [J kg-1] Gęstość strumienia wody [ kg m-2 s-1] = ------------------------Opór (r) [s m-1] Schemat przedstawiający układ oporów i magazynów wody przepływie wody przez glebaroślina-atmosfera kontinuum (GRAK) 2 1 Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Warunkiem utrzymania ciągłości strumienia soków roślinnych płynących przez roślinę jest większa intensywność absorbcji korzeniowej niż intensywność transpiracji. Brak odpowiedniej absorpcji korzeniowej prowadzi do śmierci rośliny w ciągu jednego dnia. Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Pierwszym etapem przepływu wody przez system GRAK 1 jest absorpcja przez korzenie wody z gleby. Jest ona możliwa wtedy, gdy potencjał wody w glebie jest większy niż w korzeniu. Rosnące zasolenie gleby (wzrost stężenia soli w roztworze glebowym powoduje spadek potencjału wody glebowej i zmniejszanie się gęstości strumienia wody wnikającej do korzenia. Po wzroście stężenia soli w roztworze glebowym powyżej poziomu jaki jest w wakuolach. Roślina nie pobiera wody, spowalnia wzrost, a w końcu umiera. Eksperyment 1 ma pomóc w zrozumieniu tego zjawiska. Drugim etapem jest przepływ wody z korzenia, poprze szyję 2 korzeniową do naczyń. Jeżeli roślina porażona jest chorobą grzybową powodującą zatykanie naczyń w szyi korzeniowej, to opory przepływu rosną, spada strumień wody płynący do liści, spada tempo transpiracji, roślina jest mocno ogrzewana prze słońce i rośnie jego temperatura. Ostatecznie roślina umiera. Eksperyment 2 ma pomóc w zrozumienia tego zjawiska. Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Eksperyment 1 – Wpływ zasolenia gleby. Cel eksperymentu. Odpowiedź na pytania: 1. Jakie znaczenie dla przepływu wody przez rośliny ma zasolenie gleby. 2. Jaki jest próg zasolenia tolerowany przez wybrane rośliny. Etap I – Zbieranie informacji: Uczniowie gromadzą informacje na temat siły ssącej gleby i jaką rolę w jej kształtowaniu spełnia stężenie soli w roztworze glebowym. Etap II ‑ Planowanie doświadczenia: Uczniowie przygotowują propozycje przeprowadzenia doświadczeń wykazujących wpływ stopnia zasolenia gleby na transpirację roślin i w efekcie na wzrost i rozwój. Etap III Przeprowadzenie doświadczeń laboratoryjnych. Porównanie reakcji halofitów (rośliny tolerancyjne wobec zasolenia) i halofobów (rośliny wrażliwe na zasolenie. Etap IV Seminarium – dyskusja, wyciągnięcie wniosków i przygotowanie raportu

Etap I. Zbieranie informacji: 1. Uczniowie korzystając z literatury i internetu zapoznają się ze zjawiskiem absorpcji korzeniowej i czynnikami decydującymi o mechanizmie przepływu wody z gleby do korzeni. Szczególną uwagę poświęcają roli zasolenia gleby w kształtowania siły ssącej gleby i potencjału wody w glebie. Uczą się jak obliczać ciśnienie osmotyczne roztworu glebowego na podstawie stężenia molowego tego roztworu. 2. Uczniowie zapoznają się z rodzajem roślin o różnym stopniu odporności na zasolenie gleby: gatunki roślin tolerujących wysokie zasolenie (halofity) i gatunki rośnin nie znoszących zasolenia (halofoby).

Etap II ‑ Planowanie doświadczenia: Uczniowie przygotowują propozycje przeprowadzenia doświadczeń wykazujących wpływ stopnia zasolenia gleby na transpirację roślin i w efekcie na wzrost i rozwój. 1. Na podstawie wiadomości uzyskanych w pierwszym etapie wybierają rośliny do doświadczenia; halofoby ( na schemacie doświadczenia oznaczone literą A) i halofity (Litera B). 2. Przygotowują (zgodnie z instrukcją zawartą w projekcie eksperymentu) po 6 wazonów z każdej grupy roślin. Dwa wazony z każdej grupy stanowić będą próbę kontrolną, a pozostałe 4 będą służyć do oceny stopnia zasolenia na wzrost i rozwój roślin. W każem wazonie instalujemy tensjometr. 3 W tabeli obserwacyjnej zapisujemy pod numerem „pomiar zerowy” zapisujemy wagi poszczególnych wazonów, z dokładnością do 10 gramów. Pod tabelą zapisujemy wartości wilgotności gleby i wartość siły ssącej Sm.
![Arkusz obserwacyjny Waga wazonu [kg] z dokładnością do 10 grama Data pomiar u Nr Arkusz obserwacyjny Waga wazonu [kg] z dokładnością do 10 grama Data pomiar u Nr](http://slidetodoc.com/presentation_image/3dfbafb17bbba2522ecd3d29c33f41dc/image-12.jpg)
Arkusz obserwacyjny Waga wazonu [kg] z dokładnością do 10 grama Data pomiar u Nr pomiaru Kontrolne A AA Halofoby B BB A 1 A 2 Halofity A 3 A 4 B 1 B 2 B 3 B 4
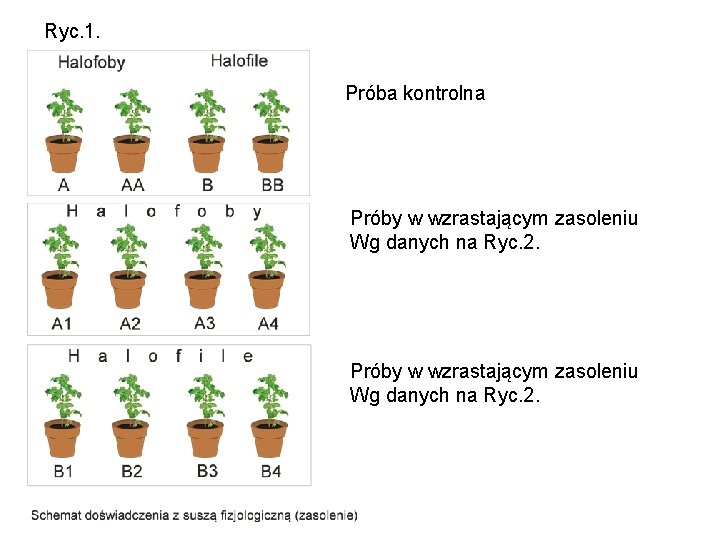
Ryc. 1. Próba kontrolna Próby w wzrastającym zasoleniu Wg danych na Ryc. 2.


Etap III Przeprowadzenie doświadczeń laboratoryjnych. Porównanie reakcji halofitów (rośliny tolerancyjne wobec zasolenia) i halofobów (rośliny wrażliwe na zasolenie. Doświadczenie prowadzone jest do chwili zamarcia roślin rosnących na najsilniej zasolonej glebie lub przez miesiąc. Szczegółówa instrukcja umieszczone jest w opisie projektu. Etap IV. Opracowanie wyników doświadczenia. Analiza statystyczna i sformułowanie wniosków. Sporządzenie raportu zawierającego część opisową, tabelaryczną i graficzną.

Eksperyment 2 – Czy rośliny gorączkują? . Cel eksperymentu. Odpowiedź na pytania: 1. Jak jest rola transpiracji dla utrzymania stanu termicznego roślin. 2. Czy chora roślina może gorączkować. Etap I - Uczniowie gromadzą informacje z literatury i Internetu na temat gospodarki wodnej roślin i znaczenia transpiracji. Etap II ‑ Planowanie doświadczenia: Uczniowie przygotowują propozycje przeprowadzenia doświadczeń wykazujących wpływ transpiracji na stan termiczny roślin, czynników wpływających na intensywność transpiracji, wpływu wybranych patogenów na transpirację i temperaturę roślin. Etap III - Przeprowadzenie doświadczeń laboratoryjnych: Ocena zmian temperatury i intensywności transpiracji, w różnych warunkach termicznych i wilgotności. Porównanie temperatury roślin zdrowych i zakażonych. Etap IV - Opracowanie wyników doświadczenia, analiza statystyczna i sformułowanie wniosków. Sporządzenie raportu zawierającego część opisową, tabelaryczną i graficzną.

Etap I - Zbieranie informacji: Uczniowie korzystając z literatury i internetu zapoznają się ze zjawiskiem transpiracji i czynnikami decydującymi o mechanizmie przepływu wody z rośliny do atmosfery. Szczególną uwagę poświęcają na zależność wielkości strumienia wody płynącego przez roślinę od stanu fitosanitarnego rośliny (choroby roślin). Uczą się tego jakie znaczenie dla procesu ewapotranspiracji ma struktura bilansu cieplnego ekosystemu.

Etap II ‑ Planowanie doświadczenia. Uczniowie przygotowują propozycje przeprowadzenia doświadczeń wykazujących wpływ transpiracji na stan termiczny roślin, czynników wpływających na intensywność transpiracji, wpływu wybranych patogenów na transpirację i temperaturę roślin. 1. Wybór roślin przydatnych do wykonania eksperymentu. Wybieramy rośliny uprawne, które są podatne na choroby grzybowe atakujące szyję korzeniową roślin. 2. Przygotowujemy zestaw 8 wazonów. W czterech umieszczamy rośliny zdrowe, a w czterech zainfekowane grzybami. Cztery wazony (Ryc. 1) przeznaczamy do przeprowadzenia eksperymentu, a pozostałe cztery stanowią rezerwę na wypadek zniszczenia jakiegoś wazonu z serii podstawowej. Wszystko wykonujemy zgodnie z instrukcja zamieszczoną w projekcie eksperymentu. 3. W Każdym wazonie umieszczamy tensjometr (T) i rurkę do nawadniania (R).

Ryc. 1. Schemat doświadczenia Warianty: W 1. Roślina zdrowa przy optymalnej wilgotności gleby W 1. Roślina zdrowa, ale ograniczony dostęp do wody. W 1. Roślina zarażona grzybem, ale przy optymalnej wilgotności gleby W 1. Roślina chora i słabo nawadniana.

Etap III – Przeprowadzenie eksperymentu. Obserwacje prowadzone są w następujący sposób i notowane w arkuszu Excel Ryc. 2. : 1. Numeruje się kolejne dni poczynając od pierwszego dnia rozpoczęcia obserwacji. 2. W pierwszym dniu notuje się: wagę wazonu, wskazania tensjometru i temperaturę roślin (korzystamy z pirometru). 3. W kolejnych dniach (zawsze o tej samej porze, którą ustali nauczyciel) odczytujemy wagę wazonów i wskazania tensjometrów, oraz temperaturę radiacyjną roślin. 4. Uzupełniamy wagę wazonów do wagi wyjściowej (poprzez dolanie odpowiedniej masy wody, innej w każdym wariancie). 5. Sporządzamy dokumentację zmian morfologicznyh roślin wykonując zdjęcia co 4 dni. Obserwacje prowadzimy do czasu zamarcia roślin chorych.
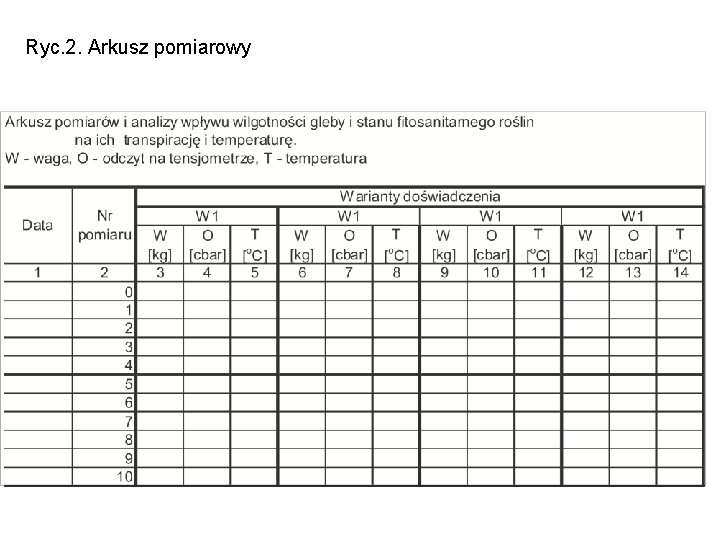
Ryc. 2. Arkusz pomiarowy

Etap IV. Opracowanie wyników doświadczenia. Analiza statystyczna i sformułowanie wniosków. Sporządzenie raportu zawierającego część opisową, tabelaryczną i graficzną.

Eksperyment III Co to znaczy, że rośliny wiążą energię Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
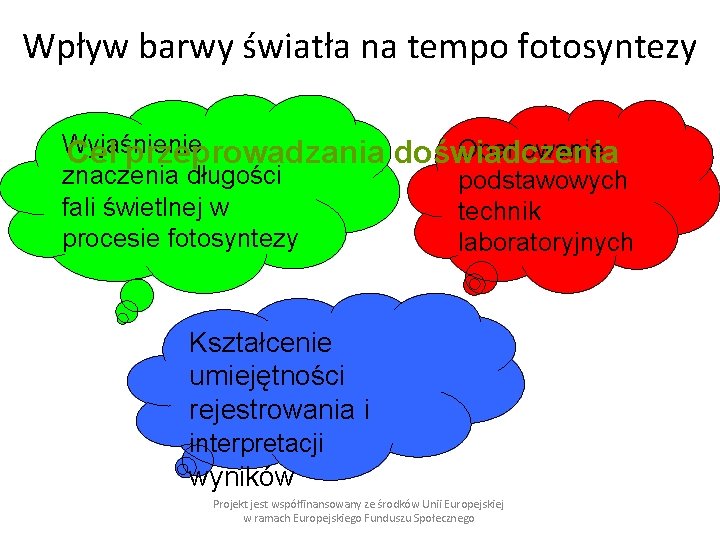
Wpływ barwy światła na tempo fotosyntezy Wyjaśnienie Cel przeprowadzania znaczenia długości fali świetlnej w procesie fotosyntezy Opanowanie doświadczenia podstawowych technik laboratoryjnych Kształcenie umiejętności rejestrowania i interpretacji wyników Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap I: Zbieranie informacji koniecznych do przeprowadzenia doświadczeń laboratoryjnych • Uczniowie gromadzą informacje z literatury i Internetu na temat czynników (w szczególności światła: intensywności i długości fali świetlnej) wpływających na proces fotosyntezy. Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap II: Planowanie doświadczenia • Uczniowie poinformowanie przez nauczyciela (prowadzącego) o możliwościach sprzętowych przygotowują propozycje przeprowadzenia doświadczeń wykazujących wpływ intensywności światła i długości fali świetlnej na tempo fotosyntezy moczarki kanadyjskiej: . Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap III: Wybór optymalnych wariantów eksperymentu Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Przewidywane wyniki doświadczenia O 2 O 2 Wielkość liter na schematach doświadczenia ilustruje przewidywany wynik – różnice w ilości wydzielonego tlenu. Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
Etap IV: Raport z części laboratoryjnej Arkusz wyników (przykład wypełnienia) Barwa światła Rezultat (ilość pęcherzyków tlenu) białe liczne czerwone nieliczne niebieskie nieliczne zielone brak Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Doświadczenie polowe Ocena tempa przyrostu biomasy w zależności od warunków siedliska Cel przeprowadzania doświadczenia Kształcenie Opanowanie umiejętności posługiwania się prostym sprzętem laboratoryjnym podstawowych technik pracy w terenie Kształcenie umiejętności wykonywania i rejestrowania pomiarów Kształcenie umiejętności interpretowania rezultatów (wyszukiwania i interpretowania zależności) Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap V: Zbieranie informacji koniecznych do przeprowadzenia doświadczeń polowych Jak oceniać produkcję pierwotną? Metody teledetekcyjne Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap V: Zbieranie informacji koniecznych do przeprowadzenia doświadczeń polowych Jak oceniać produkcję pierwotną? Pomiar fotosyntezy Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap V: Zbieranie informacji koniecznych do przeprowadzenia doświadczeń polowych Jak oceniać produkcję pierwotną? Oceny bezpośrednie w terenie Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap V: Zbieranie informacji koniecznych do przeprowadzenia doświadczeń polowych Jak obliczyć produkcję pierwotną? NPP = Bfin – B 0 +ΔD +M +Rfin – R 0 +ΔV +W +Y NPP – Całkowita produkcja pierwotna Bfin - Biomasa roślin na końcu okresu wegetacyjnego B 0 - Biomasa roślin na początku okresu wegetacyjnego ΔD - Ilość biomasy zamierającej w trakcie sezonu wegetacyjnego M - Martwa biomasa rozkładająca się w trakcie sezonu wegetacyjnego Rfin - Biomasa korzeni na końcu okresu wegetacyjnego R 0 - Biomasa korzeni na początku okresu wegetacyjnego ΔV - Ilość biomasy korzeni zamierającej w trakcie sezonu wegetacyjnego M - Biomasa martwychkorzeni rozkładająca się w trakcie sezonu wegetacyjnego Y - Biomasa opuszczająca ekosystem, np. . plon Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap VI: Planowanie doświadczeń polowych: Wybór powierzchni badawczych W dowolnym fragmencie krajobrazu wybieramy powierzchnie badawcze lokalizując je w ekosystemach różniących się warunkami siedliska, zwłaszcza wilgotnością, np. : pole, łąka, dolina rzeki (rowu) Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap VII: Wybór optymalnych wariantów doświadczeń polowych Uproszczona ocena produkcji pierwotnej W wybranych ekosystemach wyznaczamy, przy pomocy metalowych ramek, kilka par poletek badawczych. Z jednego poletka, z każdej pary pobieramy wszystkie rośliny, martwe części roślin i ściółkę. Zebrany materiał selekcjonujemy w pracowni Sąsiednie poletko pozostawiamy nienaruszoną. Materiał zostanie pobrany z niego w identyczny sposób w kolejnym terminie. Korzenie pobieramy przy pomocy próbnika glebowego. W pracowni przebieramy i płuczemy korzenie. Cały pobrany materiał suszymy w temperaturze 80 o. C, przez 48 h i ważymy. Produkcję pierwotną obliczamy według zaprezentowanych wcześniej wzorów Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Ocena wilgotności gleby Zestaw cylindrów Kopeckiego. Każdy cylinder posiada wybity numer umożliwiający jego identyfikację w terenie i w laboratorium. Pojemność cylinderka to 100 cm 3. Ułatwia to obliczenie wilgotności Cylinderek wciskamy w glebę, pobierając w ten sposób nienaruszoną próbkę gleby o objętości 100 cm 3. Próbkę gleby, w zamkniętym cylinderku przenosimy do laboratorium, ważymy (po otwarciu wieczka, a następnie suszymy) w temperaturze 80 o. C, do stałej masy (w praktyce można przyjąć czas suszenia 48 h). Wysuszoną próbkę ponownie ważymy. Różnica masy cylinderka przed i po wysuszeniu to zawartość wody (w gramach) w 100 cm 3 gleby, a więc wilgotność objętościowa w procentach Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Etap VIII Wyciągnięcie wniosków, przygotowanie raportu Arkusz wyników Rodzaj materiału Masa (I etap) Masa (II etap) Żywe rośliny Martwe części roślin Ściółka Korzenie Produkcja pierwotna netto (przybliżona) Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego Różnica

Etap VIII Wyciągnięcie wniosków, przygotowanie raportu Arkusz wyników Ekosystem Produkcja pierwotna Wilgotność gleby pole łąka brzeg rowu Wnioski: Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego

Dziękuję za uwagę Projekt jest współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
- Slides: 40