Agua corporal Relacin con el peso corporal total















![Acidosis metabólica Anion gap (normal 8 -16 m. Eq/l) ([Na+]+[K+]) – ([Cl-] +[HCO 3 Acidosis metabólica Anion gap (normal 8 -16 m. Eq/l) ([Na+]+[K+]) – ([Cl-] +[HCO 3](https://slidetodoc.com/presentation_image_h2/2782280f7237f8aed2ae3d5d15e414c8/image-21.jpg)




- Slides: 27

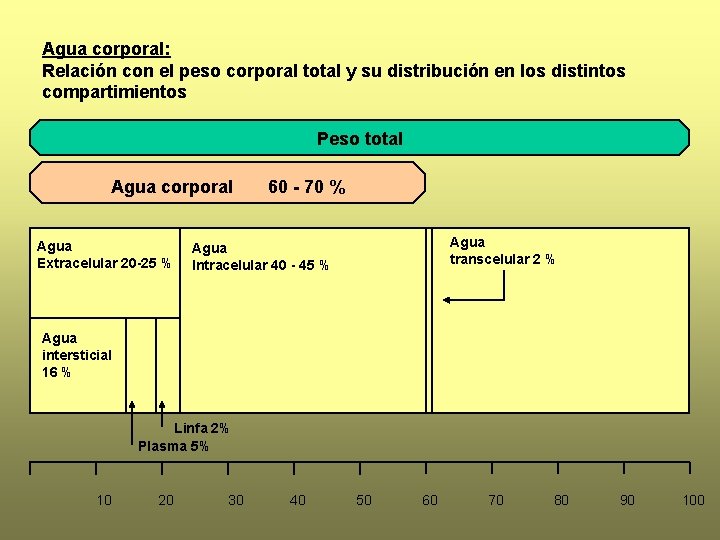
Agua corporal: Relación con el peso corporal total y su distribución en los distintos compartimientos Peso total Agua corporal Agua Extracelular 20 -25 % 60 - 70 % Agua transcelular 2 % Agua Intracelular 40 - 45 % Agua intersticial 16 % Linfa 2% Plasma 5% 10 20 30 40 50 60 70 80 90 100

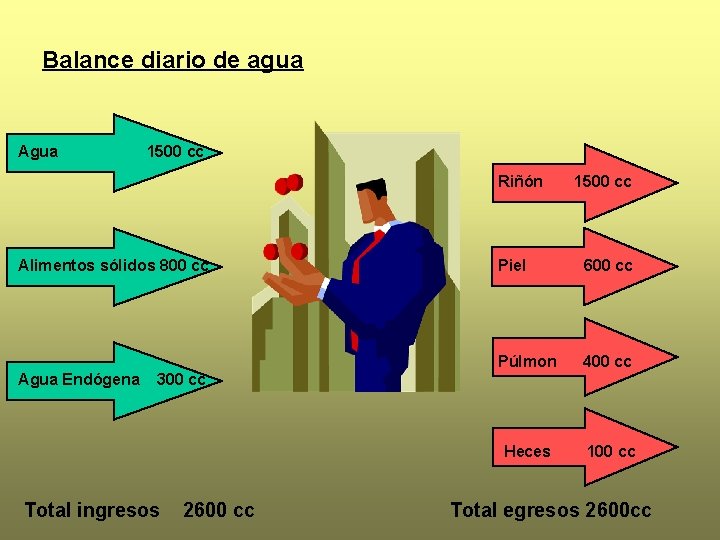
Balance diario de agua Agua 1500 cc Riñón Alimentos sólidos 800 cc Agua Endógena 1500 cc Piel 600 cc Púlmon 400 cc Heces 100 cc 300 cc Total ingresos 2600 cc Total egresos 2600 cc

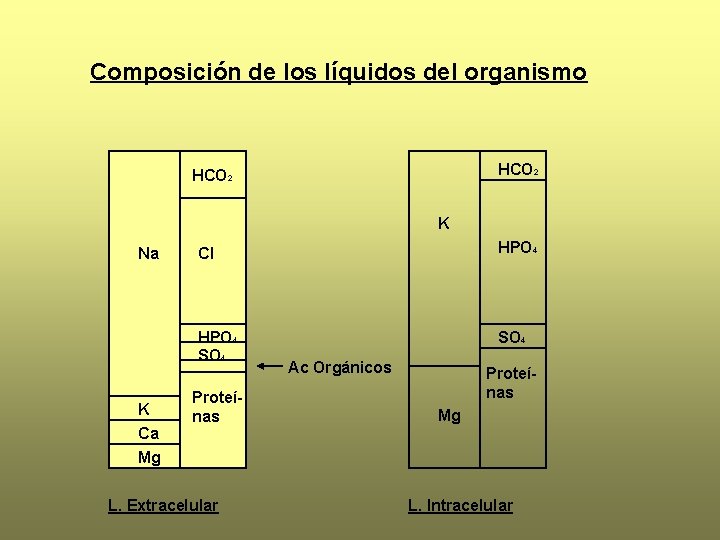
Composición de los líquidos del organismo HCO 2 K Na K Ca Mg Cl HPO 4 SO 4 Proteínas L. Extracelular Ac Orgánicos Proteínas Mg L. Intracelular

• El Na+ es el catión mas importante del L. E. C. • El agua difunde libremente a través de las membranas. • El organismo trata de mantener constante la concentración de cada uno de sus compartimentos *

Mecanismos utilizados para regular el agua y el sodio: • Mecanismo de la sed • Secreción de aldosterona (variaciones de volumen) • Secreción de H. A. D. (variaciones de concentración) *

Clasificación de las deshidrataciones: • Según la intensidad • Leve • Moderada • Severa • Según el tipo • Isotónicas (sales = agua) • Hipotónicas (sales > agua) • Hipertónicas (sales < agua) *

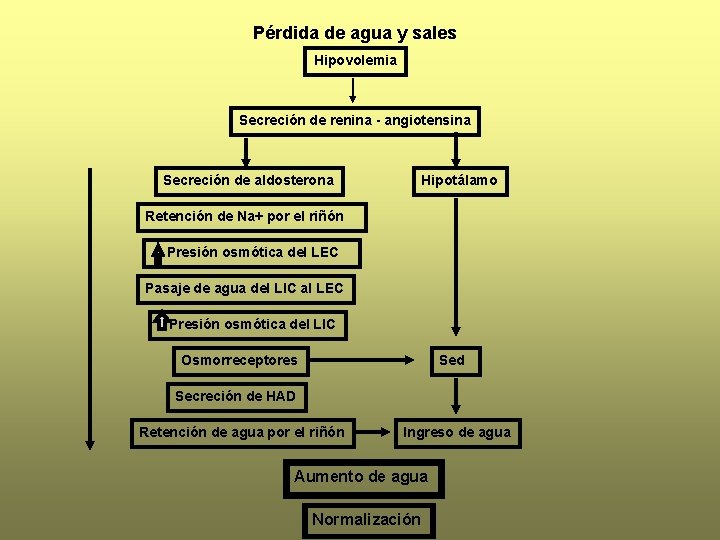
Pérdida de agua y sales Hipovolemia Secreción de renina - angiotensina Secreción de aldosterona Hipotálamo Retención de Na+ por el riñón Presión osmótica del LEC Pasaje de agua del LIC al LEC Presión osmótica del LIC Osmorreceptores Sed Secreción de HAD Retención de agua por el riñón Ingreso de agua Aumento de agua Normalización

Hiponatremia Concepto: Es la disminución de la concentración normal de sodio en el espacio intravascular. Etiologías: Patologías renales Pérdidas aumentadas por tubo digestivo Hiperhidratación Deshidratación hipotónica Fisiopatología: Disminución de la presión osmótica del plasma Consecuencias: Hipovolemia Disminución de la precarga Hipotensión Aumento de la viscosidad de la sangre Pudiendo llegar al cuadro de shock. *

Hipernatremia Concepto: Etiologías: Es el aumento de la concentración normal de sodio en el espacio intravascular. Generalmente son raros de observar y se presentan en pacientes con patologías sistémicas graves asociadas. Consecuencias: Aumento de la presión osmótica del plasma

Hipokalemia o hipopotasemia Concepto: Es la disminución de la concentración normal de potasio en el espacio intravascular. Etiologías: Disminución de la ingesta (raro). Redistribución por pasaje del LEC al LIC (insulina, alcalosis, etc. ). Aumento de las pérdidas (sistema digestivo, patología renal, diuréticos) Consecuencias: Alteración de las propiedades electrofisiológicas de las células Alteraciones de la síntesis de ARN y proteínas Alteraciones en el mantenimiento del volumen intracelular.

Hiperkalemia o hiperpotasemia Concepto: Es el aumento de la concentración normal de potasio en el espacio intravascular. Etiologías: Aumento de la ingesta (raro). Redistribución por pasaje del LIC al LEC (acidosis, hemólisis, destrucción de tejidos, etc. ). Aumento de la retención (patología renal) Consecuencias: Alteración de las propiedades electrofisiológicas de las células Alteraciones de la síntesis de ARN y proteínas Alteraciones en el mantenimiento del volumen intracelular.

Hipercalcemia Aumento en la concentración de calcio: Causas: Exceso de PTH Exceso de vitamina D Tumores Consecuencias: Náuseas, vómitos y estreñimiento Hipotonía Acortamiento del QT y arritmias cardíacas.

Hipocalcemia Disminución en la concentración de calcio: Causas: IRA o IRC Déficit o resistencia a la PTH Déficit de vitamina D Hiperfosfatemia grave Malabsorción Consecuencias: Espasmo laríngeo Convulsiones Prolongación del QT Cataratas.

Equilibrio ácido - básico Ph: Logaritmo negativo de la concentración de hidrogeniones Valor Normal: 7. 40 +/- 0. 40 (Eudremia)

Equilibrio ácido - básico Variaciones significativas del Ph ocasionan trastornos en la fisiología cardiaca, ósea, en la disponibilidad de O 2 a los tejidos, etc. Y se ha demostrado que Ph <6. 80 ó > 7. 80 implican una alta mortalidad.

Equilibrio ácido - básico Acidemia • tono vascular. • de la contractilidad miocárdica. • Trastornos en la conducción A-V, (arritmias). • Ca intramiocárdico, en reposo. • liberación del Ca (alteraciones en la relajación ventricular). • Depresor del SNC. • de la calcemia, remoción ósea, • Vasodilatación cerebral absorción de fosfatos

Equilibrio ácido - básico Alcalemia • irritabilidad miocárdica: arritmias refractarias a drogas • del calcio iónico con aparición de parestesias y tetania • del tono vascular cerebral • Desviación de la curva de disociación de la Hb a la Izquierda • Vasoespasmo coronario. • umbral convulsivo. Ondas amplias y lentas en el EEG

Equilibrio ácido - básico • Sistemas buffer químicos • Sistema respiratorio • Sistema renal

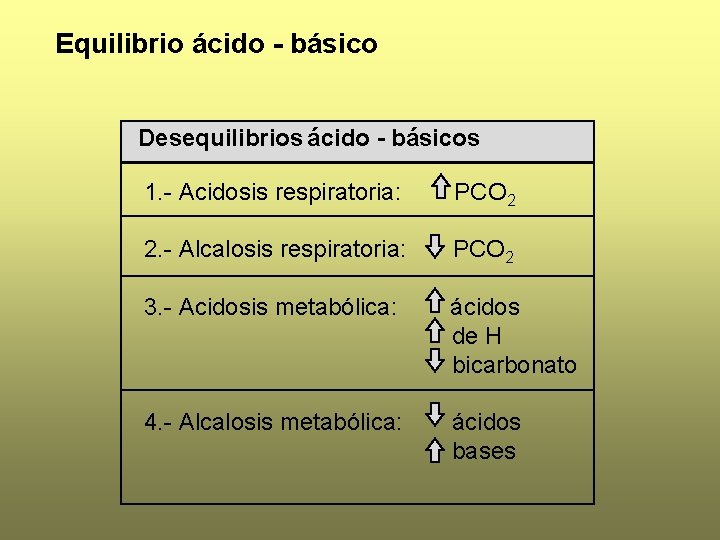
Equilibrio ácido - básico Desequilibrios ácido - básicos 1. - Acidosis respiratoria: PCO 2 2. - Alcalosis respiratoria: PCO 2 3. - Acidosis metabólica: ácidos de H bicarbonato 4. - Alcalosis metabólica: ácidos bases

Acidosis Respiratoria: CO 2 (hipoventilación) Alcalosis Respiratoria: CO 2 (hiperventilación)
![Acidosis metabólica Anion gap normal 8 16 m Eql NaK Cl HCO 3 Acidosis metabólica Anion gap (normal 8 -16 m. Eq/l) ([Na+]+[K+]) – ([Cl-] +[HCO 3](https://slidetodoc.com/presentation_image_h2/2782280f7237f8aed2ae3d5d15e414c8/image-21.jpg)
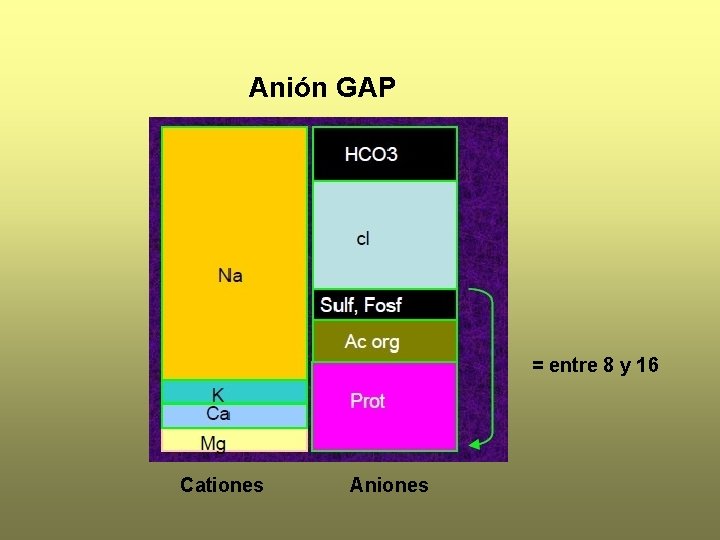
Acidosis metabólica Anion gap (normal 8 -16 m. Eq/l) ([Na+]+[K+]) – ([Cl-] +[HCO 3 -]) [ cationes] = [aniones] Anion gap representa los aniones no medidos (sulfatos, fosfatos, Ac. Libres, proteínas, etc. )

Anión GAP = entre 8 y 16 Cationes Aniones

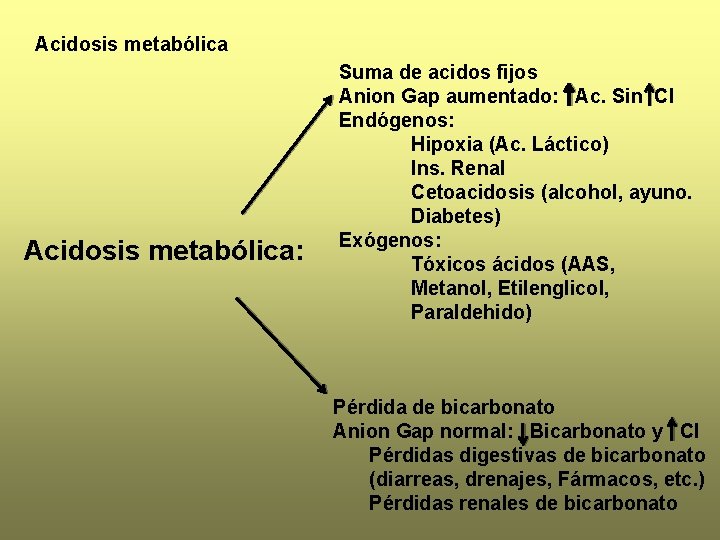
Acidosis metabólica: Suma de acidos fijos Anion Gap aumentado: Ac. Sin Cl Endógenos: Hipoxia (Ac. Láctico) Ins. Renal Cetoacidosis (alcohol, ayuno. Diabetes) Exógenos: Tóxicos ácidos (AAS, Metanol, Etilenglicol, Paraldehido) Pérdida de bicarbonato Anion Gap normal: Bicarbonato y Cl Pérdidas digestivas de bicarbonato (diarreas, drenajes, Fármacos, etc. ) Pérdidas renales de bicarbonato

Anión GAP = entre 8 y 16 Cationes Aniones

Acidosis metabólica Se debe determinar un ionograma urinario (Na + K) – Cl Valor normal = 0 o ligeramente positivo y un Ph urinario > 5 = pérdida de bicarbonato por orina < 5 = pérdida por aparato digestivo

Alcalosis metabólica 1. Pérdida de H+: Pérdida gastrointestinal Pérdida renal Desplazamiento intracelular de protones 2. Exceso de HCO 3 -: Transfusiones masivas Administración excesiva de HCO 3 Sindrome de leche y alcalinos 3. Alcalosis por disminución de volumen: Diuréticos Cloridorrea Vómitos, diarreas, etc.
