Agrobacterium tumefaciens tarafndan bitkilerde tmr oluumunun molekler mekanizmas

Agrobacterium tumefaciens tarafından bitkilerde tümör oluşumunun moleküler mekanizması Sebahattin ÖZCAN Bu bölümdeki tüm bilgiler Özcan vd. 2002’den alınmıştır.

Bitkilere Gen Aktarım Teknikleri l 1. Agrobacterium l 2. Doğrudan Gen Aktarım Teknikleri l a. Biyolistik (Partikül Tabancası) l b. Mikroenjeksiyon l c. Protoplastlara Gen Aktarımı i. Kimyasal Yöntemler l ii. Elektroparosyon l

Agrobacterium l l Bitkilerde tümör oluşumuna Agrobacterium bakterisinin neden olduğuna ilk defa Amerikalı bilim adamları Smith ve Towsend (1907) bildirmişlerdir. Agrobacterium, Rhizobiaceae familyasından, toprakta yaşayan gram-negatif bir bakteridir. İki çenekli (dikotiledon) bitkilerde A. tumefaciens kök boğazı uruna, A. rhizogenes ise saçak kök oluşumuna neden olmaktadır. Ur (tümör) oluşumuna bazı tek çenekli bitkilerde de rastlanmaktadır.

Agrobacterium l l l Hastalık önce, gövde ve köklerin bilhassa toprak yüzeyine yakın bölgelerinde küçük ve aşırı büyümeler şeklinde görülür. Gelişmenin erken döneminde tümörler az çok küremsi, beyaz ya da ten rengi ve oldukça yumuşaktır. Daha sonra, bu hücrelerin ölümü ve çürümesi sonucu dış dokular kahverengi veya siyaha döner. A. rhizogenes ile enfeksyion sonucunda da enfeksiyon bölgesinden saçak kökler oluşmaktadır.

Agrobacterium tumefaciens tarafından tümör (ur) oluşumu

Agrobacterium rhizogenes tarafından tümör (ur) oluşumu

Tümör ve Saçak Kök Oluşumu l l White ve Braun (1941) yılında bu hastalığın çok sıra Oksin ve sitokinin grubu bitki hormonları, bitki hücrelerinin in vitro şartlarda çoğalarak kallus oluşturabilmeleri için mutlak gereklidirler. Oysa, Agrobacterium tarafından bir kez tümör veya saçak kök oluşumu başlatıldıktan sonra, tümör veya saçak kökler izole edilerek steril kültür koşullarında, bakteri olmadan ve yardımcı hormonlara ihtiyaç duymadan büyütülebilmektedir. Yapılan araştırmalarda, enfeksiyon sonucu oluşan dokunun normal bitkide bulunmayan bazı aminoasitleri ve opin’ler olarak bilinen şeker türevlerini sentezlediği görülmüştür

Tümör ve Saçak Kök Oluşumu Bu bileşikler bakteri tarafından karbon ve nitrojen kaynağı olarak kullanılmaktadır. Tümörlü dokunun sentezlediği opinlerin türleri (nopalin, oktopin, agrosinopin, agropin gibi) enfekte eden bakteri hatları tarafından belirlenir. Böylece, Agrobacterium hatları oktopin ve napolin olarak iki ana grup altında toplanmaktadır.




T-DNA Aktarımında Gerekli Olan Ögeler l T-DNA (Transferred-DNA) bölgesi l Virülens (vir) bölgesi l Bakteri kromozomlarında bulunan genler.


T-DNA Bölgesi l l l T-DNA bölgesi çift sarmal Ti veya Ri plazmidi üzerinde bulunan ve bakteriden bitki hücresine aktarılarak bitkinin genomuyla birleşen küçük bir DNA parçasıdır. Enfeksiyon sonucunda bitkinin genomik DNA'sına bir veya birden fazla T-DNA aktarılabilmektedir. Oktopin ve nopalin tipi T-DNA’lar genelde birbirlerine benzemekle birlikte, bazı özellikler bakımından önemli farklılıklar gösterirler. Oktopin tipi plazmidler, bitkinin genomuyla bağımsız olarak birleşebilen TL (left/sol), TC (center/merkez) ve TR (right/sağ) olarak simgelenmiş T-DNA bölgelerine sahiptir Öte yandan, nopalin tipi plazmidlerde ise tek bir T–DNA bölgesi bulunmaktadır.

T-DNA Bölgesi l l Her iki plazmid tipinin 23 kb büyüklüğündeki TDNA'larında 13 adet gen belirlenmiştir. Oktopin tipi plazmidlerin, 13. 2 kb uzunluğundaki TLDNA'ları üzerinde 8, 7. 9 kb uzunluğundaki TR-DNA'larında ise 5 gen taşıdıkları ve TL-DNA bölgesi ile nopalin tipi plazmidin T-DNA'sı arasında büyük benzerlikler olduğu saptanmıştır. Ayrıca, oktopin tipi plazmidlerde bulunan TR bölgesi tümör oluşumu için mutlak gerekli değilken, TL-DNA kısmının oktopin sentezini kodlayan bir geni taşıdığı bilinmektedir. Diğer taraftan, nopalin türü plazmidlerdeki T-DNA bölgesinin nopalin (nos) ile agrosinopin (acs) sentezini sağlayan genleri taşıdığı, oktopin plazmidinin TR bölgesindeki iki genin mannopin sentezi için gerekli olduğu ve diğer bir gen ürününün ise mannopinin agropine dönüşümünü sağladığı bildirilmektedir.

T-DNA Bölgesi l l Bunların dışında, T-DNA bölgesinde bitkilerde oksin ve sitokininlerin üretimini katalize eden enzimleri kodlayan iaa. M (aux 1 veya tms 1), iaa. H (aux 2 veya tms 2) ve ipt (cyt veya tmr) gibi genlerin de bulunduğu tespit edilmiştir. İaa. M geni, L-triptofanın indol-asetamide dönüşümünü katalize eden mono-oksijenaz enzimini kodlarken, iaa. H geni ise hidrolitik etkisiyle indol asetamidi indol-3 -asetik asite çeviren indol asetamid hidrolazı kodlamaktadır.

T-DNA Bölgesi l l l İpt geninin ise sitokinin üretiminde görev alan dimetilalil profosfat-AMP transferaz enziminin üretiminden sorumlu olduğu bildirilmektedir. 6 b olarak isimlendirilen bir diğer genin ise yabani tütün (Nicotiana glauca) ve Kalanchoe tubiflora’da küçük tümörler oluşturduğu ifade edilmektedir. İaa. M, iaa. H, ipt ve 6 b genlerinin bitki hücrelerine aktarılmasıyla, hücrelerin hormon dengesi bozulmakta ve onkogenik (tümör oluşturan) fenotipler oluşmaktadır. Bu nedenle de; sözkonusu genlere onkogenler (onc) adı verilmektedir.

T-DNA Bölgesi l l l Oktopin ve nopalin tipi plazmidlerin T-DNA bölgeleri, sağ (RB/right border) ve soldan (LB/left border) 24 bp uzunluğundaki düzensiz nükleotid dizileri ile sınırlandırılmıştır. Bu diziler sınır dizileri olarak isimlendirilmektedir. Genelde, bu diziler arasında bulunan DNA bitki hücrelerine aktarılmaktadır. Ancak, bazı durumlarda T-DNA dışındaki bölgelerin de bitki kromozomlarıyla bütünleştiği gözlenmektedir. Sınır dizileri plazmid tipine göre farklılık gösterebilmektedir.

T-DNA Bölgesi Araştırmalar, iki T-DNA sınırı arasına yerleştirilen herhangi bir DNA parçasının kolayca bitki hücresine aktarılabildiğini göstermiştir. l Üstelik, tümör oluşturan genlerin kesici (restriksiyon) enzimler yardımıyla T-DNA bölgesinden çıkarılmasının da bitki hücresine gen aktarımını hiçbir şekilde engellemediği belirlenmiştir. l

T-DNA Bölgesi l l Tümör oluşturan genlerin çıkartıldığı plazmidler, non-onkogenik (tümör oluşturmayan) Tiplazmidler olarak adlandırılmaktadır. Araştırmalar, T-DNA’nın sağ sınır nükleotid dizisinin gen aktarımında mutlak gerekli olduğunu ortaya koyarken, sol sınırdaki parça eksilmelerinin (delesyonların) bakteriden bitki hücresine genetik materyal aktarımını etkilemediğini göstermiştir.

Farklı Agrobacterium plazmidlerine ait 24 bp’lik T-DNA sınır nükleotid dizileri Ti plazmidi/ opin tipi Sınır Nükleotid Dizisi Kaynak p. Ti. C 58/nopalin Sol Sağ TGGCAGGATATATTGTGGTGTAAA Zyprain ve TGACAGGATATATTGGCGGGTAAA Kado, 1990 p. Ti. T 37/nopalin p. Ti. T 37/ nopalin Sol Sağ TGGCAGGATATATTGTGGTGTAAA Yadav ve ark. , TGACAGGATATATTGGCGGGTAAA 1982 p. Ti 15955/oct. TL Sol Sağ CGGCAGGATATATTCAATTGTAAA TGGCAGGATATATACCGTTGTAAT Barker ve ark. , 1983 p. Ti. Ach 5/oct. TL Sol Sağ CGGCAGGATATATTCAATTGTAAA GGCAGGATATATACCGTTGTAATT Gielen ve ark. , 1984 p. Ri. A 4/agrop. TL Sol Sağ TGGCAGGATATATTGTGATGTAAA TGACAGGATATATGTTCCTGTCAT Slightom ve ark. , 1986


Virülens (vir) bölgesi l l l Vir bölgesi, T-DNA aktarımında gerekli olan ürünlerin önemli bir kısmını sağlamaktadır. Bu bölgede meydana getirilen mutasyonların, bitki hücrelerine gen aktarımını önemli ölçüde engellediği bilinmektedir. Bu bölgenin, aynı bakteri hücresinde, ancak başka bir plazmid üzerinde bulunduğu zaman da T-DNA aktarımının gerçekleşebilmesi onun “trans-hareket” bir yapıda olduğunu göstermektedir.

Virülens (vir) bölgesi l l T-DNA’nın dışında ve sol sınıra yakın olan, yaklaşık 30 -40 kb uzunluğundaki “virulens” (vir) bölgesi T-DNA aktarımında mutlak gerekli olan 6 ana operon (Vir. A, Vir. B, Vir. C, Vir. D, Vir. E ve Vir. G) ve gerekli olmayan diğer 2 operon (Vir. F ve Vir. H)’dan meydana gelmektedir. Vir. A, Vir. G ve Vir. F operonları tek gene sahipken, Vir. E, Vir. C ve Vir. H operonları ikişer gen taşımaktadır. Öte yandan, Vir. D dört, Vir. B ise 11 gen içermektedir. Vir. A ve Vir. G konstitütif (daima aktif) operonlardır.

Virülens (vir) bölgesi l l Vir. A ve Vir. G operonları vir genlerinin aktivitelerini yönlendiren pozitif bir düzenleyici sistemini kodlamaktadır. Vir. A geninin üretmiş olduğu hücre içi membran proteini yaralanmış bitki hücrelerinin salgıladığı fenolik bileşikleri tanıyarak onlarla bağlantı kurar Daha sonra Vir. A geni, muhtemelen protein fosforilasyonu ile bu bilgiyi Vir. G lokusuna aktarır. Sonuçta, uyarılan Vir. G proteini ise kendi geni ve diğer vir genleri için transkripsiyon işlemcisi görevini üstlenmektedir.

Virülens (vir) bölgesi l l Vir. D operonu, T-DNA iplikciğinin rejenerasyonunu sağlarken; Vir. C, bu bölgenin sınırlardan kesilmesinde, Vir. B ve Vir. E operonları ise T-DNA’nın bakteriden bitki hücresine hareketinde etkili olmaktadır. Vir. H operonunun T-DNA transferinde gerekli olmadığı bildirilmekle birlikte, bu lokusun kodladığı enzimlerin enfeksiyon sırasında bitkinin salgılamış olduğu bakteriyosidal ve bakteriyostatik bileşiklere karşı bakteriyi koruduğu belirtilmektedir.
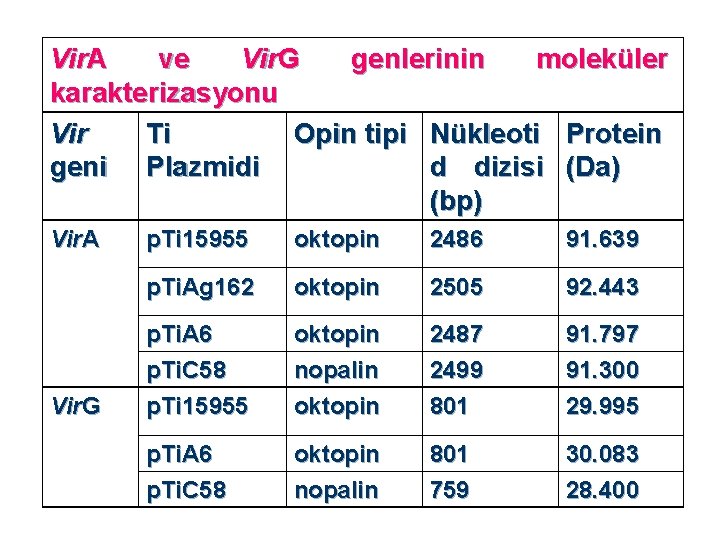
Vir. A ve Vir. G genlerinin moleküler karakterizasyonu Vir Ti Opin tipi Nükleoti Protein geni Plazmidi d dizisi (Da) (bp) Vir. A Vir. G p. Ti 15955 oktopin 2486 91. 639 p. Ti. Ag 162 oktopin 2505 92. 443 p. Ti. A 6 p. Ti. C 58 oktopin nopalin 2487 2499 91. 797 91. 300 p. Ti 15955 oktopin 801 29. 995 p. Ti. A 6 p. Ti. C 58 oktopin nopalin 801 759 30. 083 28. 400


Kromozomal genler l l Agrobacterium bakterisinin kendi kromozomu üzerinde bulunan dört adet lokus [chv. A, chv. B, psc. A (exo. C) ve att. R]; bakterinin bitki hücrelerine tutunması, yaralanmış bitki dokularında bakterinin çoğalması ve Ti plazmidi üzerinde bulunan vir genlerinin düzenlenmesinde rol oynamaktadır. Bunlardan, büyüklügü 8. 5 kb olan chv. B geninin, ß-1, 2 glukanın oluşumunda etkili olan 235 k. Da’luk bir proteini şifrelediği,

Kromozomal genler 7 kb büyüklügündeki chv. A lokusunun ise ß -1, 2 glukanın periplazm içerisine taşınması için gerekli bileşikleri sentezlediği, l 3. 0 kb’lik psc. A geninin ise nötr ve asidik yapıdaki önemli hücre dışı polisakkarid bileşiklerinin yapılmasında gerekli olduğu anlaşılmıştır. l


T-DNA Aktarımının Moleküler Mekanizması l l l Agrobacterium’dan bitki hücrelerine T-DNA aktarımı 4 ana aşamada gerçekleşmektedir 1. Agrobacterium’un bitki hücrelerine tutunması ve koloni oluşturması, 2. virülens genlerinin uyarılması, 3. T-DNA transferi, 4. T-DNA’nın bitki genomuna entegrasyonudur.

Agrobacterium’un bitki hücrelerine tutunması ve koloni oluşturması l Agrobacterium’un bitki hücrelerine tutunması ve koloni oluşturması tümör oluşumu için gerekli olan ilk aşamadır. l Agrobacterium hücrelerinin yüzeylerindeki polisakkaritlerin bitki hücrelerine tutunmada önemli rol oynadığı bildirilmektedir. l Polisakkarit sentezi için 20 kb büyüklüğündeki kromozomal att. R lokusuna ihtiyaç duyulmaktadır. Bu lokus bakterinin bitki hücresine tutunması için gerekli olan genleri taşımaktadır. l Bakteri hücre duvarına tutunduktan sonra bakteri tarafından selüloz lifleri sentezlenmekte ve böylece bitki hücre duvarında çok sayıda bakteri yığılması gözlenmektedir.

Agrobacterium’un bitki hücrelerine tutunması ve koloni oluşturması Kromozomal chv. A, chv. B ve psc. A virülens genlerinin ß-1, 2 glukan ve diğer şekerlerin sentezlenmesinde ve dolaylı olarak bakterinin tutunmasında rol aldığı belirtilmektedir l Agrobacterium enfeksiyonunun sadece düşük molekül ağırlıklı fenolik bileşikleri salgılayan, yaralanmış veya hızlı bölünen süspansiyon hücreleri ile Agrobacterium enfeksiyonuna karşı duyarlı bitki hücrelerinin bulunması durumunda gerçekleşebildiği bilinmektedir. l Bakteri yaralanmış bitki dokularının hücre duvarlarına tutunmakta ve bu olayda bitki hücre yüzeylerinde bulunan proteaz-duyarlı moleküllerin etkili olduğu belirtilmektedir l

Virülens genlerinin uyarılması Bakteri bitki hücre duvarına tutunduktan sonra, yaralanmış bitki hücrelerinden salgılanan fenolik bileşikleri, Agrobacterium’un algılamasıyla T-DNA aktarım işlemi başlatılır. l Normalde bitkilerde fitoaleksin ve lignin biyosentezinde rol aldığı tahmin edilen asetosringon (AS) gibi fenolik bileşikler, bakteri hücresine girerek vir genlerini uyarmaktadır. l

Virülens genlerinin uyarılması Fenolik bileşiklerle birlikte bu uyarılma işleminde belirli monosakkaritler de rol oynamaktadır. l Optimum T-DNA aktarımı için, sıcaklık 20 -30 ˚C arasında olmalıdır. 32 ˚C’den daha yüksek sıcaklıklar vir genlerinin ifadelerini engellemektedir. l

Virülens genlerinin uyarılması l Agrobacterium bakterisinin hücre zarı içerisinde lokalize olan algılayıcı/sensör Vir. A proteini (91. 6 k. Da) yaralanmış hücre tarafından salgılanan sinyal proteinlerini, yani fenolik bileşikleri yakalar ve uyarılır. l Uyarılan Vir. A kendi fosfatını sitoplazmik bir DNA bağlanma proteini (binding protein) olan Vir. G proteinine aktarma kapasitesine sahiptir. Vir. A tarafından fosforilizasyona uğrayan Vir. G daha sonra diger vir genlerinin ifadelerinin düzenlenmesinde transkripsiyonal faktör olarak görev yapar

T-DNA transferi l Vir genlerinin uyarılmasının sonucunda, T- DNA’nın alt sarmalının her iki 24 bp sınırının 3. ve 4. nükleotid dizileri arasındaki belirli bir noktada çentik oluşmasıyla başlar. l Bu işlem, Vir. D 1 ve Vir. D 2 proteinlerinin T-DNA sınır bölgelerindeki nükleotid dizilerini belirli noktalardan tanıyan endonükleaz etkisi tarafından gerçekleştirilmektedir. l Vir. D 1 proteininin 24 bp sınır dizilerinde DNA’yı gevşettiği, Vir. D 2’nin ise çentik oluşturduğu bildirilmektedir.

T-DNA transferi Vir. C operon ürünlerinin ise T-DNA sınır kesimini hızlandırdığı gösterilmiştir. l Kesilen noktalar, tek sarmal T-DNA bölgesi için başlama ve bitiş yerleri olarak kullanılmaktadır. T -iplikcik sentezinin sağ sınırdan başladığını, 5’ 3’ yönünde devam ettiğini ve sol sınırın yokluğunda dahi sentezin sonuçlandığını göstermektedir. l

T-DNA transferi Nopalin tipi plazmidler sadece bir T-DNA bölgesi taşıdığından dolayı tek T-iplikciği sentezlenir. Öte yandan, daha karmaşık oktopin Ti plazmidler, dört ayrı TDNA sınır dizileri tarafından çevrelenen üç ayrı T-DNA bölgesi taşıdığından, altı olası T-iplikciği üretirler. l Vir. D 2 proteini, alt sarmalı sağ sınır bölgesinden kestikten sonra tek sarmalın 5’ ucunda bağlı kalarak T-iplikciğinin serbest kalmasını ve 5’ 3’ yönünde oluşan ekzonukleolitik degredasyonu engellemektedir. l Serbest kalan T-iplikciği, Vir. E operonununca kodlanan 69 k. Da’luk tek sarmal DNA-bağlanma proteini Vir. E 2 ile kaplanarak nükleaz enzimlerinin olumsuz etkilerinden korunur. l

T-DNA transferi Ayrıca, Vir. E 2 proteini T-iplikciğini sararak, kompleksin çapını 2 nm’ye kadar düşürmekte ve bu da hücre zarı açıklıklarından geçişini kolaylaştırmaktadır. l T-iplikciğinin bitki hücrelerine aktarılmasında, Vir. D 2 proteininin pilot görevi yapmaktadır. l Vir. B proteinlerinin önemli bir kısmı bakteri ve bitki hücre zarında T-kompleksinin geçebileceği büyüklükte açıklık oluştururken, T-DNA transferinde gerekli olan temel elementleri de oluşturmaktadırlar. l

T-DNA’nın bitki genomuna entegrasyonu n n Agrobacterium’dan bitki hücrelerine T-DNA transferinin en az anlaşılan kısmı belki de TDNA’nın bitki genomuna entegrasyonudur. T-DNA çekirdeğe girdikten sonra, bir veya birkaç kopya halinde rastgele, bitki kromozomlarıyla birleşmekte ve bu birleşmede kromozomların aktif kısımları tercih edilmektedir.

T-DNA’nın bitki genomuna entegrasyonu n n Bitki hücresi içerisinde tek sarmal T-DNA kompleksinin çekirdek zarını geçerek kromozomlara yönelmesinde en önemli görevi Vir. D 2 ve Vir. E 2 proteinleri üstlenmektedir. T-DNA’nın kromozomlarla birleşme işlemini sağ sınırdan başlamakta ve karmaşık birkaç aşamada tamamlanmaktadır.

T-DNA’nın bitki genomuna entegrasyonu n n n Vir. D 2’nin bağlı bulunduğu T-iplikciği ile bitki DNA’sında mikrohomolog bölgeler açılmakta ve T-DNA’nın 3’ ucu veya bu uca yakın bölgeler bitki DNA’sında buldukları homolog bölgelerle ilk teması (sinapsis) kurmaktadır. Bitki DNA’sında 3’ 5’ yönünde yapısal açıklık oluşmakta ve bu açıklığın 3’ ucu endonükleaz enzimleri tarafından kesilerek, T-iplikciğinin Vir. D 2 proteinine bağlanan 5’ ucundaki ilk nükleotid üst sarmal bitki DNA’sıyla 5’ 3’ yönünde eşleşmektedir. T-iplikciğinin 3’ ucundaki fazla bölgeler ve açılan bitki DNA parçası endonükleaz veya 3’ 5’ ekzonükleaz enzimleri tarafından parçalanmaktadır.

T-DNA’nın bitki genomuna entegrasyonu n n n T-iplikciğinin Vir. D 2’ye bağlanan 5’ ucu ve diğer 3’ ucu, kesilen bölgeden bitkinin alt sarmal DNA’sı ile birleşmektedir. T-iplikciğinin 3’ 5’ yönündeki bitki DNA sarmalına entegrasyonu tamamlandıktan sonra, bitki DNA’sı onarılmakta ve T-iplikciği replikasyonla çift sarmal DNA’ya dönüşmektedir. T-DNA, köken olarak prokaryotik yapıda olmasına karşın, bitkinin kromozomuyla bütünleşmesinden sonra ökaryotik kromatin yapı özelliklerine uyum sağlamaktadır. T-DNA’nın opin sentezi ve onc genlerinin transkripsiyonları neticesinde opin üretimi ve tümör oluşumu meydana gelmektedir.



“T-pilus” Teorisi Son yıllarda yapılan araştırmalarda, Agrobacterium’dan bitki hücrelerine Tkompleksinin aktarılmasında yukarıda belirtilen mekanizma haricinde degişik teoriler ortaya atılmıştır. l Bunlardan ilkinde; “T-pilus” olarak adlandırılan bir nükleoprotein kompleksinin T-DNA aktarımında köprü görevi yaptığı belirtilmektedir. l T-pilus 10 nm çapında olup, ortasında yaklaşık 2 nm çapında bir lumen (boşluk) bulunmaktadır. l

“T-pilus” Teorisi T-pilus’unun moleküler bir şırınga görevi yaparak Tkompleksini bitki hücre sitoplazmasına enjekte ettiği bildirilmektedir. l Diğer bir teoriye göre de; T-pilus kompakt bir yapıya dönüşerek, bakteri hücresini bitki hücresine doğru çekmekte ve bakteri ile bitki hücre zarı arasında gerçekleşen füzyondan sonra, Vir. B proteinleri tarafından oluşturulan gözenekten T-kompleksi bitki hücresine aktarılmaktadır. l

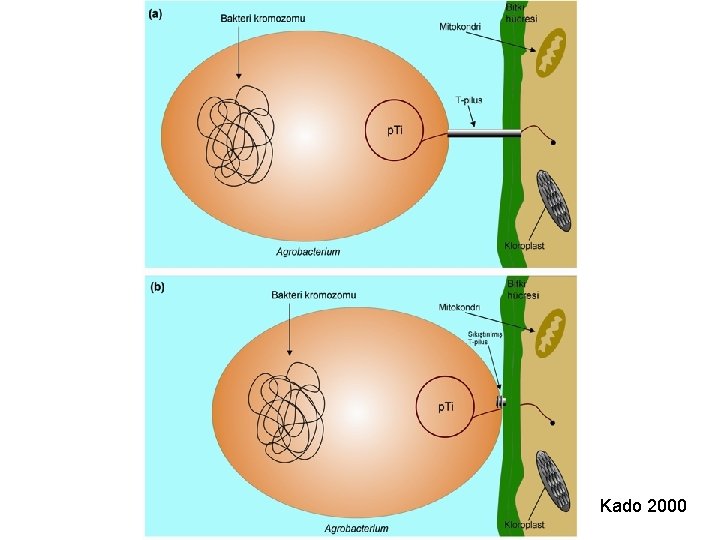
Kado 2000
- Slides: 51