Agrgation Interne Equilibre chimique Plan de la prsentation

Agrégation Interne Equilibre chimique

Plan de la présentation �I) Présentation générale du sujet �II) Développement post bac : �III) Partie pédagogique : l’équilibre chimique au cycle terminal

I) Présentation générale du sujet 1) Définitions de base �Soit un système chimique dans lequel se produit la réaction suivante : Σ νi Ri = Σ νi Pi avec v 1 la vitesse de la réaction dans le sens 1 et v-1 la vitesse de la réaction dans le sens inverse �On dit que l’équilibre chimique est atteint lorsque les deux vitesses de réaction sont égales (et non nulles). �L’équilibre chimique est donc un équilibre stationnaire, les quantités de matières n’évoluent plus dans le temps mais dynamique car les deux réactions ont lieu simultanément et à la même vitesse.

Constante d’équilibre (Guldberg et Waage) �Avec l’approche cinétique, dans le cas d’une transformation élémentaire, si v 1 =k 1 Π a(Ri)νi et v-1 =k-1 Π a(Pi)νi , alors l’égalité des vitesses donne la formule suivante : k 1 Π a(Ri)νi = k-1 Π a(Pi)νi ou encore k 1/k-1 = Π a(Pi)νi/a(Ri)νi Le rapport K = k 1/k-1 est une constante qui ne dépend que de la température est appelé constante d’équilibre.
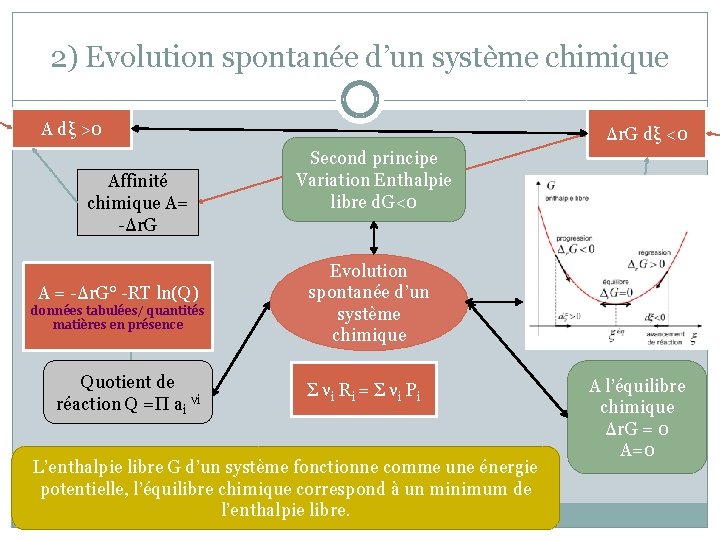
2) Evolution spontanée d’un système chimique A dξ >0 Affinité chimique A= -Δr. G A = -Δr. G° -RT ln(Q) données tabulées/ quantités matières en présence Quotient de réaction Q =Π ai νi Δr. G dξ <0 Second principe Variation Enthalpie libre d. G<0 Evolution spontanée d’un système chimique Σ ν i Ri = Σ ν i Pi L’enthalpie libre G d’un système fonctionne comme une énergie potentielle, l’équilibre chimique correspond à un minimum de l’enthalpie libre. A l’équilibre chimique Δr. G = 0 A=0
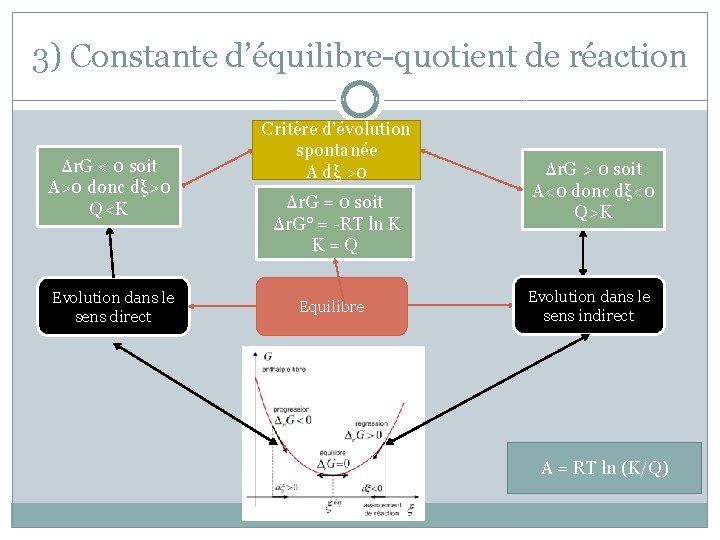
3) Constante d’équilibre-quotient de réaction Δr. G < 0 soit A>0 donc dξ>0 Q<K Evolution dans le sens direct Critère d’évolution spontanée A dξ >0 Δr. G = 0 soit Δr. G° = -RT ln K K=Q Equilibre Δr. G > 0 soit A<0 donc dξ<0 Q>K Evolution dans le sens indirect A = RT ln (K/Q)
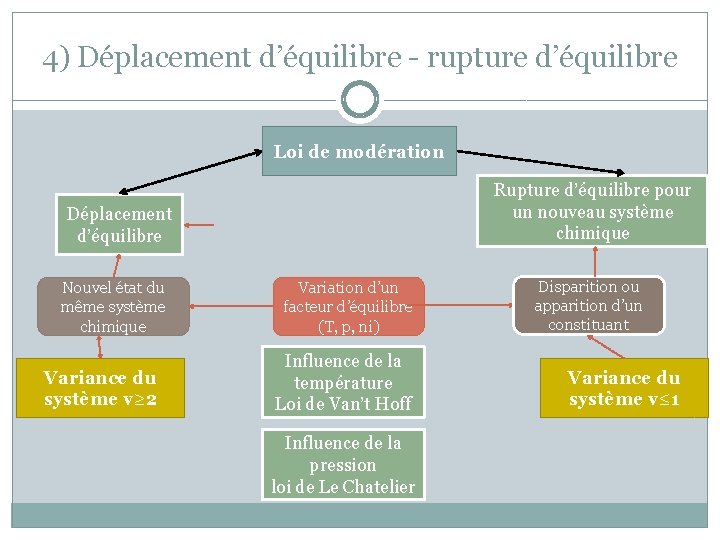
4) Déplacement d’équilibre - rupture d’équilibre Loi de modération Rupture d’équilibre pour un nouveau système chimique Déplacement d’équilibre Nouvel état du même système chimique Variance du système v≥ 2 Variation d’un facteur d’équilibre (T, p, ni) Influence de la température Loi de Van’t Hoff Influence de la pression loi de Le Chatelier Disparition ou apparition d’un constituant Variance du système v≤ 1

Conclusion L’étude des équilibres et notamment de leur constante permet de nombreuses applications en chimie analytique notamment : �Quantitativité d’une réaction de titrage (K>104) �Comparaison de la force d’un acide (comparaison des Ka) �Etudes d’équilibres de complexation (par les Kd) �Calculs des potentiels d’oxydoréduction Elle permet également l’optimisation d’un procédé chimique afin d’en améliorer le rendement en jouant sur les paramètres de la réaction (température, pression, composition du système, volume…)

II) Développement post bac : oxydation du monoxyde de cobalt à haute température 1) Public ciblé Classe de PC* 2) Prérequis �Loi d’action de masse �Équation d’état des gaz parfaits �Approximation d’Ellingham

3) Enoncé Un récipient de volume Vi = 10, 0 L contient initialement n 1=1, 00 mol de monoxyde de cobalt et n 2=0, 300 mol de dioxygène. Le récipient est maintenu à la température de 1150 K mais subit une compression de volume jusqu’à atteindre un volume final de Vf = 1, 00 L. Indiquer les espèces présentes dans le récipient en fonction du volume V, puis tracer l’allure de la courbe donnant P en fonction de V.

4) Résolution 1) Hypothèses �Le dioxygène se comporte comme un gaz parfait �Les deux oxydes sont totalement non miscibles 2) Données thermodynamiques à 298 K Δr. H° 1 = -364, 6 k. Jmol-1 et Δr. S° 1 = -318, 2 Jmol-1 K-1 3) Méthode -calcul de l’affinité chimique -calcul de la variance
- Slides: 11