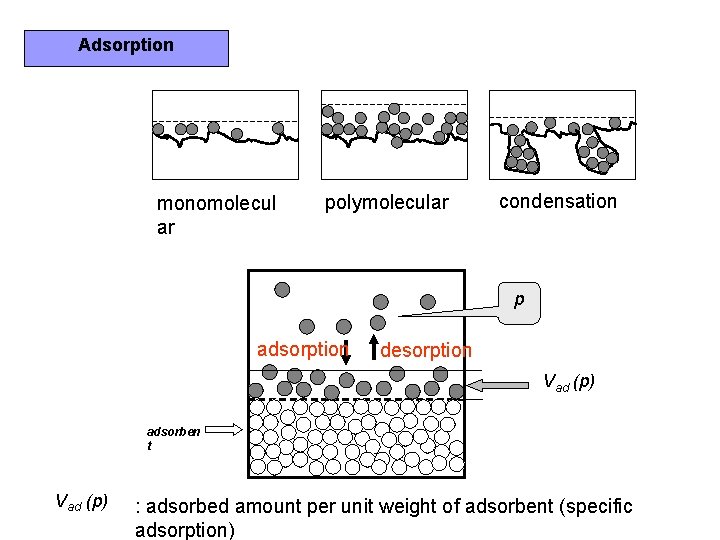
Adsorption monomolecul ar polymolecular condensation p adsorption desorption





- Slides: 11


Adsorption monomolecul ar polymolecular condensation p adsorption desorption Vad (p) adsorben t Vad (p) : adsorbed amount per unit weight of adsorbent (specific adsorption)

A gázadszorpció szükségszerűen exoterm, azaz növekvő hőmérséklet csökkenő adszorpcióhoz vezet egyensúlyban. Az entrópia csökken!

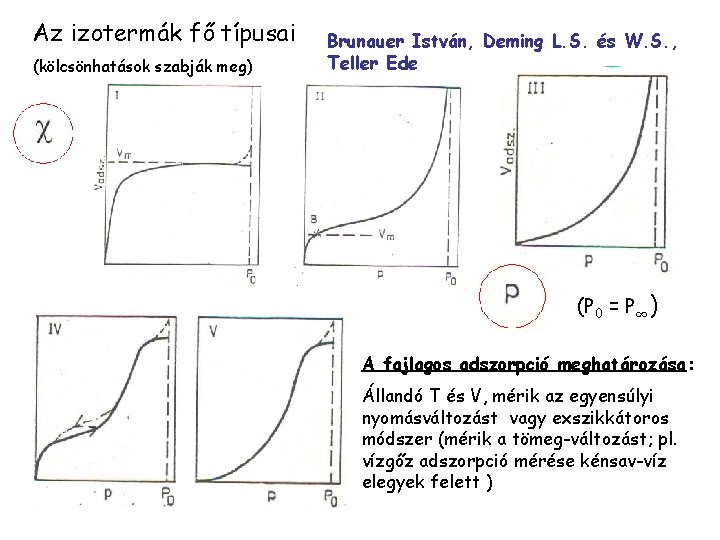
Az izotermák fő típusai (kölcsönhatások szabják meg) Brunauer István, Deming L. S. és W. S. , Teller Ede (P 0 = P∞) A fajlagos adszorpció meghatározása: Állandó T és V, mérik az egyensúlyi nyomásváltozást vagy exszikkátoros módszer (mérik a tömeg-változást; pl. vízgőz adszorpció mérése kénsav-víz elegyek felett )

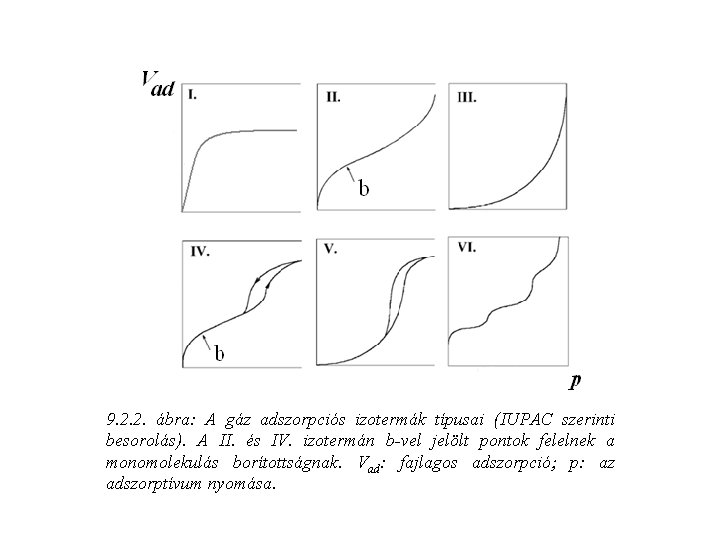
9. 2. 2. ábra: A gáz adszorpciós izotermák típusai (IUPAC szerinti besorolás). A II. és IV. izotermán b-vel jelölt pontok felelnek a monomolekulás borítottságnak. Vad: fajlagos adszorpció p: az adszorptívum nyomása.

Izoterma egyenletek: fajlagos felület meghatározása Langmuir-izoterma és egyenlet (kinetikai levelezetés) Dinamikus egyensúlyban: Feltételek: Monomolekulás borítottság Adszorpció aktív centrumokon történik A diff. adszorpciós hő független a borítottságtól (ritkán teljesül) Langmuir izoterma-egyenlet (l. korábban a Gibbs- és Szyszkowski egyenletek összevetéséből) χm: a monomolekulás adszorpció

Linearizálva: as: fajlagos felület (m 2/g) φ: adszorptívum fajlagos felületigénye (m 2/mol)

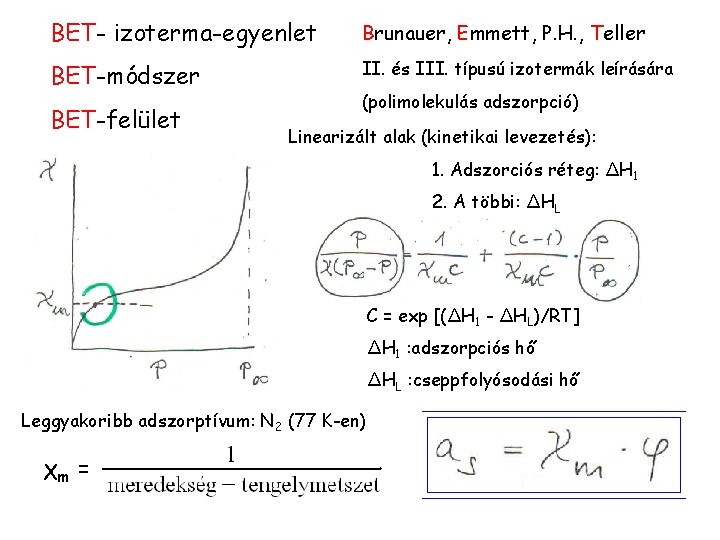
BET- izoterma-egyenlet Brunauer, Emmett, P. H. , Teller BET-módszer II. és III. típusú izotermák leírására BET-felület (polimolekulás adszorpció) Linearizált alak (kinetikai levezetés): 1. Adszorciós réteg: ΔH 1 2. A többi: ΔHL C = exp [(ΔH 1 - ΔHL)/RT] ΔH 1 : adszorpciós hő ΔHL : cseppfolyósodási hő Leggyakoribb adszorptívum: N 2 (77 K-en) χm =

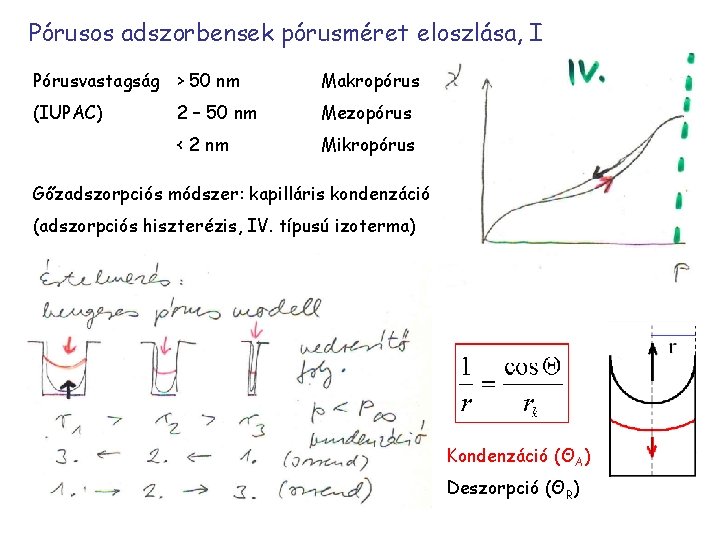
Pórusos adszorbensek pórusméret eloszlása, I Pórusvastagság > 50 nm Makropórus (IUPAC) 2 – 50 nm Mezopórus < 2 nm Mikropórus Gőzadszorpciós módszer: kapilláris kondenzáció (adszorpciós hiszterézis, IV. típusú izoterma) Kondenzáció (ΘA) Deszorpció (ΘR)

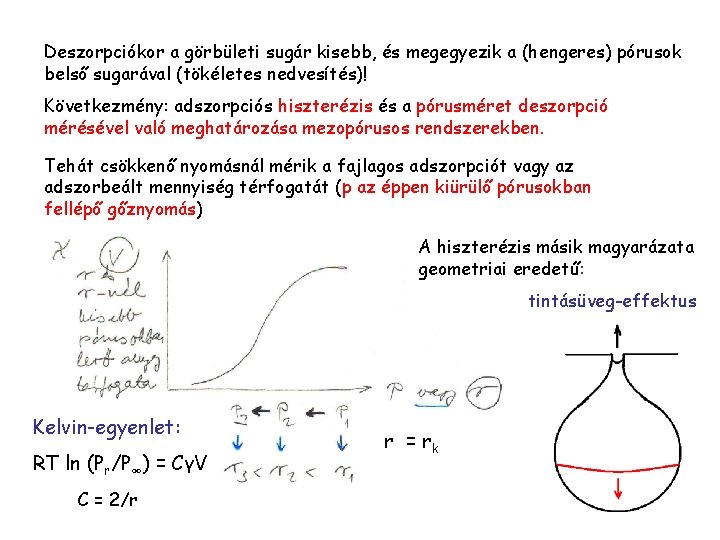
Deszorpciókor a görbületi sugár kisebb, és megegyezik a (hengeres) pórusok belső sugarával (tökéletes nedvesítés)! Következmény: adszorpciós hiszterézis és a pórusméret deszorpció mérésével való meghatározása mezopórusos rendszerekben. Tehát csökkenő nyomásnál mérik a fajlagos adszorpciót vagy az adszorbeált mennyiség térfogatát (p az éppen kiürülő pórusokban fellépő gőznyomás) A hiszterézis másik magyarázata geometriai eredetű: tintásüveg-effektus Kelvin-egyenlet: RT ln (Pr/P∞) = CγV C = 2/r r = rk

Pórusos adszorbensek pórusméret eloszlása, II Hg-porozimetria (hengeres pórusmodell) Vákumozás után mért mennyiségek: Bepréselt Hg térfogata (V) Alkalmazott nyomás (p) Ismerni kell a Hg felületi feszültségét és peremszögét a kérdéses felszínen. →