Adieu les myalgies Par Raphael Pinto et Clo







![Méthode Mots-clés utilisés : [ «Déficience en Vitamine D» OU «Suppléments alimentaires» ] ET Méthode Mots-clés utilisés : [ «Déficience en Vitamine D» OU «Suppléments alimentaires» ] ET](https://slidetodoc.com/presentation_image_h2/6b162d84ab44c9cd5d69e2982351ef5a/image-8.jpg)
















- Slides: 33

Adieu les myalgies! Par Raphael Pinto et Cloé Poulin-Groulx CLSC du Marigot Sources images: http: //static. tvtropes. org/pmwiki/pub/images/popeye. jpg http: //www. pulsetoday. co. uk/clinical-specialties/cardiovascular/rosuvastatin-does-more-harm-than-good-claims-academic/20009477. article

Aucun conflit d’intérêt à déclarer

Vos patients se sont-ils déjà plaint de myalgies en lien avec leur statine ? Source image: http: //wetpaint. com/wp-content/uploads/2015/03/w 630_022615 greysanatomyseason 11 episode 1316 -1424975963. jpg

Pourquoi ce sujet ? • Idée venue lors d’une discussion avec notre pharmacienne dans notre GMF-U • Traitement de choix de la dyslipidémie (↓ mortalité cardiovasculaire) • Effets secondaires des statines, dont celui d’intérêt : o. Impact au niveau musculaire : • Myalgie, myopathie, myosite, myonécrose, rhabdomyolyse • 20% des patients présentent des myalgies secondaires aux statines. • #1 des raisons de non-compliance/arrêt de médication

Facteurs de risque de myalgie • Déficience en vitamine D • Génétique • Dose élevée de statine • Indice de masse corporelle faible • Sexe féminin • Dysfonction endocrinienne (thyroïdienne/parathyroïdienne) ou rénale/hépatique • Fibromyalgie ou polymyalgie rhumatismale • Abus d’alcool • Interaction médicamenteuse (exemple : Fibrate, Clarythromycine, Amiodarone, Diltiazem, Fluconazole) • Antécédents de myalgie/rhabdomyolyse

Pathophysiologie • Plusieurs récepteurs de la vitamine D à la surface des cellules musculaires. • Métabolisme des statines dépend du Cytochrome P 450 (CYP-3 A 4). o Si déficience en vitamine D → « shunt préférentiel » Source Image : https: //en. wikipedia. org/wiki/Competitive_inhibition

Pathophysiologie (suite) Hypothèses pour expliquer la destruction musculaire par les statines 1) Beta-oxydation →lésions musculaires. 2) Inhibition de la voie du mevalonate → Baisse de production d’énergie musculaire. 3) Fort terrain génétique : rôle important Donc, complications musculaires de déficience en vitamine D : • Douleurs musculosquelettiques non-spécifiques • Faiblesses musculaires proximales • Prolonge le temps nécessaire pour le pic de contractions/relaxations.
![Méthode Motsclés utilisés Déficience en Vitamine D OU Suppléments alimentaires ET Méthode Mots-clés utilisés : [ «Déficience en Vitamine D» OU «Suppléments alimentaires» ] ET](https://slidetodoc.com/presentation_image_h2/6b162d84ab44c9cd5d69e2982351ef5a/image-8.jpg)
Méthode Mots-clés utilisés : [ «Déficience en Vitamine D» OU «Suppléments alimentaires» ] ET [ «Myalgie» OU «Intolérance aux statines» ] ET [ «Statine» OU «Inhibiteurs du HMG-Co. A réductase» ] FILTRES/INCLUSIONS: Anglais ou français Humains seulement Adultes 18 ans et plus EXCLUSIONS: séries de cas, lettre aux éditeurs

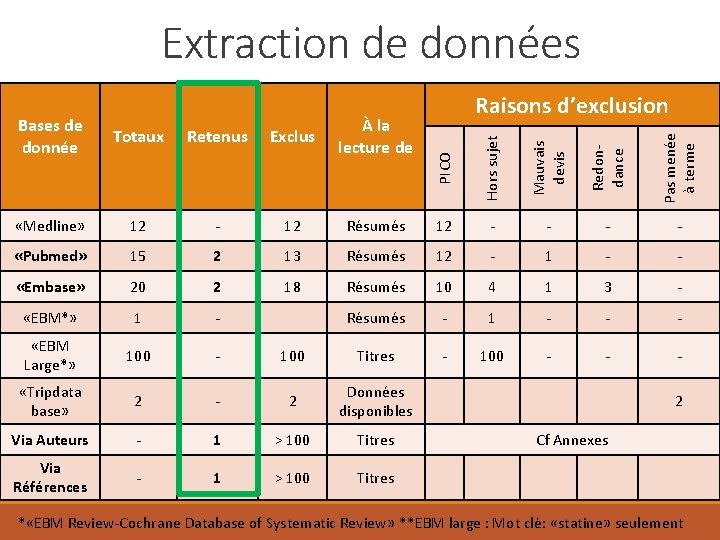
Extraction de données Bases de donnée Totaux Retenus Exclus À la lecture de PICO Hors sujet Mauvais devis Redondance Pas menée à terme Raisons d’exclusion «Medline» 12 - 12 Résumés 12 - - «Pubmed» 15 2 13 Résumés 12 - 1 - - «Embase» 20 2 18 Résumés 10 4 1 3 - «EBM*» 1 - Résumés - 1 - - - «EBM Large*» 100 - 100 Titres - 100 - - - «Tripdata base» 2 - 2 Données disponibles Via Auteurs - 1 > 100 Titres Via Références - 1 > 100 Titres 2 Cf Annexes * «EBM Review-Cochrane Database of Systematic Review» **EBM large : Mot clé: «statine» seulement

DESCRIPTION DES ÉTUDES

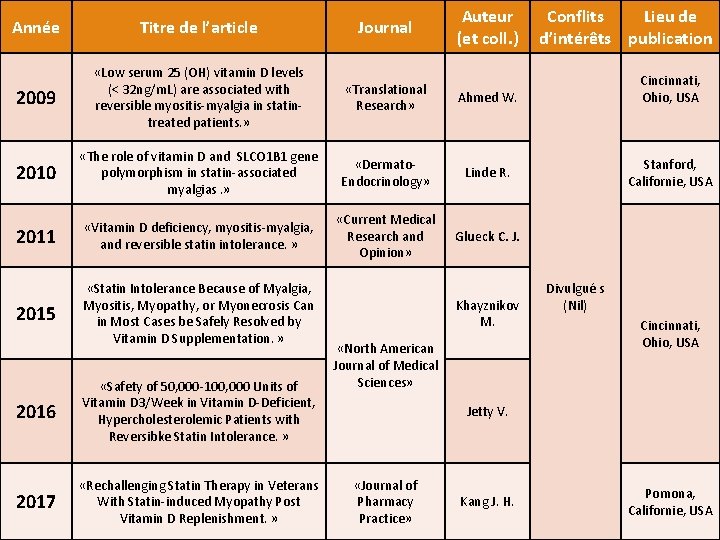
Auteur (et coll. ) Année Titre de l’article Journal 2009 «Low serum 25 (OH) vitamin D levels (< 32 ng/m. L) are associated with reversible myositis-myalgia in statintreated patients. » «Translational Research» Ahmed W. 2010 «The role of vitamin D and SLCO 1 B 1 gene polymorphism in statin-associated myalgias. » «Dermato. Endocrinology» Linde R. 2011 «Vitamin D deficiency, myositis-myalgia, and reversible statin intolerance. » «Current Medical Research and Opinion» Glueck C. J. 2015 «Statin Intolerance Because of Myalgia, Myositis, Myopathy, or Myonecrosis Can in Most Cases be Safely Resolved by Vitamin D Supplementation. » 2016 «Safety of 50, 000 -100, 000 Units of Vitamin D 3/Week in Vitamin D-Deficient, Hypercholesterolemic Patients with Reversibke Statin Intolerance. » 2017 «Rechallenging Statin Therapy in Veterans With Statin-induced Myopathy Post Vitamin D Replenishment. » Khayznikov M. «North American Journal of Medical Sciences» Conflits Lieu de d’intérêts publication Cincinnati, Ohio, USA Stanford, Californie, USA Divulgué s (Nil) Cincinnati, Ohio, USA Jetty V. «Journal of Pharmacy Practice» Kang J. H. Pomona, Californie, USA

MÉTHODE

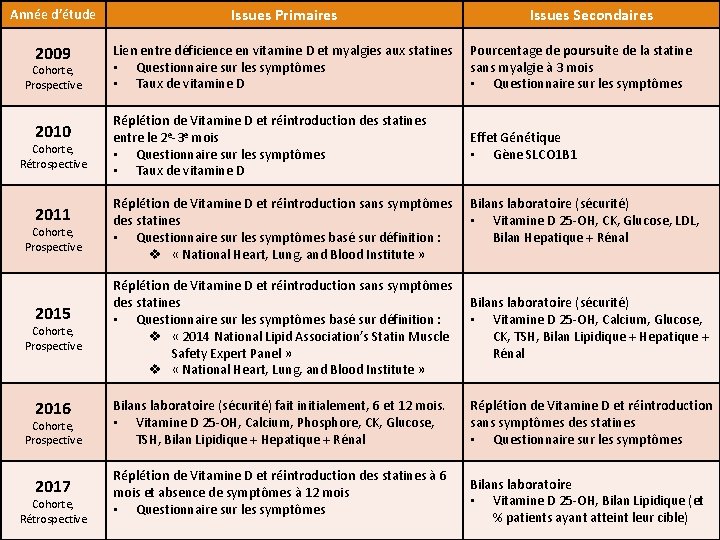
Année d’étude Issues Primaires 2009 Lien entre déficience en vitamine D et myalgies aux statines • Questionnaire sur les symptômes • Taux de vitamine D Pourcentage de poursuite de la statine sans myalgie à 3 mois • Questionnaire sur les symptômes Réplétion de Vitamine D et réintroduction des statines entre le 2 e-3 e mois • Questionnaire sur les symptômes • Taux de vitamine D Effet Génétique • Gène SLCO 1 B 1 Cohorte, Prospective 2010 Cohorte, Rétrospective 2011 Cohorte, Prospective 2015 Cohorte, Prospective 2016 Cohorte, Prospective 2017 Cohorte, Rétrospective Réplétion de Vitamine D et réintroduction sans symptômes des statines • Questionnaire sur les symptômes basé sur définition : v « National Heart, Lung, and Blood Institute » Issues Secondaires Bilans laboratoire (sécurité) • Vitamine D 25 -OH, CK, Glucose, LDL, Bilan Hepatique + Rénal Réplétion de Vitamine D et réintroduction sans symptômes des statines • Questionnaire sur les symptômes basé sur définition : v « 2014 National Lipid Association’s Statin Muscle Safety Expert Panel » v « National Heart, Lung, and Blood Institute » Bilans laboratoire (sécurité) • Vitamine D 25 -OH, Calcium, Glucose, CK, TSH, Bilan Lipidique + Hepatique + Rénal Bilans laboratoire (sécurité) fait initialement, 6 et 12 mois. • Vitamine D 25 -OH, Calcium, Phosphore, CK, Glucose, TSH, Bilan Lipidique + Hepatique + Rénal Réplétion de Vitamine D et réintroduction sans symptômes des statines • Questionnaire sur les symptômes Réplétion de Vitamine D et réintroduction des statines à 6 mois et absence de symptômes à 12 mois • Questionnaire sur les symptômes Bilans laboratoire • Vitamine D 25 -OH, Bilan Lipidique (et % patients ayant atteint leur cible)

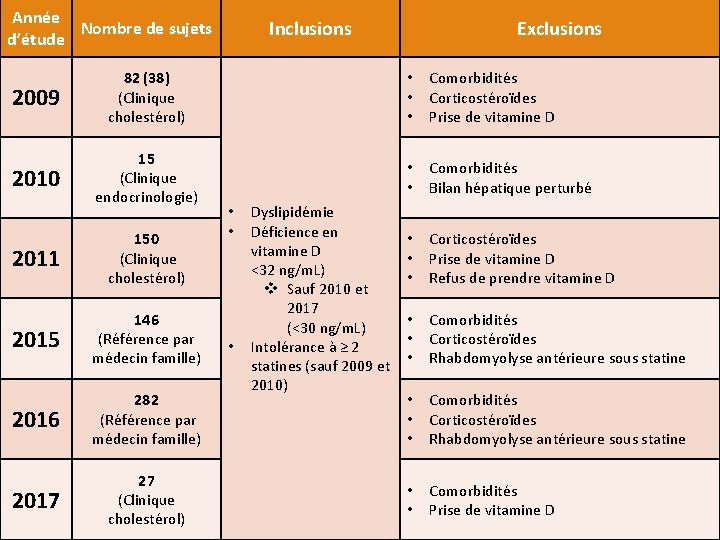
Année Nombre de sujets d’étude Inclusions Exclusions 2009 82 (38) (Clinique cholestérol) • • • Comorbidités Corticostéroïdes Prise de vitamine D 2010 15 (Clinique endocrinologie) • • Comorbidités Bilan hépatique perturbé • • • Corticostéroïdes Prise de vitamine D Refus de prendre vitamine D • • • Comorbidités Corticostéroïdes Rhabdomyolyse antérieure sous statine • • Comorbidités Prise de vitamine D 2011 150 (Clinique cholestérol) 2015 146 (Référence par médecin famille) 2016 282 (Référence par médecin famille) 2017 27 (Clinique cholestérol) • • • Dyslipidémie Déficience en vitamine D <32 ng/m. L) v Sauf 2010 et 2017 (<30 ng/m. L) Intolérance à ≥ 2 statines (sauf 2009 et 2010)

RÉSULTATS

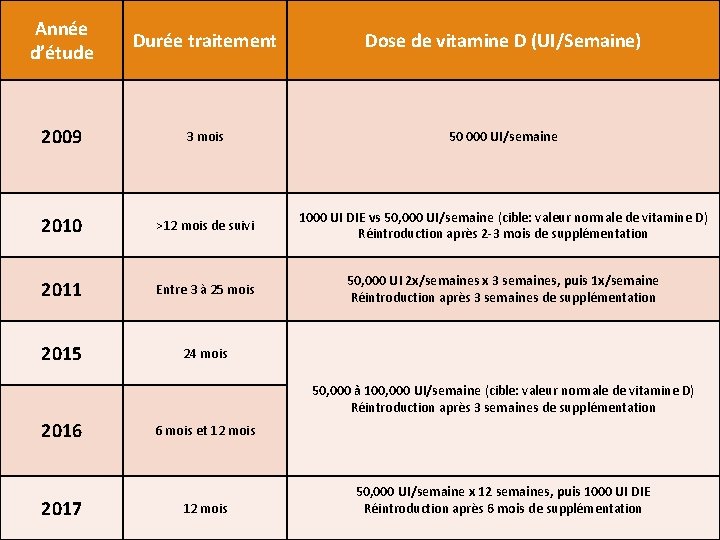
Année d’étude Durée traitement Dose de vitamine D (UI/Semaine) 2009 3 mois 50 000 UI/semaine 2010 >12 mois de suivi 1000 UI DIE vs 50, 000 UI/semaine (cible: valeur normale de vitamine D) Réintroduction après 2 -3 mois de supplémentation 2011 Entre 3 à 25 mois 50, 000 UI 2 x/semaines x 3 semaines, puis 1 x/semaine Réintroduction après 3 semaines de supplémentation 2015 24 mois 50, 000 à 100, 000 UI/semaine (cible: valeur normale de vitamine D) Réintroduction après 3 semaines de supplémentation 2016 2017 6 mois et 12 mois 50, 000 UI/semaine x 12 semaines, puis 1000 UI DIE Réintroduction après 6 mois de supplémentation

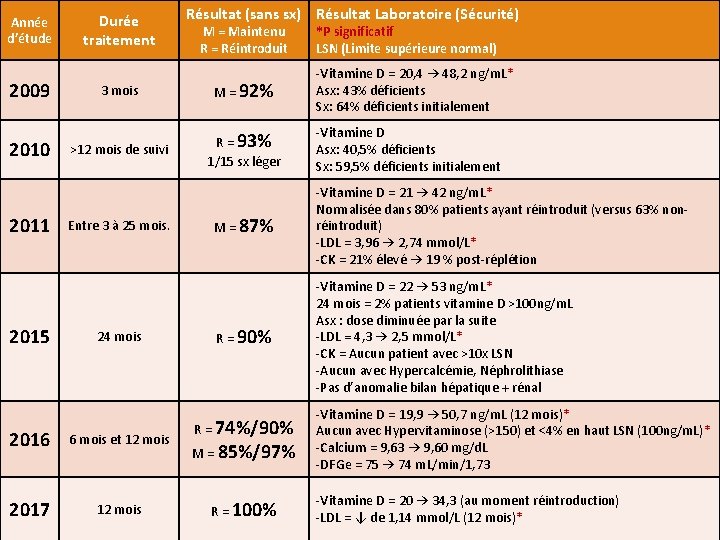
Année d’étude 2009 2010 2011 2015 Durée traitement Résultat (sans sx) Résultat Laboratoire (Sécurité) M = Maintenu R = Réintroduit 3 mois M = 92% >12 mois de suivi R = 93% 1/15 sx léger Entre 3 à 25 mois. 24 mois 2016 6 mois et 12 mois 2017 12 mois *P significatif LSN (Limite supérieure normal) -Vitamine D = 20, 4 → 48, 2 ng/m. L* Asx: 43% déficients Sx: 64% déficients initialement -Vitamine D Asx: 40, 5% déficients Sx: 59, 5% déficients initialement M = 87% -Vitamine D = 21 → 42 ng/m. L* Normalisée dans 80% patients ayant réintroduit (versus 63% nonréintroduit) -LDL = 3, 96 → 2, 74 mmol/L* -CK = 21% élevé → 19 % post-réplétion R = 90% -Vitamine D = 22 → 53 ng/m. L* 24 mois = 2% patients vitamine D >100 ng/m. L Asx : dose diminuée par la suite -LDL = 4, 3 → 2, 5 mmol/L* -CK = Aucun patient avec >10 x LSN -Aucun avec Hypercalcémie, Néphrolithiase -Pas d’anomalie bilan hépatique + rénal R = 74%/90% M = 85%/97% R = 100% -Vitamine D = 19, 9 → 50, 7 ng/m. L (12 mois)* Aucun avec Hypervitaminose (>150) et <4% en haut LSN (100 ng/m. L)* -Calcium = 9, 63 → 9, 60 mg/d. L -DFGe = 75 → 74 m. L/min/1, 73 -Vitamine D = 20 → 34, 3 (au moment réintroduction) -LDL = ↓ de 1, 14 mmol/L (12 mois)*

Et la sécurité dans tout ça? • La peau absorbe 10, 000 à 25, 000 UI de vitamine D/jour d’exposition adéquate au soleil. • Hypercalcémie cliniquement significative : vitamine D > à 240 ng/ml. • Garland et coll: 3667 sujets|10 000 UI/jour o aucun dosage > à 200 ng/m. L • 1934 à 1946 = Usage de dose supra-physiologique pour le traitement de polyarthrite rhumatoïde, asthme et tuberculose (jusqu’à 600 000 UI/jour) o Décès par hypercalcémie (d’où crainte actuelle des hautes doses)

Synthèse des résultats : q 6 études en faveur de la supplémentation v. Réintroduire = 74% à 100% v. Maintenir = 85% à 97% q. Sécuritaire v. Pas d’hypercalcinose ni néphrocalcinose v. Pas d’hypervitaminose v. Pas d’impact sur le bilan hépatique, rénal q. Pas d’étude en défaveur

Discussion (Forces des études) • Issues/Méthodes plutôt comparables entre elles • Suivi long terme (3 mois à 25 mois) • Bons critères d’inclusion/exclusion o Limite facteur de confusion quant à l’origine de la douleur. • Impact sur la sécurité évalué • Validité externe : • Population de référence similaire à la nôtre : Nord Américaine • Mais, redondances des auteurs; Limité aux États-unis

Discussion (Faiblesses des études) • Absence de randomisation • Absence de double aveugle • Facteurs de confusion : o. Différentes statines utilisées lors de la réintroduction o Ex: 2010 = 64% des patients o Moins métabolisées par CYP-3 A 4. . . Majore les résultats o Doses moins fortes lors de la réintroduction.

Discussion (Faiblesses des études) • Subjectivité des douleurs musculosquelettiques ◦ Utilisation de questionnaire basé sur définitions (pour 2011 -2015) ◦ Pas accès aux questionnaires exacts • Perte au suivi : o Aucun pour 2010, 2011, 2017 o 2009 = 44 pertes au suivi (sur 82 patients) similaires* en terme âge/sexe/IMC/Vitamine D o 2015 = 146 → 134 (24 mois) → 103 (12 mois) → 82 (6 mois); pas d’information sur la démographie o 2016 = 282 → 112 (6 et 12 mois); pas d’information sur la démographie

Conclusion pour le clinicien : Pour la supplémentation! Source image: https: //6. viki. io/image/40 fbb 04260794 a 689 c 1 cf 9 b 2 e 83 bdd 0 d. jpeg? x=b&s=460 x 268&e=t&f=t&cb=1

Changement sur notre pratique • Hautes doses (50 000 UI/sem) : o Indication = Myalgie franche aux statines avec dosage dans 3 mois pour ajustement dose (viser dose minimale efficace) v Dosage initiale selon prescripteur o Sécuritaire et aucun effet secondaire noté aux doses prescrites o Réponse rapide (effet attendu en quelques jours à quelques semaines) o Couvert par la RAMQ = Discussion avec pharmacien en date du 2018 -05 -15 : Ø Dosage élevé de 50 000 -100 000 U/semaine serait couvert par RAMQ si prescrit sous forme de « D-Tabs 10 000 U/semaine» , 5 à 10 comprimés. Ø Devrait aussi expliciter la raison de prescription aux pharmaciens. • Prescrire d’emblée à faible dose (10 000 UI/sem) : o Avantages: § Facile à prescrire (prise 1 x/sem) § Traitement des comorbidités (ex : Ostéoporose) § Crainte des patients quant aux effets secondaires des statines o Désavantages : § Financier $ § Polypharmacie Source image: https: //ohmy. disney. com/wp-content/uploads/2014/02/Olaf-from-Frozen-running-in-a-field. jpg

Alternatives • Privilégier les statines causant moins de myalgies : o Rosuvastatine (Crestor) o Pravastatine (Pravachol) o Fluvastatine (Lescol) • Réduire la dose de la statine (dose minimale efficace) • Prise de statine 1 jour/2 • Changer de classe d’hypolipémiant (ex : Ézétimibe)

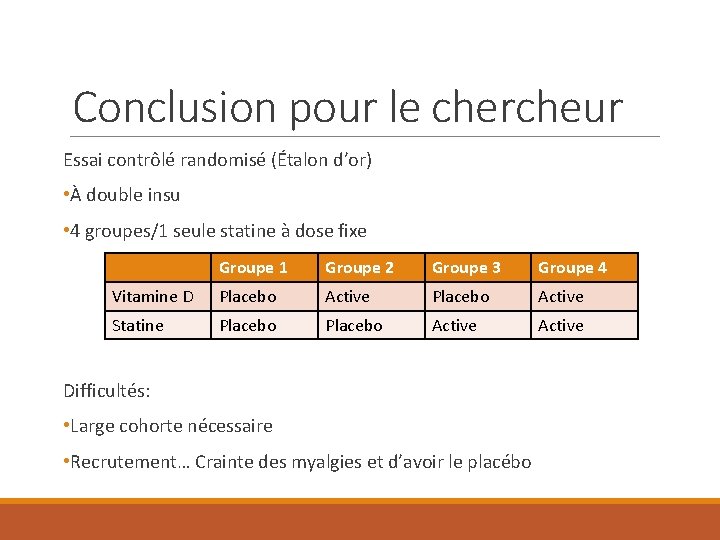
Conclusion pour le chercheur Essai contrôlé randomisé (Étalon d’or) • À double insu • 4 groupes/1 seule statine à dose fixe Groupe 1 Groupe 2 Groupe 3 Groupe 4 Vitamine D Placebo Active Statine Placebo Active Difficultés: • Large cohorte nécessaire • Recrutement… Crainte des myalgies et d’avoir le placébo

Merci! Questions

Références • Michalska-Kasiczak M, Sahebkar A, Mikhailidis DP, et al; Lipid and Blood Pressure Meta-analysis Collaboration (LBPMC) Group. Analysis of vitamin D levels in patients with and without statin-associated myalgia—a systematic review and metaanalysis of 7 studies with 2420 patients. Int J Cardiol. 2015; 178: 111 -116 • Ahmed W, Naseer K, Glueck CJ, et al. Low serum 25 (OH) vitamin D levels (<32 ng/m. L) are associated with reversible myositis-myalgia in statin-treated patients. Transl Res. 2009; 153(1): 11 -16. • Khayznikov M, Hemachrandra K, Pandit R, Kumar A, Wang P, Glueck CJ. Statin intolerance because of myalgia, myositis, myopathy, or myonecrosis can in most cases be safely resolved by vitamin D supplementation. North Am J Med Sci 2015; 7: 86 -93.

• Charles J. Glueck, Shaaista B. Budhani, Silpa S. Masineni, Cesar Abuchaibe, Naseer Khan, Ping Wang & Naila Goldenberg (2011) Vitamin D deficiency, myositis– myalgia, and reversible statin intolerance, Current Medical Research and Opinion, 27: 9, 1683 -1690, DOI: 10. 1185/03007995. 2011. 598144 • Glueck CJ, Abuchaibe C, Wang P. Symptomatic myositismyalgia in hypercholesterolemic statin-treated patients with concurrent vitamin D defi ciency leading to statin intolerance may reflect a reversible interaction between vitamin D defi ciency and statins on skeletal muscle. Med Hypotheses. 2011; 77: 658 -61. • Paul Lee, Jerry R. Greenfield, Lesley V. Campbell. Vitamin D insufficiency-a novel mechanism of statin-induced myalgia? Letters to the editor. Clinical Endocrinology. 2009; 71: 154 -156 • Randy Linde, Lihong Peng, Manisha Desai & David Feldam (2010) The role of vitamin D and SLCOB 1 gene polymorphism in statin-associated myalgias. Dermato. Endocrinology, 2: 2, 77 -84, DOI: 10. 4161/derm. 2. 2. 13509

• Jetty V, Glueck CJ, Wang P, Shah P, Prince M, Lee K, et al. Safety of 50, 000 -100, 000 units of vitamin D 3/week in vitamin D-defi cient, hypercholesterolemic patients with reversible statin intolerance. North Am J Med Sci 2016; 8: 156 -62. • Jenny H. Kang et all. Rechallenging Statin Therapy in Veterans with Statin-Induced Myopathy Post Vitamin D Replenishment. Journal of Pharmacy Practice 2017; Vol 30(5) 521 -527. • Collège des médecins de famille du Canada. Treize examens et traitements sur lesquels les médecins et les patients devraient s’intérroger. Fiche Choisir avec Soins. Janvier 2018

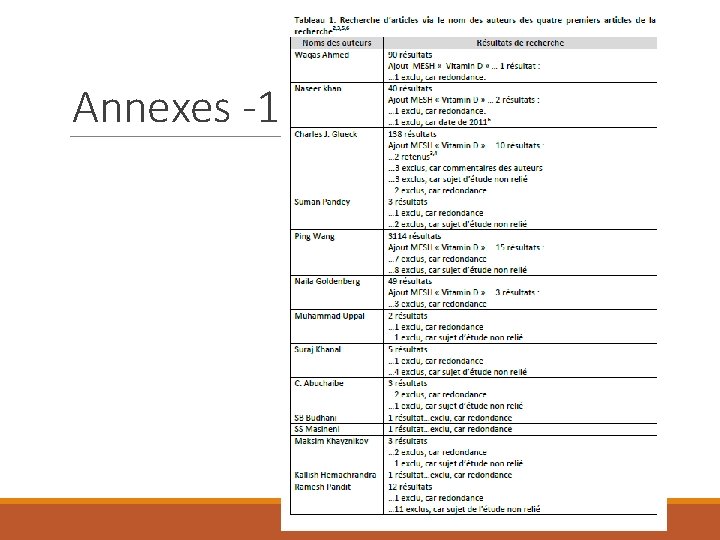
Annexes -1

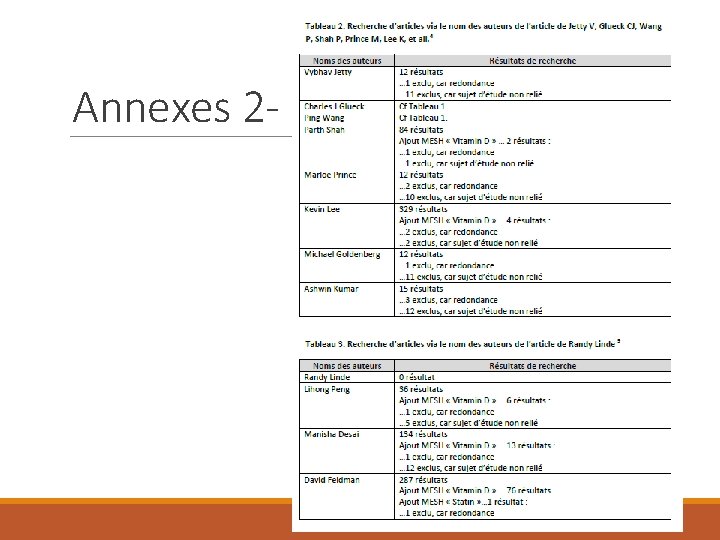
Annexes 2 -

Annexes 3 - Définitions : • « 2014 National Lipid Association’s Statin Muscle Safety Expert Panel » • « National Heart, Lung, and Blood Institute » ___ • Myalgie : Inconfort musculaire tel que douleur non-spécifique, raideur, sensibilité ou crampe avec un niveau de CK normal. • Myopathie : Faiblesse musculaire avec ou sans élévation des CK. • Myosite : Inflammation musculaire • Myonécrose : Inconfort musculaire symptomatique avec élévation des CK (compare au niveau de base); Léger (3 -10 x LSN), modéré (10 -50 x LSN) et sévère (≥ 50 LSN). • Rhabdomyolyse clinique : Myonécroses avec myoglobinurie ou insuffisance rénale aigue.