ADEILEDD ATOMIG TGAU Cemeg CBAC Uned 1 1

ADEILEDD ATOMIG TGAU Cemeg CBAC Uned 1 - 1. 2 TGAU Gwyddoniaeth (Dwyradd) CBAC Uned 2 - 2. 2
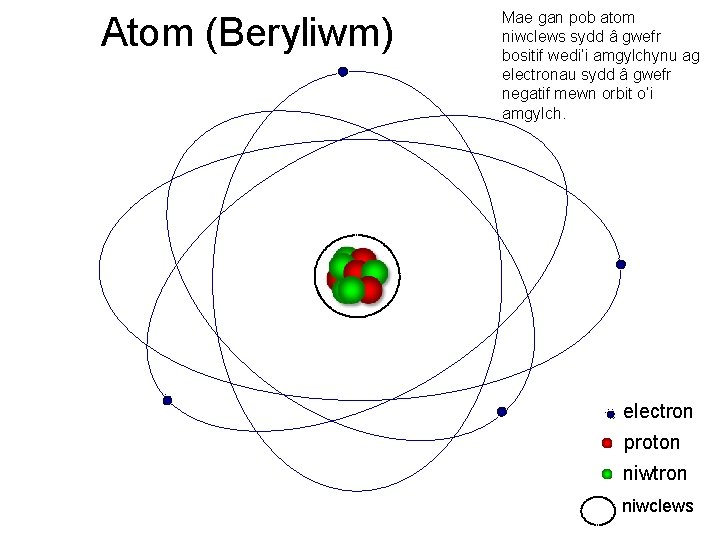
Atom (Beryliwm) Mae gan pob atom niwclews sydd â gwefr bositif wedi’i amgylchynu ag electronau sydd â gwefr negatif mewn orbit o’i amgylch. electron proton niwtron niwclews
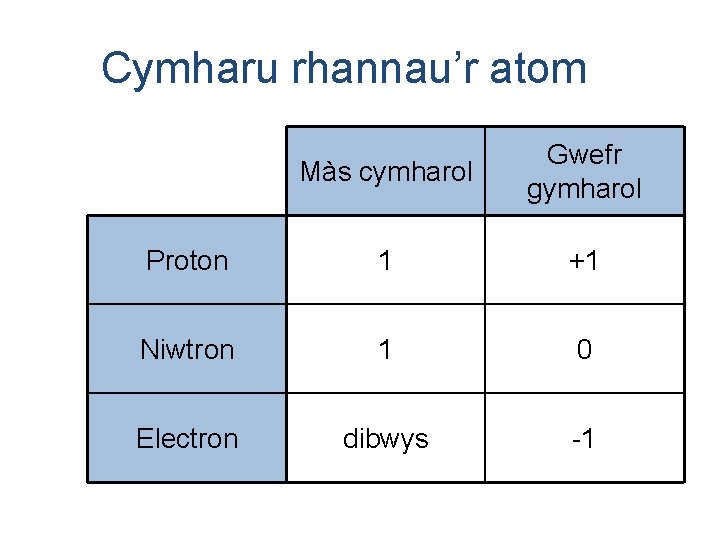
Cymharu rhannau’r atom Màs cymharol Gwefr gymharol Proton 1 +1 Niwtron 1 0 Electron dibwys -1

Yr atom niwtral ac ïonau Nid oes gwefr drydanol gan yr atom cyfan am fod yr un nifer o brotonau positif yn y niwclews ag sydd o electronau negatif sy’n cylchdroi o gwmpas y niwclews. Nid oes gwefr gan niwtron, felly nid yw nifer y niwtronau’n cyfrannu at wefr yr atom. Os yw’r atom yn COLLI electron, mae yna brinder o wefrau negatif, ac felly mae’r atom yn fwy POSITIF. Mae ganddo wefr bositif gyflawn. Mae gennym ïon positif. Yn yr achos yma…. 4 proton positif 4 electron negatif Os yw’r atom yn ENNILL electron, mae yna ormodedd o wefrau negatif, ac felly mae’r atom yn fwy NEGATIF. Mae ganddo wefr negatif gyflawn. Mae gennym ïon negatif.
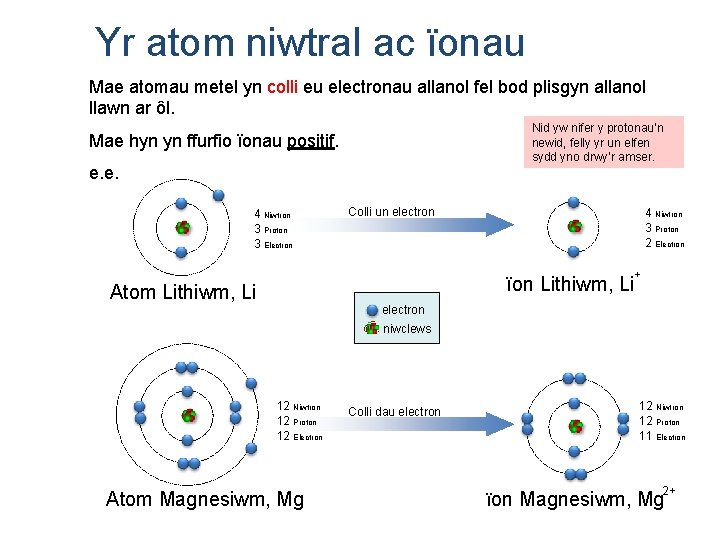
Yr atom niwtral ac ïonau Mae atomau metel yn colli eu electronau allanol fel bod plisgyn allanol llawn ar ôl. Nid yw nifer y protonau’n newid, felly yr un elfen sydd yno drwy’r amser. Mae hyn yn ffurfio ïonau positif. e. e. 4 Niwtron 3 Proton 3 Electron Colli un electron 4 Niwtron 3 Proton 2 Electron + ïon Lithiwm, Li Atom Lithiwm, Li electron niwclews 12 Niwtron 12 Proton 12 Electron Atom Magnesiwm, Mg Colli dau electron 12 Niwtron 12 Proton 11 Electron 2+ ïon Magnesiwm, Mg
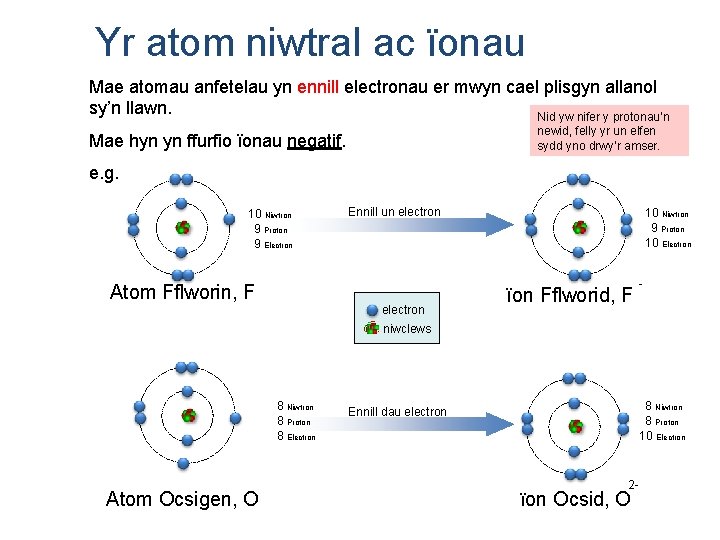
Yr atom niwtral ac ïonau Mae atomau anfetelau yn ennill electronau er mwyn cael plisgyn allanol sy’n llawn. Nid yw nifer y protonau’n newid, felly yr un elfen sydd yno drwy’r amser. Mae hyn yn ffurfio ïonau negatif. e. g. 10 Niwtron 9 Proton 9 Electron Atom Fflworin, F Ennill un electron 10 Niwtron 9 Proton 10 Electron ïon Fflworid, F - niwclews 8 Niwtron 8 Proton 8 Electron Atom Ocsigen, O 8 Niwtron 8 Proton 10 Electron Ennill dau electron 2 - ïon Ocsid, O
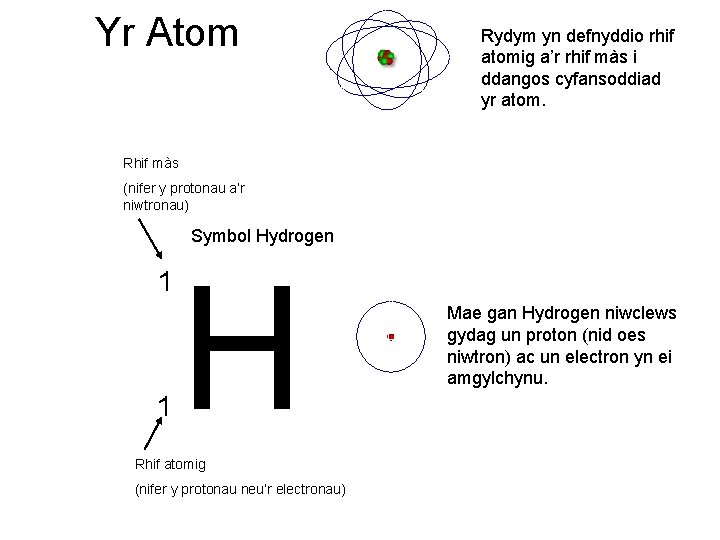
Yr Atom Rydym yn defnyddio rhif atomig a’r rhif màs i ddangos cyfansoddiad yr atom. Rhif màs (nifer y protonau a’r niwtronau) Symbol Hydrogen 1 1 H Rhif atomig (nifer y protonau neu’r electronau) Mae gan Hydrogen niwclews gydag un proton (nid oes niwtron) ac un electron yn ei amgylchynu.
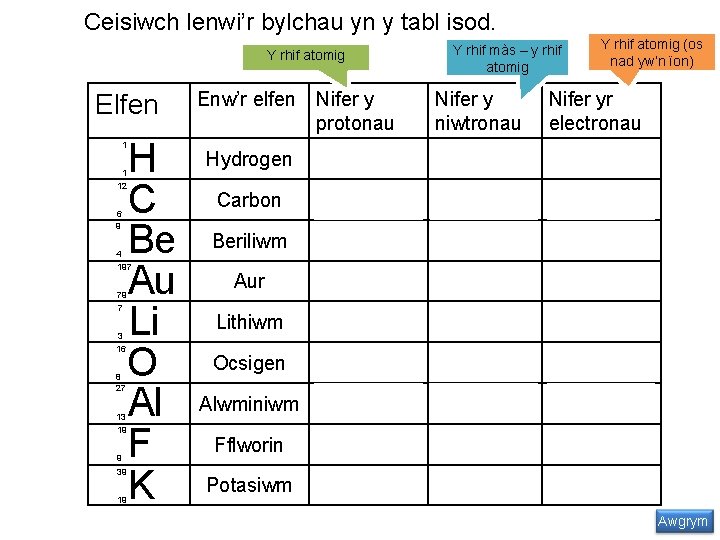
Ceisiwch lenwi’r bylchau yn y tabl isod. Y rhif màs – y rhif atomig Y rhif atomig Elfen H C Be Au Li O Al F K 1 1 12 6 9 4 197 79 7 3 16 8 27 13 19 9 39 19 Enw’r elfen Hydrogen Carbon Beriliwm Aur Lithiwm Ocsigen Alwminiwm Fflworin Potasiwm Nifer y protonau 1 6 4 79 3 8 13 9 19 Nifer y niwtronau 0 6 5 118 4 8 14 10 20 Y rhif atomig (os nad yw’n ïon) Nifer yr electronau 1 6 4 79 3 8 13 9 19 Awgrym

Isotopau Atomau o’r un elfen yw isotopau – mae ganddyn nhw’r un nifer o brotonau ac electronau ond nifer gwahanol o niwtronau. e. e. Clorin Mae gan clorin ddau isotop Clorin-35 a Clorin-37 35 17 Cl 37 17 Cl Protons Protonau 17 ? Neutrons Niwtronau 18 ? 20 ? Electrons Electronau 17 ? Mae’r rhain yn isotopau gan eu bod yn Why arecynnwys these yr un nifer isotopes? o brotonau ond gwahanol nifer o niwtronau.

Màs atomig cymharol(Ar) Gan fod gwahanol elfennau yn cynnwys nifer gwahanol o isotopau, mae eu màs atomig cymharol yn cael ei ddangos yn aml, sef gwerth cymedrig ar gyfer isotopau’r elfen honno (nid yw’n rif cyfan gan amlaf). Er enghraifft: Mae sampl clorin yn cynnwys 25% clorin-37 a 75% clorin -35 Ar (Cl) = (% x màs atomig) + (% x màs isotopig ) 100 Ar (Cl) = (25 x 37) + (75 x 35) 100 = 3550 100 = 35. 5
- Slides: 10