Actividad enzimtica 2013 2 Qu es un catalizador

















- Slides: 32

Actividad enzimática 2013 -2


¿Qué es un catalizador? Es una molécula inorgánica u orgánica que incrementa notablemente la velocidad de las reacciones químicas sin ser modificada o consumida en la reacción Hay de 2 tipos en biología: A) Enzimas proteicas B) Enzimas de RNA

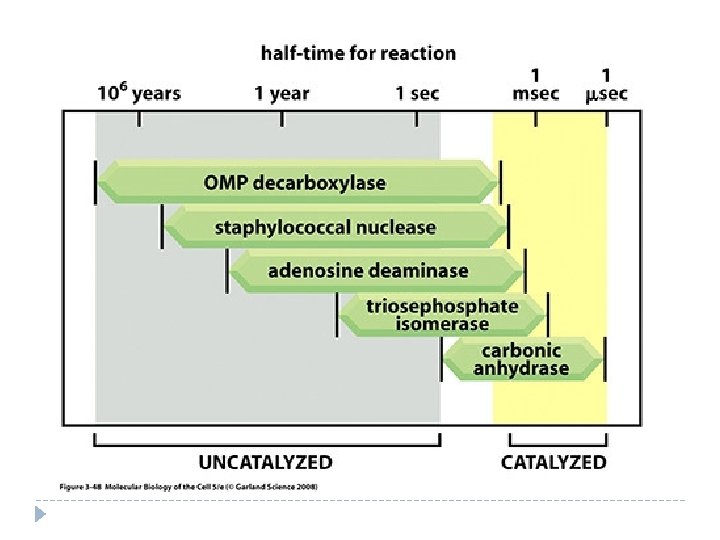
Enzimas Las enzimas son catalizadores que aceleran la velocidad de una reacción y no se consumen o modifican durante ésta.


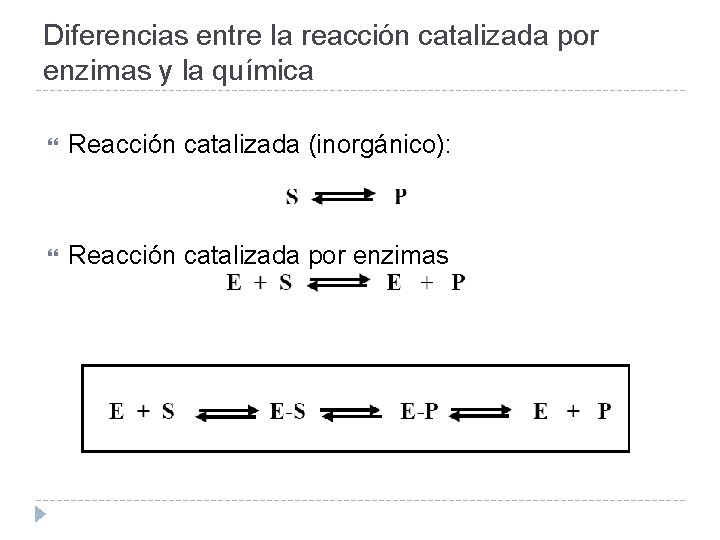
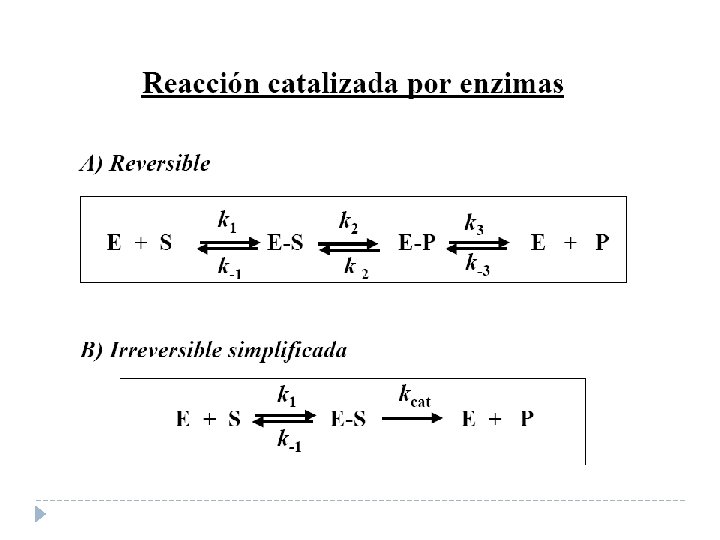
Diferencias entre la reacción catalizada por enzimas y la química Reacción catalizada (inorgánico): Reacción catalizada por enzimas





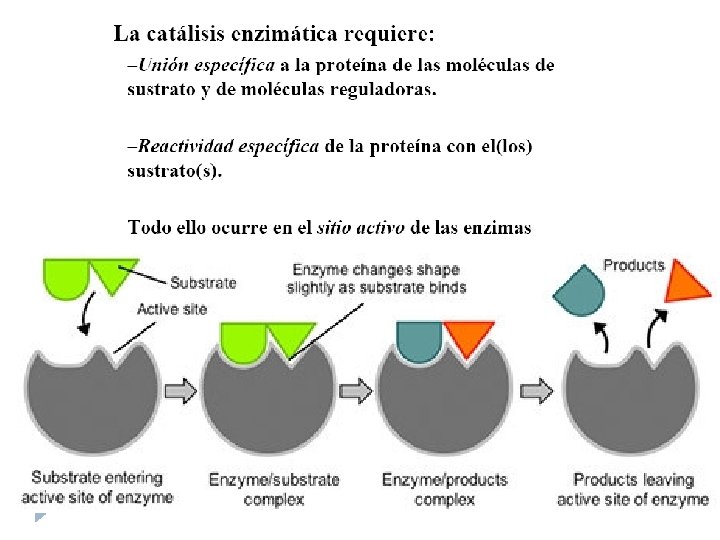
Llave y cerradura E. Fisher, 1894 La enzima tiene un sitio (el sitio activo de la enzima) en el que encaja perfectamente el sustrato, al unirse ambos se lleva a cabo la catálisis

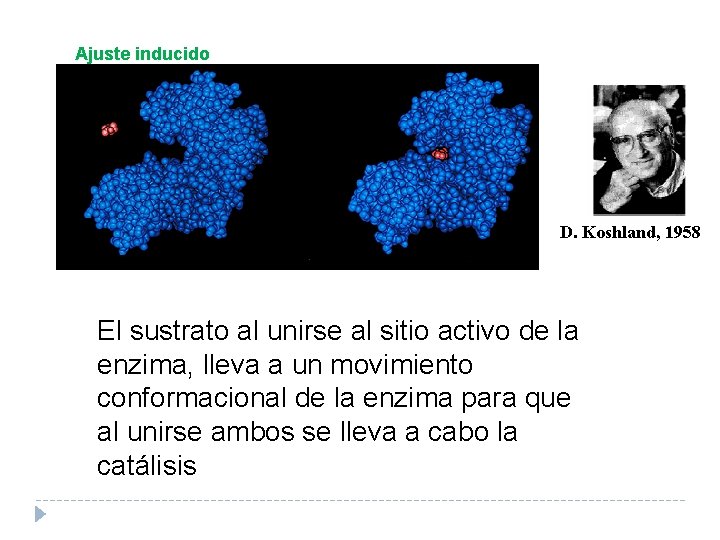
Ajuste inducido D. Koshland, 1958 El sustrato al unirse al sitio activo de la enzima, lleva a un movimiento conformacional de la enzima para que al unirse ambos se lleva a cabo la catálisis

Cofactores Moléculas orgánicas


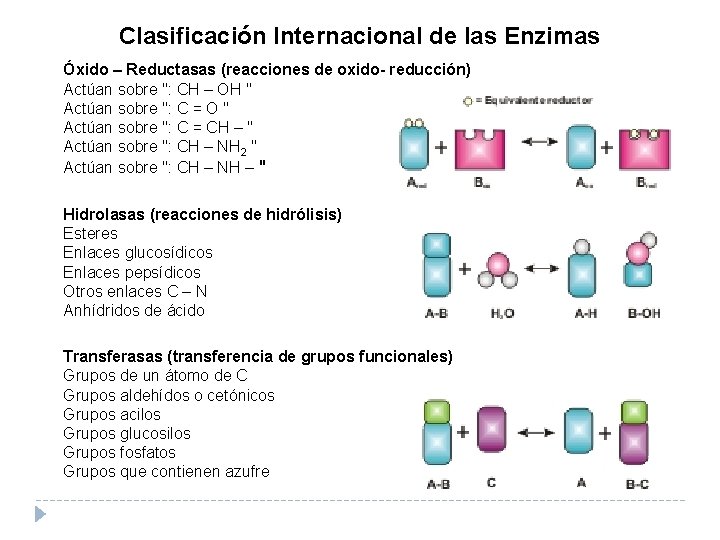
Clasificación Internacional de las Enzimas Óxido – Reductasas (reacciones de oxido- reducción) Actúan sobre ": CH – OH " Actúan sobre ": C = O " Actúan sobre ": C = CH – " Actúan sobre ": CH – NH 2 " Actúan sobre ": CH – NH – " Hidrolasas (reacciones de hidrólisis) Esteres Enlaces glucosídicos Enlaces pepsídicos Otros enlaces C – N Anhídridos de ácido Transferasas (transferencia de grupos funcionales) Grupos de un átomo de C Grupos aldehídos o cetónicos Grupos acilos Grupos glucosilos Grupos fosfatos Grupos que contienen azufre

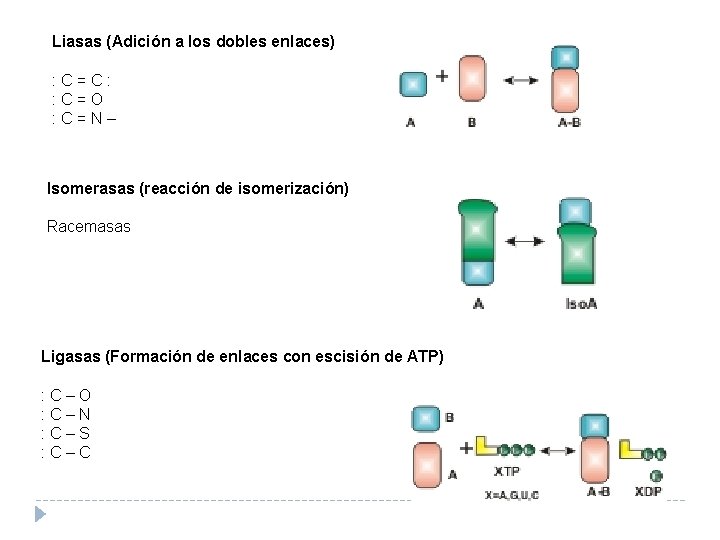
Liasas (Adición a los dobles enlaces) : C=C: : C=O : C=N– Isomerasas (reacción de isomerización) Racemasas Ligasas (Formación de enlaces con escisión de ATP) : C–O : C–N : C–S : C–C


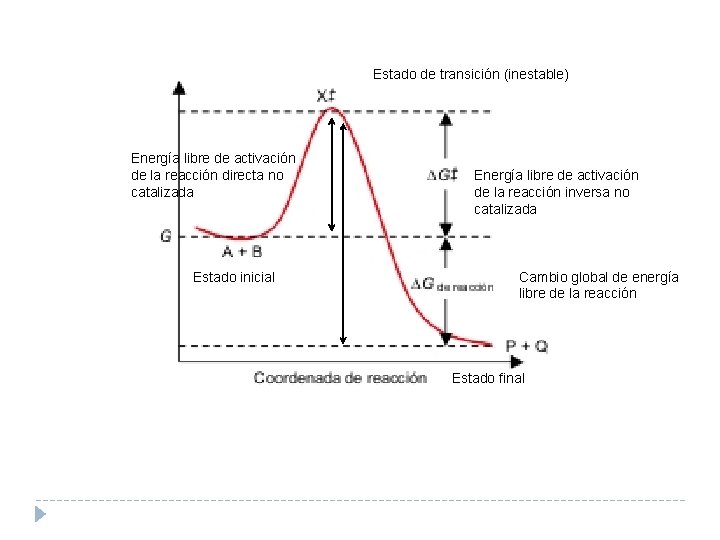
Estado de transición (inestable) Energía libre de activación de la reacción directa no catalizada Estado inicial Energía libre de activación de la reacción inversa no catalizada Cambio global de energía libre de la reacción Estado final

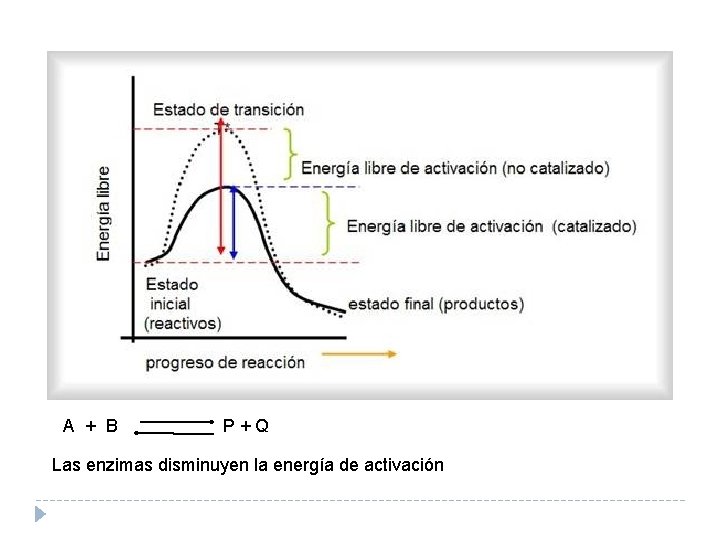
A + B P+Q Las enzimas disminuyen la energía de activación


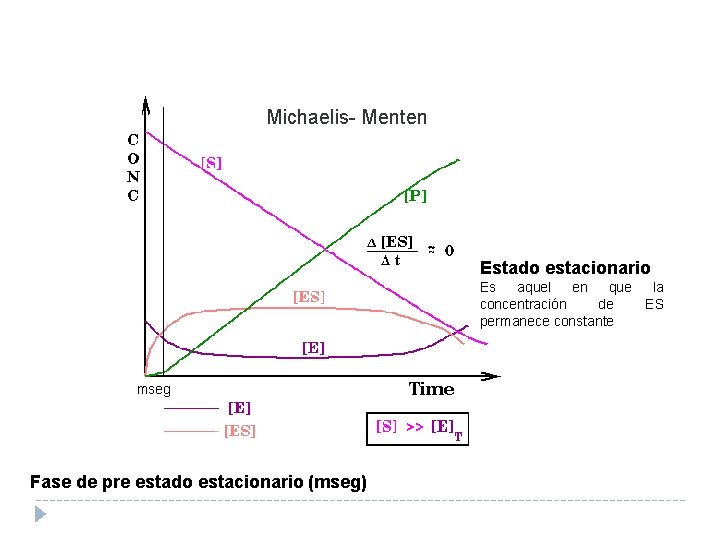
Michaelis- Menten Estado estacionario Es aquel en que la concentración de ES permanece constante mseg Fase de pre estado estacionario (mseg)

Actividad enzimática = Velocidad Actividad y velocidad enzimática son términos ambos dados para lo mismo describir como un sustrato o producto se convierte en producto por unidad de tiempo



Diseño de un ensayo enzimático Para el diseño de un ensayo enzimático se requiere conocer la reacción que se analiza: A) Cuáles son las especies que se requieren: sustrato, la o las coenzimas, el o los cofactores, entre otros; B) La estequiometría completa, C) Los efectos de p. H, temperatura y fuerza iónica sobre la actividad de la enzima.

Continúa… Debe de estar disponible un método para identificar y monitorear cualquier cambio físico, químico o biológico que ocurre durante la conversión del sustrato a producto. Técnicas para determinar los cambios concentraciones de sustrato o producto: A. B. C. D. Espectrofotometría Fluorometría La titulación ácido-base El conteo radioactivo en las

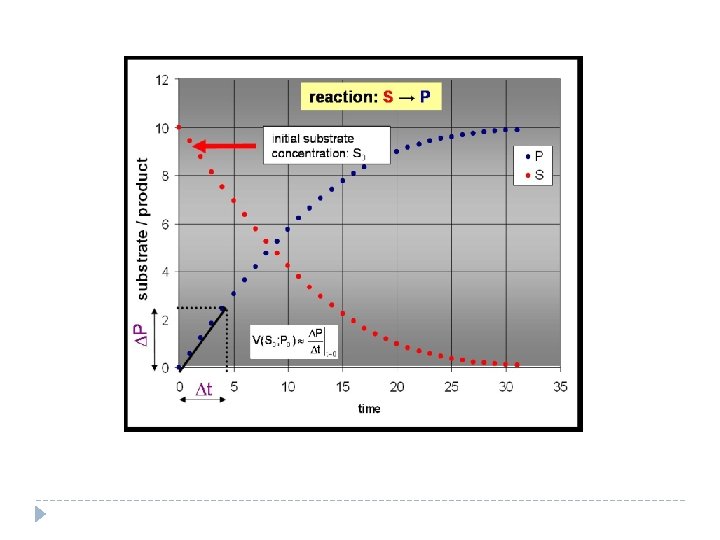
Velocidad inicial de una reacción Ocurre en los primeros minutos de la reacción, en donde existe una relación lineal que se mantiene cuando el consumo del sustrato no va más allá del 5% de la concentración inicial. Los cambios en la linealidad de la reacción pueden deberse a una o varias causas: El decremento en la concentración de sustrato La desnaturalización de la enzima La inhibición causada por el producto de la reacción

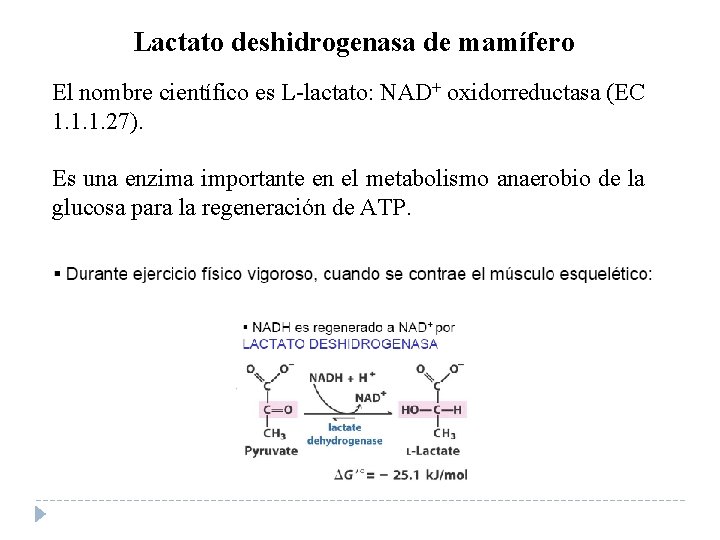
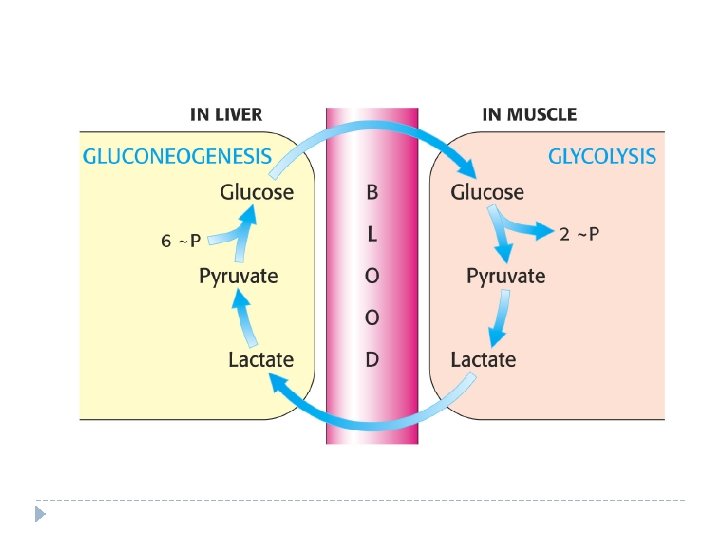
Lactato deshidrogenasa de mamífero El nombre científico es L-lactato: NAD+ oxidorreductasa (EC 1. 1. 1. 27). Es una enzima importante en el metabolismo anaerobio de la glucosa para la regeneración de ATP.


Características de la LDH Tetrámero cada subunidad tiene un peso molecular de 35 k. Da. Subunidad H predomina en el corazón Subunidad M predomina en el músculo y el hígado

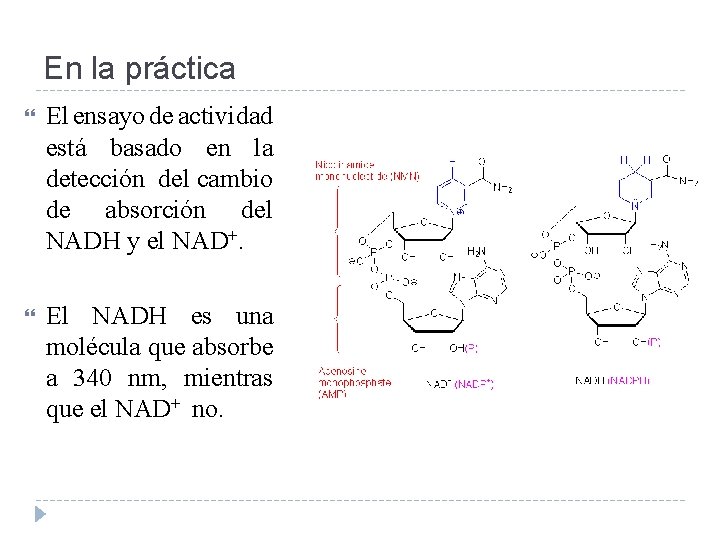
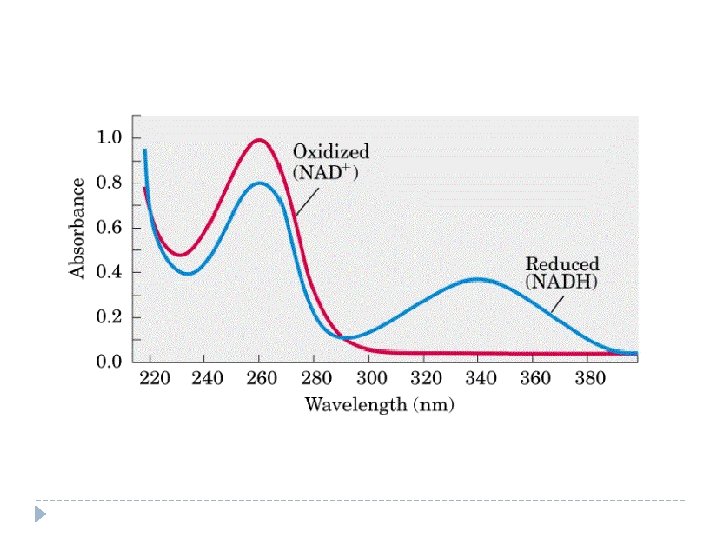
En la práctica El ensayo de actividad está basado en la detección del cambio de absorción del NADH y el NAD+. El NADH es una molécula que absorbe a 340 nm, mientras que el NAD+ no.
