ACIDOS Y BASES CONCEPTOS DE LEWIS Y BRONSTEDLOWRY

ACIDOS Y BASES. CONCEPTOS DE LEWIS Y BRONSTED-LOWRY. Subtema 1. 4 www. lainter. edu. mx 1

Contenidos (1) 1. - Características de ácidos y basees 2. - Evolución histórica del concepto de ácido y base. 1. 1. Teoría de Arrhenius. Limitaciones. 2. 2. Teoría de Brönsted-Lowry. 2. 3. Teoría de Lewis ( ) 3. - Equilibrio de ionización del agua. Concepto de p. H. 4. - Fuerza de ácidos y bases. 4. 1. Ácidos y bases conjugadas. 4. 2. Relación entre Ka y Kb. 4. 3. Cálculos de concentraciones en equilibrio, p. H, constantes, grado de disociación www. lainter. edu. mx 2 www. lainter. edu. mx

Contenidos (2) 5. - Reacciones de hidrólisis de sales (estudio cualitativo). 5. 1. Sales procedentes de ácido fuerte y base débil. 5. 2. Sales procedentes de ácido débil y base fuerte. 5. 3. Sales procedentes de ácido débil y base débil. 5. 4. Sales procedentes de ácido fuerte y base fuerte. 5. 5. Calculo de concentraciones y p. H. ( ) 6. - Disoluciones amortiguadoras. ( ) 7. - Indicadores de ácido-base. ( ) 8. - Valoraciones de ácido-base (volumetrías). 8. 1. Neutralización (práctica de laboratorio). www. lainter. edu. mx 3 www. lainter. edu. mx

Características ÁCIDOS: • Tienen sabor agrio. • Son corrosivos para la piel. • Enrojecen ciertos colorantes vegetales. • Disuelven sustancias • Atacan a los metales desprendiendo H 2. • Pierden sus propiedades al reaccionar con bases. BASES: • Tiene sabor amargo. • Suaves al tacto pero corrosivos con la piel. • Dan color azul a ciertos colorantes vegetales. • Precipitan sustancias disueltas por ácidos. • Disuelven grasas. • Pierden sus propiedades al reaccionar con ácidos. www. lainter. edu. mx 4 www. lainter. edu. mx

Definición de Arrhenius • Publica en 1887 su teoría de “disociación iónica” – Hay sustancias (electrolitos) que en disolución se disocian en cationes y aniones. • ÁCIDO: Sustancia que en disolución acuosa disocia ÁCIDO: cationes H+. • BASE: Sustancia que en disolución acuosa disocia BASE: aniones OH–. www. lainter. edu. mx 5 www. lainter. edu. mx

Disociación • ÁCIDOS: • AH (en disolución acuosa) A– + H+ • Ejemplos: – HCl (en disolución acuosa) Cl– + H+ – H 2 SO 4 (en disolución acuosa) SO 42– + 2 H+ • BASES: • BOH (en disolución acuosa) B + + OH– • Ejemplo: – Na. OH (en disolución acuosa) Na+ + OH– www. lainter. edu. mx 6 www. lainter. edu. mx

Neutralización • Se produce al reaccionar un ácido con una base por formación de agua: • H+ + OH– — H 2 O • El anión que se disoció del ácido y el catión que se disoció de la base quedan en disolución inalterados (sal disociada): • Na. OH +HCl — H 2 O + Na. Cl (Na+ + Cl–) www. lainter. edu. mx 7 www. lainter. edu. mx

Teoría de Brönsted-Lowry. • • ÁCIDOS: “Sustancia que en disolución cede H+”. BASES: “Sustancia que en disolución acepta H+”. www. lainter. edu. mx 8 www. lainter. edu. mx
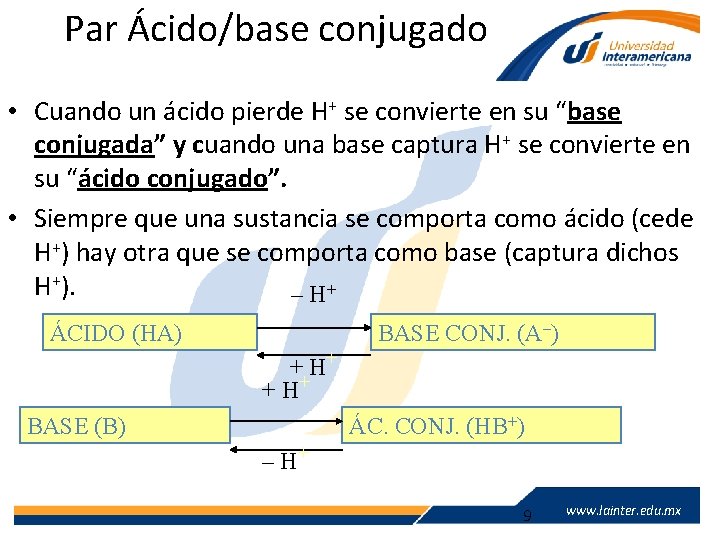
Par Ácido/base conjugado • Cuando un ácido pierde H+ se convierte en su “base conjugada” y cuando una base captura H+ se convierte en su “ácido conjugado”. • Siempre que una sustancia se comporta como ácido (cede H+) hay otra que se comporta como base (captura dichos H+). – H+ ÁCIDO (HA) BASE CONJ. (A–) + H+ BASE (B) ÁC. CONJ. (HB+) – H+ www. lainter. edu. mx 9 www. lainter. edu. mx

Ejemplo de par Ácido/base conjugado Disociación de un ácido: • HCl (g) + H 2 O (l) H 3 O+(ac) + Cl– (ac) • En este caso el H 2 O actúa como base y el HCl al perder el H+ se transforma en Cl– (base conjugada) Disociación de una base: • NH 3 (g) + H 2 O (l) NH 4+ + OH– • En este caso el H 2 O actúa como ácido pues cede H+ al NH 3 que se transforma en NH 4+ (ácido conjugado) www. lainter. edu. mx 10 www. lainter. edu. mx

Teoría de Lewis ( ) ÁCIDOS: • “Sustancia que contiene al menos un átomo capaz de aceptar un par de electrones y formar un enlace covalente coordinado”. BASES: • “Sustancia que contiene al menos un átomo capaz de aportar un par de electrones para formar un enlace covalente coordinado”. www. lainter. edu. mx 11 www. lainter. edu. mx

Teoría de Lewis (Ejemplos) • HCl (g) + H 2 O (l) H 3 O+(ac) + Cl– (ac) En este caso el HCl es un ácido porque contiene un átomo (de H) que al disociarse y quedar como H+ va a aceptar un par de electrones del H 2 O formando un enlace covalente coordinado (H 3 O+). • NH 3 (g) + H 2 O (l) NH 4+ + OH– En este caso el NH 3 es una base porque contiene un átomo (de N) capaz de aportar un par de electrones en la formación del +). enlace covalente coordinado (NH www. lainter. edu. mx 4 12

Teoría de Lewis (cont. ) • De esta manera, sustancias que no tienen átomos de hidrógeno, como el Al. Cl 3 pueden actuar como ácidos: • Al. Cl 3 + : NH 3 Cl 3 Al: NH 3 • Cl H | | | Cl–Al + : N–H Cl–Al N–H | | Cl H www. lainter. edu. mx 13 www. lainter. edu. mx

Equilibrio de ionización del agua. • La experiencia demuestra que el agua tiene una pequeña conductividad eléctrica lo que indica que está parcialmente disociado en iones: • 2 H 2 O (l) H 3 O+(ac) + OH– (ac) • H 3 O+ · OH– Kc = —————— H 2 O 2 • Como H 2 O es constante por tratarse de un líquido, llamaremos Kw = Kc · H 2 O 2 • conocido como “producto iónico del agua” producto iónico del agua www. lainter. edu. mx 14 www. lainter. edu. mx

Concepto de p. H. • El valor de dicho producto iónico del agua es: KW (25ºC) = 10– 14 M 2 • En el caso del agua pura: • ———– + – H 3 O = OH = 10– 14 M 2 = 10– 7 M • Se denomina p. H a: • Y para el caso de agua pura, como H 3 O+ =10– 7 M: www. lainter. edu. mx • p. H = – log 10– 7 = 7 15 www. lainter. edu. mx

Tipos de disoluciones • • • Ácidas: H 3 O+ > 10– 7 M p. H < 7 Básicas: H 3 O+ < 10– 7 M p. H > 7 Neutras: H 3 O+ = 10– 7 M p. H = 7 En todos los casos: Kw = H 3 O+ · OH– luego si H 3 O+ aumenta (disociación de un ácido), entonces OH– debe disminuir para que el producto de ambas concentraciones continúe valiendo 10– 14 M 2 www. lainter. edu. mx 16 www. lainter. edu. mx
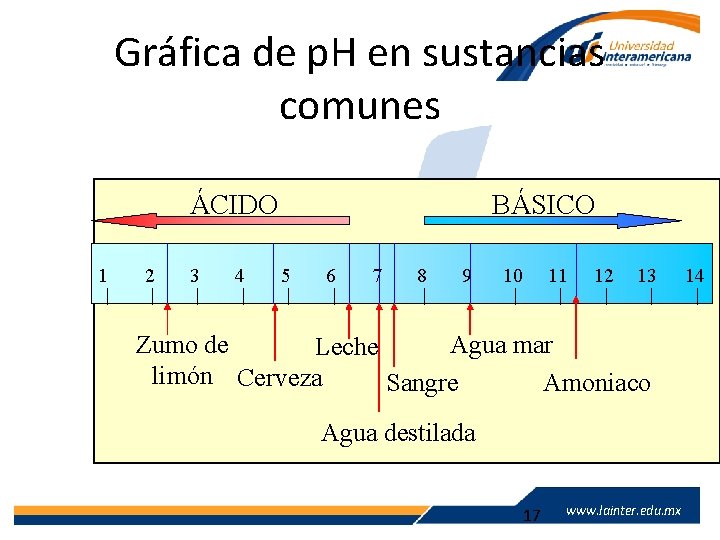
Gráfica de p. H en sustancias comunes ÁCIDO 1 2 3 4 BÁSICO 5 6 7 8 9 10 11 12 13 14 Zumo de Agua mar Leche limón Cerveza Sangre Amoniaco Agua destilada www. lainter. edu. mx 17 www. lainter. edu. mx

18 Concepto de p. OH. • A veces se usa este otro concepto, casi idéntico al de p. H: • Como Kw = H 3 O+ · OH– = 10– 14 M 2 • Aplicando logaritmos y cambiando el signo tendríamos: • p. H + p. OH = 14 • para una temperatura de 25ºC. www. lainter. edu. mx

Ejemplo: El p. H de una disolución acuosa es 12, 6. • • ¿Cual será la OH– y el p. OH a la temperatura de 25ºC? p. H = – log H 3 O+ = 12, 6, de donde se deduce que: H 3 O+ = 10–p. H = 10– 12, 6 M = 2, 5 · 10– 13 M Como Kw = H 3 O+ · OH– = 10– 14 M 2 entonces: KW 10– 14 M 2 OH– = —————— = 0, 04 M H 3 O+ 2, 5 · 10– 13 M • p. OH = – log OH– = – log 0, 04 M = 1, 4 • Comprobamos como p. H + p. OH = 12, 6 + 1, 4 = 14 www. lainter. edu. mx 19 www. lainter. edu. mx

Problema de Selectividad (Marzo 97) Ejercicio A: Una disolución de ácido sulfú-rico tiene una densidad de 1, 2 g/ml y una riqueza del 20 % en peso. a) Calcule su concentración expresada en a) moles/litro y en gramos/litro. b) Calcule el p. H de una b) disolución preparada diluyendo mil veces la anterior. a) ms a) % = —— x 100 = ——— x 100 mdn Vdn x d ms % x d 20 x 1, 2 g conc (g/L) = ————— = 240 g/L – 3 Vdn 100 10 L x 100 ns ms conc(g/L) 240 g/L Molaridad = ———— Vdn x Ms Ms 98 g/mol Molaridad = 2, 45 mol/L +] = –log (2 x 2, 45 x 10– 3 M) = 2, 35 b) p. H = –log [H O b) 2, 35 3 www. lainter. edu. mx 20

Electrolitos fuertes y débiles • Electrolitos fuertes: ( ) Están totalmente disociados – Ejemplos: HCl (ac) Cl– + H+ Na. OH (ac) Na+ + OH– • Electrolitos débiles: ( ) Están disociados parcialmente – Ejemplos: CH 3–COOH (ac) CH 3–COO– + H+ NH (ac)+ H O NH + + OH– 3 2 4 www. lainter. edu. mx 21 www. lainter. edu. mx
![Electrolitos fuertes y débiles Ácido fuerte [HA] [A–] [H+] Ácido débil [HA] [A–] [H Electrolitos fuertes y débiles Ácido fuerte [HA] [A–] [H+] Ácido débil [HA] [A–] [H](http://slidetodoc.com/presentation_image_h/afa607c06fb4831d50b5d743f16a737c/image-22.jpg)
Electrolitos fuertes y débiles Ácido fuerte [HA] [A–] [H+] Ácido débil [HA] [A–] [H + ] www. lainter. edu. mx 22 www. lainter. edu. mx

Ejemplo: Justifica porqué el ión HCO 3– • • actúa como ácido frente al Na. OH y como base frente al HCl. El Na. OH proporciona OH– a la disolución: Na. OH (ac) Na+ + OH– por lo que HCO 3– + OH– CO 32– + H 2 O es decir, el ión HCO 3– actúa como ácido. • • El HCl proporciona H+ a la disolución: HCl (ac) H+ + Cl– por lo que HCO 3– + H+ H 2 CO 3 (CO 2 + H 2 O) es decir, el ión HCO 3– actúa como base www. lainter. edu. mx 23 www. lainter. edu. mx

Fuerza de ácidos. • En disoluciones acuosas diluidas ( H 2 O constante) la fuerza de un ácido HA depende de la constante de equilibrio: • HA + H 2 O A– + H 3 O+ A– · H 3 O+ Kc = —————— Kc · H 2 O = —————— HA · H 2 O HA constante de disociación (K acidez) www. lainter. edu. mx 24 www. lainter. edu. mx

Fuerza de ácidos (cont. ). • Según el valor de Ka hablaremos de ácidos fuertes o débiles: • Si Ka > 100 El ácido es fuerte y estará fuerte disociado casi en su totalidad. • Si Ka < 1 El ácido es débil y estará sólo parcialmente disociado. • Por ejemplo, el ácido acético (CH 3–COOH) es un ácido débil ya que su Ka = 1, 8 · 10– 5 M www. lainter. edu. mx 25 www. lainter. edu. mx
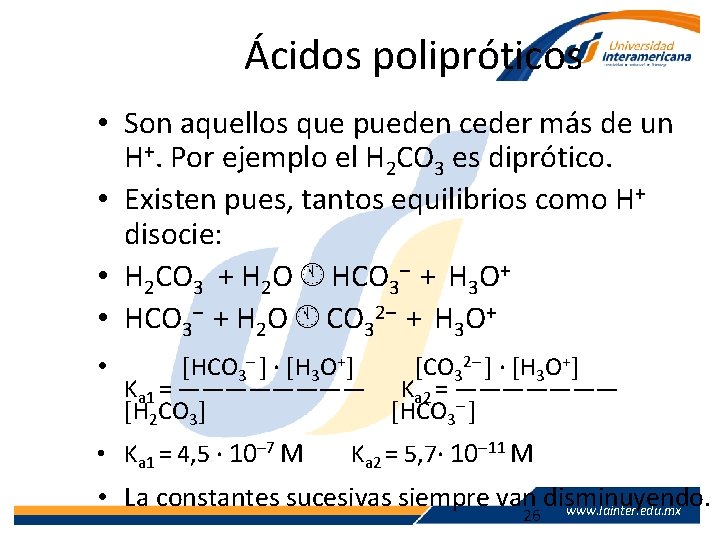
Ácidos polipróticos • Son aquellos que pueden ceder más de un H+. Por ejemplo el H 2 CO 3 es diprótico. • Existen pues, tantos equilibrios como H+ disocie: • H 2 CO 3 + H 2 O HCO 3– + H 3 O+ • HCO 3– + H 2 O CO 32– + H 3 O+ • HCO 3– · H 3 O+ CO 32– · H 3 O+ Ka 1 = ———— Ka 2 = ——————— H 2 CO 3 HCO 3– • Ka 1 = 4, 5 · 10– 7 M Ka 2 = 5, 7· 10– 11 M • La constantes sucesivas siempre van disminuyendo. www. lainter. edu. mx 26

Ejemplo: Sabiendo que las constantes de acidez del ácido fosfórico son: Ka 1 = 7, 5 x 10– 3, Ka 2 = 6, 2 x 10– 8 y Ka 3 = 2, 2 x 10– 13, calcular las concentraciones de los iones H 3 O+, H 2 PO 4–, HPO 42– y PO 43– en una disolución de H 3 PO 4 0, 08 M. Equilibrio 1: H 3 PO 4 + H 2 O H 2 PO 4– + H 3 O+ c. in. (mol/l): 0, 08 0 c. eq. (mol/l): 0, 08 – x x x = 0, 021 www. lainter. edu. mx 27 www. lainter. edu. mx
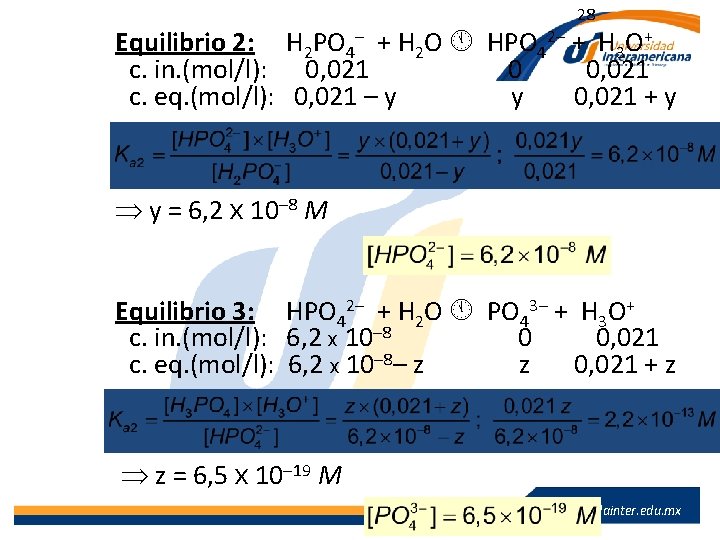
28 Equilibrio 2: H 2 PO 4– + H 2 O HPO 42– + H 3 O+ c. in. (mol/l): 0, 021 0, 021 c. eq. (mol/l): 0, 021 – y 0, 021 + y y = 6, 2 x 10– 8 M Equilibrio 3: HPO 42– + H 2 O PO 43– + H 3 O+ c. in. (mol/l): 6, 2 x 10– 8 0, 021 c. eq. (mol/l): 6, 2 x 10– 8– z 0, 021 + z z = 6, 5 x 10– 19 M www. lainter. edu. mx
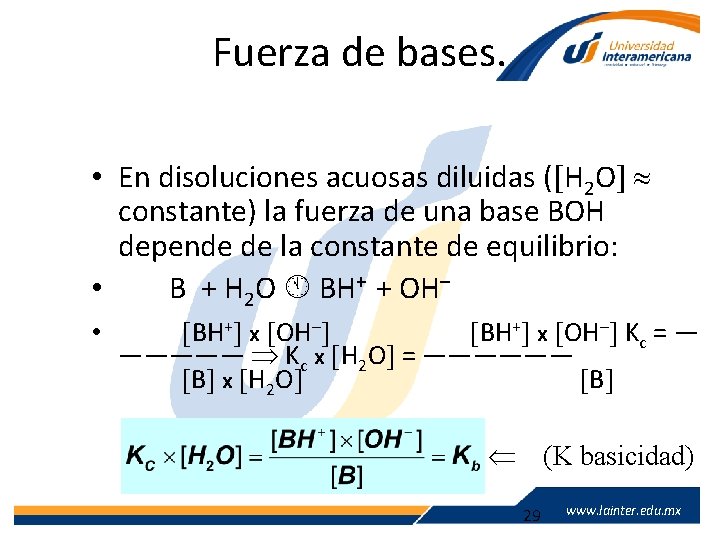
Fuerza de bases. • En disoluciones acuosas diluidas ( H 2 O constante) la fuerza de una base BOH depende de la constante de equilibrio: • B + H 2 O BH+ + OH– • BH+ x OH– Kc = — ————— Kc x H 2 O = —————— B x H 2 O B (K basicidad) www. lainter. edu. mx 29 www. lainter. edu. mx

Fuerza de ácidos y bases (p. K) • Al igual que el p. H se denomina p. K a: • p. Ka= – log Ka ; p. Kb= – log Kb • Cuanto mayor es el valor de Ka o Kb mayor es la fuerza del ácido o de la base. • Igualmente, cuanto mayor es el valor de p. Ka o p. Kb menor es la fuerza del ácido o de la base. www. lainter. edu. mx 30 www. lainter. edu. mx

Ejemplo: Determinar el p. H y el p. OH de una disolución 0, 2 M de NH 3 sabiendo que Kb (25ºC) = 1, 8 · 10– 5 M • Equilibrio: NH 3 + H 2 O NH 4+ + OH– • conc. in. (mol/l): 0, 2 0 0 • conc. eq. (mol/l): 0, 2 – x x • NH 4+ x OH– x 2 Kb = ——————— = 1, 8 x 10– 5 M NH 3 0, 2 – x • De donde se deduce que x = OH– = 1, 9 x 10– 3 M • p. OH = – log OH– = – log 1, 9 x 10– 3 = 2, 72 • p. H = 14 – p. OH = 14 – 2, 72 = 11, 28 www. lainter. edu. mx 31 www. lainter. edu. mx
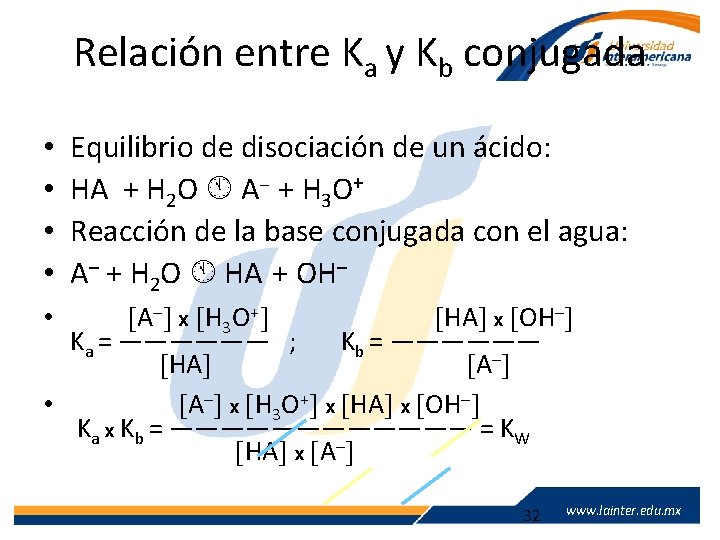
Relación entre Ka y Kb conjugada • • Equilibrio de disociación de un ácido: HA + H 2 O A– + H 3 O+ Reacción de la base conjugada con el agua: A– + H 2 O HA + OH– A– x H 3 O+ HA x OH– Ka = —————— ; Kb = —————— HA A– • A– x H 3 O+ x HA x OH– Ka x Kb = —————— = KW HA x A– • www. lainter. edu. mx 32 www. lainter. edu. mx

Relación entre Ka y Kb conjugada (cont. ). • En la práctica, esta relación (Ka x Kb = KW) significa que: • Si un ácido es fuerte su base conjugada es débil. • Si un ácido es débil su base conjugada es fuerte. • A la constante del ácido o base conjugada en la reacción con el agua se le suele llamar constante de hidrólisis (Kh). www. lainter. edu. mx 33 www. lainter. edu. mx

Ejemplo: Calcular la Kb del KCN si sabemos que la Ka del HCN vale 4, 9 · 10– 10 M. • El HCN es un ácido débil (constante muy pequeña). Por tanto, su base conjugada, el CN –, será una base relativamente fuerte. Su reacción con el agua será: • CN– + H 2 O HCN + OH– • KW 10– 14 M 2 – 5 Kb = —————— = 2, 0 x 10 M Ka 4, 9 x 10– 10 M www. lainter. edu. mx 34 www. lainter. edu. mx

Relación entre la constante y el grado de disociación “ ” • En la disociación de un ácido o una base • Igualmente: • En el caso de ácidos o bases muy débiles (Ka/c o Kb/c < 10– 4), se desprecia frente a 1 con lo que: Ka = c 2 (Kb = c 2 ) • De donde: www. lainter. edu. mx 35 www. lainter. edu. mx

Problema de Selectividad (Marzo 98) Ejemplo: Una disolución de HBO 2 10 -2 M tiene un de p. H de 5, 6. a) Razone si el ácido y su base a) conjugada serán fuertes o débiles. b) Calcule la constante b) de disociación del ácido (Ka). c) Cal-cule, si es posible, la c) constante de basicidad del ion borato (Kb). d) Si 100 ml de d) esta disolución de HBO 2 se mezclan con 100 ml de una disolución 10 -2 M de hidróxido sódico, ¿qué concentración a)de la base conjugada se obtendrá? [H O+] = 10–p. H = 10– 5, 6 = 2, 51 x 10– 6 M 3 =[H 3 O+]/c = 2, 51 x 10– 6 M/ 10 -2 M = 2, 51 x 10– 4 lo que significa que está disociado en un 0, 025 % luego se trata de un ácido débil. Su base conjugada, BO 2–, será pues, relativamente fuerte. b) K b) a = c x 2 = 10 -2 M x(2, 51 x 10– 4)2 = 6, 3 x 10– 10 c) K c) b = Kw/Ka = 10– 14/ 6, 3 x 10– 10 = 1, 58 x 10– 5 www. lainter. edu. mx 36–] = 5 d) Se neutralizan exactamente: [BO x 10– 3 M d) 2

Problema Selectividad (Junio 98) Ejercicio B: En un laboratorio se tienen dos matraces, uno conteniendo 15 ml de HCl cuya concentración es 0, 05 M y el otro 15 ml de ácido etanoico (acético) de concentración 0, 05 M a) Calcule el p. H de cada una de ellas. b) ¿Qué cantidad de a) b) agua se deberá añadir a la más ácida para que el p. H de las dos disoluciones sea el mismo? Dato: Ka (ácido etanoico) = a) HCl es ácido fuerte luego está totalmente disociado, a) x 10 -5 1, 8 por lo que [H 3 O+] = 0, 05 M p. H = –log [H 3 O+] = –log 0, 05 = 1, 30 CH 3 COOH es ácido débil por lo que: Ka 1, 8 · 10 -5 M = —— = ————— = 0, 019 c 0, 05 M [H 3 O+] = c = 0, 05 M x 0, 019 = 9, 5 x 10 -4 M p. H = –log [H 3 O+] = –log 9, 5 x 10 -4 = 3, 0 37 www. lainter. edu. mx

Problema Selectividad (Junio 98) Ejercicio B: En un laboratorio se tienen dos matraces, uno conteniendo 15 ml de HCl cuya concentración es 0, 05 M y el otro 15 ml de ácido etanoico (acético) de concentración 0, 05 M a) Calcule el p. H de cada una de ellas. b) ¿Qué cantidad de a) b) agua se deberá añadir a la más ácida para que el p. H de las dos disoluciones sea el mismo? Dato: Ka (ácido etanoico) = 1, 8 x 10 -5 + b) n (H b) 3 O ) en HCl = V x Molaridad = 0, 015 l x 0, 05 M = = 7, 5 x 10 -4 mol. Para que el p. H sea 3, 0 [H 3 O+] = 10 -3 M que será también la [HCl] ya que está totalmente disociado. El volumen en el que deberán estar disueltos estos moles es: V = n/Molaridad = 7, 5 x 10 -4 mol/ 10 -3 mol·l-1 = 0, 75 litros www. lainter. edu. mx 38 www. lainter. edu. mx Luego habrá que añadir (0, 75 – 0, 015) litros = 735 ml

Hidrólisis de sales • Es la reacción de los iones de una sal con el agua. • Sólo es apreciable cuando estos iones proceden de un ácido o una base débil: • Hidrólisis ácida (de un catión): • NH 4+ + H 2 O NH 3 + H 3 O+ • Hidrólisis básica (de un anión): • CH 3–COO– + H 2 O CH 3–COOH + OH– www. lainter. edu. mx 39 www. lainter. edu. mx

Tipos de hidrólisis. • Según procedan el catión y el anión de un ácido o una base fuerte o débil, las sales se clasifican en: • Sales procedentes de ácido fuerte y base fuerte. – Ejemplo: Na. Cl • Sales procedentes de ácido débil y base fuerte. – Ejemplo: Na. CN • Sales procedentes de ácido fuerte y base débil. – Ejemplo: NH 4 Cl • Sales procedentes de ácido débil y base débil. – Ejemplo: NH 4 CN www. lainter. edu. mx 40 www. lainter. edu. mx

Sales procedentes de ácido fuerte y base fuerte. • Ejemplo: Na. Cl • NO SE PRODUCE HIDRÓLISIS ya que tanto el Na+ que es un ácido muy débil como el Cl – que es una base muy débil apenas reaccionan con agua. Es decir los equilibrios: • Na+ + 2 H 2 O Na. OH + H 3 O+ • Cl– + H 2 O HCl + OH– • están muy desplazado hacia la izquierda. www. lainter. edu. mx 41 www. lainter. edu. mx

Sales procedentes de ácido débil y base fuerte. – Ejemplo: Na+CH 3–COO • 3 • SE PRODUCE HIDRÓLISIS BÁSICA ya que el Na+ es un ácido muy débil y apenas reacciona con agua, pero el CH 3–COO– es una base fuerte y si reacciona con ésta de forma significativa: • CH 3–COO– + H 2 O CH 3–COOH + OH– • lo que provoca que el p. H > 7 (dis. básica). www. lainter. edu. mx 42 www. lainter. edu. mx

Sales procedentes de ácido Ejemplo: NH 4 fuerte y base débil. Cl • 4 • SE PRODUCE HIDRÓLISIS ÁCIDA ya que el NH 4+ es un ácido relativamente fuerte y reacciona con agua mientras que el Cl– es una base débil y no lo hace de forma significativa: • NH 4+ + H 2 O NH 3 + H 3 O+ • lo que provoca que el p. H < 7 (dis. ácida). www. lainter. edu. mx 43 www. lainter. edu. mx

Sales procedentes de ácido débil Ejemplo: NH 4 CN y base débil. • 4 • En este caso tanto el catión NH 4+ como el anión CN– se hidrolizan y la disolución será ácida o básica según qué ion se hidrolice en mayor grado. • Como Kb(CN–) = 2 · 10– 5 M y Ka(NH 4+) = 5, 6 · 10– 10 M , en este caso, la disolución es básica ya que Kb(CN–) es mayor que Ka(NH 4+) www. lainter. edu. mx 44 www. lainter. edu. mx
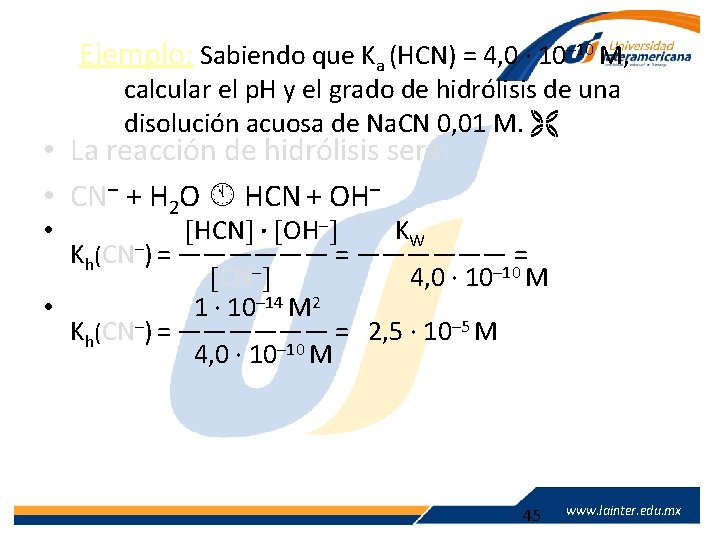
Ejemplo: Sabiendo que Ka (HCN) = 4, 0 · 10– 10 M, calcular el p. H y el grado de hidrólisis de una disolución acuosa de Na. CN 0, 01 M. • La reacción de hidrólisis será: • CN– + H 2 O HCN + OH– HCN · OH– KW Kh(CN–) = —————— = CN– 4, 0 · 10– 10 M • 1 · 10– 14 M 2 Kh(CN–) = —————— = 2, 5 · 10– 5 M 4, 0 · 10– 10 M • www. lainter. edu. mx 45 www. lainter. edu. mx
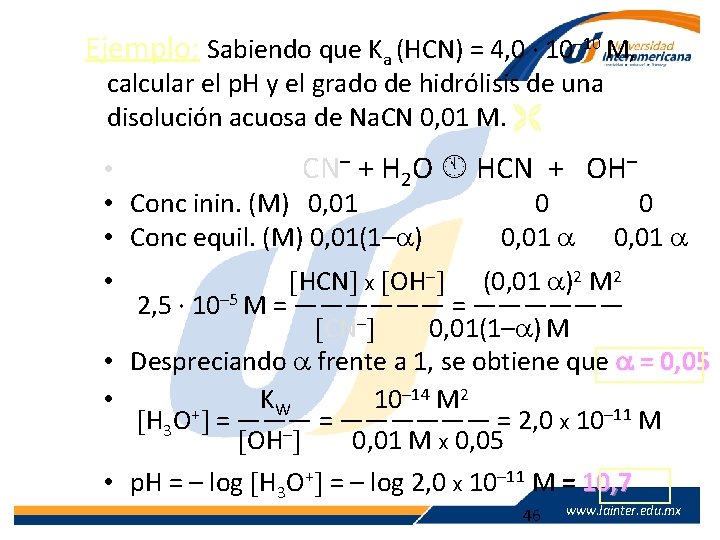
Ejemplo: Sabiendo que Ka (HCN) = 4, 0 · 10– 10 M, calcular el p. H y el grado de hidrólisis de una disolución acuosa de Na. CN 0, 01 M. • CN– + H 2 O HCN + OH– • Conc inin. (M) 0, 01 0 0 • Conc equil. (M) 0, 01(1– ) 0, 01 HCN x OH– (0, 01 )2 M 2 2, 5 · 10– 5 M = —————— CN– 0, 01(1– ) M • Despreciando frente a 1, se obtiene que = 0, 05 – 14 M 2 • K 10 W + H 3 O = —————— = 2, 0 x 10– 11 M OH– 0, 01 M x 0, 05 • • p. H = – log H 3 O+ = – log 2, 0 x 10– 11 M = 10, 7 www. lainter. edu. mx 46 www. lainter. edu. mx

Problema de Selectividad (Septiembre 98) Ejercicio C: Razone utilizando los equilibrios correspondientes, si los p. H de las disoluciones que se relacionan seguidamente son ácidos, básicos o neutros. a) Acetato potásico 0, 01 M; b) Nitrato sódico 0, 01 M; c) b) c) Sulfato amónico 0, 01 M; d) Hidróxido de bario 0, 01 M. d) a) Acetato potásico: p. H básico, ya que a) p. H básico CH 3–COO– + H 2 O CH 3–COOH + OH– por ser el ác. acetico débil, mientras que el K+ no reacciona con agua por ser el KOH base fuerte. – b) nitrato sódico: p. H neutro, ya que ni el anión NO b) p. H neutro 3 ni el catión Na+ reaccionan con agua por proceder el primero del HNO 3 y del Na. OH el segundo, ambos electrolitos fuertes. www. lainter. edu. mx 47 www. lainter. edu. mx

Problema de Selectividad (Septiembre 98) Ejercicio C: Razone utilizando los equilibrios correspondientes, si los p. H de las disoluciones que se relacionan seguidamente son ácidos, básicos o neutros. a) Acetato potásico 0, 01 M; b) Nitrato sódico 0, 01 M; c) b) c) Sulfato amónico 0, 01 M; d) Hidróxido de bario 0, 01 M. d) c) Sulfato amónico: p. H ácido, ya que c) p. H ácido NH 4+ + H 2 O NH 3 + H 3 O+ por ser el amoniaco débil, mientras que el SO 42– no reacciona con agua por ser el H 2 SO 4 ácido fuerte. d) hidróxido de bario: p. H básico pues se trata de una d) p. H básico base fuerte (los hidróxidos de los metales alcalinos y alcalino-térreos son bases bastantes fuertes) www. lainter. edu. mx 48 www. lainter. edu. mx

Disoluciones amortiguadoras (tampón) • Son capaces de mantener el p. H después de añadir pequeñas cantidades tanto de ácido como de base. Están formadas por: • Disoluciones de ácido débil + sal de dicho ácido débil con catión neutro: – Ejemplo: ácido acético + acetato de sodio. • Disoluciones de base débil + sal de dicha base débil con anión neutro: – Ejemplo: amoniaco y cloruro de amonio. www. lainter. edu. mx 49 www. lainter. edu. mx
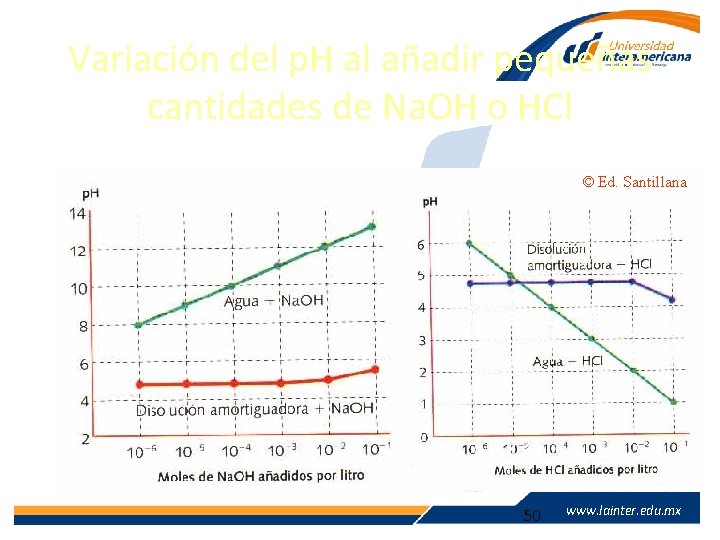
Variación del p. H al añadir pequeñas cantidades de Na. OH o HCl © Ed. Santillana www. lainter. edu. mx 50 www. lainter. edu. mx

Ejemplo: Calcular el p. H de una disolución tampón formada por una concentración 0, 2 M de ácido acético y 0, 2 M de acetato de sodio. Ka (CH 3–COOH) = 1, 8 · 10– 5 M. • El acetato está totalmente disociado: • CH 3–COONa CH 3–COO– + Na+ • El ácido acético se encuentra en equilibrio con su base conjugada (acetato): • H 2 O + CH 3–COOH CH 3–COO– + H 3 O+ • cin (M) 0, 2 0 • ceq (M) 0, 2 – x 0, 2 + x x www. lainter. edu. mx 51 www. lainter. edu. mx

Ejemplo: Calcular el p. H de una disolución tampón • formada por una concentración 0, 2 M de ácido acético y 0, 2 M de acetato de – 5 M sodio. Ka (CH 3–COOH) = 1, 8 · 10 – + 2 CH 3–COO · H 3 O (0, 2+x) · x M 1, 8 · 10– 5 M = —————— CH 3–COOH (0, 2 – x) M • De donde se deduce que: • x = H 3 O+ = 1, 8 · 10– 5 M • p. H = – log H 3 O+ = 4, 74 www. lainter. edu. mx 52 www. lainter. edu. mx

Indicadores de p. H (ácido- base) • Son sustancias que cambian de color al pasar de la forma ácida a la básica: • HIn + H 2 O In– + H 3 O+ forma ácida forma básica • El cambio de color se considera apreciable cuando [HIn] > 10·[In–] o [HIn]< 1/10·[In–] • In– · H 3 O+ HIn Ka = —————— H 3 O+ = Ka · ——— HIn In– www. lainter. edu. mx • p. H = p. Ka + log In– / HIn = p. Ka 55 1
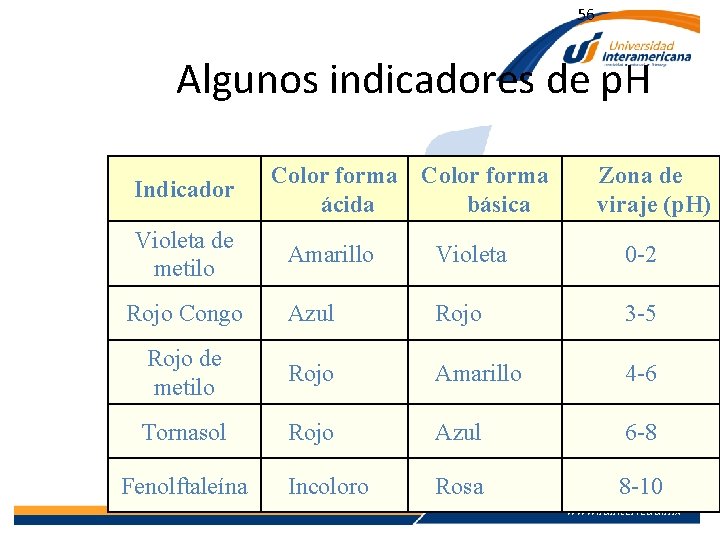
56 Algunos indicadores de p. H Indicador Violeta de metilo Color forma ácida básica Zona de viraje (p. H) Amarillo Violeta 0 -2 Rojo Congo Azul Rojo 3 -5 Rojo de metilo Rojo Amarillo 4 -6 Tornasol Rojo Azul 6 -8 Incoloro Rosa 8 -10 Fenolftaleína www. lainter. edu. mx
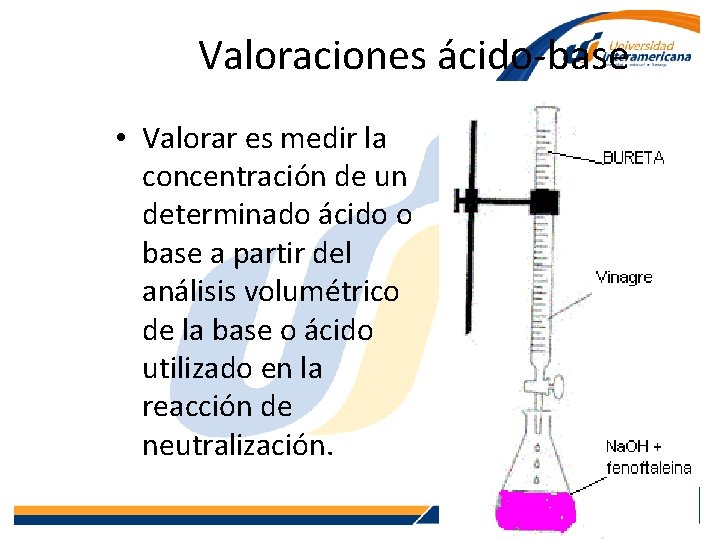
Valoraciones ácido-base • Valorar es medir la concentración de un determinado ácido o base a partir del análisis volumétrico de la base o ácido utilizado en la reacción de neutralización. www. lainter. edu. mx 57 www. lainter. edu. mx
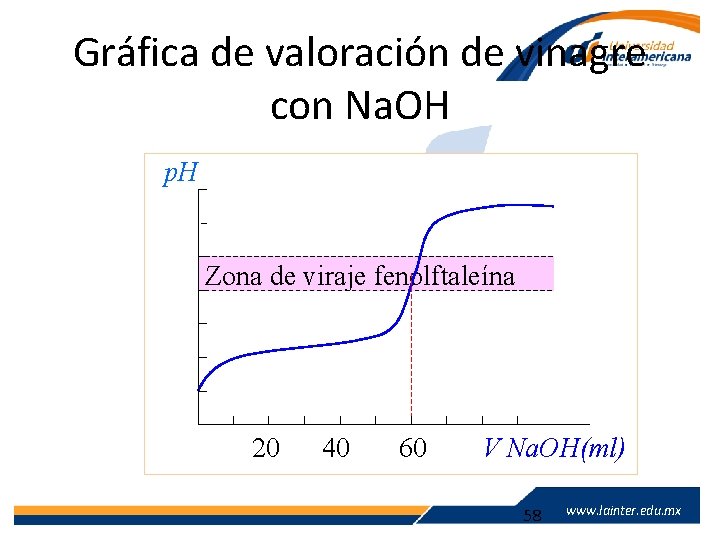
Gráfica de valoración de vinagre con Na. OH p. H 1210 8 6 Zona de viraje fenolftaleína 4 2 20 40 60 V Na. OH(ml) www. lainter. edu. mx 58 www. lainter. edu. mx

Valoraciones ácido-base. • La neutralización de un ácido/base con una base/ácido de concentración conocida se consigue cuando n(OH–) = n(H 3 O+). • La reacción de neutralización puede escribirse: b Ha. A + a B(OH)b Ba. Ab + a·b H 2 O • En realidad, la sal Ba. Ab (a. Bb+ + b. Aa–) se encuentra disociada, por lo que la única reacción es: H 3 O+ + OH– 2 H 2 O n(ácido) x a = n(base) www. lainter. edu. mx 59 x b
![Simulación Valoraciones ácido-base • Vácido x [ácido] x a = Vbase x [base] x Simulación Valoraciones ácido-base • Vácido x [ácido] x a = Vbase x [base] x](http://slidetodoc.com/presentation_image_h/afa607c06fb4831d50b5d743f16a737c/image-58.jpg)
Simulación Valoraciones ácido-base • Vácido x [ácido] x a = Vbase x [base] x b • Todavía se usa mucho la concentración expresada como Normalidad: • Normalidad = Molaridad x n (H u OH) • Vácido x Nácido = Vbase x Nbase • En el caso de sales procedentes de ácido o base débiles debe utilizarse un indicador que vire al p. H de la sal resultante de la neutralización. www. lainter. edu. mx 60 www. lainter. edu. mx

Ejemplo: 100 ml de una disolución de H 2 SO 4 se Vídeo neutralizan con 25 ml de una disolución 2 M de Al(OH)3 ¿Cuál será la [H 2 SO 4]? 3 H 2 SO 4 + 2 Al(OH)3 3 SO 42– +2 Al 3+ + 6 H 2 O • 25 ml x 2 M x 3 = 100 ml x Mácido x 2 • De donde: • 25 ml x 2 M x 3 Mácido = ——————— = 0, 75 M 100 ml x 2 • [H 2 SO 4] = 0, 75 M • Vácido x Nácido = Vbas x Nbase (Nbase= 3 x Mbase) • 100 ml x Nácido = 25 ml x 6 N • Nácido = 1, 5 N Mácido= Nácido/2 = 0, 75 M www. lainter. edu. mx 61

Ejemplo: 100 ml de una disolución de H 2 SO 4 se neutralizan con 25 ml de una disolución 2 M de Al(OH)3 ¿Cuál será la [H 2 SO 4]? • Podríamos haber calculado n(H 2 SO 4) a partir del cálculo estequiométrico, pues conocemos n(Al(OH)3 = V· M = 25 ml · 2 M = 50 mmoles 3 H 2 SO 4 + 2 Al(OH)3 3 SO 42– +2 Al 3+ + 6 H 2 O 3 mol H 2 SO 4 2 mol Al(OH)3 ————— = —————— n(H 2 SO 4) 50 mmoles • n(H 2 SO 4) = 75 mmol • n (H 2 SO 4) 75 mmol [H 2 SO 4] = ————— = 0, 75 M www. lainter. edu. mx 62 www. lainter. edu. mx V(H 2 SO 4) 100 ml
Problema de Selectividad (Septiembre 97) Ejercicio D: Si 10, 1 ml de vinagre han necesitado 50, 5 ml de una base 0, 2 N para su neutralización. a) Cuál será la normalidad del ácido en el vinagre; b) Suponiendo que su acidez se debe al ácido acético (ácido etanoico). ¿Cuál es el porcentaje en peso del ácido acético si la densidad del vinagre es de 1, 06 g/ml? • a) Vácido x Nácido = Vbase x Nbase 50, 5 ml x 0, 2 N Nácido = —————— = 1 N Mácido = 1 M 10, 1 ml • b) Supongamos que tenemos un litro de vinagre: • m(á. acético) = Molaridad x M x V = = 1 mol/L x 60 g/mol x 1 L = 60 g • msoluto 60 g % = ———— x 100 = www. lainter. edu. mx 5, 66 % 63 www. lainter. edu. mx mdisolución 1060 g
- Slides: 61