Acidos Poliprticos ACIDO S POLIPROTICOS Solubilidad de precipitados

Acidos Polipróticos
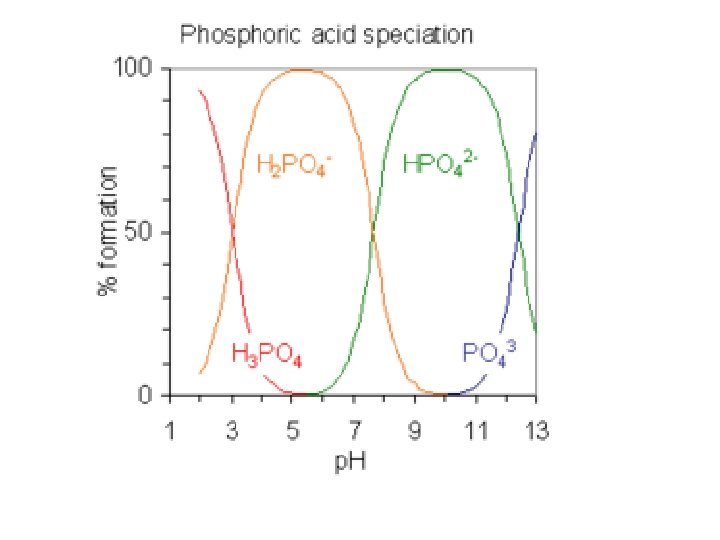

ACIDO S POLIPROTICOS
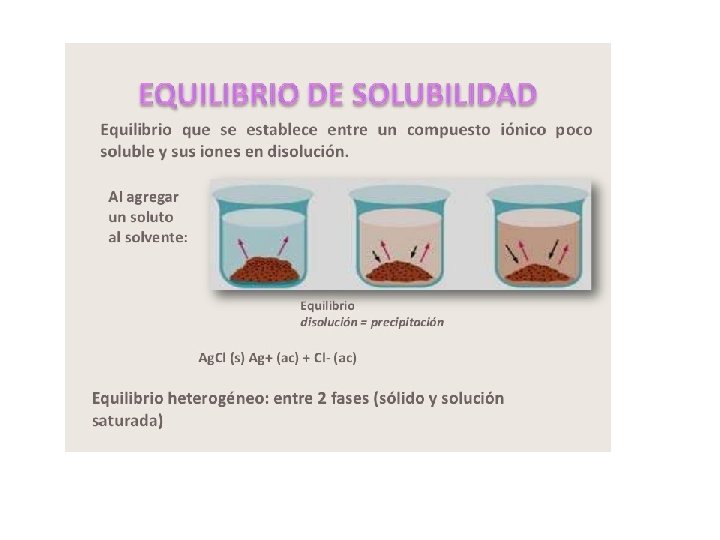
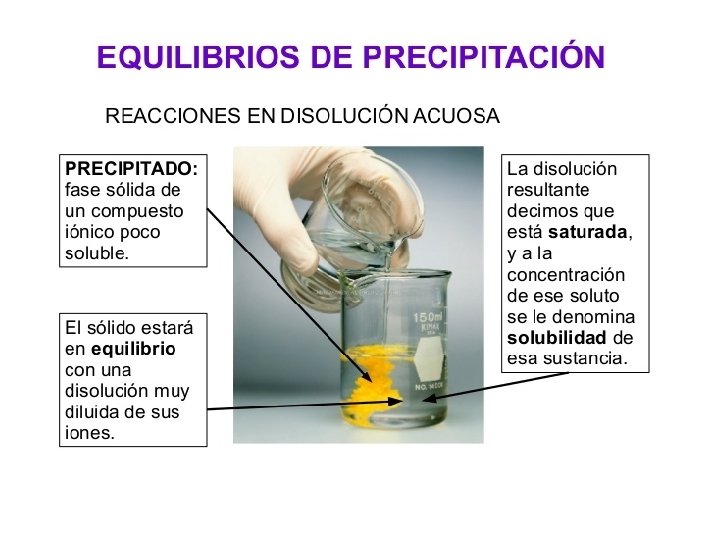


Solubilidad de precipitados en presencia de agentes complejantes La solubilidad de un precipitado a menudo aumenta en presencia de reactivos que forman complejos con el anión o el catión del sólido. Al (OH)3 (s) Al+3 + 3 OH+ 6 FAl. F 63 -

Influencia del p. H en la Solubilidad de precipitados La solubilidad de los precipitados que contienen un ion con propiedades básicas, un catión con propiedades ácidas, o ambos, depende del p. H.

Efecto del ion común La presencia de un ión que sea el mismo que alguno de los producidos en la disociación hace que el producto iónico (Q) sea mayor que el Kps , entonces el equilibrio se desplaza hacia la formación del precipitado

Formación de otro precipitado más insoluble Una forma de disolver un precipitado es formar otro más insoluble, de manera que ha medida que se va formando el segundo precipitado se disuelve el primero.

Separaciones por precipitación El procedimiento consiste en adicionar un reactivo que precipita uno de los iones en forma total, dejando al resto en solución. La factibilidad y el éxito de las separaciones pueden predecirse, en condiciones ideales, por los métodos de cálculo.

Continuo Clase en el Pizarrón Reacciones Acido-Base Consideremos el Ca. F 2 Sal proveniente de un ácido débil y de una base fuerte 1) Ca F 2 Ca +2 + 2 F- Kps = [Ca+2] [ F-]2 Kps = 4 x 10 -11 [Ca+2] = S [F-]= 2 S => Kps = S (2 s)2 = 4 S 3 S = 2, 2 x 10 -4
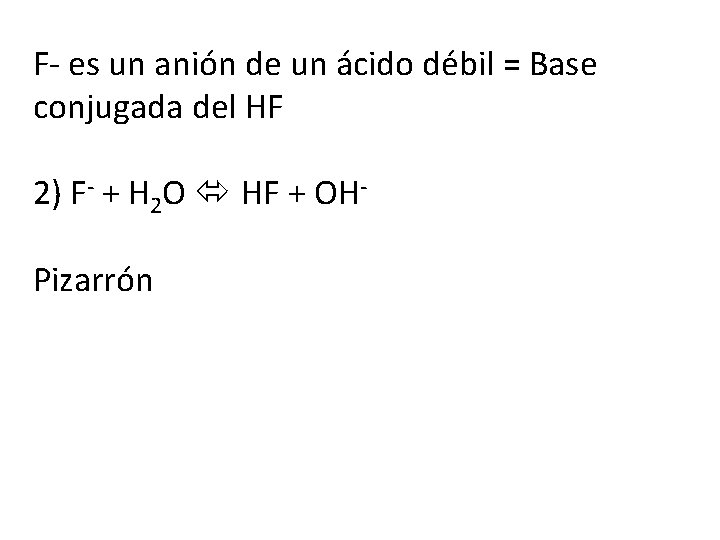
F- es un anión de un ácido débil = Base conjugada del HF 2) F- + H 2 O HF + OHPizarrón
- Slides: 13