ACIDOS CARBOXILICOS RCOOH Los compuestos que contienen al
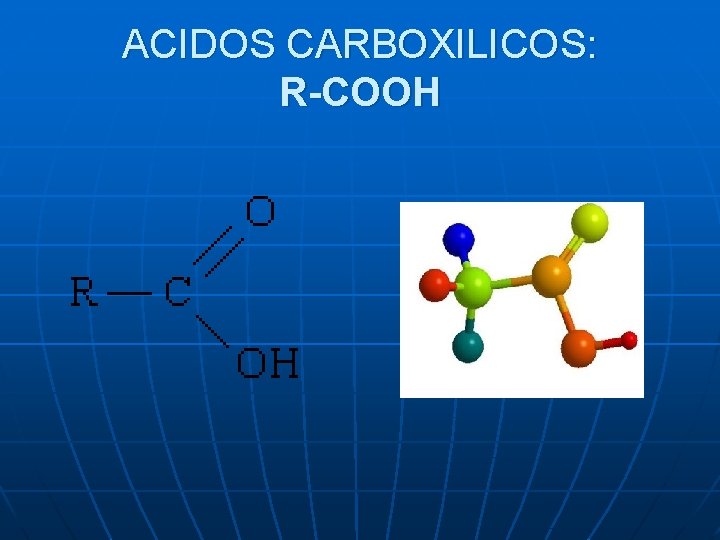
ACIDOS CARBOXILICOS: R-COOH
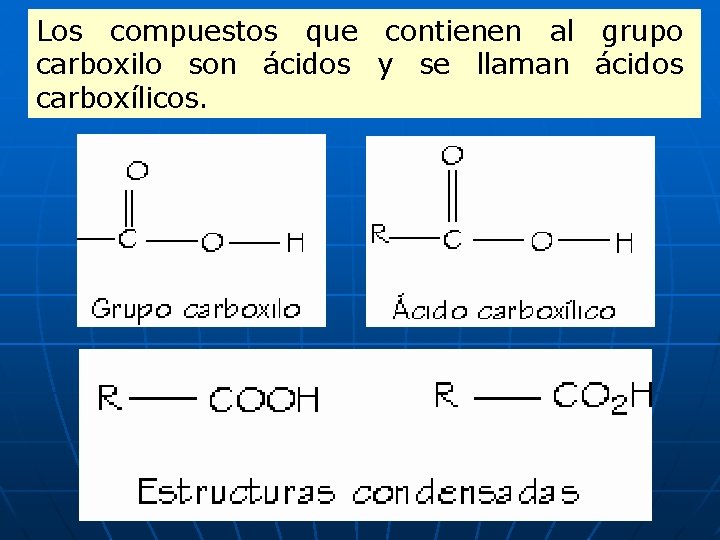
Los compuestos que contienen al grupo carboxilo son ácidos y se llaman ácidos carboxílicos.

ACIDOS CARBOXILICOS O C-OH n Grupo funcional: COOH n O Carboxilo: Carbonilo C + hidroxilo

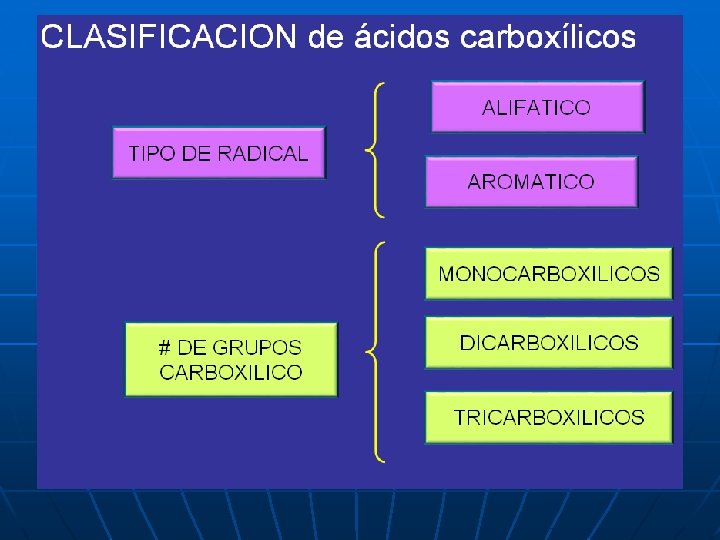
CLASIFICACION 1. Alifáticos: R-COOH Ej. CH 3 CH 2 -COOH n 2. Aromáticos: Ar-COOH Ej. n COOH Acido Benzoico

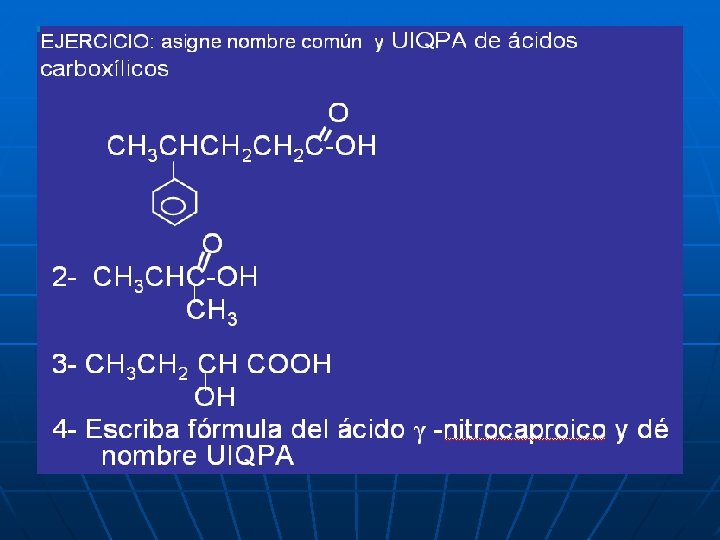
NOMENCLATURA 1. 2. 3. Numerar la cadena más larga que contiene el grupo COOH. Carbono uno: el que contiene el COOH. El nombre comienza con la palabra Acido, seguido con el alcano básico con el sufijo OICO. Ej. Acido Metanoico HCOOH. Acido propanoico CH 3 CH 2 COOH 3 2 1

4. Se nombra la posición del sustituyente numerando a partir del COOH. Ej. n CH 3 -CH-COOH (IUPAC, Acido- 2 bromo propanoico) Br n CH 2= CH-COOH (IUPAC, Acido propenoico). n

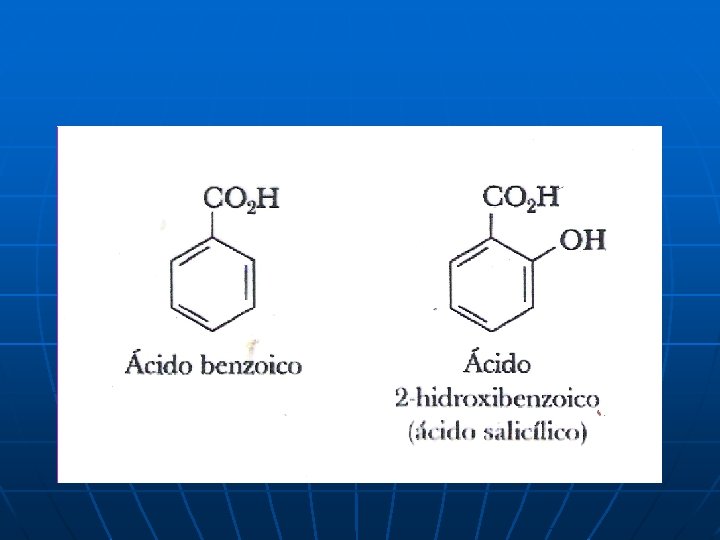
n n n ACIDOS AROMATICOS: El aromático es el ácido benzoico y a los sustituidos se les da el nombre como derivados de éste. Si el aromático no se encuentra enlazado directamente al COOH, el aromático se menciona como sustituyente. Acido benzoico: COOH Acido 3 -cloro benzoico : Cl COOH
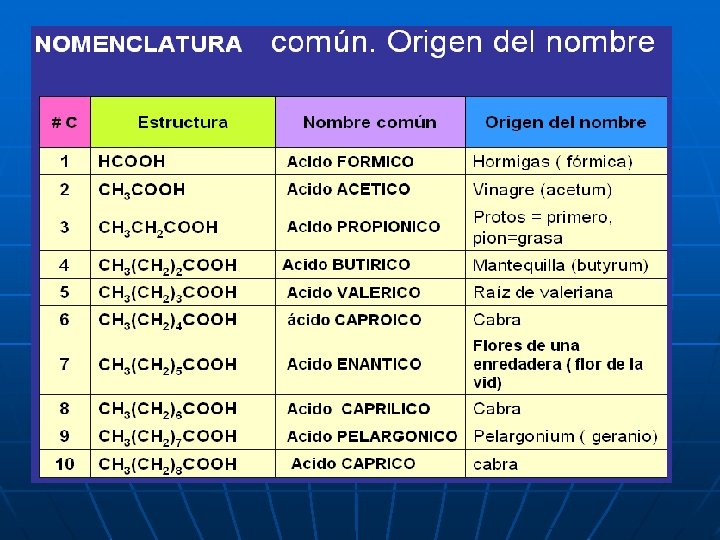
COMUN: n Nombre de acuerdo a la procedencia del ácido. Ej. n Ácido fórmico (Es el más sencillo). n Ácido Acético n Ácido Propiónico

Nonbre común con ramificaciones no carbonados n n Se da el nombre dando la posición del sustituyente, por las letras , , . Indican posición del carbono, respecto al COOH. Ej. C- C- C -C -C- C-OOH
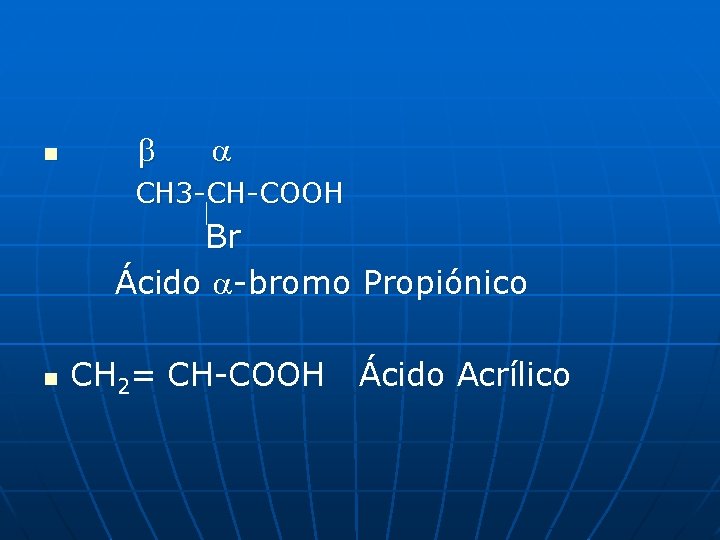
n CH 3 -CH-COOH Br Ácido -bromo Propiónico n CH 2= CH-COOH Ácido Acrílico
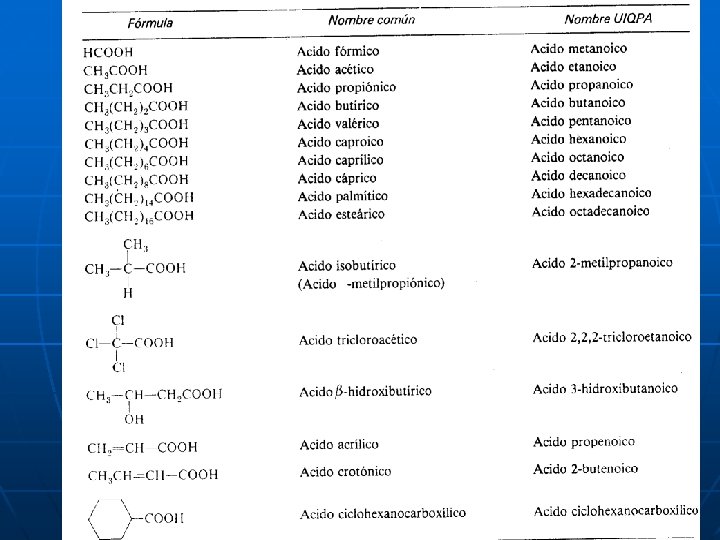

PROPIEDADES FISICAS: n n Puntos de ebullición elevados, son mayores que los alcoholes de igual peso molecular debido a puentes de hidrógeno entre sí. Los ácidos carboxílicos de bajo peso molecular son solubles, a mayor peso molecular menor solubilidad.

PROPIEDADES FISICAS: n n n Los de bajo peso molecular son líquidos incoloros de olor desagradable. Secreciones de ganado caprino: Acido caproico, de 5 – 10 C tienen olor a cabra. De 10 carbonos en adelante son sólidos cerosos y baja volatilidad, no tienen olor.

PROPIEDADES FISICAS: n Por la formación de los puentes de hidrógenos existen como moléculas dobles: “DIMEROS”

PROPIEDADES QUIMICAS. OXIDACIÓN: n Son los productos finales de la Oxidación de Aldehídos y alcoholes primarios. Ej. R-COH + KMn. O 4 R-COOH
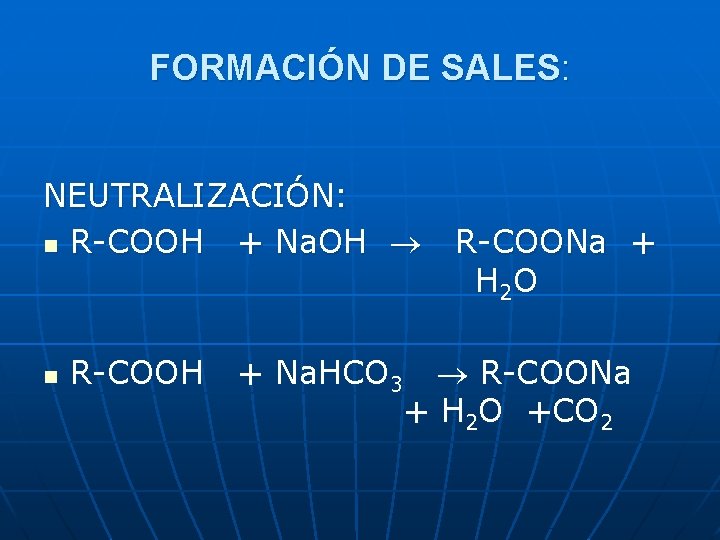
FORMACIÓN DE SALES: NEUTRALIZACIÓN: n R-COOH + Na. OH n R-COOH R-COONa + H 2 O + Na. HCO 3 R-COONa + H 2 O +CO 2

Reaccionan con bases formando sales. Acido acético Acetato de sodio Acido etanoico Etanoato de sodio
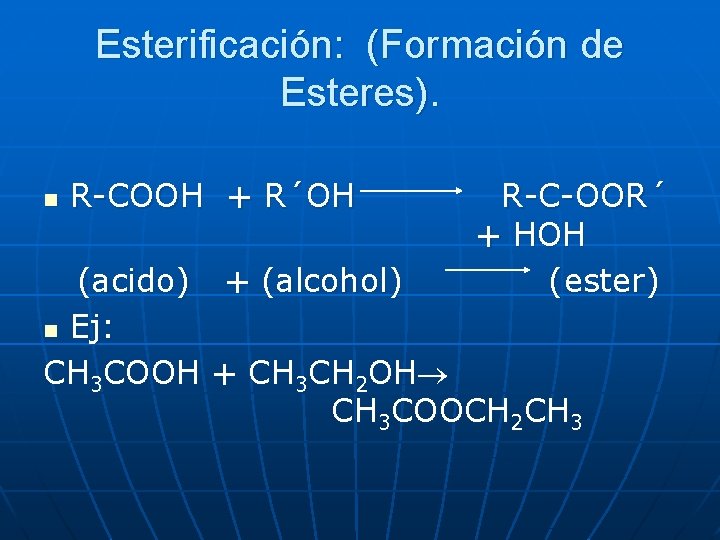
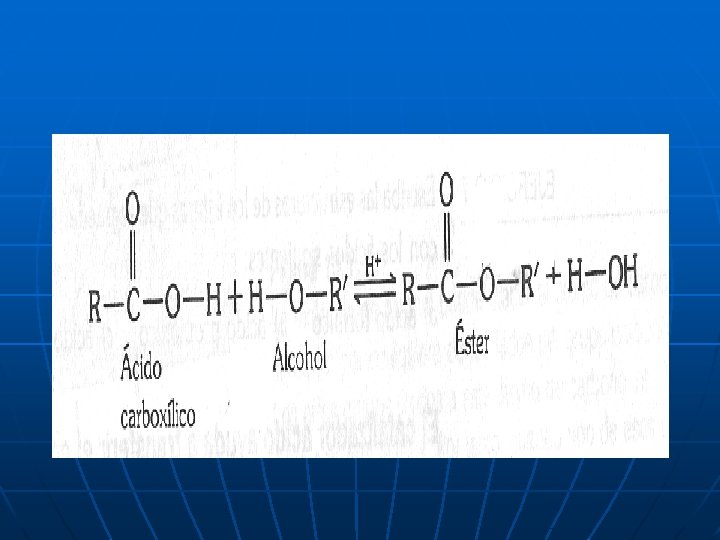
Esterificación: (Formación de Esteres). n R-COOH + R´OH (acido) n Ej: CH 3 COOH + (alcohol) R-C-OOR´ + HOH (ester) + CH 3 CH 2 OH CH 3 COOCH 2 CH 3

EJERCICIO: 1. 2. Haga la ecuación cuando reacciona el reacción cuando reacciona el ácido isovalerico con el Na. HCO 3 Haga la ecuación cuando reacciona el reacción cuando reacciona el ácido beta clorobutanoico con el alcohol isopropílico
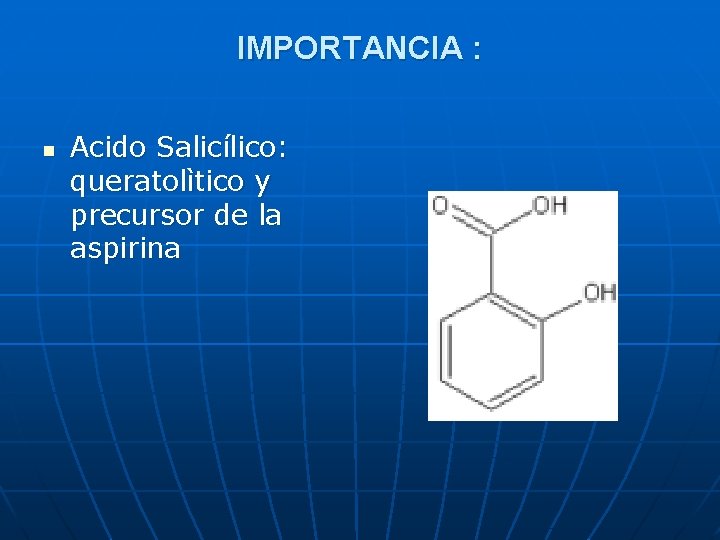
IMPORTANCIA : n Acido Salicílico: queratolìtico y precursor de la aspirina

IMPORTANCIA n Se encuentra presente en las proteínas
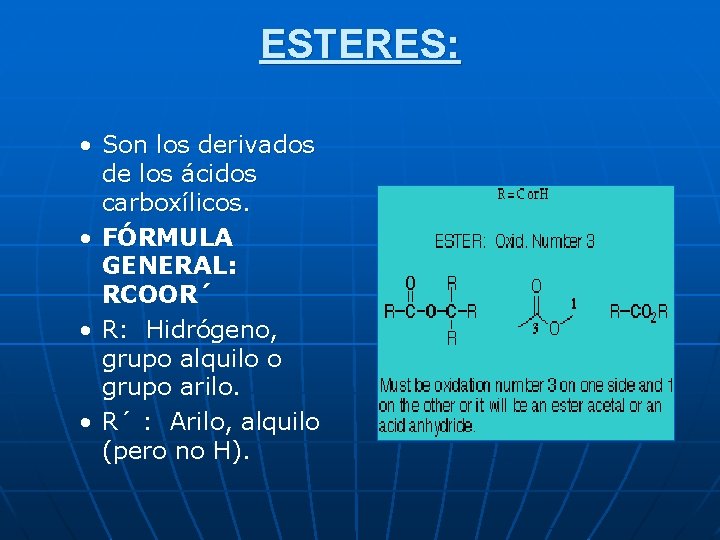
ESTERES: • Son los derivados de los ácidos carboxílicos. • FÓRMULA GENERAL: RCOOR´ • R: Hidrógeno, grupo alquilo o grupo arilo. • R´ : Arilo, alquilo (pero no H).

Aspirina (Ácido acetil salicílico)

IMPORTANCIA n n Los ésteres se encuentran en grasas y aceites vegetales. Los esteres en general presentan olores placenteros. Los sabores artificiales son mezclas de ésteres.
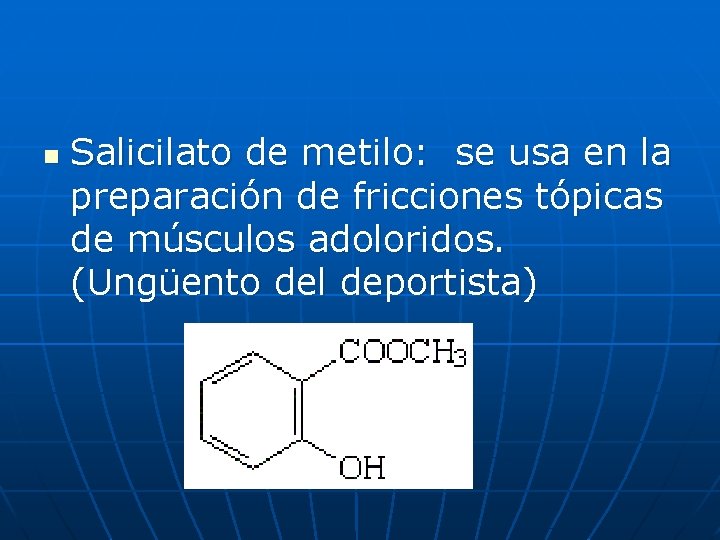
n Salicilato de metilo: se usa en la preparación de fricciones tópicas de músculos adoloridos. (Ungüento del deportista)

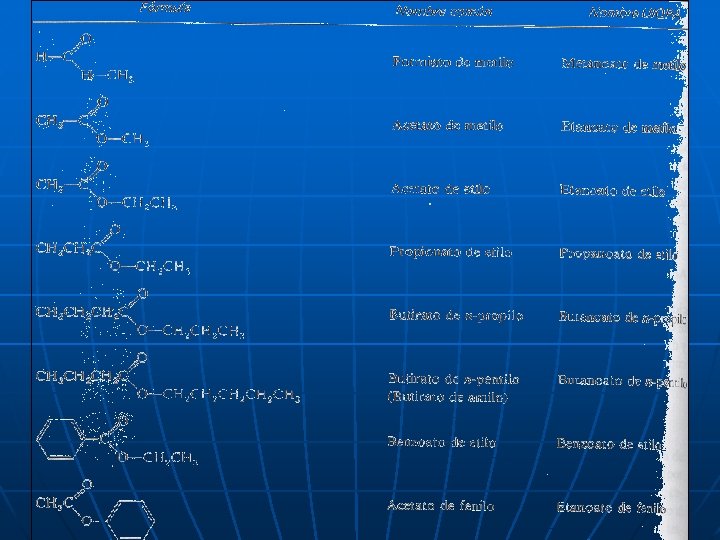
NOMENCLATURA. COMÚN: El nombre de un éster se forma con el nombre común del ácido, cambiando el sufijo ICO por ATO, seguido de la conjunción DE, y el nombre del grupo alquilo derivado del alcohol. n UIQPA: La porción alcohólica termina en ilo y la parte derivada del ácido en ato. n

PROPIEDADES FISICAS: n No forman puentes de hidrógeno entre sí, por lo que el punto de ebullición es menor a ácidos carboxílicos y alcoholes de similar peso molecular.

PROPIEDADES FISICAS: n n n Punto de ebullición: Ácido carboxílico > alcohol > éster > alcano Tiene similar punto de ebullición a las cetonas y aldehídos de peso molecular parecido. Menos densos que el agua.

PROPIEDADES FISICAS: n n Punto de Ebullición aumenta conforme aumenta la masa molar. Son menos solubles en agua que los ácidos y los alcoholes.

Tio esteres: n Es un éster con azufre en lugar de oxígeno REPRESENTACION: R-CO-SR n Ej: n O CH 3 -C-SCH 3 Tio acetato de metilo n IMPORTANCIA: • Presente en compuestos biològicos como acetilcoenzima A
- Slides: 36