ACIDOS CARBOXILICOS ESTERES Y AMIDAS Semana 22 Licda

ACIDOS CARBOXILICOS , ESTERES Y AMIDAS Semana 22 Licda. Lilian Guzmán Melgar

Grupo Funcional Los ácidos carboxílicos tienen el grupo funcional : O -C-OH -CO 2 H -COOH 2

El nombre ácido carboxílico describe al grupo funcional de dos maneras: 1. La palabra carboxílico es una contracción de las palabras carbonilo e hidroxilo, que son las dos unidades estructurales en el grupo. 2. Se agrega el término ácido, ácido debido a las propiedades ácidas de esta familia de compuestos 3
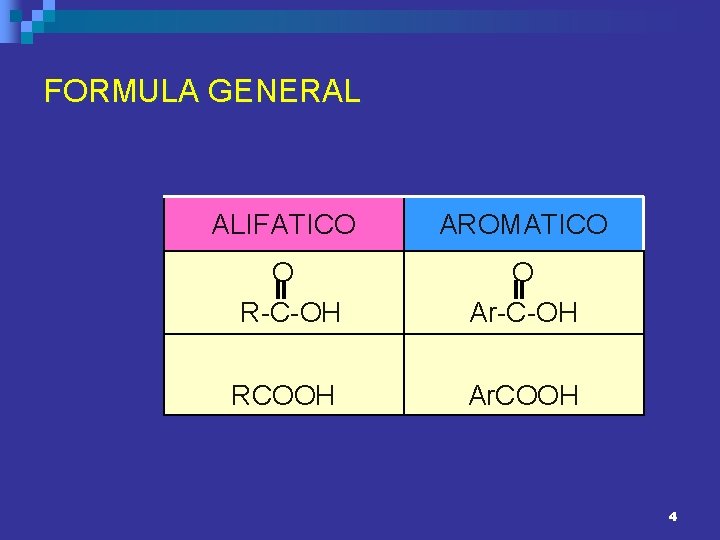
FORMULA GENERAL ALIFATICO AROMATICO O R-C-OH O Ar-C-OH RCOOH Ar. COOH 4
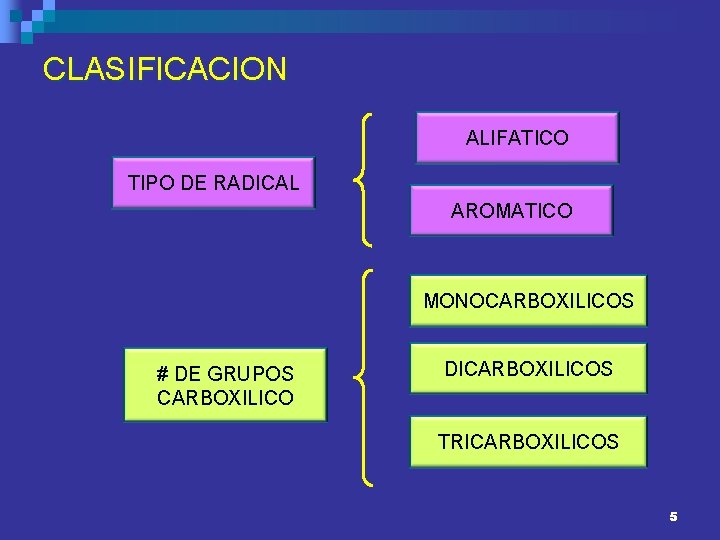
CLASIFICACION ALIFATICO TIPO DE RADICAL AROMATICO MONOCARBOXILICOS # DE GRUPOS CARBOXILICO DICARBOXILICOS TRICARBOXILICOS 5

TIPO RADICAL ALIFATICO AROMATICO EJEMPLO: Posee un radical alifático CH 3 CH 2 COOH Posee un radical aromático EJEMPLO: COOH 6
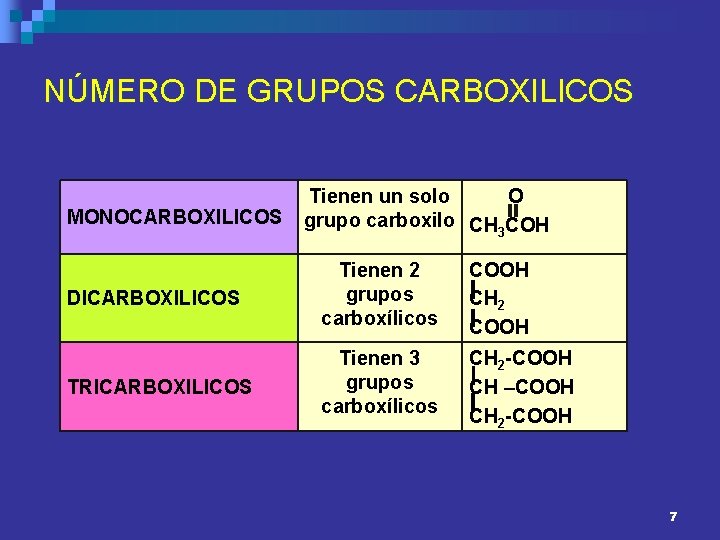
NÚMERO DE GRUPOS CARBOXILICOS MONOCARBOXILICOS Tienen un solo O grupo carboxilo CH 3 COH DICARBOXILICOS Tienen 2 grupos carboxílicos COOH CH 2 COOH TRICARBOXILICOS Tienen 3 grupos carboxílicos CH 2 -COOH CH –COOH CH 2 -COOH 7
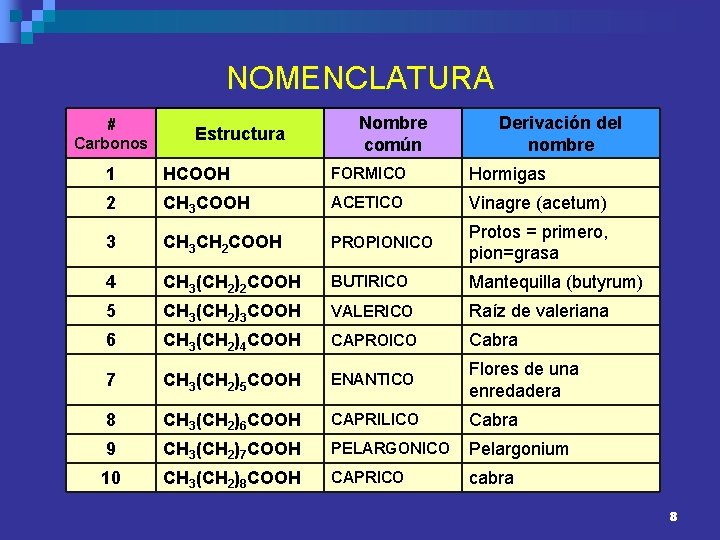
NOMENCLATURA # Carbonos Estructura Nombre común Derivación del nombre 1 HCOOH FORMICO Hormigas 2 CH 3 COOH ACETICO Vinagre (acetum) 3 CH 3 CH 2 COOH PROPIONICO Protos = primero, pion=grasa 4 CH 3(CH 2)2 COOH BUTIRICO Mantequilla (butyrum) 5 CH 3(CH 2)3 COOH VALERICO Raíz de valeriana 6 CH 3(CH 2)4 COOH CAPROICO Cabra 7 CH 3(CH 2)5 COOH ENANTICO Flores de una enredadera 8 CH 3(CH 2)6 COOH CAPRILICO Cabra 9 CH 3(CH 2)7 COOH PELARGONICO Pelargonium 10 CH 3(CH 2)8 COOH CAPRICO cabra 8

NOMENCLATURA COMUN Los ácidos sustituidos se les da nombre ubicando la posición de los sustituyentes por medio de las letras griegas. O C – C – C- OH EJEMPLO O CH 3 CHCH 2 C-OH CH 3 9

UIQPA REGLAS: 1. Se toma como hidrocarburo básico el que corresponda a la cadena continua más larga que contenga el grupo carboxilo O C-C-C-OH 5 4 2. 3 2 1 El nombre comienza con las palabras ácido seguida por el del alcano básico al cual se le añade el sufijo “ ico ”. 10
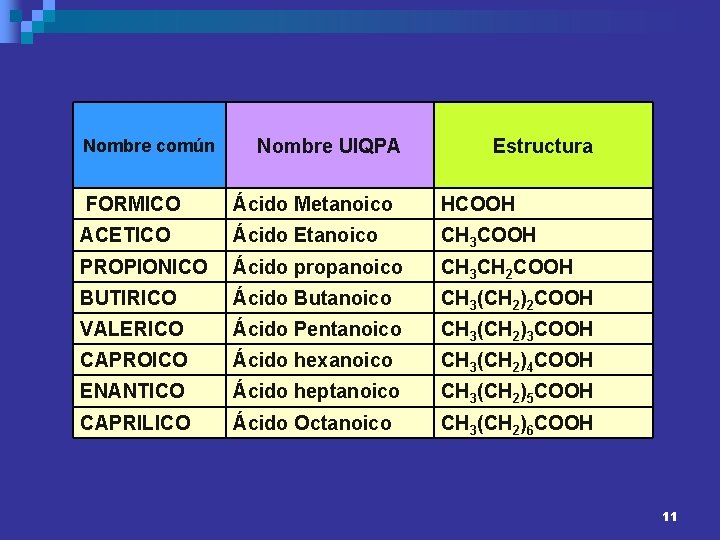
Nombre común Nombre UIQPA Estructura FORMICO Ácido Metanoico HCOOH ACETICO Ácido Etanoico CH 3 COOH PROPIONICO Ácido propanoico CH 3 CH 2 COOH BUTIRICO Ácido Butanoico CH 3(CH 2)2 COOH VALERICO Ácido Pentanoico CH 3(CH 2)3 COOH CAPROICO Ácido hexanoico CH 3(CH 2)4 COOH ENANTICO Ácido heptanoico CH 3(CH 2)5 COOH CAPRILICO Ácido Octanoico CH 3(CH 2)6 COOH 11
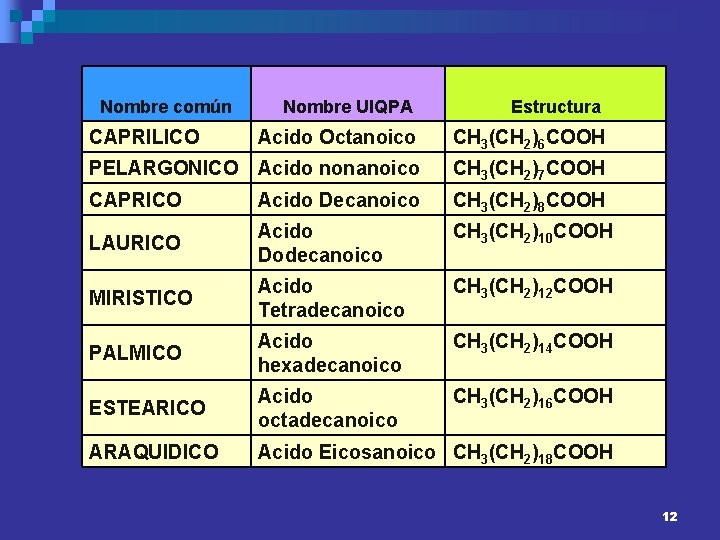
Nombre común Nombre UIQPA Estructura Acido Octanoico CH 3(CH 2)6 COOH PELARGONICO Acido nonanoico CH 3(CH 2)7 COOH CAPRICO Acido Decanoico CH 3(CH 2)8 COOH LAURICO Acido Dodecanoico CH 3(CH 2)10 COOH MIRISTICO Acido Tetradecanoico CH 3(CH 2)12 COOH PALMICO Acido hexadecanoico CH 3(CH 2)14 COOH ESTEARICO Acido octadecanoico CH 3(CH 2)16 COOH ARAQUIDICO Acido Eicosanoico CH 3(CH 2)18 COOH CAPRILICO 12
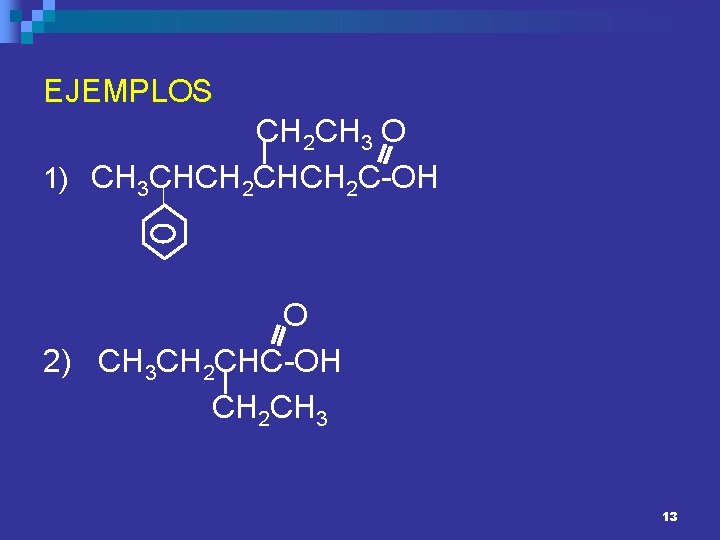
EJEMPLOS CH 2 CH 3 O 1) CH 3 CHCH 2 C-OH O 2) CH 3 CH 2 CHC-OH CH 2 CH 3 13
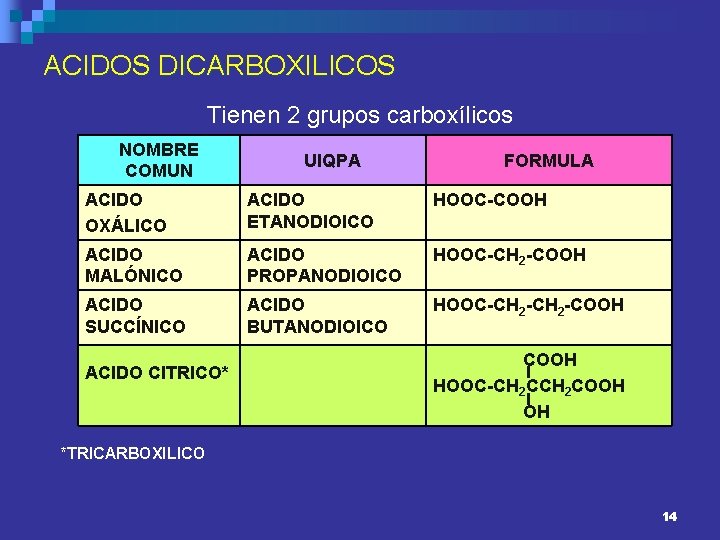
ACIDOS DICARBOXILICOS Tienen 2 grupos carboxílicos NOMBRE COMUN UIQPA FORMULA ACIDO OXÁLICO ACIDO ETANODIOICO HOOC-COOH ACIDO MALÓNICO ACIDO PROPANODIOICO HOOC-CH 2 -COOH ACIDO SUCCÍNICO ACIDO BUTANODIOICO HOOC-CH 2 -COOH ACIDO CITRICO* COOH HOOC-CH 2 COOH OH *TRICARBOXILICO 14

PROPIEDADES FISICAS § Los primeros 9 miembros de la serie son líquidos, § § incoloros y olor desagradable. Los ácidos de C 6, C 8 y C 10 todos poseen olores “a cabra”. Los ácidos con mas de 10 átomos de carbono son sólidos cerosos y por su baja volatilidad son inodoros. Los homólogos inferiores son solubles en agua. La solubilidad decrece a partir del ácido butírico. Todos los ácidos son solubles en alcohol, benceno, CCl 4 y éter. 15
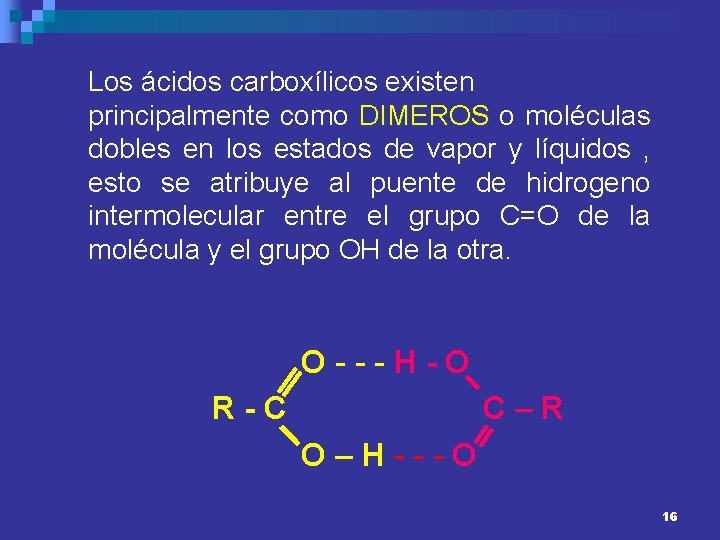
Los ácidos carboxílicos existen principalmente como DIMEROS o moléculas dobles en los estados de vapor y líquidos , esto se atribuye al puente de hidrogeno intermolecular entre el grupo C=O de la molécula y el grupo OH de la otra. O---H-O R-C C–R O–H---O 16
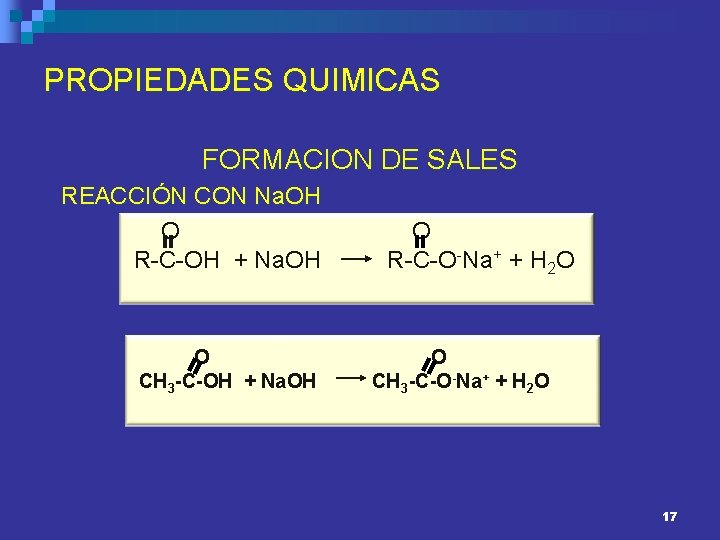
PROPIEDADES QUIMICAS FORMACION DE SALES REACCIÓN CON Na. OH O R-C-OH + Na. OH O CH 3 -C-OH + Na. OH O R-C-O-Na+ + H 2 O O CH 3 -C-O-Na+ + H 2 O 17
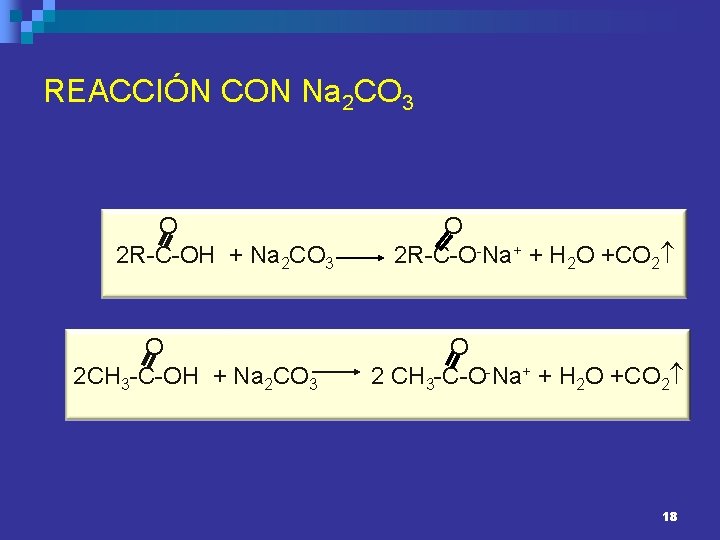
REACCIÓN CON Na 2 CO 3 O 2 R-C-OH + Na 2 CO 3 O 2 CH 3 -C-OH + Na 2 CO 3 O 2 R-C-O-Na+ + H 2 O +CO 2 CH 3 -C-O-Na+ + H 2 O +CO 2 18
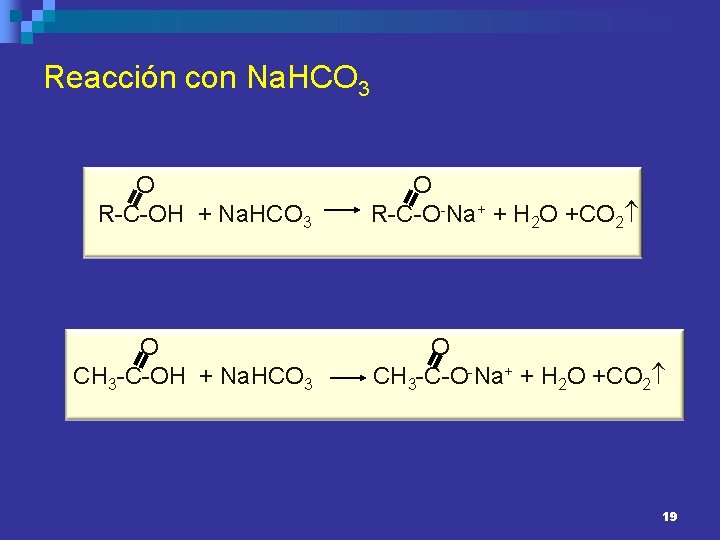
Reacción con Na. HCO 3 O R-C-OH + Na. HCO 3 O CH 3 -C-OH + Na. HCO 3 O R-C-O-Na+ + H 2 O +CO 2 O CH 3 -C-O-Na+ + H 2 O +CO 2 19
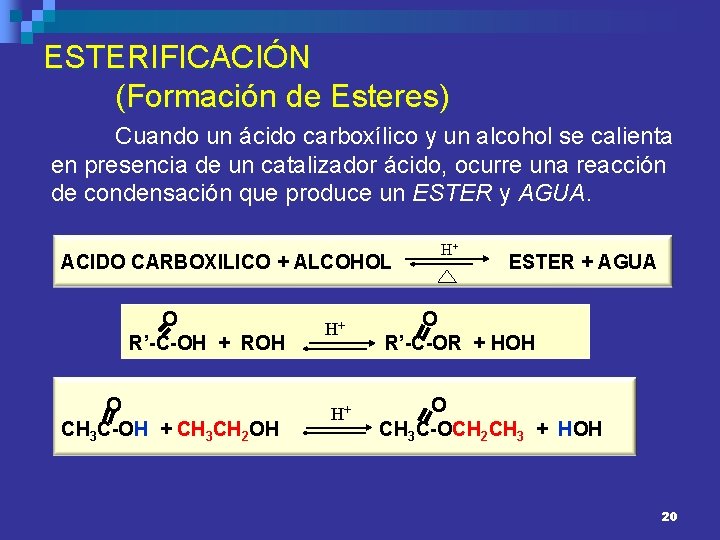
ESTERIFICACIÓN (Formación de Esteres) Cuando un ácido carboxílico y un alcohol se calienta en presencia de un catalizador ácido, ocurre una reacción de condensación que produce un ESTER y AGUA. ACIDO CARBOXILICO + ALCOHOL O R’-C-OH + ROH O CH 3 C-OH + CH 3 CH 2 OH H+ H+ H+ ESTER + AGUA O R’-C-OR + HOH O CH 3 C-OCH 2 CH 3 + HOH 20

Importancia de los ácidos O COH Acido Benzoico Solido incoloro. El ácido benzoico y sus derivados sólo se pueden utilizar para conservar alimentos con un p. H ácido. Protege sobre todo contra el moho 21
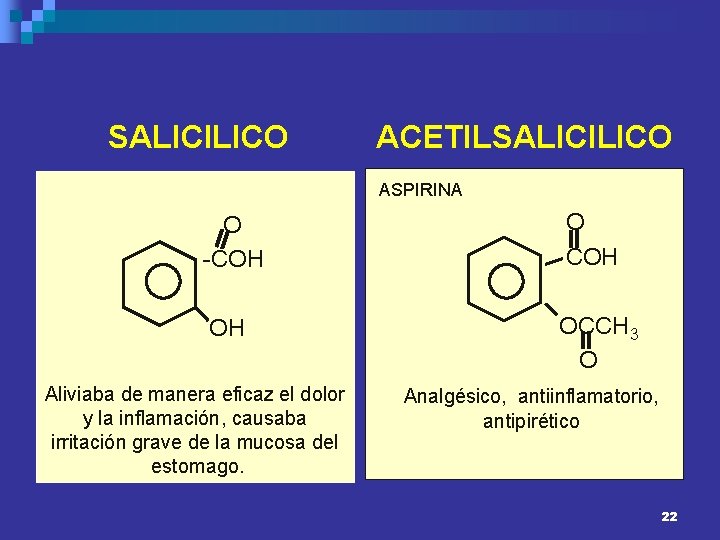
SALICILICO ACETILSALICILICO ASPIRINA O -COH OH OCCH 3 O Aliviaba de manera eficaz el dolor y la inflamación, causaba irritación grave de la mucosa del estomago. Analgésico, antiinflamatorio, antipirético 22

ESTERES Los esteres son los derivados mas importantes de los ácidos carboxílicos. FORMULA GENERAL O R-C-OR’ R-COO-R’ Donde R puede ser un hidrógeno, un grupo alquilo o arilo y donde R’ puede ser alquilo, arilo pero NO hidrógeno. 23

NOMENCLATURA 1) Primero se menciona la porción ácida y luego la porción alquílica o arílica. 2) Tanto en la nomenclatura común como en la UIQPA la terminación “ico” ico del ácido se reemplaza por el sufijo “ato”. ato 24
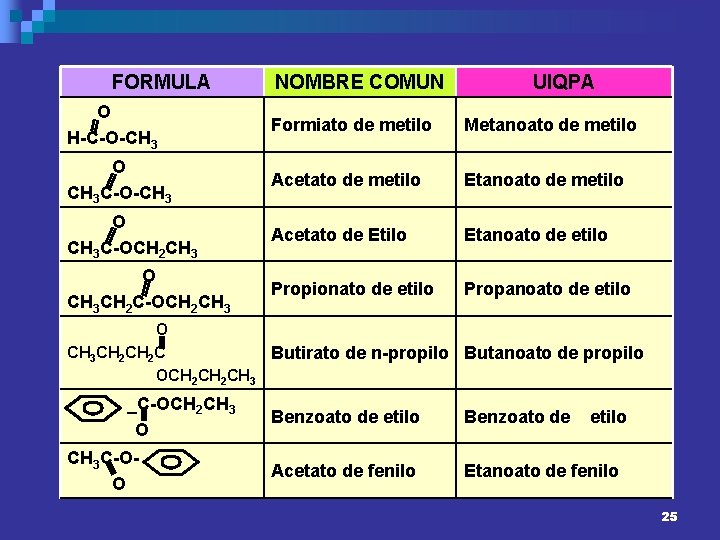
FORMULA NOMBRE COMUN UIQPA O H-C-O-CH 3 Formiato de metilo Metanoato de metilo O CH 3 C-O-CH 3 Acetato de metilo Etanoato de metilo O CH 3 C-OCH 2 CH 3 Acetato de Etilo Etanoato de etilo O CH 3 CH 2 C-OCH 2 CH 3 Propionato de etilo Propanoato de etilo O CH 3 CH 2 C Butirato de n-propilo Butanoato de propilo OCH 2 CH 3 _C-OCH 2 CH 3 O CH 3 C-OO Benzoato de etilo Acetato de fenilo Etanoato de fenilo 25

PROPIEDADES FISICAS n A diferencia de los ácidos carboxílicos de los cuales se derivan los esteres poseen olores agradables. n El aroma de muchas flores y frutos se debe a la presencia de esteres. n Estos se emplean en la fabricación de perfumes y como saborizantes en la fabricación de dulces y bebidas no alcohólicas. n La mayor parte de esteres son líquidos, incoloros, insolubles y menos densos que el agua. 26
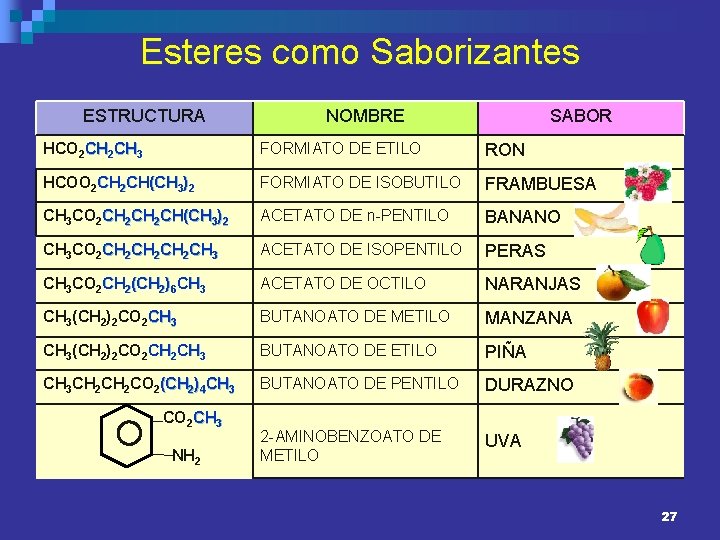
Esteres como Saborizantes ESTRUCTURA NOMBRE SABOR HCO 2 CH 3 FORMIATO DE ETILO RON HCOO 2 CH(CH 3)2 FORMIATO DE ISOBUTILO FRAMBUESA CH 3 CO 2 CH 2 CH(CH 3)2 ACETATO DE n-PENTILO BANANO CH 3 CO 2 CH 2 CH 3 ACETATO DE ISOPENTILO PERAS CH 3 CO 2 CH 2(CH 2)6 CH 3 ACETATO DE OCTILO NARANJAS CH 3(CH 2)2 CO 2 CH 3 BUTANOATO DE METILO MANZANA CH 3(CH 2)2 CO 2 CH 3 BUTANOATO DE ETILO PIÑA CH 3 CH 2 CO 2(CH 2)4 CH 3 BUTANOATO DE PENTILO DURAZNO 2 -AMINOBENZOATO DE METILO UVA CO 2 CH 3 NH 2 27

Salicilato de Metilo También llamado esencia de gaulteria. O Con olor agradable. -C-OCH 3 Fármaco de acción balsámica, analgésica OH y suavizante. Se emplea en pomadas, Linimentos, enjuagues bucales, pastas dentales 28

AMIDAS Pueden considerarse como derivados de los ácidos carboxílicos, en donde el grupo hidroxilo es sustituidos por el grupo amino. GRUPO AMINO -NH 2 29 O R–C–N-
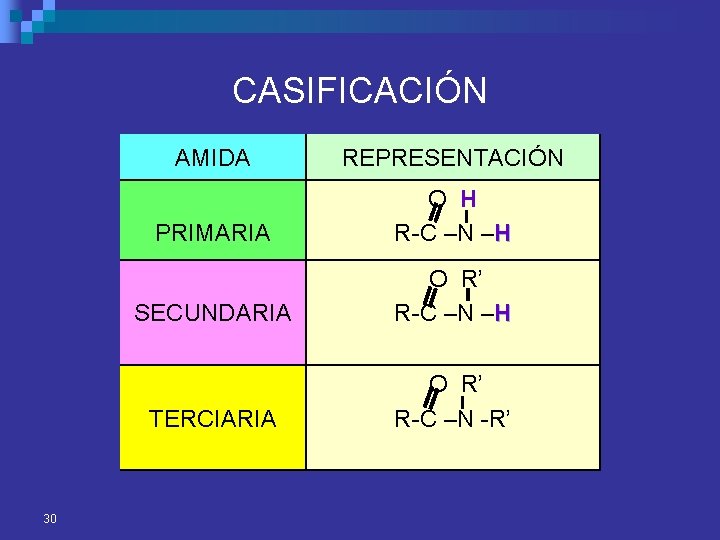
CASIFICACIÓN 30 AMIDA REPRESENTACIÓN PRIMARIA O H R-C –N –H SECUNDARIA O R’ R-C –N –H TERCIARIA O R’ R-C –N -R’

NOMENCLATURA n n 31 A las amidas se les da nombre como derivados de los ácidos carboxílicos. Las terminaciones ico del nombre común o la terminación oico del nombre UIQPA se reemplaza por el sufijo amida Los sustituyentes Alquílicos y arílicos unidos al nitrógeno se mencionan como prefijos, precedidos de la letra “N” del nombre de la amida simple.
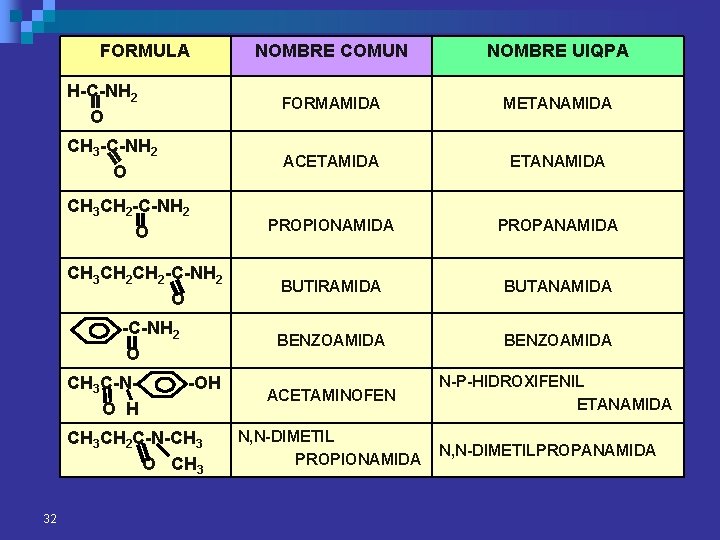
FORMULA NOMBRE COMUN NOMBRE UIQPA H-C-NH 2 O FORMAMIDA METANAMIDA CH 3 -C-NH 2 O ACETAMIDA ETANAMIDA PROPIONAMIDA PROPANAMIDA BUTIRAMIDA BUTANAMIDA BENZOAMIDA ACETAMINOFEN N-P-HIDROXIFENIL ETANAMIDA CH 3 CH 2 -C-NH 2 O CH 3 C-NO H -OH CH 3 CH 2 C-N-CH 3 O CH 3 32 N, N-DIMETIL PROPIONAMIDA N, N-DIMETILPROPANAMIDA
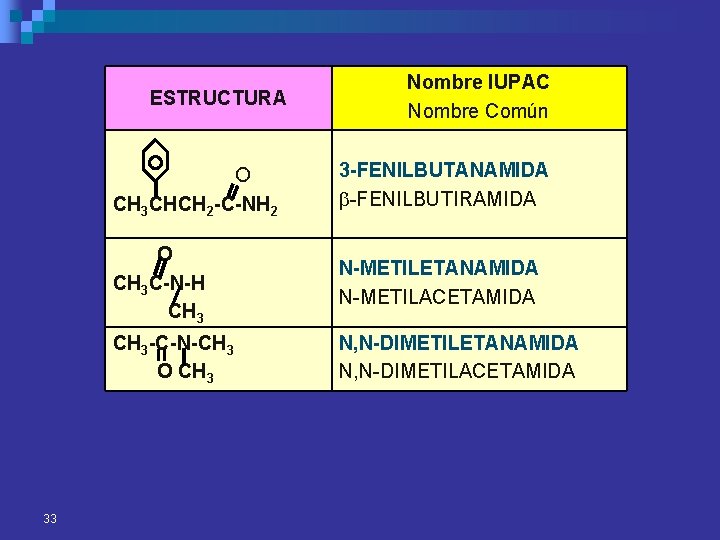
ESTRUCTURA 33 Nombre IUPAC Nombre Común O CH 3 CHCH 2 -C-NH 2 3 -FENILBUTANAMIDA b-FENILBUTIRAMIDA O CH 3 C-N-H CH 3 N-METILETANAMIDA N-METILACETAMIDA CH 3 -C-N-CH 3 O CH 3 N, N-DIMETILETANAMIDA N, N-DIMETILACETAMIDA

Importancia del Enlace Amida: se denomina al enlace Carbonilo-nitrógeno Enlace Amida O - C - N- Son importantes e indispensables para la vida, las proteínas contienen muchos aminoácidos unidos entre si mediante enlaces amida. 34

Tioesteres Análogos azufrados de los esteres Formula General: O R-C-SR’ 35
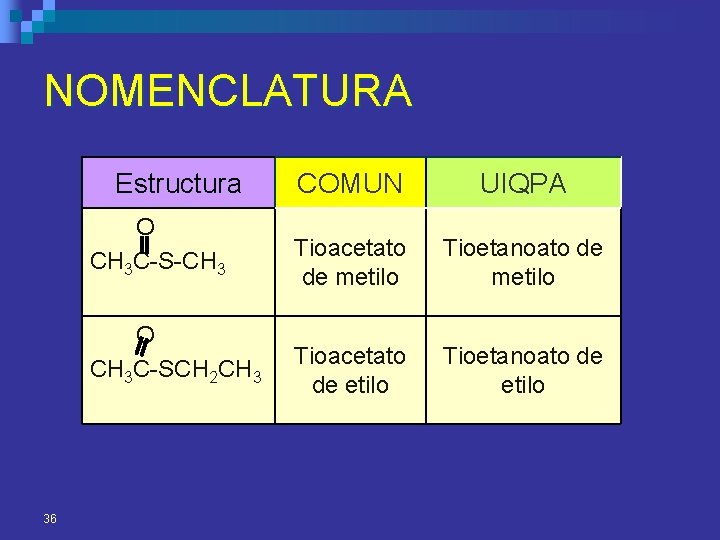
NOMENCLATURA Estructura 36 COMUN UIQPA O CH 3 C-S-CH 3 Tioacetato de metilo Tioetanoato de metilo O CH 3 C-SCH 2 CH 3 Tioacetato de etilo Tioetanoato de etilo

Fin 37
- Slides: 37