ACIDOS CARBOXILICOS ESTERES AMIDAS Semana 22 2020 Diapositivas

ACIDOS CARBOXILICOS , ESTERES, AMIDAS. Semana 22 -- 2020 Diapositivas con cuadros e imágenes proporcionados por Licda: Lilian Guzmán

Grupo Funcional Los ácidos carboxílicos tienen el grupo funcional carboxilo que se puede representar de las siguientes maneras: O -C-OH -CO 2 H -COOH Posee el grupo carbonilo+ radical hidroxilo se le denomina : “carboxilo”. Se les llama ácidos, pues son los más ácidos entre los compuestos orgánicos. 2

El nombre ácido carboxílico describe al grupo funcional de dos maneras: 1. La palabra carboxílico es una contracción de las palabras carbonilo e hidroxilo, dos unidades estructurales presentes en el grupo. 2. Se agrega el término ácido, ácido debido a las propiedades ácidas que presentan ya que son donadores de H+ ( protones). Son ácidos débiles por lo tanto cada uno de ellos tiene una Ka. 3

Acidez de los ácidos carboxílicos Los ácidos carboxílicos son ácidos débiles, por lo tanto su ionización es reversible y poseen una Ka. Ejemplo : RCOOH ⇄ RCOO - + H + Ej: CH 3 COOH ⇄ CH 3 COO - + H + Ka = [ CH 3 COO -] [H+] Ka = 1. 8 x 10 -5 [CH 3 COOH] Observe en la ecuación en el lado de los productos al ión H + ( H 3 O+), característica de las definiciones de ácidos ( Arrhenius, Bronsted-Lowry ). Note: El Hidrogeno que se disocia es el que se halla en el grupo –COOH, no los que están en el resto de la cadena carbonada. 4

Ka de algunos ácidos. Note que al aumentar el número de carbonos, su Ka disminuye generalmente ( se hacen menos ácidos) #C Estructura Ka 1 HCOOH 1. 8 x 10 -4 2 CH 3 COOH 1. 8 x 10 -5 3 CH 3 CH 2 COOH 1. 3 x 10 -5 4 CH 3(CH 2)2 COOH 1. 5 x 10 -5 5
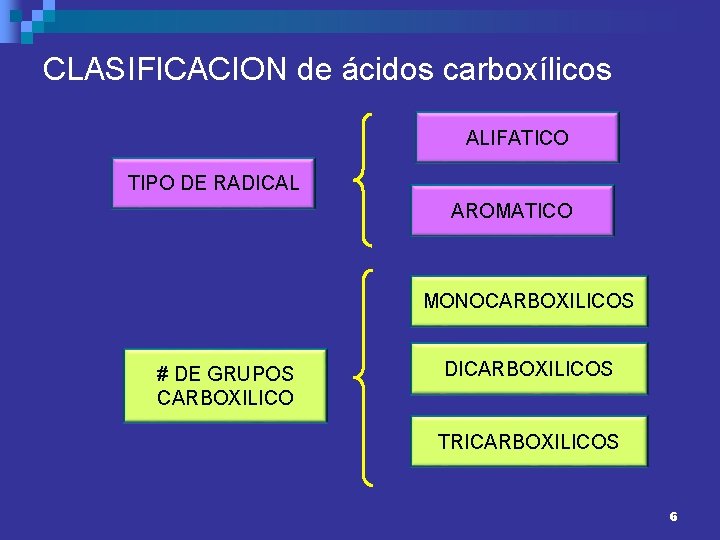
CLASIFICACION de ácidos carboxílicos ALIFATICO TIPO DE RADICAL AROMATICO MONOCARBOXILICOS # DE GRUPOS CARBOXILICO DICARBOXILICOS TRICARBOXILICOS 6

TIPO RADICAL Y Fórmula general ALIFATICO R-COOH AROMATICO Ar. COOH EJEMPLO: Posee un radical alifático CH 3 CH 2 COOH Posee un radical aromático EJEMPLO: COOH 7

NÚMERO DE GRUPOS CARBOXILICOS MONOCARBOXILICOS Tienen un solo O grupo carboxilo CH 3 COH DICARBOXILICOS Tienen 2 grupos carboxílicos COOH CH 2 COOH TRICARBOXILICOS Tienen 3 grupos carboxílicos CH 2 -COOH CH –COOH CH 2 -COOH 8
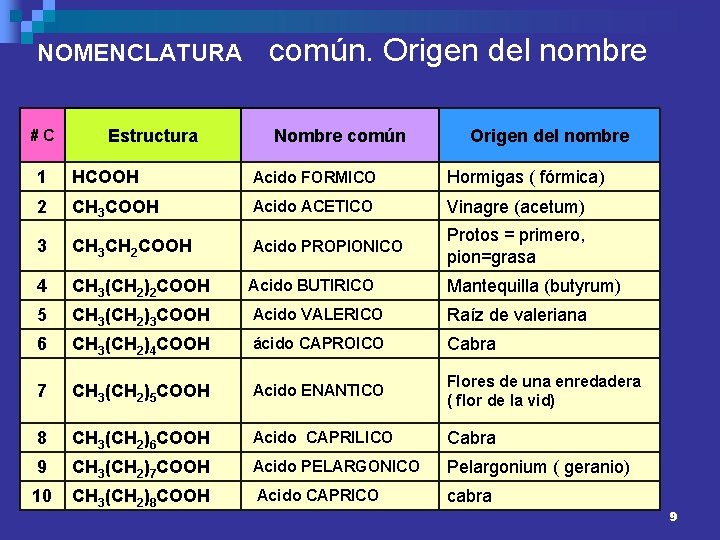
NOMENCLATURA #C Estructura común. Origen del nombre Nombre común Origen del nombre 1 HCOOH Acido FORMICO Hormigas ( fórmica) 2 CH 3 COOH Acido ACETICO Vinagre (acetum) 3 CH 3 CH 2 COOH Acido PROPIONICO Protos = primero, pion=grasa 4 CH 3(CH 2)2 COOH Acido BUTIRICO Mantequilla (butyrum) 5 CH 3(CH 2)3 COOH Acido VALERICO Raíz de valeriana 6 CH 3(CH 2)4 COOH ácido CAPROICO Cabra 7 CH 3(CH 2)5 COOH Acido ENANTICO Flores de una enredadera ( flor de la vid) 8 CH 3(CH 2)6 COOH Acido CAPRILICO Cabra 9 CH 3(CH 2)7 COOH Acido PELARGONICO Pelargonium ( geranio) 10 CH 3(CH 2)8 COOH Acido CAPRICO cabra 9

NOMENCLATURA COMUN de los ácidos carboxílicos sustituidos. Se ubica la posición de los sustituyentes por medio de letras griegas. Al carbono a la par del grupo carboxilo se le asigna la letra α. C – C – COOH EJEMPLO O CH 3 CHCH 2 C-OH NO 2 Acido - nitrobutírico Escriba la estructura del ácido α- hidroxivalérico. 10

Nomenclatura UIQPA para ácidos carboxílicos. Reglas. 1) Se antepone la palabra ácido y se nombran como derivados del alcano que los origina, añadiendo la palabra «ico» . 2)Si hay sustituyentes, sus posiciones se dan por números siendo el carbono carboxílico el número 1. Ejemplo: Br o CH 3 -CH 2 -CH-CH 2 -C-OH 5 4 3 2 Nombre: ácido 3 -Bromopentanoico 1 Escriba estructura del : ácido 4 -isopropil-3 -nitroheptanoico 11
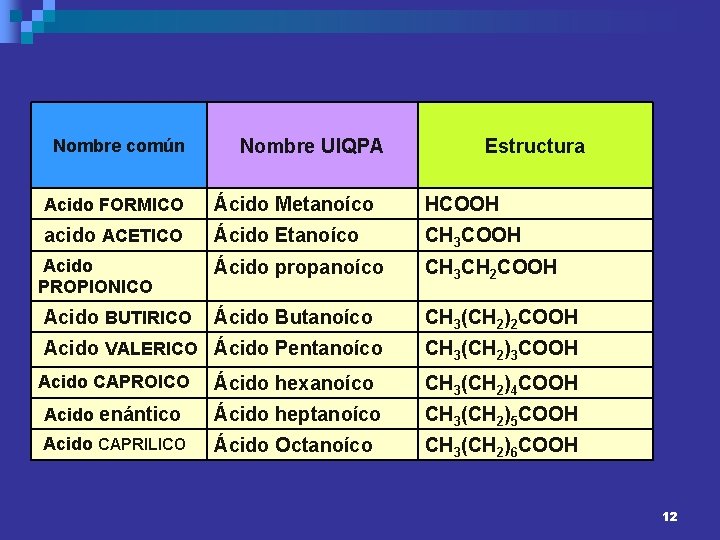
Nombre común Nombre UIQPA Estructura Acido FORMICO Ácido Metanoíco HCOOH acido ACETICO Ácido Etanoíco CH 3 COOH Ácido propanoíco CH 3 CH 2 COOH Ácido Butanoíco CH 3(CH 2)2 COOH Acido PROPIONICO Acido BUTIRICO Acido VALERICO Ácido Pentanoíco CH 3(CH 2)3 COOH Acido CAPROICO Ácido hexanoíco CH 3(CH 2)4 COOH Acido enántico Ácido heptanoíco CH 3(CH 2)5 COOH Acido CAPRILICO Ácido Octanoíco CH 3(CH 2)6 COOH 12
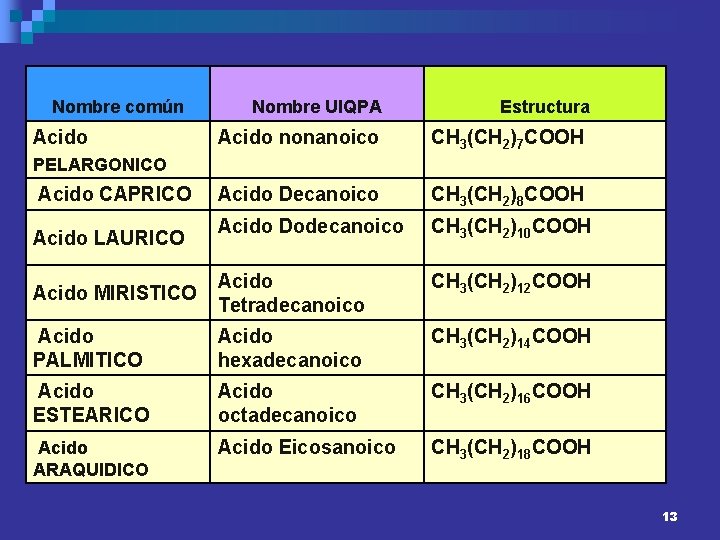
Nombre común Acido Nombre UIQPA Estructura Acido nonanoico CH 3(CH 2)7 COOH Acido Decanoico CH 3(CH 2)8 COOH Acido Dodecanoico CH 3(CH 2)10 COOH Acido MIRISTICO Acido Tetradecanoico CH 3(CH 2)12 COOH Acido PALMITICO Acido hexadecanoico CH 3(CH 2)14 COOH Acido ESTEARICO Acido octadecanoico CH 3(CH 2)16 COOH Acido ARAQUIDICO Acido Eicosanoico CH 3(CH 2)18 COOH PELARGONICO Acido CAPRICO Acido LAURICO 13
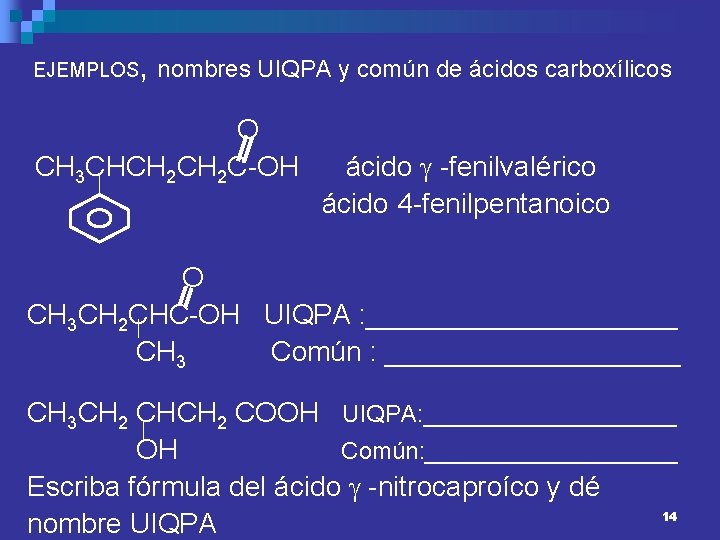
EJEMPLOS , nombres UIQPA y común de ácidos carboxílicos O CH 3 CHCH 2 C-OH ácido -fenilvalérico ácido 4 -fenilpentanoico O CH 3 CH 2 CHC-OH UIQPA : __________ CH 3 Común : __________ CH 3 CH 2 CHCH 2 COOH UIQPA: __________ OH Común: __________ Escriba fórmula del ácido -nitrocaproíco y dé 14 nombre UIQPA
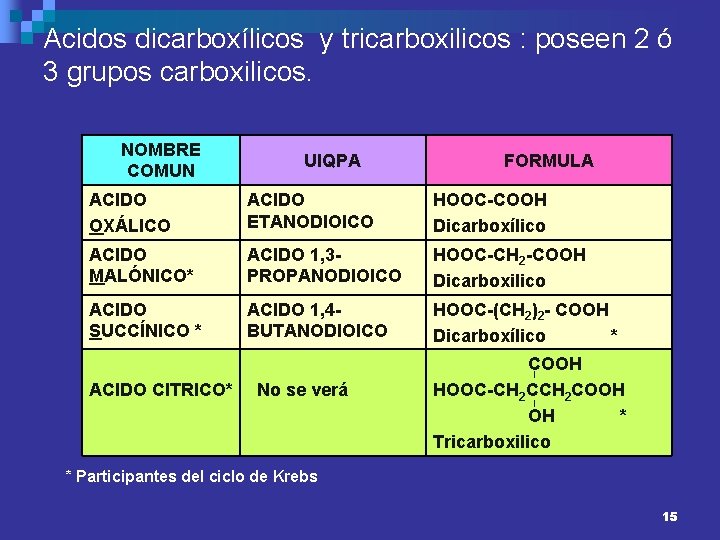
Acidos dicarboxílicos y tricarboxilicos : poseen 2 ó 3 grupos carboxilicos. NOMBRE COMUN UIQPA FORMULA ACIDO OXÁLICO ACIDO ETANODIOICO HOOC-COOH Dicarboxílico ACIDO MALÓNICO* ACIDO 1, 3 PROPANODIOICO HOOC-CH 2 -COOH Dicarboxilico ACIDO SUCCÍNICO * ACIDO 1, 4 BUTANODIOICO HOOC-(CH 2)2 - COOH Dicarboxílico * ACIDO CITRICO* No se verá COOH HOOC-CH 2 COOH OH * Tricarboxilico * Participantes del ciclo de Krebs 15

PROPIEDADES FISICAS § Están entre los compuestos orgánicos más polares § Los primeros 9 son líquidos, incoloros y olor desagradable. Con más de 10 carbonos, son sólidos cerosos, e inodoros. § Los ácidos de 6 C, 8 C, 10 C ( Caproíco, caprílico y caprico ) poseen olores a «cabra» § Los que poseen de 1 -5 C, son solubles en agua. § Debido a que forman dímeros por puentes de Hidrogeno, sus puntos de ebullición son más altos que alcoholes, cetonas y aldehídos de masa molecular similar. 16
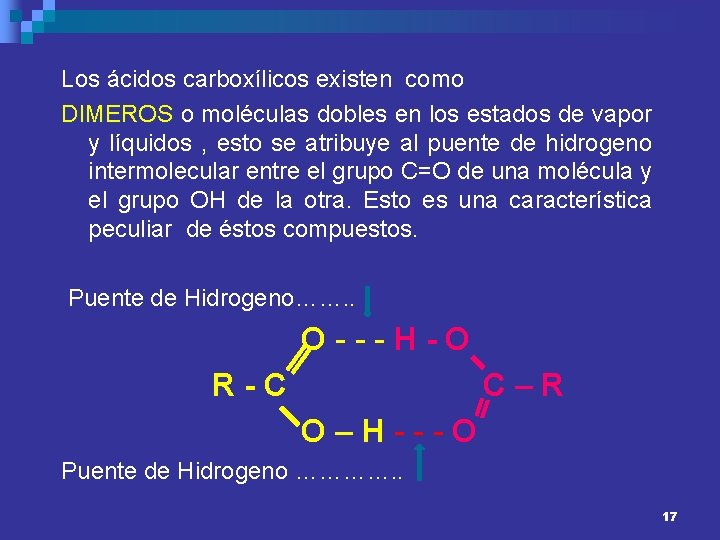
Los ácidos carboxílicos existen como DIMEROS o moléculas dobles en los estados de vapor y líquidos , esto se atribuye al puente de hidrogeno intermolecular entre el grupo C=O de una molécula y el grupo OH de la otra. Esto es una característica peculiar de éstos compuestos. Puente de Hidrogeno……. . O---H-O R-C C–R O–H---O Puente de Hidrogeno …………. . 17

Importancia biológica y médica de los ácidos carboxílicos : A- Forman parte de biomoleculas importantes: Los ácidos grasos que forman lípidos, son ácidos carboxílicos. Ejemplo: Acido Hexadecanoico ( acido palmítico ) CH 3 (CH 2)14 COOH, forma parte de la tripalmitina, presente en el aceite de palma. 18

B-Forman parte del metabolismo: Ej: el producto de la fermentación láctica: ácido láctico es un ácido carboxílico CH 3 CHCOOH OH Nombre UIQPA: ácido 2 -propanoico Nombre común : ácido -hidroxipropionico Otros ácidos carboxílicos como el ácido malónico, succínico y cítrico, participan del ciclo de Krebs 19

C- Cuerpos cetónicos formados en la matriz mitocondrial del hígado principalmente y en menor proporción en el riñón: son ácidos carboxílicos. Proporcionan energía al corazón y cerebro, en determinadas condiciones: Acido acetoacético: CH 3 COCH 2 COOH Acido β-hidroxibutirico CH 3 CHCH 2 COOH OH UIQPA: acido 3 -hidroxibutanoico 20

D- Algunos son medicamentos: El ácido carboxílico, llamado ácido valproico: Usado para tratamiento de la epilepsia, trastorno bipolar, demencia por VIH, atrofia muscular espinal ( enfermedad autosómica recesiva) CH 3 CH 2 CHCOOH CH 2 CH 3 Acido 2 -propilpentanoico ( UIQPA) Acido -propilvalérico 21
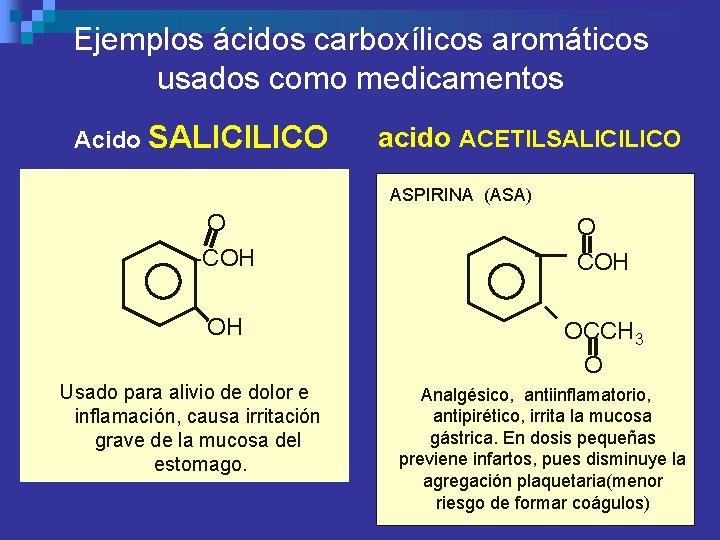
Ejemplos ácidos carboxílicos aromáticos usados como medicamentos Acido SALICILICO acido ACETILSALICILICO ASPIRINA (ASA) O -COH OH OCCH 3 O Usado para alivio de dolor e inflamación, causa irritación grave de la mucosa del estomago. Analgésico, antiinflamatorio, antipirético, irrita la mucosa gástrica. En dosis pequeñas previene infartos, pues disminuye la agregación plaquetaria(menor riesgo de formar coágulos)
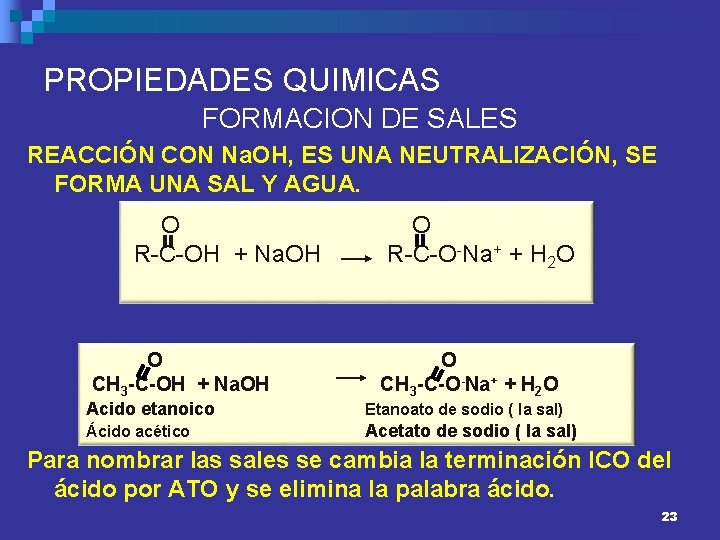
PROPIEDADES QUIMICAS FORMACION DE SALES REACCIÓN CON Na. OH, ES UNA NEUTRALIZACIÓN, SE FORMA UNA SAL Y AGUA. O R-C-OH + Na. OH O CH 3 -C-OH + Na. OH O R-C-O-Na+ + H 2 O O CH 3 -C-O-Na+ + H 2 O Acido etanoico Etanoato de sodio ( la sal) Ácido acético Acetato de sodio ( la sal) Para nombrar las sales se cambia la terminación ICO del ácido por ATO y se elimina la palabra ácido. 23
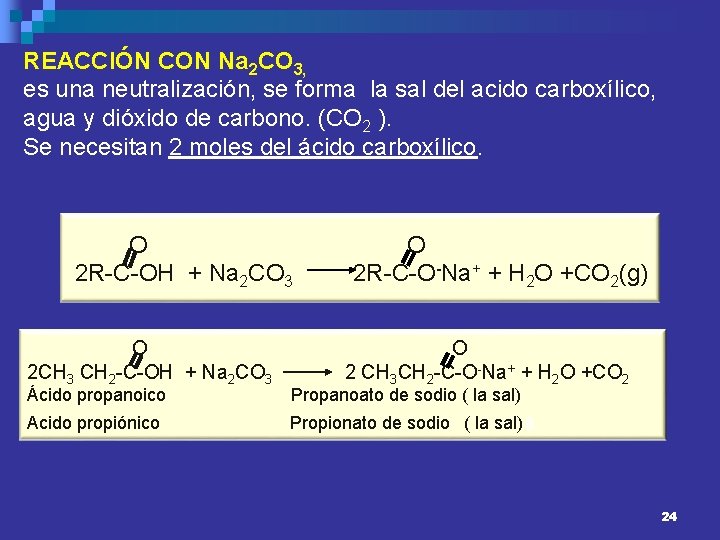
REACCIÓN CON Na 2 CO 3, es una neutralización, se forma la sal del acido carboxílico, agua y dióxido de carbono. (CO 2 ). Se necesitan 2 moles del ácido carboxílico. O 2 R-C-OH + Na 2 CO 3 O 2 CH 3 CH 2 -C-OH + Na 2 CO 3 O 2 R-C-O-Na+ + H 2 O +CO 2(g) O 2 CH 3 CH 2 -C-O-Na+ + H 2 O +CO 2 Ácido propanoico Propanoato de sodio ( la sal) Acido propiónico Propionato de sodio ( la sal)á 24
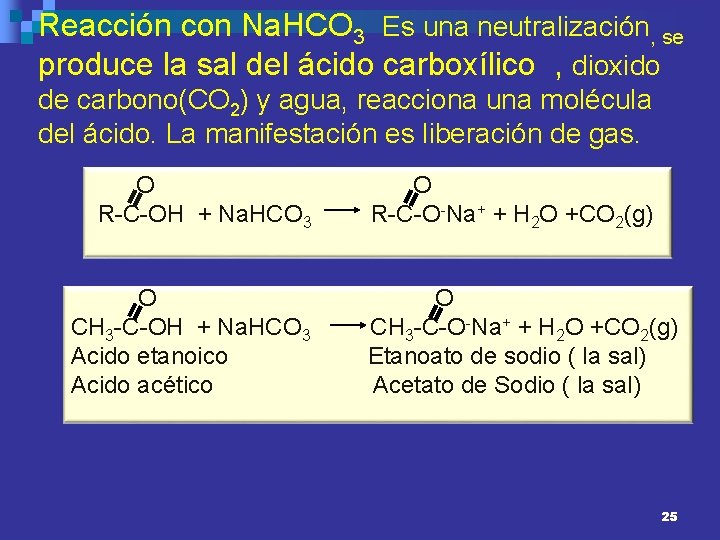
Reacción con Na. HCO 3 Es una neutralización, se produce la sal del ácido carboxílico , dioxido de carbono(CO 2) y agua, reacciona una molécula del ácido. La manifestación es liberación de gas. O R-C-OH + Na. HCO 3 O CH 3 -C-OH + Na. HCO 3 Acido etanoico Acido acético O R-C-O-Na+ + H 2 O +CO 2(g) O CH 3 -C-O-Na+ + H 2 O +CO 2(g) Etanoato de sodio ( la sal) Acetato de Sodio ( la sal) 25
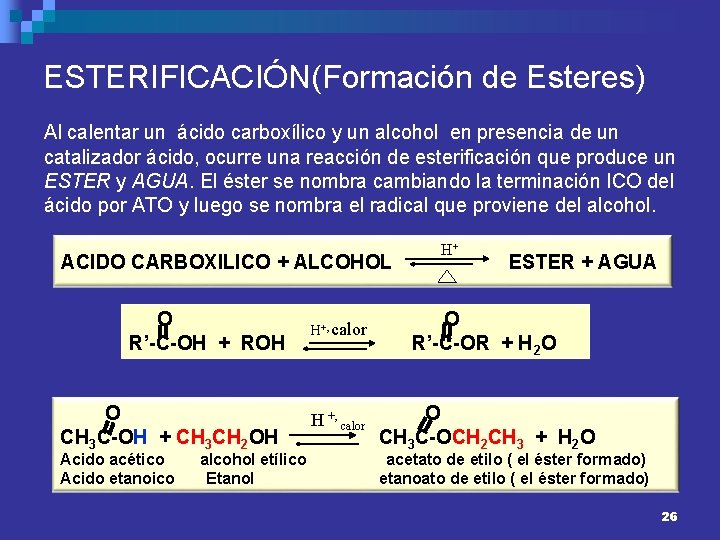
ESTERIFICACIÓN(Formación de Esteres) Al calentar un ácido carboxílico y un alcohol en presencia de un catalizador ácido, ocurre una reacción de esterificación que produce un ESTER y AGUA. El éster se nombra cambiando la terminación ICO del ácido por ATO y luego se nombra el radical que proviene del alcohol. ACIDO CARBOXILICO + ALCOHOL O R’-C-OH + ROH O CH 3 C-OH + CH 3 CH 2 OH Acido acético Acido etanoico alcohol etílico Etanol H+ ESTER + AGUA H+, calor O R’-C-OR + H 2 O H +, calor O CH 3 C-OCH 2 CH 3 + H 2 O acetato de etilo ( el éster formado) etanoato de etilo ( el éster formado) 26

ESTERES Los esteres son los derivados mas importantes de los ácidos carboxílicos. FORMULA GENERAL O R-C-OR’ R-COO-R’ Donde R puede ser un hidrógeno en caso de que el ácido carboxílico sea el metanoíco ó fórmico ( el más pequeño de los ácidos carboxílicos, o bién un grupo alquilo o arilo y donde R’ ( porción proveniente del alcohol) puede ser alquilo, arilo pero NO hidrógeno, ya que el alcohol más pequeño posee un radical metilo ( -CH 3 ). 27

NOMENCLATURA 1 -Primero se menciona la porción que proviene del ácido. Tanto en nomenclatura común como en UIQPA la terminación “ico” ico del ácido se reemplaza por el sufijo “ato”. ato Luego se da el nombre del radical proveniente del alcohol, terminado en «o» 28
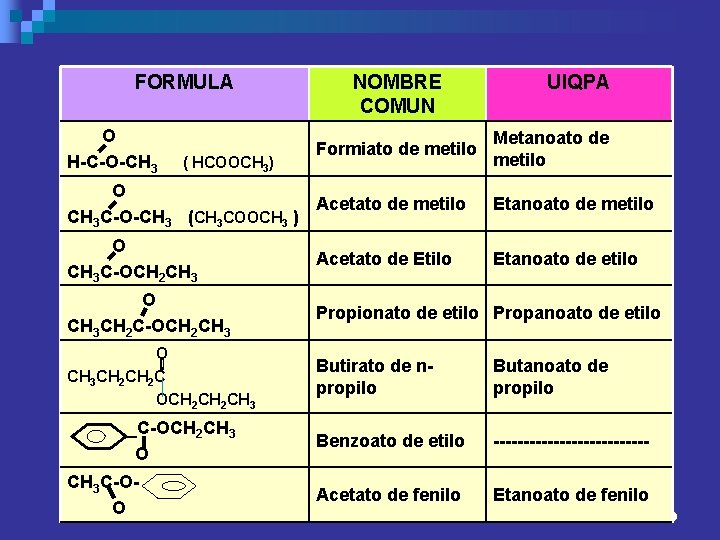
FORMULA O H-C-O-CH 3 ( HCOOCH 3) NOMBRE COMUN Formiato de metilo UIQPA Metanoato de metilo O Acetato de metilo CH 3 C-O-CH 3 (CH 3 COOCH 3 ) Etanoato de metilo O CH 3 C-OCH 2 CH 3 Acetato de Etilo Etanoato de etilo O CH 3 CH 2 C-OCH 2 CH 3 Propionato de etilo Propanoato de etilo O CH 3 CH 2 C OCH 2 CH 3 Butirato de npropilo Butanoato de propilo Benzoato de etilo ------------- Acetato de fenilo Etanoato de fenilo _C-OCH 2 CH 3 O CH 3 C-OO 29

PROPIEDADES FISICAS Poseen puntos de ebullición más altos que los alcanos y éteres, pero más bajos que alcoholes y ácidos carboxílicos de masa molecular similar, ya que no forman puentes de Hidrógeno de forma significativa. La mayor parte de esteres son líquidos, incoloros, de 1 a 5 C son solubles en agua. A diferencia de los ácidos carboxílicos de los cuales se derivan, los esteres poseen olores agradables. El aroma de muchas flores y frutos se debe a la presencia de esteres. Por eso se usan en la fabricación perfumes, de dulces y bebidas. Puntos de ebullición de esteres respecto a otras familias: Alcanos y éteres < esteres < alcoholes < ácidos carboxílicos 30
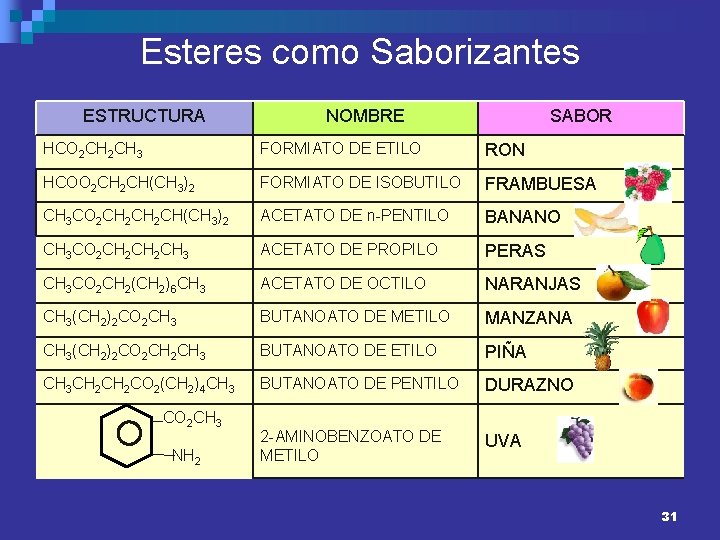
Esteres como Saborizantes ESTRUCTURA NOMBRE SABOR HCO 2 CH 3 FORMIATO DE ETILO RON HCOO 2 CH(CH 3)2 FORMIATO DE ISOBUTILO FRAMBUESA CH 3 CO 2 CH 2 CH(CH 3)2 ACETATO DE n-PENTILO BANANO CH 3 CO 2 CH 2 CH 3 ACETATO DE PROPILO PERAS CH 3 CO 2 CH 2(CH 2)6 CH 3 ACETATO DE OCTILO NARANJAS CH 3(CH 2)2 CO 2 CH 3 BUTANOATO DE METILO MANZANA CH 3(CH 2)2 CO 2 CH 3 BUTANOATO DE ETILO PIÑA CH 3 CH 2 CO 2(CH 2)4 CH 3 BUTANOATO DE PENTILO DURAZNO 2 -AMINOBENZOATO DE METILO UVA CO 2 CH 3 NH 2 31

Salicilato de Metilo También llamado esencia de gaulteria o de Wintergreen O Con olor agradable. -C-OCH 3 Fármaco de acción balsámica, analgésica OH y suavizante. Se emplea en pomadas, linimentos, enjuagues bucales, pastas dentales 32

AMIDAS Pueden considerarse como derivados de los ácidos Función amida RCONH 2 O R -C – N En el nitrógeno pueden haber uno ó dos grupos alquilo ó arilo sustituyentes de uno ó los dos Hidrógenos del grupo amino -NH 2 33
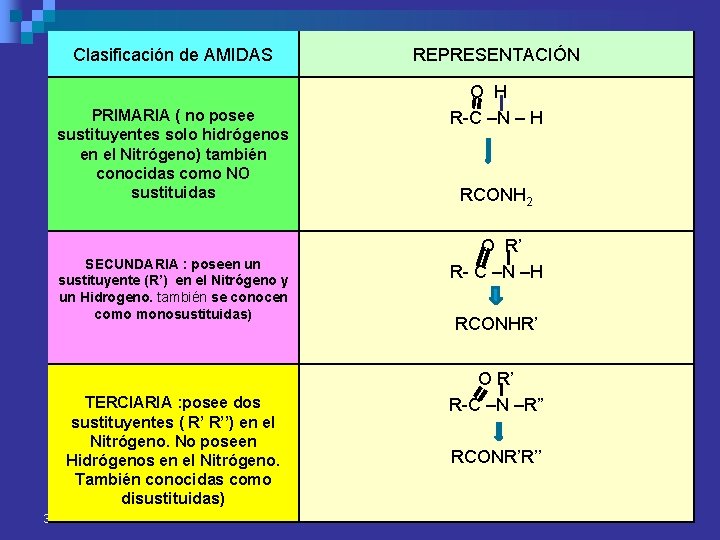
Clasificación de AMIDAS PRIMARIA ( no posee sustituyentes solo hidrógenos en el Nitrógeno) también conocidas como NO sustituidas SECUNDARIA : poseen un sustituyente (R’) en el Nitrógeno y un Hidrogeno. también se conocen como monosustituidas) TERCIARIA : posee dos sustituyentes ( R’ R’’) en el Nitrógeno. No poseen Hidrógenos en el Nitrógeno. También conocidas como disustituidas) 34 REPRESENTACIÓN O H R-C –N – H RCONH 2 O R’ R- C –N –H RCONHR’ O R’ R-C –N –R” RCONR’R’’

NOMENCLATURA Las amidas se nombran como derivados de los n n ácidos carboxílicos. Las terminaciones ico del nombre común o la terminación oico del nombre UIQPA se reemplaza por el sufijo amida Los radicales unidos al nitrógeno se mencionan en orden alfabético precedidos de la letra “N” para indicar que están como sustituyentes en el Nitrógeno y no en el carbono. Ejemplos 35

FORMULA NOMBRE COMUN NOMBRE UIQPA H-C-NH 2 O FORMAMIDA METANAMIDA CH 3 -C-NH 2 O ACETAMIDA ETANAMIDA PROPIONAMIDA PROPANAMIDA BUTIRAMIDA BUTANAMIDA CH 3 CH 2 -C-NH 2 O CH 3 C-NO H BENZAMIDA -OH CH 3 CH 2 C-N-CH 3 O CH 3 36 ACETAMINOFEN N, N-DIMETIL PROPIONAMIDA Fenilmetanamida N-p-HIDROXIFENIL ETANAMIDA N, N-DIMETILPROPANAMIDA
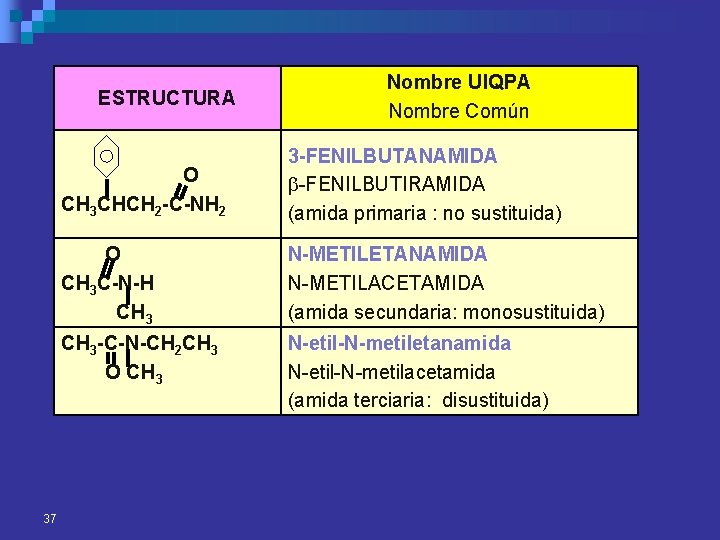
ESTRUCTURA 37 Nombre UIQPA Nombre Común O CH 3 CHCH 2 -C-NH 2 3 -FENILBUTANAMIDA -FENILBUTIRAMIDA (amida primaria : no sustituida) O CH 3 C-N-H CH 3 N-METILETANAMIDA N-METILACETAMIDA (amida secundaria: monosustituida) CH 3 -C-N-CH 2 CH 3 O CH 3 N-etil-N-metiletanamida N-etil-N-metilacetamida (amida terciaria: disustituida)

Importancia del Enlace Amida: se denomina al enlace Carbonilo-nitrógeno Enlace Amida O - C - N- Presente en las proteínas y péptidos. Y otras biomoléculas. La unión entre aminoácidos en la cadena peptídica de las proteínas es a través de enlaces amida ( enlaces peptídicos). 38

Propiedades físicas de las amidas La amida de un carbono : formamida (metanamida), es líquida todas las demás son sólidas. Son inodoras, incoloras. Las menores son solubles en agua. Poseen puntos de ebullición anormalmente altos, debido a la polaridad del grupo amida, por lo tanto forman atracciones dipolares y además puentes de hidrogeno, debido al grupo amino. – NH 2. Las amidas terciarias no poseen Hidrogeno, por eso NO forman puentes de Hidrogeno. Puntos de ebullición en las Amidas: Primarias > Secundarias > Terciarias 39

Ejercicios: De la estructura y clasifique a los siguientes compuestos como Ester, o Amidas ( 1ª, 2ª, 3ª ) a) Valerato de isopropilo. b) Benzoato de etilo c) N, N-dietilbutiramida Cuál es el nombre UIQPA. d) Que acido carboxílico y que alcohol, origina al siguiente éster Butanoato de sec-butilo. Leer Químicas y salud, indicadas en el documento: Macro y Microcontenidos.

Complete el siguiente cuadro: Se procede a la hidrolisis de derivados de ácidos carboxílicos Obteniendose los siguientes productos: Productos de Hidrolisis Compuesto original: Ester / Amida Nombre del éster Formula del o amida original éster o amida original Acido pentanoico y 1 -pentanol Acido caprico y etilmetil amina. 41

Algunas amidas de importancia en la salud y medicina. Nombre Importancia Urea Producto final del metabolismo de las proteínas en el organismo, es la forma como elimina nuestro organismo el Nitrógeno proveniente de las proteínas. Acetaminofén y Fenacetin Componentes del TYLENOL , fármaco que reduce la fiebre y el dolor, pero con poco efecto antiinflamatorio. Fenobarbital, Pentobarbital y secobarbital Amidas cíclicas del ácido barbitúrico, en dosis pequeñas son sedantes y en dosis mayores inductores del sueño. Forman hábito. Meprobamato y diazepan Actúan como sedantes, tranquilizantes e inductores del sueño. 42

Haga los siguientes ejercicios pagina 590: 15. 33 , 15. 35, 15. 57. Respuestas pág. . 592 43
- Slides: 43