ACIDOS BASES Y ELECTROLITOS Semana Nmero 12 2016

ACIDOS , BASES Y ELECTROLITOS Semana Número 12 / 2016 Nota: diapositivas con imágenes, cuadros, proporcionadas por la Licda: Lilian Guzmán Melgar

ACIDOS Y BASES ACIDO Tiene sabor agrio y pueden producir sensación de picazón en la piel. Su nombre viene del latín acidus = agrio Ej. Jugo de limón, vinagre, aguas gaseosas BASE Tiene un sabor amargo y sensación jabonosa en la piel. Ejemplo; : antiácidos, limpiavidrios, jabón. 2

Definiciones : ARRHENIUS ACIDO : Sustancia que produce iones hidrogeno (H+), al disociarse en agua + El H+ es un protón que en solución acuosa se hidrata y se convierte en ión Hidronio (H 3 O+) ; pero se representa como H+ H + + H 2 O → H 3 O + Ejs de ácidos: HCl , HNO 3 , , H 2 SO 4 , H 2 CO 3 Ej de disociación del HCl + H 2 O → H 3 O+(ac) + Cl - (ac) La ecuación anterior puede simplificarse , omitiendo el H 2 O como reactivo y se coloca al H + en lugar de H 3 O+ HCl H+ + Cl - BASE : Sustancias que liberan, iones hidróxido (OH-), al disociarse en agua. Ejemplo : Na. OH, KOH, Ba(OH)2 Na. OH → Na+ + OH 3

Definiciones : BRONSTED-LOWRY ACIDO: Sustancia que dona un protón , (ion H+) a otra sustancia. BASE: Sustancia que acepta un protón HCl + NH 3 → NH 4+ + Cl. ACIDO BASE Note el HCl dona un protón al NH 3, el cual lo acepta , por lo tanto se define al HCl como ácido y al NH 3 como base. 4
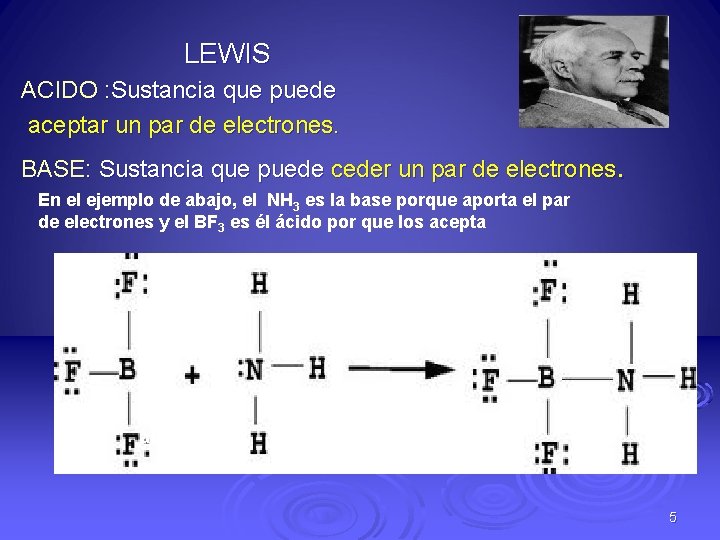
LEWIS ACIDO : Sustancia que puede aceptar un par de electrones. BASE: Sustancia que puede ceder un par de electrones. En el ejemplo de abajo, el NH 3 es la base porque aporta el par de electrones y el BF 3 es él ácido por que los acepta acido Base acido 5
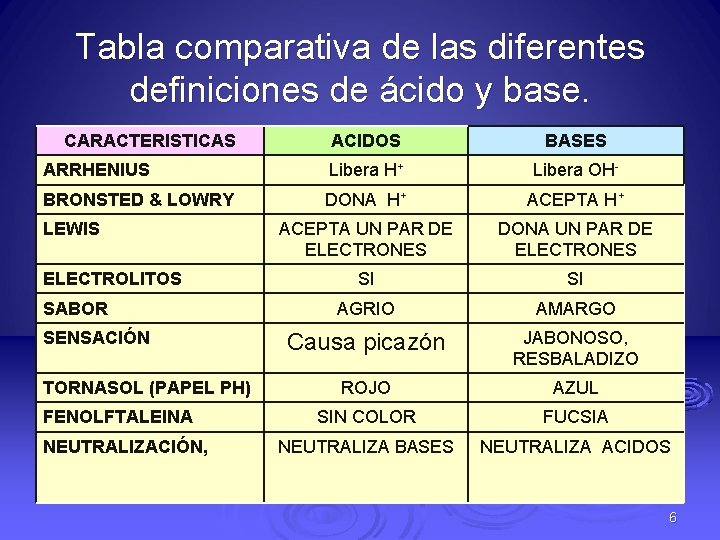
Tabla comparativa de las diferentes definiciones de ácido y base. CARACTERISTICAS ACIDOS BASES ARRHENIUS Libera H+ Libera OH- BRONSTED & LOWRY DONA H+ ACEPTA UN PAR DE ELECTRONES DONA UN PAR DE ELECTRONES SI SI AGRIO AMARGO Causa picazón JABONOSO, RESBALADIZO ROJO AZUL SIN COLOR FUCSIA NEUTRALIZA BASES NEUTRALIZA ACIDOS LEWIS ELECTROLITOS SABOR SENSACIÓN TORNASOL (PAPEL PH) FENOLFTALEINA NEUTRALIZACIÓN, 6

IONIZACION Ø 7

Electrolito: Sustancia que en solución acuosa esta disociada en iones y conduce la electricidad. Electrolito FUERTE § Se disocian al 100%. § Buen conductor de la electricidad § La reacción de ionización ocurre en un solo sentido(irreversible). § No poseen Ka ni Kb. § Ej: base fuerte KOH → K+ + OHEj. acido fuerte H NO 3 → H++ NO 3 - Electrolito DEBIL § Se disocian en un pequeño %. § Conduce poco la electricidad. § Su reacción de ionización es reversible y poseen Ka si son ácidos ó Kb si son bases. C 6 H 5 COOH ⇄ H+ + C 6 H 5 COOKa = 6. 5 x 10 -5 NH 3 + H 2 O ⇄ NH 4+ + OHKb = 1. 8 x 10 -5 8
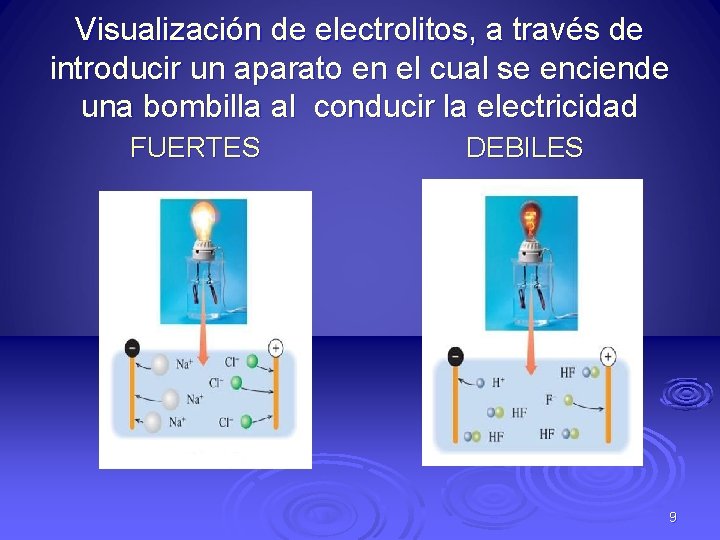
Visualización de electrolitos, a través de introducir un aparato en el cual se enciende una bombilla al conducir la electricidad FUERTES DEBILES 9

NO ELECTROLITO Sustancias que en solución ó fundidos ( en caso de sólidos) o en estado líquido ( en caso de líquidos, . Ej: alcohol, gasolina )NO conducen la electricidad. ( En éste caso no se enciende la bombilla) Ej : Aceite • Alcohol • Gasolina • Azúcar azúcar 10

IONIZACION DEL AGUA El agua en forma pura es mala conductora de electricidad, debido a que se ioniza muy poco. H 2 O + H 2 O ⇄ H 3 O+ + OHA 25°C, en el agua pura: la [ H+ ] = [OH-] y tiene el siguiente valor. [H+] = 0. 00000010 = 1 x 10 -7 M [OH-] = 0. 00000010 = 1 x 10 – 7 M 11
![Constante de Producto Iónico del agua (Kw) Kw = [H+] [OH-] Kw = [1. Constante de Producto Iónico del agua (Kw) Kw = [H+] [OH-] Kw = [1.](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-12.jpg)
Constante de Producto Iónico del agua (Kw) Kw = [H+] [OH-] Kw = [1. 0 x 10 -7 ] [1 x 10 - 7] Kw = 1. 0 x 10 -14 KH O = 1. 0 x 10 -14 2 12

¿Cómo influye la adición de un ácido (H+)y de una base ( OH-) al agua o soluciones acuosas, en las concentraciones de iones hidrógeno e hidroxilo ? Al añadir un ácido se liberan H+ [ H+] Si ↑[ H+ ] [OH-] ↓ hasta que [ H+] [OH-] = 1. 0 x 10 -14 Al añadir una base, se liberan OH- [OH - ] Si ↑[OH -] [H+ ] ↓ hasta que [H+] [OH-] = 1. 0 x 10 -14 13
![En soluciones Acidas: Acidas [H+] >1. 0 x 10 -7 En soluciones Alcalinas: [H En soluciones Acidas: Acidas [H+] >1. 0 x 10 -7 En soluciones Alcalinas: [H](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-14.jpg)
En soluciones Acidas: Acidas [H+] >1. 0 x 10 -7 En soluciones Alcalinas: [H Alcalinas +] < 1. 0 x 10 -7 En soluciones Neutras: [H+] es igual a 1. 0 x 10 -7 Ej: Una muestra de bilis tiene una [OH-] de 1. 0 x 10 -5 ¿Cuál es la [H+] ? . Se usa Kw y se despeja [H+] [OH-] = 1 x 10 -14 [ H + ] = 1 x 10 -14 / [ OH - ] [ H + ] = 1 x 10 -14 / 10 x 10 -5 [ H + ] = 1 x 10 -9 14

ACIDOS Y BASES FUERTES ACIDOS FUERTES: - Se ionizan casi en un 100%. _Tienen una ionización irreversible. - No poseen Ka. HCl Ácido Clorhídrico HBr Ácido Bromhídrico HI Ácido Yodhídrico H 2 SO 4 Ácido sulfúrico HNO 3 Ácido Nítrico 15

ÁCIDOS DÉBILES Se ionizan en pequeña proporción. § Tienen una ionización reversible § Poseen una constante de ionización (Ka) La que puede calcularse de la sig. Forma. Ejemplo ácido acético § HC 2 H 3 O 2 ⇄ H+ + C 2 H 3 O 2 Ka= Ka [H+] [C 2 H 3 O 2 -] [HC 2 H 3 O 2] Ejemplo de ácidos débiles HCOOH Ka= 2. 1 x 10 -4 HF Ka = 7. 2 x 10 -4 Ácido Fórmico HCN Acido Ka= 4. 9 x 10 -10 cianhídrico Ácido Fluorhídrico CH 3 CHOHCOOH Ka = 1. 4 x 10 -4 Ácido láctico 16

BASE FUERTE Se ionizan casi en un 100 % § Tiene una ionización irreversible. § No poseen Kb. § Na. OH KOH Hidróxido de Sodio Hidróxido de Potasio 17

BASE DEBIL § § § Se ionizan parcialmente en agua Tienen una ionización reversible Poseen una constante de ionización (Kb), la cual puede calcularse de la siguiente manera. NH 3 + H 2 O ⇄ NH 4+ + OH§ Kb = [ NH 4+] [ OH -] § [NH 3] § Note: no se toma en cuenta a el H 2 O en la expresión de Kb ni en K a Ejemplo de bases débiles C 6 H 5 NH 2 NH 3 Kb: 4. 0 x 10 -10 Kb = 1. 8 x 10 -5 Anilina Amoniaco 18

p. H El p. H es la medida de la concentración de iones hidronio [H 3 O+ ] ó [ H+] en una solución. Y se calcula: p. H = - log [H+] Ej emplo : Calcule el p. H de una solución que posee [ H + ] =0. 00065. Resolución p. H = -log 6. 5 x 10 – 4 = 3. 18 19
![El agua pura tiene una [H+] = 1 x 10 -7 y un p. El agua pura tiene una [H+] = 1 x 10 -7 y un p.](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-20.jpg)
El agua pura tiene una [H+] = 1 x 10 -7 y un p. H 7. § Toda solución neutra tiene un p. H 7 § Toda solución ácida tiene un p. H menor 7 § Toda solución básica tiene un p. H mayor 7 NEUTRO 1 2 3 4 5 MAS ACIDO 6 7 8 9 10 11 12 13 14 MAS BASICO 20
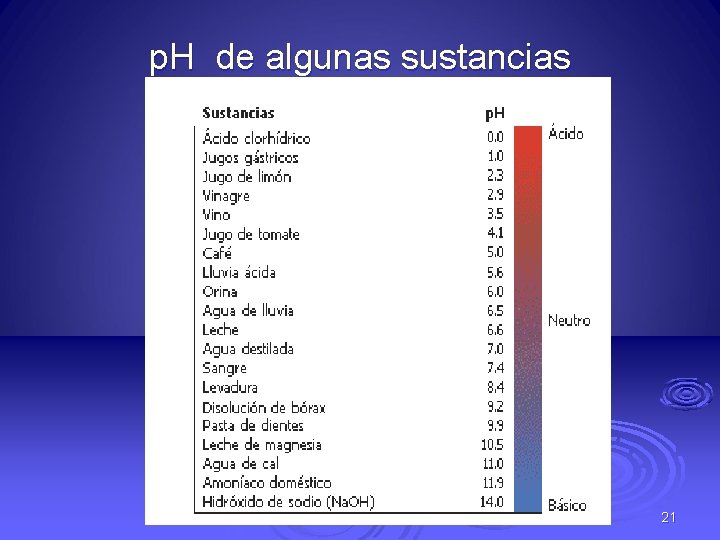
p. H de algunas sustancias 21
![p. OH Es la medida de la concentración de iones hidroxilo [OH-]en una solución: p. OH Es la medida de la concentración de iones hidroxilo [OH-]en una solución:](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-22.jpg)
p. OH Es la medida de la concentración de iones hidroxilo [OH-]en una solución: Se calcula de la sig. Forma p. OH = - log [OH-] Para toda solución acuosa : p. H + p. OH = 14 p. H = 14 -p. OH y p. OH = 14 - p. H Ej. Si el p. H de una solución es 3. 2. Cuál es el valor de el p. OH. ? Resp: p. H + p. OH = 14 – p. H p. OH = 14 – 3. 2 = 10. 8 22
![Continuación… ejercicios Ej: Si [OH-] en una solución es 0. 05, cuál será el Continuación… ejercicios Ej: Si [OH-] en una solución es 0. 05, cuál será el](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-23.jpg)
Continuación… ejercicios Ej: Si [OH-] en una solución es 0. 05, cuál será el valor del p. OH y el p. H: Resp: p. OH = -log [ OH-] p. OH = -log 0. 05 p. OH= 1. 30 p. H = 14 -p. OH PH= 14 -1. 30 = 12. 7 Como el cálculo de p. H nos da 12. 7 la solución es básica ó alcalina 23
![Ø Para calcular [H+ ], use Kw : Ø [ H+] [OH-] = 1 Ø Para calcular [H+ ], use Kw : Ø [ H+] [OH-] = 1](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-24.jpg)
Ø Para calcular [H+ ], use Kw : Ø [ H+] [OH-] = 1 x 10 -14 Ahora despeje [H+] [ H+] = 1 x 10 -14 = 1 x 10 -14 = 2 x 10 -13 Ø [OH -] 0. 05 24
![Calculo del valor de [H +] y [OH-] a partir de valores de p. Calculo del valor de [H +] y [OH-] a partir de valores de p.](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-25.jpg)
Calculo del valor de [H +] y [OH-] a partir de valores de p. H Ø Use las siguientes fórmulas: Ø [H+] = 10 – p. H y [OH -] = 10 - p. OH Ø Ej: Calcule [H+] de una solución cuyo p. H es 3. 7. Ø Resp: [H+] = 10 -p. H = 10 – 3. 7 = 0. 000199 ó sea [H +] =1. 99 x 10 -4 Ø Ej. Calcule [OH -] si el p. OH de una solución es 2. 8 Ø Resp: [OH - ] = 10 -p. OH = 10 -2. 8 = 0. 00158 Ø ó sea que [ OH-] = 1. 58 x 10 -3

Procedimiento para calcular p. H de ácidos fuertes Los ácidos fuertes como son la mayoría de hidrácidos y oxácidos : HCl , HNO 3, etc , se ionizan casi en un 100 %, por lo tanto la [ H + ] es igual a la concentración molar del ácido. Ø EJ # 1 : cual es el p. H de una solución de HCl 0. 066 M Ø Se considera que la [ H + ] es igual a la [ ácido ] Ø Resp: p. H = - log [H + ] * p. H = - log 0. 066 Ø p. H = 1. 18 Ø * note usamos la concentración molar del ácido (HCl): que en éste caso es 0. 006. Ø Ejercicio: Calcule el p. H de una solución de HNO 3 0. 0035 M

Procedimiento para calcular el p. H de bases fuertes La mayoría de Hidróxidos que poseen un solo radical OH, son bases fuertes , se ionizan casi en un 100 %, por eso la [ OH - ] es igual a la Molaridad de la base. Ej: Calcule el p. H de una solución de Na. OH 0. 024 M. Resolución: Ø Considere que [OH -] es igual a la [ Na. OH ] [ OH -] = 0. 024 p. OH = -log [OH-] p. OH = -log 0. 024 p. OH = 1. 62. Aplique : p. H + p. OH = 14 p. H = 14 – p. OH p. H = 14 – 1. 62 p. H = 12. 38. También puede resolverlo aplicando K w = [ H + ] [ OH -] = 1. 0 x 10 – 14, despejar [ H +] [H +] = 1 x 10 -14 / [OH] [ H + ] = 1 x 10 -14 /0. 024 = 4. 16 x 10 -13 p. H = -log [H +] p. H = – log 4. 16 x 10 -13 p. H = 12. 38 Ø Note en ambos procedimientos se llega a la misma respuesta
![Resuelve los siguientes ejercicios Calcular el p. H de las sigs, soluciones: 1) [H+] Resuelve los siguientes ejercicios Calcular el p. H de las sigs, soluciones: 1) [H+]](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-28.jpg)
Resuelve los siguientes ejercicios Calcular el p. H de las sigs, soluciones: 1) [H+] = 2. 5 x 10 -5 4) p. OH = 4. 2 2) Na. OH 0. 020 M 5) HCl 0. 50 M 3) [OH-] = 2. 0 x 10 -8 6) Na. OH 0. 28 M Calcule la [H+] y [OH-] en soluciones con : 7) p. H= 5. 5 8) p. OH = 4 9) p. H = 1. 8 28

Calculo de p. H y p. OH para ácidos y bases débiles Debido a que éstas sustancias, se ionizan en un pequeño porcentaje, sus reacciones de ionización generalmente son reversibles, pudiendo así calculár una: Ø Ka= Constante de disociación del ácido débil Ø Kb: constante de disociación de la base débil Ø Los valores de Ka y Kb varían y son diferentes para cada ácido y base débil Ø A continuación se presenta la expresión de Ka y Kb y cálculos relacionados. Ø 29

Expresión de Ka para ácidos débiles y Kb para bases débiles. Ka para un ácido débil. Ø CH 3 COOH + H 2 O * ⇋ CH 3 COO - + H + Ø Ka = [CH 3 COO - ] [ H + ] Ø [ CH 3 COOH ] Ø Kb para una base débil Ø CH 3 NH 2 + H 2 O * ⇋ CH 3 NH 3 + + OH – Kb = [ CH 3 NH 3 + ] [ OH -] [ CH 3 NH 2] Ø * Note no se toma en cuenta la [ H 2 O] ya que ésta generalmente permanece constante. En la Ka y Kb, las concentraciones de los productos van en el numerador y el reactivo en el denominador.

% de Ionización en ácidos y bases débiles, como éstos se ionizan en pequeño porcentaje, se calcula el % de ionización de la siguiente manera Ácidos : % de ionización = [H+] x 100 [ácido] Bases: % de Ionización = [OH-] x 100 [base ] 31
![Ø Calcule la [H+], el p. H y el % de ionización en una Ø Calcule la [H+], el p. H y el % de ionización en una](http://slidetodoc.com/presentation_image_h2/eb5bba05eebc6594298418a47ad49e99/image-32.jpg)
Ø Calcule la [H+], el p. H y el % de ionización en una solución 0. 3 M de ácido acético ( CH 3 COOH) con Ka=1. 8 x 10 -5. Resolución: CH 3 COOH ⇄ CH 3 COO- + H+ x x Como NO conocemos el % de ionización, le asignamos el valor de X a cada una de las especies ionizadas. Entonces Ka = [CH 3 COO-] [H+] 1. 8 x 10 -5 = (x)(x) l. 8 x 10 -5 = X 2 [CH 3 COOH ] 0. 3 X 2 = 1. 8 x 10 -5 (0. 3) X =√ 5. 4 x 10 -6 0. 3 x = 2. 32 x 10 -3 Como X = [H+] = 2. 32 x 10 -3 p. H = -log [H+] = -log 2. 32 x 10 -3 = 2. 63 p. H = 2. 63. Ahora podemos calcular el % de ionización de la sig. Manera: % ionización = [H+] x 100 [CH 3 COOH] % ionización = 2. 32 x 10 -3 x 100 = 0. 77 % 0. 3

Ejemplo de cálculo de Ka y p. H a partir de el % de ionización. Calcule Ka y el p. H de una solución 0. 25 M de ácido fórmico ( HCOOH ) si se ioniza en un 6 %. Resolución. a- Escriba reacción de ionización del ácido fórmico: Ø HCOOH ⇋ HCOO - + H+ Ø Las concentraciones son Ø [ HCOOH] = 0. 25 ( valor ya dado en el problema) [ HCOO - ] = 6 % x 0. 25 M / 100 % = 1. 5 x 10 - 2 * [H+ ] = 6 %x 0. 25 m / 100 % = 1. 5 x 10 -2 * * Ambas son iguales, se ionizan en la misma proporción. Ø Ahora Ø Ka = [ HCOO - ] [ H + ] Ka = (1. 5 x 10 -2) ( 1. 5 x 10 -2] Ø [ HCOOH ] ( 0. 25 ) Respuesta: Ka = 2. 25 x 10 – 4 = 9. 0 x 10 -4 Ka = 9. 0 x 10 -4 Ø 0. 25 Ø Ahora calcule p. H. Como [ H + ] = 1. 5 x 10 -2 Ø p. H = - log [ H + ] p. H = - log 1. 5 x 10 - 2 = 1. 82 Ø Respuesta p. H : 1. 82 Ø

Ø Calculo de p. H y % de ionización en una base débil. Para calcular p. H: En el caso de las bases al disociarse liberan radicales OH -, Por lo tanto es recomendable calcular el p. OH y luego aplicar p. H = 14 - p. OH. Ø Para el porcentaje de ionización, se calcula [ OH - ] y se procede de igual manera que con los ácidos débiles. Ø A continuación se proporcionan ejemplos de éstos casos. 34

Ø Ej: calcule el p. H de una solución de 0. 3 M de trimetilamina C 3 H 9 N si Kb = 6. 0 x 10 -5. C 3 H 9 N + H 2 O ⇋ C 3 H 9 NH + + OHØ 0. 3 x x Ø Kb = [C H NH +] [OH-] 3 9 [C 3 H 9 NH ] Ø 6 x 10 -5 = (x)(x) /0. 3 Ø X =√ 6 x 10 -5 x 0. 3 = 4. 2 x 10 -3 como X = [OH -] [ OH-] = 4. 2 x 10 -3 Ø p. OH = –log 4. 2 x 10 -3 = 2. 38 35

cont ejercicio Entonces p. H = 14 -p. OH p. H = 142. 38 =11. 62 Respuesta : p. H = 11. 62 % de ionización = [ OH - ] x 100 [ C 9 N 3 H] % ionización = 4. 2 x 10 -3 x 100 = 1. 4 % 0. 3 36

EJERCICIOS 1)Para una solución de ácido acético (HC 2 H 3 O 2) 0. 10 M calcular : El % de ionización del ácido acético si la constante de ionización (Ka) del ácido es 1. 8 x 10 -5. HC 2 H 3 O 2 ⇄ H+ + C 2 H 3 O 2 - 37

2) Calcule el p. H y % de ionización de una solución de anilina 0. 05 M, Kb = 4. 5 x 10 -10. C 6 H 5 NH 2 ⇄ C 6 H 5 NH 3+ + OH- 38

3) ¿Cuál es la Ka y el p. H de una solución de Acido fluorhídrico (HF) 0. 3 M ionizada un 3. 2%? HF ⇄ H+ + F- 39

Comente “quimica verde pág. 299 “Lluvia ácida” y química y salud pág. 302. “Antiácidos”.
- Slides: 40