Acidobazick reakce I 2011 E T Kyseliny a

Acidobazické reakce I 2011 E. T.

Kyseliny a zásady Výpočty p. H silných a slabých kyselin a zásad

Pojem kyseliny a zásady (podle Brønsteda) Kyselina: HA látka, která odštěpuje H+ + kyselina Akonjugovaná báze Zásada (báze): B + H+ báze látka, která váže H+ BH+ konjugovaná kyselina
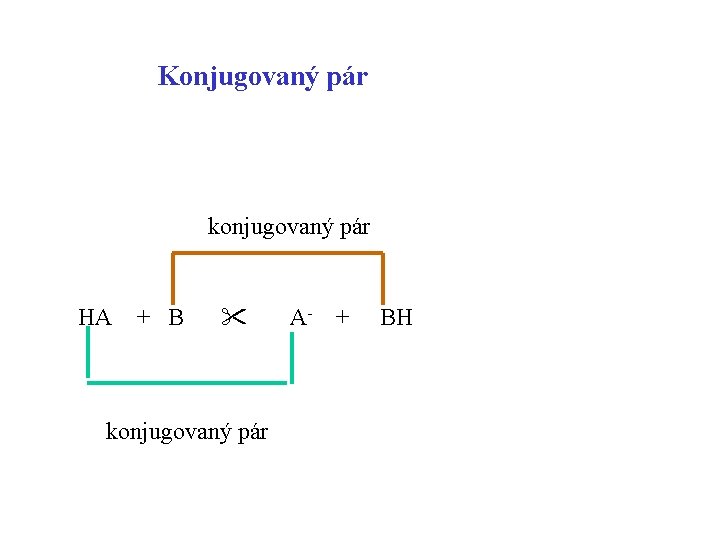
Konjugovaný pár konjugovaný pár HA + B konjugovaný pár A- + BH

Výpočty p. H silných kyselin a zásad Silné kyseliny a silné hydroxidy jsou silnými elektrolyty. Ve zjednodušených výpočtech předpokládáme, že ve vodě zcela disociují HA + H 2 O H 3 O+ + AU jednosytné kyseliny je pak koncentrace H+ stejná jako celková koncentrace c. HA a p. H lze počítat jako p. H = - log H 3 O+ = - log c. HA p. OH = - log OH- = -log c. OH

Vypočtěte p. H roztoku kyseliny dusičné o koncentraci 0, 01 mol/l. Řešení: p. H = - log H 3 O+ = - log c. HA = - log 0, 01 = 2 Další příklady viz podklady pro práci v semináři

Disociace slabých kyselin a zásad Slabá jednosytná kyselina HA + H 2 O H 3 O+ + A- Slabá jednosytná zásada B + H 2 O BH+ + OH- rovnovážná konstanta disociační konstanta (protonizační konstanta)
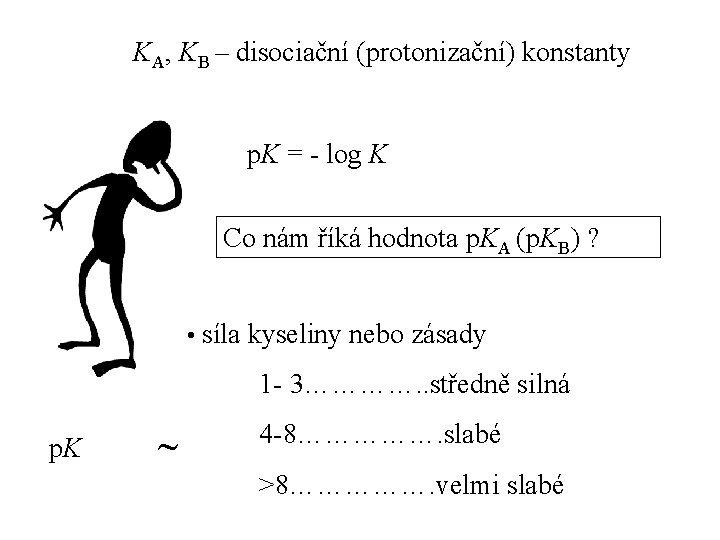
KA, KB – disociační (protonizační) konstanty p. K = - log K Co nám říká hodnota p. KA (p. KB) ? • síla kyseliny nebo zásady 1 - 3…………. . středně silná p. K 4 -8……………. slabé >8……………. velmi slabé
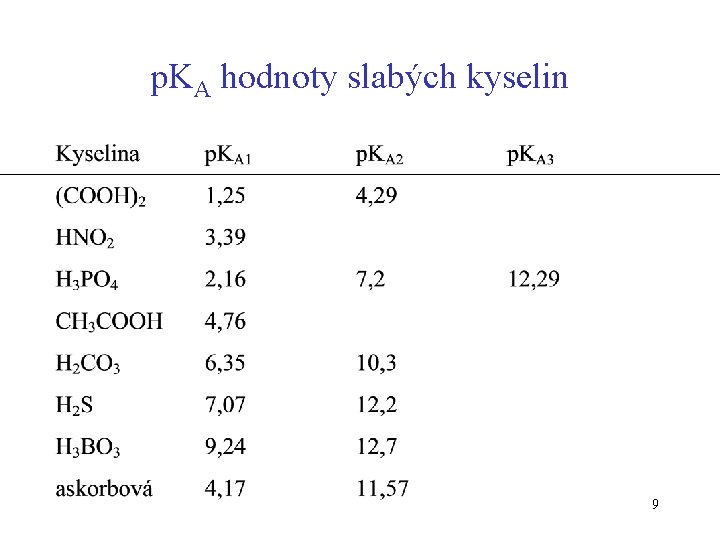
p. KA hodnoty slabých kyselin 9
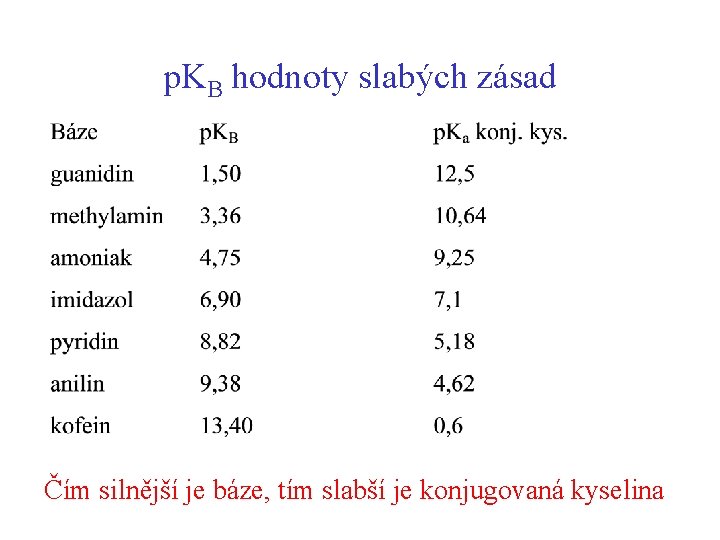
p. KB hodnoty slabých zásad Čím silnější je báze, tím slabší je konjugovaná kyselina

Vztah KA a KB ( p. KA a p. KB) KA. KB = Kv = 1. 10 -14 p. KA+ p. KB = 14
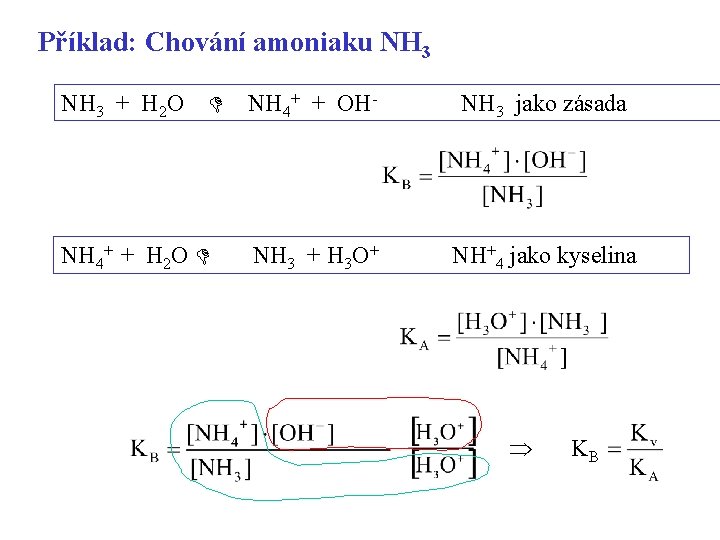
Příklad: Chování amoniaku NH 3 + H 2 O NH 4+ + H 2 O NH 4+ + OH- NH 3 jako zásada NH 3 + H 3 O+ NH+4 jako kyselina KB

Zjednodušené výpočty p. H slabých kyselin a zásad Slabá jednosytná kyselina o celkové koncentraci c. HA HA + H 2 O H 3 O + + A -

Pro úpravu vztahu zavedeme 2 zjednodušení: 1. Koncentrace disociovaných molekul u slabé kyseliny je velmi malá ve srovnání s nedisociovanými: c. HA>> H+ [HA] = (c. HA – [H+]) [HA] c. HA 2. Z jedné molekuly vzniká disociací stejný počet kationtů a aniontů: [H+] = [A-]
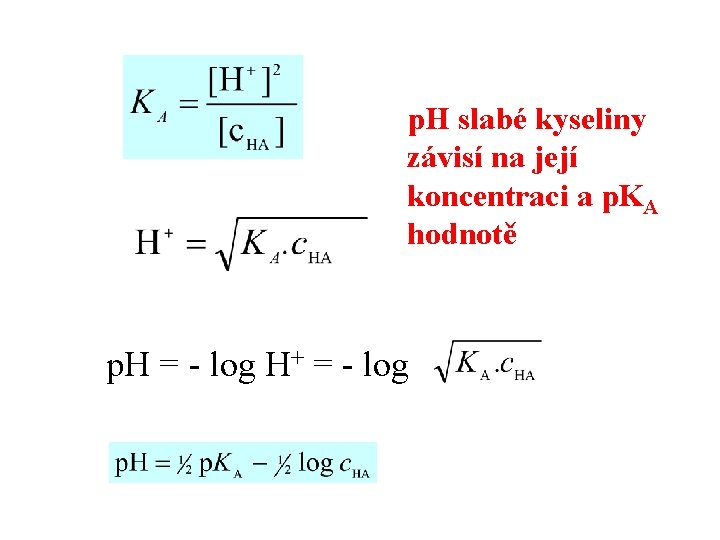
p. H slabé kyseliny závisí na její koncentraci a p. KA hodnotě p. H = - log H+ = - log

Porovnání p. H silné a slabé kyseliny o stejné koncentraci HCl c=0, 1 mol/l p. H = -log c. HA = - log 0, 1 = 1 CH 3 COOH c=0, 1 mol/l p. H = 2, 35 + 0, 5 = 2, 85 p. KA = 4, 7

Slabá jednosytná báze: B + H 2 O BH+ + OH-
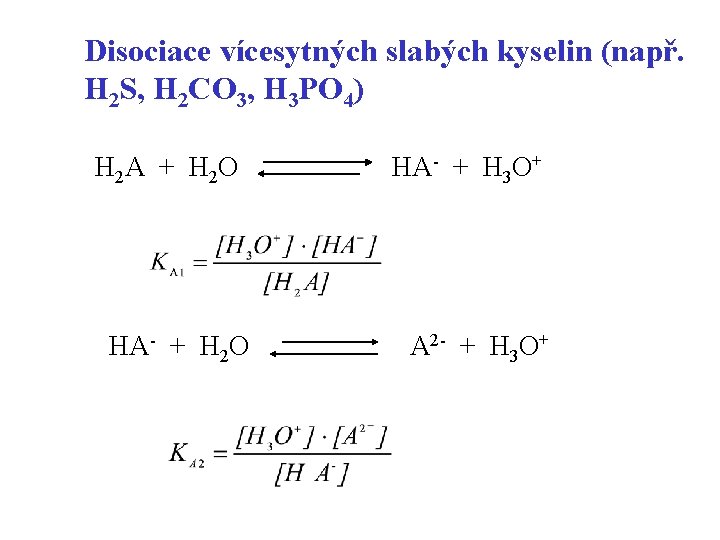
Disociace vícesytných slabých kyselin (např. H 2 S, H 2 CO 3, H 3 PO 4) H 2 A + H 2 O HA- + H 3 O+ A 2 - + H 3 O+

Hodnoty p. KA se obvykle výrazně liší Pokud koncentrace kyseliny není příliš nízká a rozdíl v p. K je větší jak 3, ionizaci do dalšího stupně lze zanedbat a uvažovat, že ve vodném roztoku převažují ionty z disociace do 1. stupně (neplatí tedy pro kys. sírovou) 19

Hydrolýza solí

Hydrolýza solí reakce aniontů slabých kyselin nebo kationtů slabých zásad s vodou ovlivňuje p. H roztoku soli

Soli vznikají reakcí mezi kyselinou a zásadou – neutralizací. Při neutralizační reakci není vždy výsledné p. H neutrální. Všechny soli disociují ve vodném roztoku, ale jen některé hydrolyzují Hydrolyzují pouze ty soli, v nichž je obsažen kation slabé zásady nebo anion slabé kyseliny

Rozdíly v reaktivitě iontů („silné“ a „slabé“ ionty) Cl- CH 3 COOH 2 O CH 3 COOH + OH- Cl- je divácký (spectator) anion, nereaguje s vodou CH 3 COO- je anion slabé kyseliny, má tendenci reagovat s vodou a tvořit kyselinu octovou. Reakcí s vodou se vytvoří takové množství CH 3 COOH, aby byla zachována rovnováha daná disociační konstantou
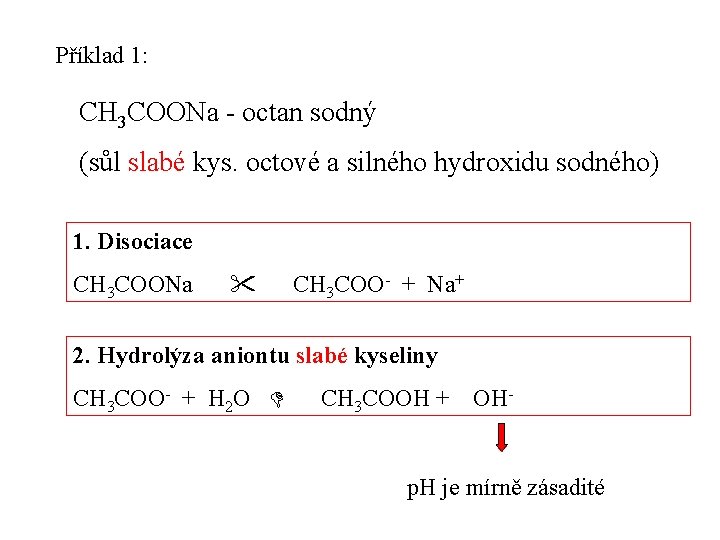
Příklad 1: CH 3 COONa - octan sodný (sůl slabé kys. octové a silného hydroxidu sodného) 1. Disociace CH 3 COONa CH 3 COO- + Na+ 2. Hydrolýza aniontu slabé kyseliny CH 3 COO- + H 2 O CH 3 COOH + OH- p. H je mírně zásadité

Příklad 2: NH 4 Cl - chlorid amonný (sůl slabé báze amoniaku a silné kyseliny chlorovodíkové, také např. pyridinium chlorid, pyrrolidinium bromid atd. ) 1. Disociace NH 4 Cl NH 4+ + Cl- 2. Hydrolýza kationtu slabé báze NH 4+ + H 2 O H 3 O+ + NH 3 p. H je mírně kyselé

Příklad 3: Cu. Cl 2 - chlorid měďnatý (sůl kationtu Cu 2+ odvozeného od slabého hydroxidu a silné kyseliny chlorovodíkové) 1. Disociace Cu. Cl 2 Cu 2+ + 2 Cl- 2. Vznik aquakomplexu Cu 2+ + 6 H 2 O [Cu(H 2 O)6]2+ 3. Hydrolýza komplexního aquakationtu [Cu(H 2 O)6 ]2+ + H 2 O [Cu(H 2 O)5 OH]+ + H 3 O+ p. H je mírně kyselé
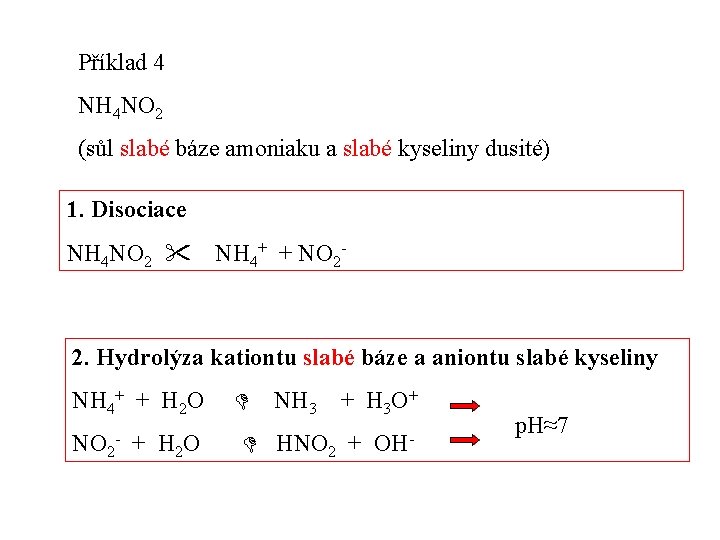
Příklad 4 NH 4 NO 2 (sůl slabé báze amoniaku a slabé kyseliny dusité) 1. Disociace NH 4 NO 2 NH 4+ + NO 2 - 2. Hydrolýza kationtu slabé báze a aniontu slabé kyseliny NH 4+ + H 2 O NO 2 - + H 2 O NH 3 + H 3 O+ HNO 2 + OH- p. H≈7
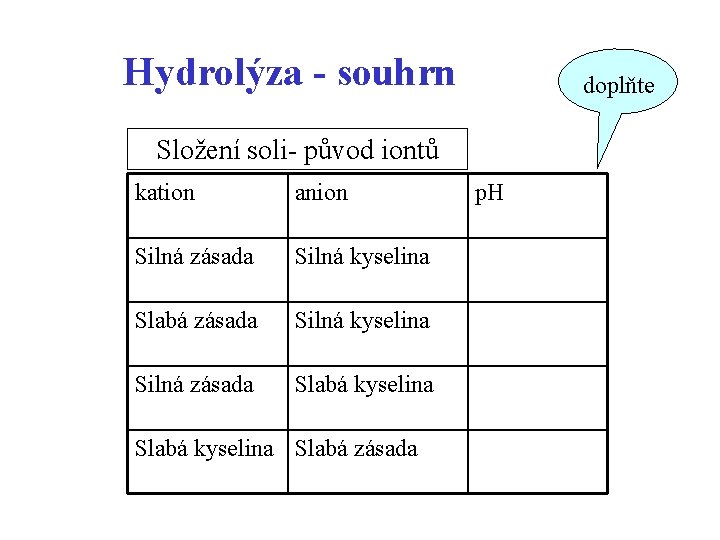
Hydrolýza - souhrn doplňte Složení soli- původ iontů kation anion Silná zásada Silná kyselina Slabá zásada Silná kyselina Silná zásada Slabá kyselina Slabá zásada p. H
- Slides: 28