Acidobazick reakce CH4 Chemick reakce a dje DUM


Acidobazické reakce CH-4 Chemické reakce a děje, DUM č. 9 první ročník čtyřletého studia Mgr. Radovan Sloup Gymnázium Sušice 2 Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II

opakování: acidobazické reakce chemické reakce: podle typu přenášených částic • acidobazické reakce (protolytické) – dochází k + přenosu kationtu H (proton) • redoxní (oxidačně - redukční reakce) – dochází k přenosu elektronů e • komplexotvorné – dochází k přenosu skupin (iontů) za vzniku koordinačně - kovalentní vazby (donor - akceptorová vazba)
acidobazické reakce (protolytické) V těchto reakcích dochází k přesunu vodíkového kationtu H+, v podstatě protonu – protolytické, mezi kyselinou a zásadou – acidobazické. 1. neutralizace: reakce kyseliny se zásadou, vzniká sůl 2. kyseliny a voda – acidobazické indikátory Na. OH +HCl → Na. Cl + H 2 O = přenos H+

acidobazické reakce teorie kyselin a zásad 1. Arrheniova teorie: kyselina je látka schopná ve vodném roztoku odštěpit vodíkový kation H+ HCl → H+ + Clzásada je látka schopná ve vodném roztoku odštěpit hydroxidový anion OH- Na. OH → Na+ + OH-

acidobazické reakce teorie kyselin a zásad 2. Brönstedtova - Lowryho teorie: kyselina je částice (molekula, iont) schopná odštěpit proton (vodíkový kation H+) HCl → H+ + Clzásada je částice (molekula, iont) schopná vázat proton (vodíkový kation H+) acidobazické reakce jsou reakce mezi kyselinou a zásadou HCl + H 2 O → Cl- + H 3 O+
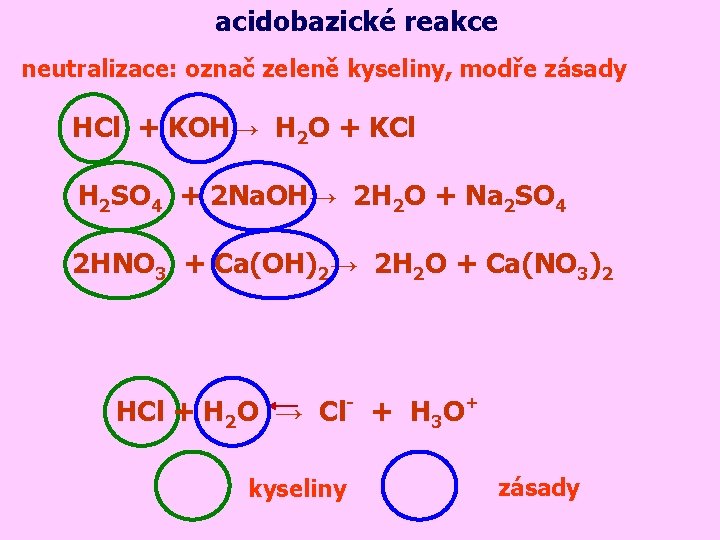
acidobazické reakce neutralizace: označ zeleně kyseliny, modře zásady HCl + KOH→ H 2 O + KCl H 2 SO 4 + 2 Na. OH→ 2 H 2 O + Na 2 SO 4 2 HNO 3 + Ca(OH)2→ 2 H 2 O + Ca(NO 3)2 HCl + H 2 O → Cl- + H 3 O+ kyseliny zásady

doplň reakce podle předpokládaného průběhu: HNO 3 + H 2 O → 2 HCl + Ca(OH)2 → NO-3 + H 3 O+ Ca. Cl 2 + 2 H 2 O Al(OH)3 + 3 HCl → Al. Cl 3 + 3 H 2 O Mg(OH)2 +2 HCl → Mg. Cl 2 + 2 H 2 O

zařaď reakce podle tepelného zabarvení: 2 K + 2 H 2 O → Ca. CO 3 → 2 Al + 6 HCl → 2 KOH + H 2 exotermní Ca. O + CO 2 endotermní 2 Al. Cl 3 + 3 H 2 exotermní Mg(OH)2 +2 HCl → Mg. Cl 2 + 2 H 2 O exotermní O 2 + 2 C → 2 CO 2 exotermní

ACIDOBAZICKÉ REAKCE Vytvořeno v rámci projektu Gymnázium Sušice - Brána vzdělávání II Autor: Mgr. Radovan Sloup, Gymnázium Sušice Předmět: Chemie (Chemické reakce a děje) Třída: první ročník čtyřletého studia Označení: VY_32_INOVACE_Ch-4_09 Datum vytvoření: červen 2013 Anotace a metodické poznámky Acidobazické reakce je možné definovat jako reakci kyseliny se zásadou, jako protolytickou reakci, jako neutralizaci. Neutralizace je možné demonstrovat acidobazickým indikátorem. V průběhu prezentace je popsán průběh protolytických reakcí. Jsou zmíněny teorie kyselin a zásad a rozdíly v chápání látek. Během prezentace se objevuje několik cvičení k procvičení tématu. Použité materiály: Honza, J. ; Mareček, A. ; Chemie pro čtyřletá gymnázia (1. díl). Brno: Da. Ta. Print, 1995; ISBN 80 -900066 -6 -3 Vše je vytvořeno pomocí nástrojů Power Point 2003 Materiály jsou určeny pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízení. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 10