Acido Il ruolo del rene nella regolazione dellequilibrio

Acido Il ruolo del rene nella regolazione dell’equilibrio Base acido-base

La regolazione della concentrazione degli ioni idrogeno è simile alla regolazione di qualunque altro ione, dovendo esistere un equilibrio fra intake ed escrezione. Benché il rene rivesta il ruolo fondamentale nel controllo di questo equilibrio, esistono molti sistemi che esercitano uno stretto controllo sul valore del p. H.

* Tutti gli enzimi hanno un p. H ideale attorno al quale lavorano. Questo perché la carica sui vari La concentrazione degli idrogenioni è strettamente aa può cambiare e questo a sua volta si riflette in controllata perché tutti i sistemi enzimatici hanno un una variazione dei legami all’interno della meccanismo di funzionamento che dipende al valore molecola conseguente variazione della + è molto bassa del p. H*. La concentrazione degli H struttura terziaria della proteina. Questo può portare ad una denaturazione dell’enzima che non-5 rispetto a quella di altri ioni ed è circa 4 · 10 riesce più a catalizzare le reazioni m. Eq/l.

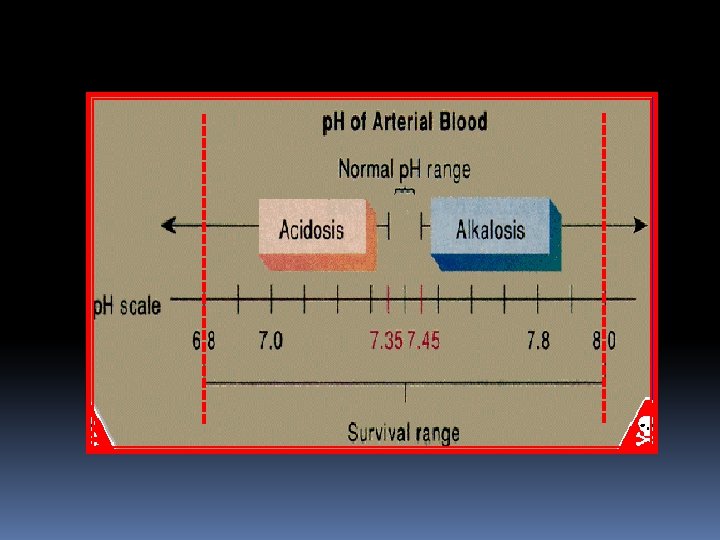
Considerata la bassa concentrazione di ioni H+ nel sangue è meglio esprimere questo valore in termini logaritmici come: p. H= log 1/[H+] = -log [H+] da cui si ricava che il valore di p. H è inversamente proporzionale alla concentrazione degli idrogenioni. Il normale valore del p. H arterioso è 7. 40, mentre quello venoso è circa 7. 35 per la presenza di maggiori quantità di CO 2 rilasciata dai tessuti.

Questi valori devono essere assolutamente costanti con possibilità di minime variazioni (7. 35 ≤ p. H ≤ 7. 42). Il p. H intracellulare è normalmente più basso perché il metabolismo cellulare produce acidi. Il p. H delle urine può variare fra 4. 5 e 8. 0 a seconda delle necessità. Il p. H più basso nell’organismo si ritrova nello stomaco durante la digestione, dove si arriva fino a 0. 8.

Definizione di acido e base Acido è una sostanza che in soluzione acquosa libera ioni idrogeno H+ oppure secondo un’altra definizione una sostanza che è capace di donare protoni. Ad esempio HCl in acqua si ionizza in ioni H+ e Cl-. Similmente H 2 CO 3 si dissocia formando H+ e HCO 3 -

Base è una sostanza che in soluzione acquosa libera ioni ossidrilici OH- oppure è uno ione o una molecola oppure è che può accettare ioni idrogeno. Per esempio HCO 3 - è una base perché accetta ioni H+ per formare acido carbonico. In genere le proteine funzionano come basi perché gli aa carichi negativamente tendono ad attrarre ioni H+. L’emoglobina ed altre proteine plasmatiche sono fra le basi più importanti dell’organismo.

Si definisce acido forte un acido che rapidamente e totalmente si dissocia per formare H+ e X- (HCl), mentre un acido debole è un acido che si dissocia lentamente e non completamente (H 2 CO 3). Similmente si definisce base forte una base che accetta ioni H+ facilmente (OH- che lega ioni H+ per formare acqua). Una base debole accetta ioni H+ più difficilmente (HCO 3 -).

The degree of dissociation is described by the dissociation constant of the acid which equals the product of the concentration of the dissociated forms of the acid divided by the concentration of the free acid. The higher the dissociation constant the stronger the acid.

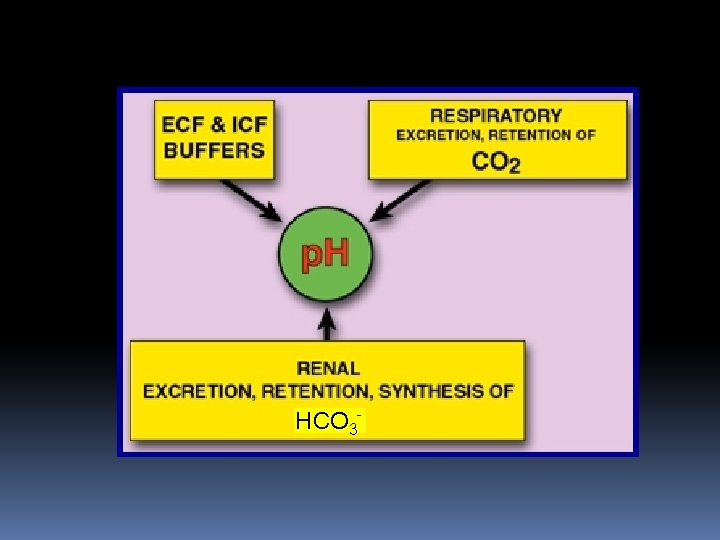
Sistemi di difesa dell’organismo v La prima linea di difesa è rappresentata dai sistemi tampone plasmatici e intracellulari. Tutti questi sistemi contribuiscono sulla base del loro valore di p. K e della loro concentrazione. Particolarmente importante è il sistema CO 2 -HCO 3 - che è il principale tampone extracellulare. La sua importanza deriva dal fatto che le due componenti del sistema possono essere regolate in maniera indipendente.

v Il secondo meccanismo è costituito dal sistema repiratorio che regola Pco 2 plasmatica in risposta a variazioni di p. H, controllando escrezione o ritenzione della CO 2 prodotta metabolicamente

v Il terzo meccanismo è rappresentato dal sistema renale che gioca un doppio ruolo: i. regola l’escrezione o la ritenzione di HCO 3 - (la componente basica del sistema tampone CO 2 -HCO 3 -) ii. regola la formazione ex-novo di HCO 3 - distrutto nel buffer di acidi forti prodotti metabolicamente. Per ogni HCO 3 - riassorbito o rigenerato un H+ è secreto nel fluido tubulare
HCO 3 -

I principali meccanismi coinvolti nel controllo acidobase a livello renale sono: • Riassorbimento e sintesi ex-novo di HCO 3 • Secrezione di H+ nel lume tubulare • Produzione e trasporto di ioni ammonio • Buffer urinari che reagiscono con i protoni secreti HCO 3 -/H 2 CO 3, HPO 4=/H 2 PO 4 - e NH 3/NH 4+

più abbondante più adatto come p. K fondamentali all’interno della cellula

Quando c’è una variazione nella concentrazione degli idrogenioni, i sistemi buffer reagiscono entro pochi secondi per minimizzare le variazioni di p. H. La seconda linea di difesa è rappresentata dal sistema respiratorio che elimina CO 2 dall’organismo. Questi due sistemi controllano il valore di p. H finché non interviene il sistema renale che elimina l’eccesso di acido o base dall’organismo. Questo sistema, benché sia il più efficace, è però anche il più lento a rispondere.

Un sistema tampone è formato da un acido debole e dal suo sale. La coppia HA e CA, dove HA è l’acido debole, C è un catione e A l’anione, forma un sistema tampone. In soluzione l’interazione fra queste forme può essere così rappresentata.

Se la concentrazione di idrogenioni aumenta, la reazione si sposta a sinistra, mentre a destra se la concentrazione di idrogenioni diminuisce, in modo da minimizzare le variazioni di H+. Questi sistemi buffer sono fondamentali per tamponare l’eccesso di H+ che deriva dall’ingestione esterna e dalla produzione endogena.

Va detto che i sistemi tampone possono arginare le variazioni di p. H ma hanno una capacità limitata e quindi non possono da soli invertire la tendenza alla variazione

Sistema HCO 3 – H 2 CO 3 Il sistema buffer più diffuso è il sistema bicarbonato che prevede: i. un acido debole H 2 CO 3 ii. un sale di bicarbonato Na. HCO 3 L’acido debole viene formato nell’organismo dalla reazione di idratazione della CO 2 + H 2 O ↔ H 2 CO 3 catalizzata dall’enzima anidrasi carbonica che è abbondante nelle pareti degli alveoli polmonari e nelle cellule dell’epitelio tubulare.

Il sistema di buffer completo è dato da: CO 2 + H 2 O ↔ H 2 CO 3 H+ + HCO 3 AC eccesso di H+ Quando si aggiunge un acido forte come HCl, l’aumento degli idrogenioni sposta la reazione verso sinistra formando acido carbonico che a sua volta forma CO 2 e acqua. L’eccesso di anidride carbonica stimola l’attività respiratoria per eliminarla (iperventilazione). Quando si aggiunge una base forte come Na. OH questa si combina con acido carbonico per formare ione bicarbonato.

In questo modo una base forte (Na. OH) è sostituita da una base debole (Na. HCO 3). L’acido carbonico diminuisce nel processo di titolazione e quindi la CO 2 a sua volta diminuisce per idratarsi e formare nuovo H 2 CO 3. La respirazione viene rallentata (ipoventilazione) e così l’eliminazione di CO 2.
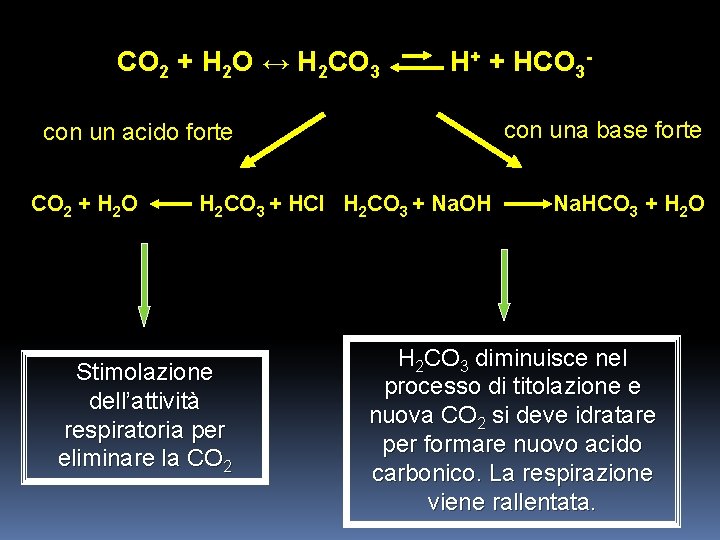
CO 2 + H 2 O ↔ H 2 CO 3 H+ + HCO 3 con una base forte con un acido forte CO 2 + H 2 O H 2 CO 3 + HCl H 2 CO 3 + Na. OH Stimolazione dell’attività respiratoria per eliminare la CO 2 Na. HCO 3 + H 2 O H 2 CO 3 diminuisce nel processo di titolazione e nuova CO 2 si deve idratare per formare nuovo acido carbonico. La respirazione viene rallentata.
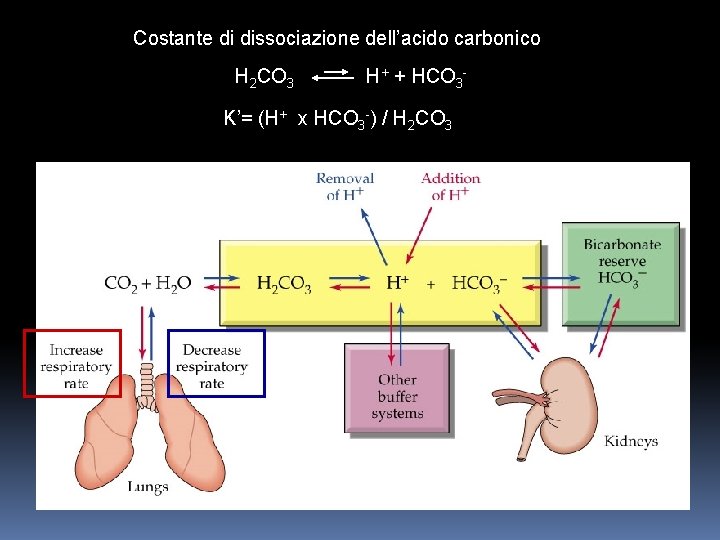
Costante di dissociazione dell’acido carbonico H 2 CO 3 H+ + HCO 3 K’= (H+ x HCO 3 -) / H 2 CO 3


H+ = K x (0. 03 x PCO 2 / HCO 3 -) L’equazione sotto riportata rappresenta l’equazione di Handerson-Hasselbalch per il sistema bicarbonato. p. K vale circa 6. 1 e 0. 03 · Pa. CO 2 sta ad indicare che 0. 03 m. M di H 2 CO 3 è presente nel sangue per ogni mm. Hg di PCO 2

La concentrazione (riassorbimento e produzione exnovo) del bicarbonato è regolata principalmente dal sistema renale, mentre la pressione parziale della CO 2 nel fluido extracellulare è controllata dalla rate respiratoria (iper o ipoventilazione). Questo tampone ha quindi il vantaggio di essere sotto il controllo di due sistemi che giocano nella regolazione del p. H.

► Quando un’alterazione dell’equilibrio acido-base deriva da variazioni del bicarbonato si parla di disordini acido-base metabolici ► Quando l’alterazione deriva da variazioni della PCO 2 si parla di disordini acido-base di tipo respiratorio
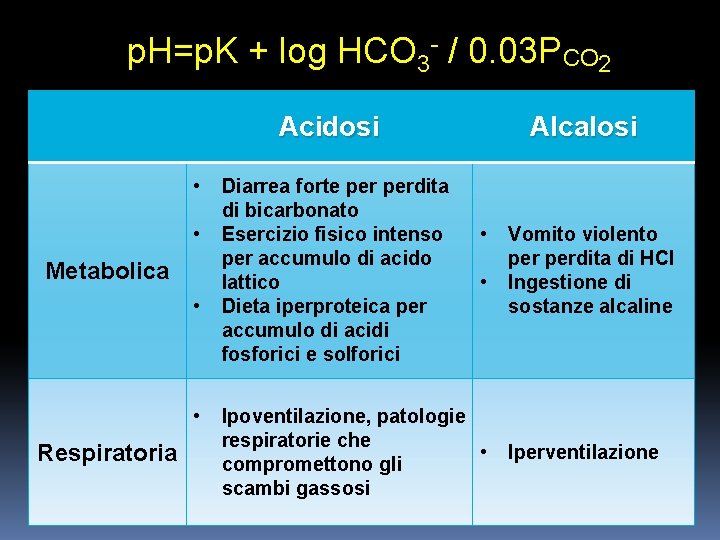
p. H=p. K + log HCO 3 - / 0. 03 PCO 2 Acidosi • • Metabolica • • Respiratoria Diarrea forte perdita di bicarbonato Esercizio fisico intenso per accumulo di acido lattico Dieta iperproteica per accumulo di acidi fosforici e solforici Alcalosi • • Ipoventilazione, patologie respiratorie che • compromettono gli scambi gassosi Vomito violento perdita di HCl Ingestione di sostanze alcaline Iperventilazione
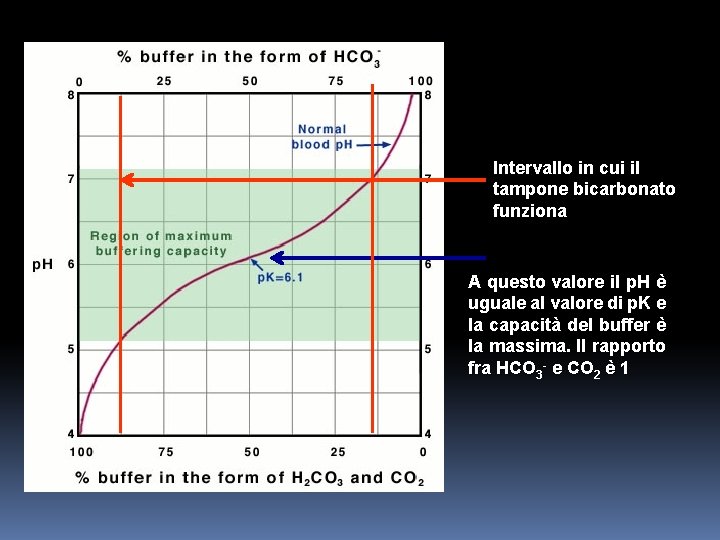
Intervallo in cui il tampone bicarbonato funziona A questo valore il p. H è uguale al valore di p. K e la capacità del buffer è la massima. Il rapporto fra HCO 3 - e CO 2 è 1


Sistema fosfato L’acido fosforico si trasforma rapidamente in diidrogeno fosfato, H 2 PO 4 - è un buffer eccellente poiché può tanto riprendere un H+ formando acido fosforico, quanto cedere un altro idrogeno a formare HPO 42 -. In condizioni estreme può infine cedere l’ultimo idrogeno.

Se H 2 PO 4 - è in una soluzione acida, la reazione si sposta a sinistra a formare H 3 PO 4, mentre se è in una soluzione basica la reazione procede verso destra. Quindi questo sistema può accettare o donare ioni H+ a seconda della soluzione in cui si trova.

Il tampone fosfato è meno importante del sistema bicarbonato perché nei fluidi extracellulari è molto meno concentrato. Risulta invece un sistema importante a livello renale perché il fosfato si concentra nel tubulo renale ed inoltre il p. H nel tubulo è inferiore a 7. 4 portandosi quindi molto vicino al p. K del sistema fosfato che quindi ha un ottimo potere tampone. Il sistema fosfato è un ottimo tampone intracellulare dove risulta molto concentrato ed inoltre anche qui il p. H intracellulare è molto vicino al p. K del sistema rendendolo quindi molto efficace.

Effetto tampone delle proteine Gli aa possono accettare o donare ioni idrogeno rendendoli buffer eccellenti. Ogni proteina ha tipicamente centinaia di aa, cosicché le proteine sono ottimi buffer. Si trovano nel sangue e all’interno delle cellule. Al normale p. H del sangue gli aa sono in genere carichi negativamente e quindi funzionano bene come accettori di protoni, cioè come basi.
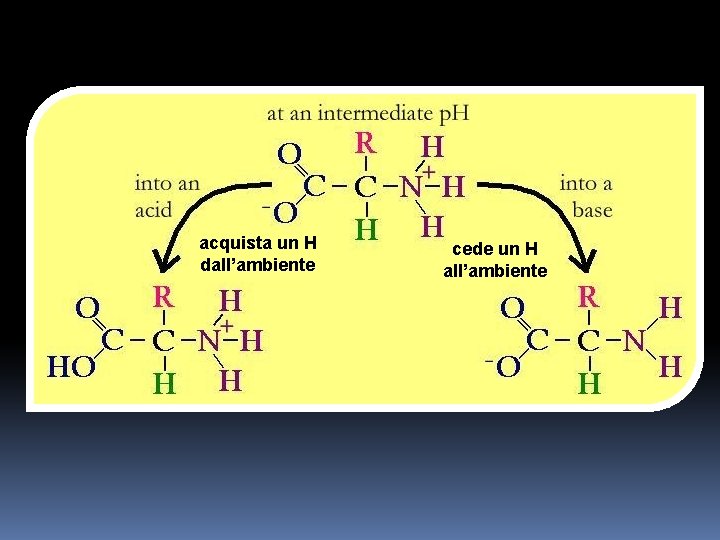
acquista un H dall’ambiente cede un H all’ambiente

N. B. : Va detto che l’organismo è orientato principalmente all’eliminazione di acidi, che derivano tanto dal metabolismo corporeo (volatili e fissi) quanto dall’introduzione esterna. Esistono poche fonti significative di alcali negli alimenti e nel metabolismo

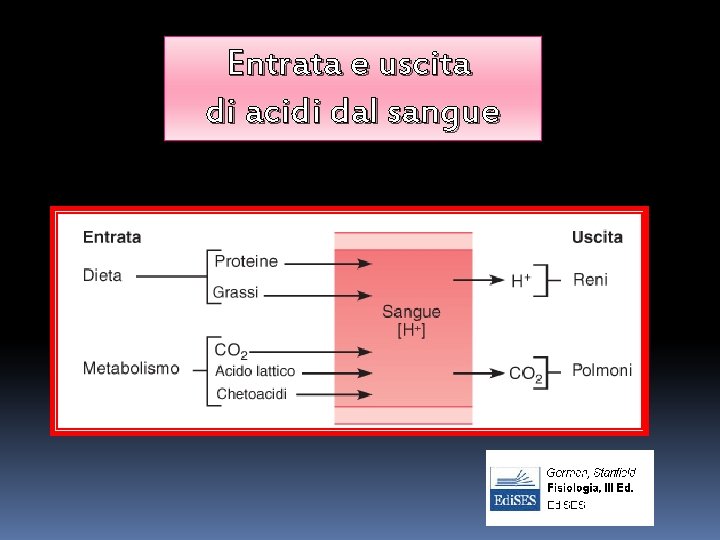
Entrata e uscita di acidi dal sangue

CO 2 è il prodotto finale del metabolismo cellulare ossidativo: C 6 H 12 O 6 + 6 O 2 -----> 6 CO 2 + 6 H 2 O + 38 ATP È una molecola piccola e neutra che diffonde attraverso la membrana cellulare e forma H 2 CO 3 per idratazione catalizzata dall’anidrasi carbonica (AC), nei globuli rossi e nelle cellule dell’epitelio tubulare. È detta acido volatile perché è un gas e come tale è rapidamente eliminata a livello polmonare.
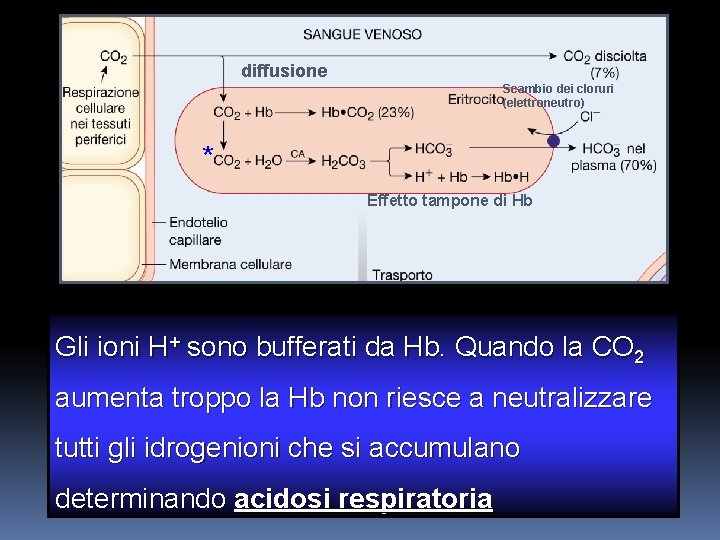
diffusione Scambio dei cloruri (elettroneutro) * Effetto tampone di Hb Gli ioni H+ sono bufferati da Hb. Quando la CO 2 aumenta troppo la Hb non riesce a neutralizzare tutti gli idrogenioni che si accumulano determinando acidosi respiratoria

Acidi non-volatili Gli acidi non-volatili (detti anche fissi o metabolici) sono acidi prodotti da fonti differenti dalla CO 2. Derivano dal catabolismo incompleto di carboidrati, grassi e proteine. Di fatto l’unico acido volatile è proprio la CO 2. Gli acidi fissi più comuni sono acido fosforico, acido solforico, acido lattico, acido acetoacetico e beta-idrossibutirrico. Gli acidi non volatili sono esceti dai reni fatta eccezione per l’acido lattico che viene rimetabolizzato dall’organismo e non escreto. Gli acidi fissi ammontano a circa 70 -80 m. Eq/die.

In the ECF most of these acids are buffered by reaction of the H+ with HCO 3 - forming H 2 CO 3 which dissociates into CO 2 and H 2 O. The CO 2 can be excreted by the lung and the H 2 O by the kidney leaving the sodium salt of the acid in the ECF. This reaction minimizes the change in p. H and in the process decreases the amount of HCO 3 - available for further buffering of nonvolatile acids. The kidney is responsible for elimination of the acid anions produced in this way while conserving the Na+ associated with them and regenerating the HCO 3 - lost in the buffering reaction.
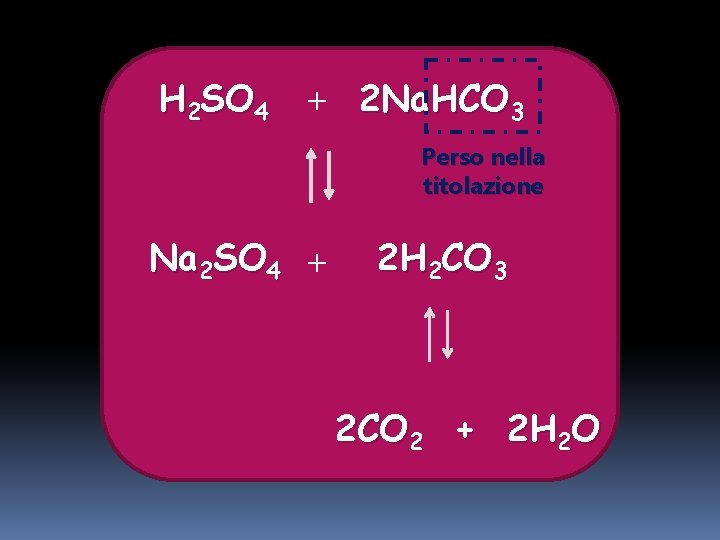
H 2 SO 4 + 2 Na. HCO 3 Perso nella titolazione Na 2 SO 4 + 2 H 2 CO 3 2 CO 2 + 2 H 2 O

In totale per recuperare il bicarbonato filtrato (4320 m. Eq/die) e per ripristinare quello perso nella titolazione di acidi fissi (80 m. Eq/die) devono essere secreti idrogenioni in questa misura: 4320 + 80 = 4400 m. Eq H+ secreti dal tubulo


I reni regolano il p. H arterioso eliminando urine acide o basiche, cioè regolando l’escrezione renale di idrogeno e bicarbonato. L’eliminazione di urina acida consente di eliminare l’eccesso di acido, mentre l’escrezione di urine basiche rimuove basi dai fluidi extracellulari. Il bicarbonato è filtrato a livello glomerulare e i protoni sono secreti a livello tubulare e quindi rimossi dal sangue. Se secrezione H+ > filtrazione HCO 3 - urine acide Se secrezione H+ < filtrazione HCO 3 - urine basiche

Se la concentrazione di ioni idrogeno nel sangue cresce, i reni ne aumentano la secrezione, aumentano il riassorbimento di bicarbonato e la sintesi di nuovo bicarbonato. Se la concentrazione di ioni idrogeno nel sangue diminuisce, i reni riducono la secrezione di ioni idrogeno e il riassorbimento di bicarbonato
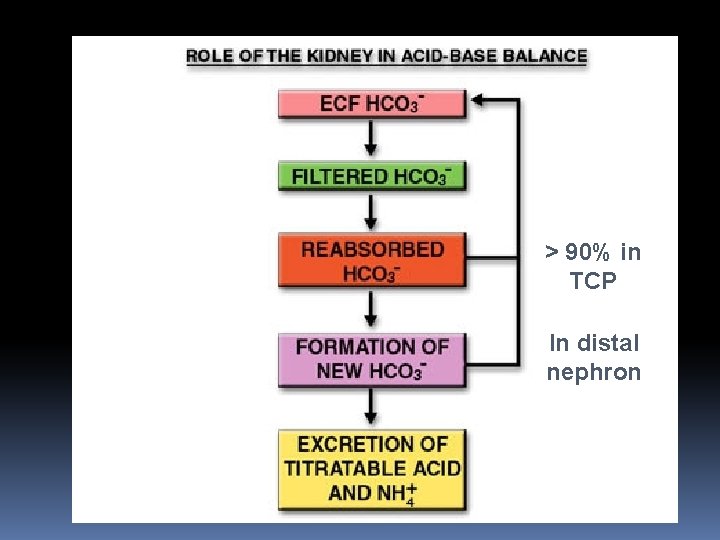
> 90% in TCP In distal nephron

Quindi: i reni regolano il p. H attraverso tre meccanismi: riassorbimento del bicarbonato filtrato secrezione di ioni idrogeno produzione di nuovi ioni bicarbonato

In linea di massima per semplicità possiamo dire che il riassorbimento di bicarbonato filtrato avviene praticamente del tutto in TCP (90 -95%), mentre il nefrone distale è coinvolto nella produzione di NUOVO bicarbonato per ricostituire quello perso nella titolazione di acidi metabolici

Secrezione di ioni H+ e riassorbimento di bicarbonato nel tubulo renale Secrezione di idrogenioni e riassorbimento di bicarbonato avvengono in ogni parte del nefrone fatta eccezione per TDs e TAs dell’ansa. Per poter riassorbire un bicarbonato deve essere secreto un idrogenione. La secrezione di ioni H+ avviene con modalità differenti nelle varie parti del nefrone.

Tubulo contorto prossimale A questo livello troviamo un contro-trasporto Na-H grazie al gradiente stabilito dalla Na-K ATPasi basolaterale. In questo modo sono secreti giornalmente 3900 m. Eq di H+. Il p. H non varia perché per ogni idrogenione secreto viene riassorbito il bicarbonato. Il fluido tubulare diviene molto acido solo nel nefrone distale.
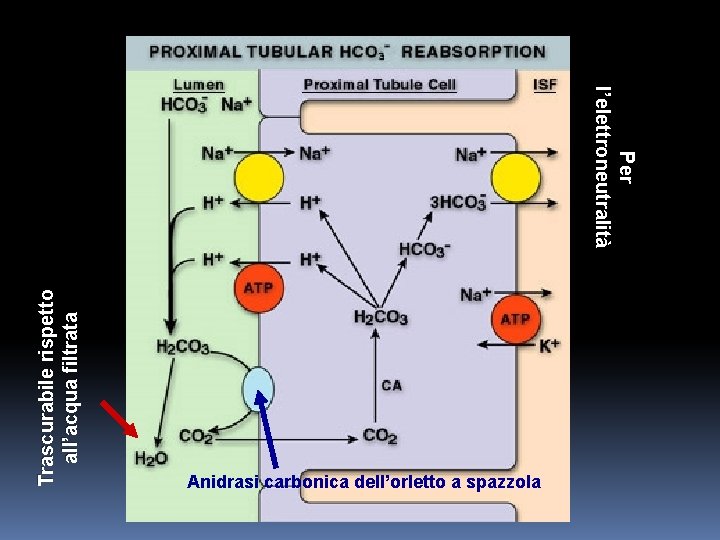
Trascurabile rispetto all’acqua filtrata Per l’elettroneutralità Anidrasi carbonica dell’orletto a spazzola

i. CO 2 nella cellula viene idratata in presenza dell’anidrasi carbonica ii. H 2 CO 3 si dissocia in H+ e HCO 3 - iii. H+ in contro-trasporto con Na+ è secreto nel lume dove si combina con HCO 3 - filtrato per dare acido carbonico che si dissocia in acqua e anidride carbonica iv. HCO 3 - è riassorbito nel sangue

Va notato che l’antiporto Na-H è un trasporto che lavora ad alta velocità ma con un gradiente basso. Questo significa che appena il bicarbonato è stato riassorbito e il lume inizia ad acidificare, il trasportatore si blocca.
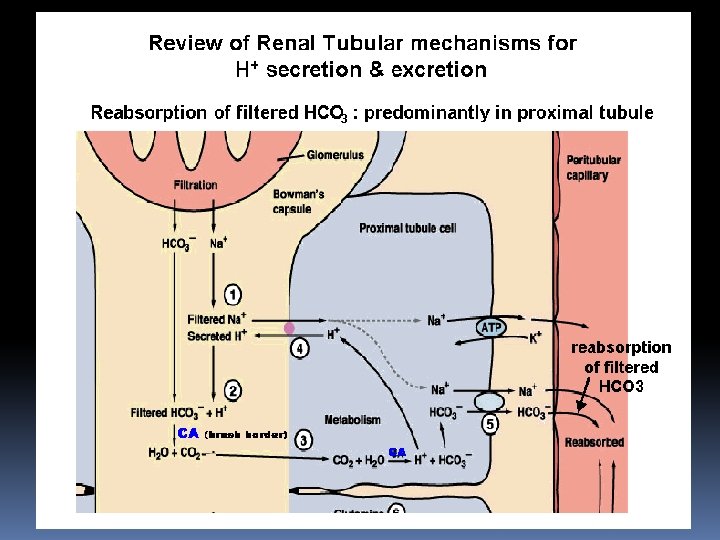

I protoni, combinandosi con il bicarbonato filtrato mantengono il gradiente necessario alla secrezione di protoni nel lume, fino a quando il bicarbonato viene riassorbito. Ogni volta che si forma uno ione idrogeno nelle cellule dell’epitelio tubulare, si forma anche ione bicarbonato che viene riassorbito nel sangue.

In alcalosi metabolica c’è un eccesso di ioni bicarbonato. Il bicarbonato non viene quindi totalmente riassorbito perché il sistema di trasporto satura, ma rimane nelle urine per essere escreto. La secrezione di protoni non riesce a bilanciare il carico filtrato di bicarbonato.
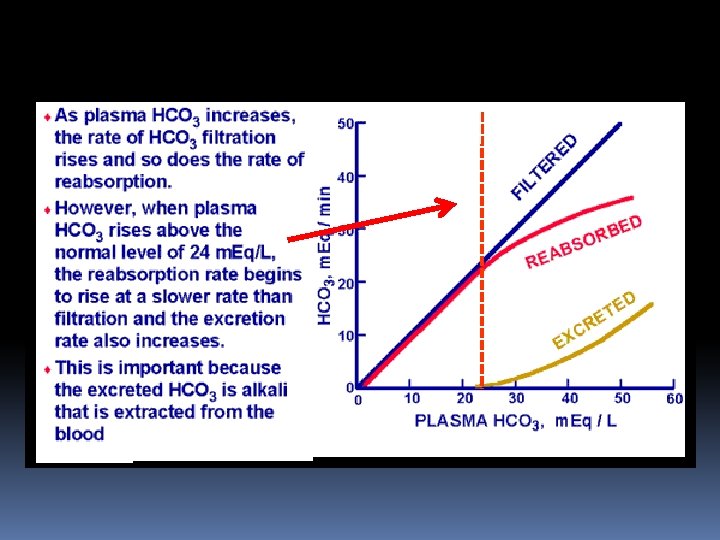

In acidosi metabolica (diminuzione di bicarbonato che verrà totalmente riassorbito) o respiratoria (aumento di PCO 2) viene stimolata la secrezione di idrogenioni lungo il nefrone. Questi ioni H+ devono essere titolati da sistemi tampone (fosfato ed ammonio) ed eliminati come sali per generare bicarbonato ex-novo

Secrezione di H+ in TCD e DC La secrezione di ioni H+ nella parte distale del TCD e nel DC avviene attraverso un meccanismo di trasporto attivo. La maggiore differenza con TCP è proprio che in questa parte del nefrone esiste una pompa idrogenionica che muove gli ioni H+ dall’interno della cellula, dove si formano a partire dalla reazione di idratazione della CO 2 ad opera dell’anidrasi carbonica, al lume tubulare.

In questa parte del nefrone la pompa riesce a stabilire un gradiente idrogenionico altissimo che porta il p. H fino a circa 4. 5 che è il limite inferiore raggiungibile nel rene. Questo avviene ad opera delle cellule intercalate la cui pompa protonica è una pompa a bassa velocità ma ad altissimo gradiente. Per ogni protone pompato un nuovo bicarbonato passa nel sangue.
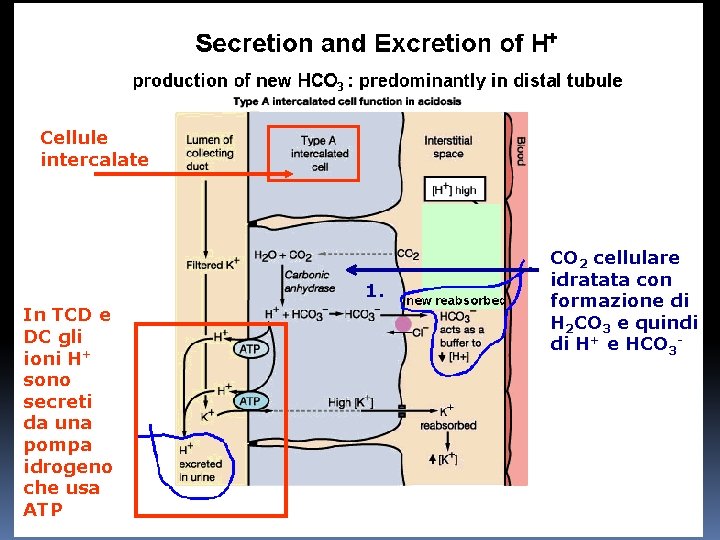
Cellule intercalate 1. In TCD e DC gli ioni H+ sono secreti da una pompa idrogeno che usa ATP CO 2 cellulare idratata con formazione di H 2 CO 3 e quindi di H+ e HCO 3 -

Sintesi di bicarbonato ex-novo In caso di acidosi, quando si presenta la necessità di eliminare un eccesso di ioni H+, solo una piccola parte di idrogenioni può rimanere in forma ionica nelle urine, perché altrimenti il valore di p. H scenderebbe troppo danneggiando il tessuto. Per fare un esempio, per eliminare 80 m. Eq/die di idrogenioni derivati da acidi non-volatili, bisognerebbe eliminare 2667 litri di urina se gli idrogenioni rimanessero in forma ionica!!!!!

Quando gli ioni H+ sono in eccesso rispetto al bicarbonato filtrato, gli ioni H+ sono tamponati da altri sistemi tampone che sono il sistema fosfato e il tampone ammoniacale. In questo modo si formano nuovi ioni bicarbonato che sono riassorbiti: questa quota costituisce il bicarbonato ex-novo.

Tampone fosfato Entrambi i componenti del sistema tampone sono concentrati nelle urine perché sono scarsamente riassorbiti essendo in forma ionica. Il trasporto tubulare massimo è inferiore rispetto al filtrato per cui si concentra nelle urine. Inoltre le urine sono sempre lievemente acide rispetto al LEC e quindi il tampone lavora ad un p. H vicino al p. K, situazione ideale per un sistema tampone.
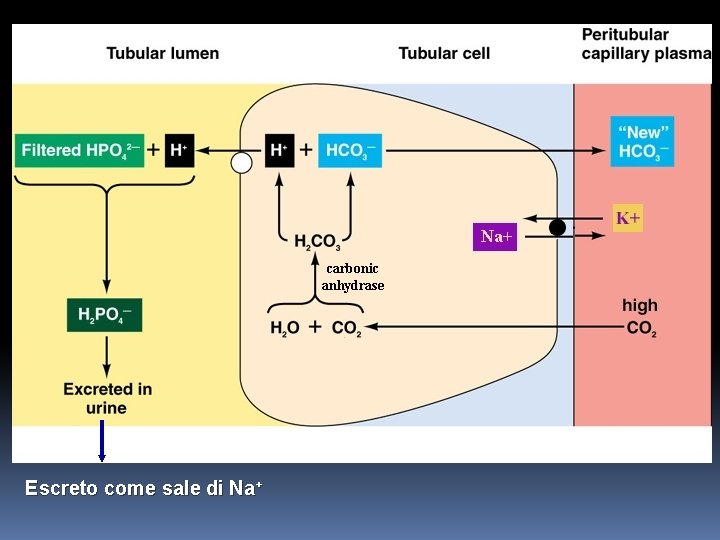
Escreto come sale di Na+

Quindi, tutte le volte che uno ione idrogeno secreto nel lume tubulare, si combina con un buffer che non sia bicarbonato, l’effetto netto è l’aggiunta di nuovo bicarbonato nel sangue.

Questo avviene tutte le volte che tutto il bicarbonato è stato riassorbito per la titolazione degli H+. Quando il tampone bicarbonato è esaurito nel filtrato, si presenta la necessità di nuovo bicarbonato e titolazione con un altro buffer.

Tampone ammoniacale Il secondo sistema tampone è il sistema formato da Va detto che questo tampone ammoniaca (NH 3 accettore di idrogenioni) e ione entra in gioco nei casi di grave ammonio (NH 4+ donatore di idrogenioni). Quest’ultimo è acidosi promuovendo sintesi di formato dalla glutammina che è trasportata attivamente bicarbonato ex-novo già a livello all’interno del TCP, del TAS, TCD e DC. del TCP Il trasporto di ioni ammonio è diverso a seconda che si parli di TCP o DC. Nel primo caso (TCP) viene immesso ione ammonio nel lume tubulare e lo ione bicarbonato è riassorbito.
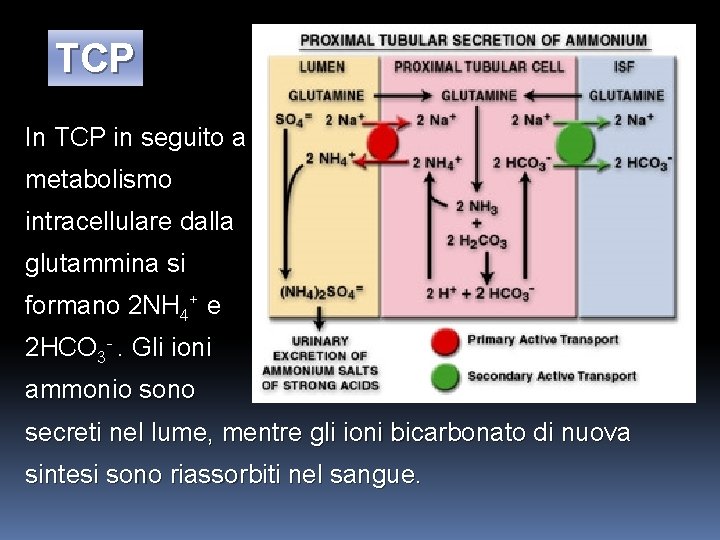
TCP In TCP in seguito a metabolismo intracellulare dalla glutammina si formano 2 NH 4+ e 2 HCO 3 -. Gli ioni ammonio sono secreti nel lume, mentre gli ioni bicarbonato di nuova sintesi sono riassorbiti nel sangue.

Nel nefrone distale la membrana tubulare non è permeabile allo ione ammonio e quindi è secreta ammoniaca che lega idrogenioni formando ioni NH 4+ che restano intrappolati nel lume.
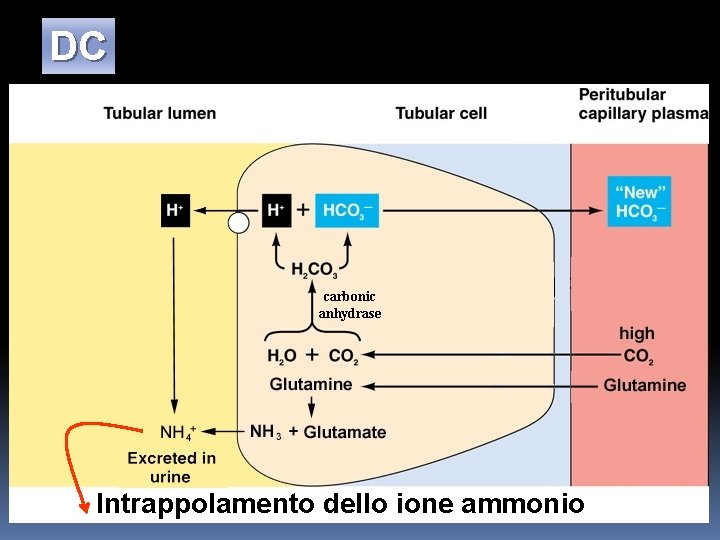
DC Intrappolamento dello ione ammonio

Come il sistema renale risponde a situazioni di acidosi o alcalosi? Il rene forma ed estrae dal compartimento extracellulare un fluido che contiene un eccesso di alcali o di basi. Ø La concentrazione del bicarbonato plasmatico controlla la velocità di filtrazione e quindi il grado al quale il bicarbonato è riassorbito ed escreto. Ø La pressione parziale di CO 2 nel sangue influenza la rate di secrezione di protoni

Acidosi: aumento dell’escrezione netta di idrogenioni, con aumento dell’escrezione di ioni ammonio. Sintesi ex-novo di bicarbonato riassorbito nel sangue Alcalosi: escrezione di ioni ammonio a zero, mentre aumenta l’escrezione di ioni bicarbonato. Quindi perdita netta di bicarbonato dal sangue (secrezione acida negativa) e nessuna sintesi ex-novo di bicarbonato

Respiratory Disturbances Respiratory disturbances of acid base balance are caused by changes in pulmonary ventilation which result in a change in ECF PCO 2.

Renal Compensation The renal compensation for the increased PCO 2 in respiratory acidosis is to increase ECF HCO 3 accomplished by maximizing HCO 3 - retention and increasing the generation of new HCO 3 -. The increase in HCO 3 - reabsorption is facilitated by the stimulatory effect of elevated PCO 2 and decreased p. H on renal tubular H+ secretion. The increased generation of new HCO 3 - is driven by increased formation of titratable acid and the acidotic stimulus to secretion of NH 4+.

Renal Compensation The renal compensation for respiratory alkalosis is to lower the ECF HCO 3 - concentration. The decreased ECF PCO 2 and increased p. H inhibit renal tubular H+ secretion thereby decreasing reabsorption of HCO 3 -. Formation of titratable acid and secretion of NH 4+ are also inhibited by the elevated p. H and no new HCO 3 - is generated.


Respiratory Compensation Respiratory compensation for metabolic acidosis is driven primarily by central chemoreceptors.
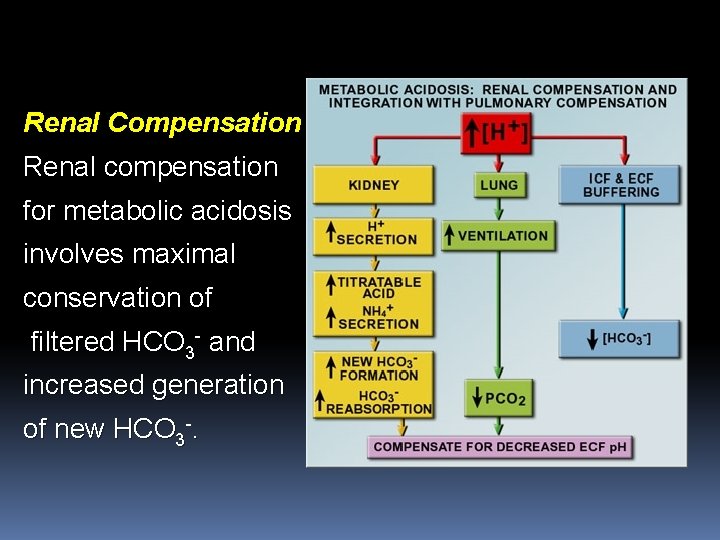
Renal Compensation Renal compensation for metabolic acidosis involves maximal conservation of filtered HCO 3 - and increased generation of new HCO 3 -.

Respiratory compensation In metabolic alkalosis the respiratory response to the increased p. H is hypoventilation.
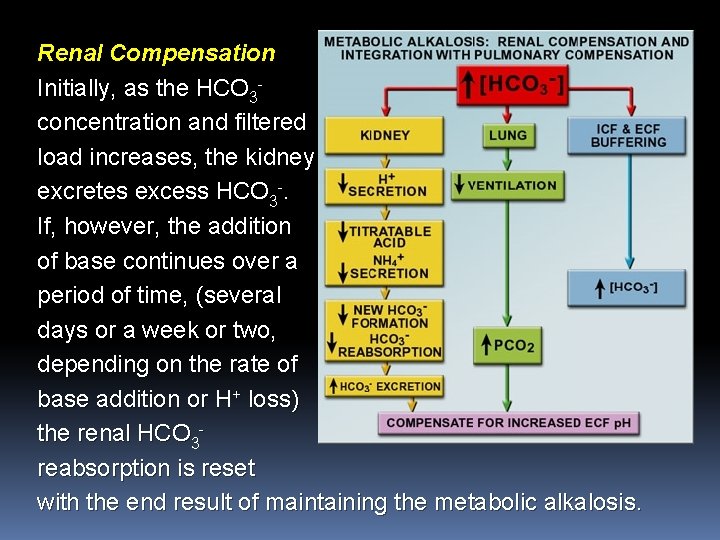
Renal Compensation Initially, as the HCO 3 - concentration and filtered load increases, the kidney excretes excess HCO 3 -. If, however, the addition of base continues over a period of time, (several days or a week or two, depending on the rate of base addition or H+ loss) the renal HCO 3 - reabsorption is reset with the end result of maintaining the metabolic alkalosis.
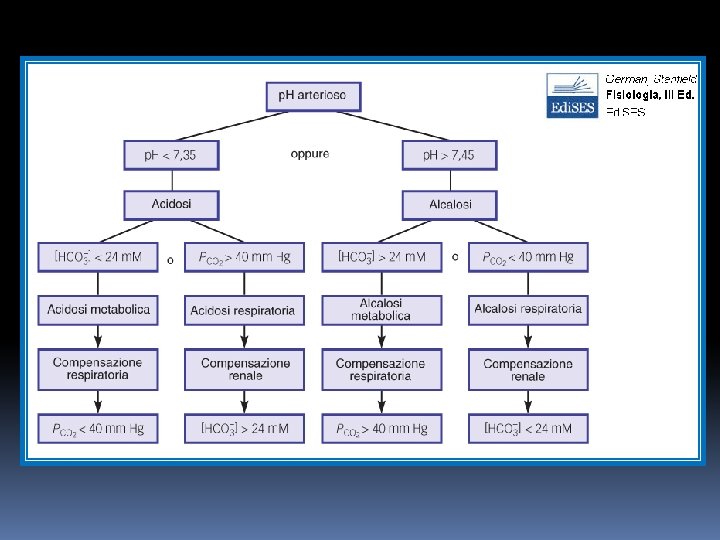
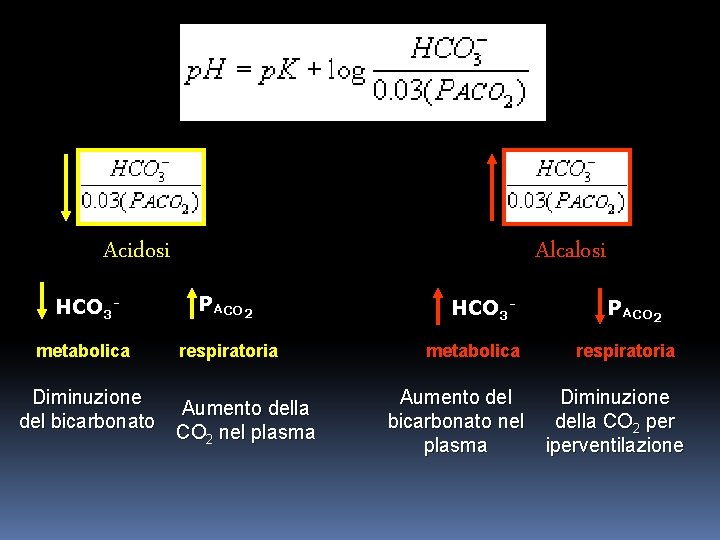
Alcalosi Acidosi HCO 3 - PACO 2 metabolica respiratoria Diminuzione del bicarbonato Aumento della CO 2 nel plasma HCO 3 metabolica PACO 2 respiratoria Aumento del Diminuzione bicarbonato nel della CO 2 per plasma iperventilazione
- Slides: 87