Acido base Profesora Ayleen Espinoza Saavedra Objetivo identificar

Acido - base Profesora: Ayleen Espinoza Saavedra

Objetivo: identificar y distinguir un acido de una base

Ácidos Son sustancias puras con sabor característico: Acido acético Acido cítrico Acido málico Químicamente, los ácidos se dividen en: Ácidos binarios o hidrácidos No metal + hidrogeno hidrácido Ácidos ternarios u oxácidos: Óxido ácido + agua oxácido

Características de los ácidos El ion hidrogeno (H+) es su contribuyente propio de estos Poseen sabor agrio- acido Algunas otras conducen electricidad en disolución acuosa Algunos son corrosivos Reaccionan con bases produciendo sales Reaccionar con algunos metales desprendiendo hidrogeno Descomponen a los carbonatos y bicarbonatos metalidos, liberando CO 2 gaseoso.

Hidróxidos o bases ÓXIDO BÁSICO + AGUA HIDRÓXIDO Co. O + H 2 O===> Co(OH)2 Pb. O 2 + 2 H 2 O===> Pb(OH)4

Características de los Hidróxidos (bases) Ión o radical hidrocilo (OH-) propio de estos Presentan sabor a lejía ( como jabón) Son resbaladizas al tacto Conducen la corriente eléctrica en disolución acuosa Generalmente son corrosivas Poseen propiedades de jabones y detergentes Disuelven los aceites y el azufre Reaccionan con los ácidos para producir sales
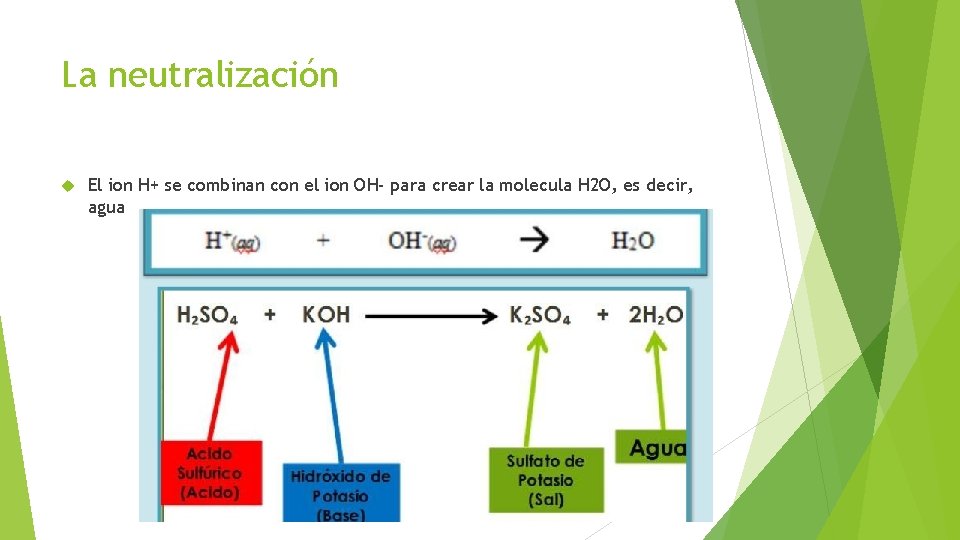
La neutralización El ion H+ se combinan con el ion OH- para crear la molecula H 2 O, es decir, agua

Solubilidad del dióxido de carbono en el agua solubilidad del CO 2 en el agua pura a 25ºC es de 1, 45 g/L El dióxido de carbono es un óxido de un no metal que puede reaccionar con el agua para formar el ácido carbónico, H 2 CO 3 CO 2(g) + H 2 O(l) ↔ H 2 CO 3(aq)

Ejercicio

Teorías ácido-base Analizar base y aplicar las teorías de ácido

Teoría de Arrhenius “disociación iónica” (1887) Hay sustancias (electrolitos) que en disolución se disocian en cationes y aniones. ÁCIDO: Sustancia que en disolución acuosa disocia cationes H+ BASE: Sustancia que en disolución acuosa disocia aniones OH– Las bases poseen en su estructura el ion OH Los ácidos poseen en su estructuras átomos de H
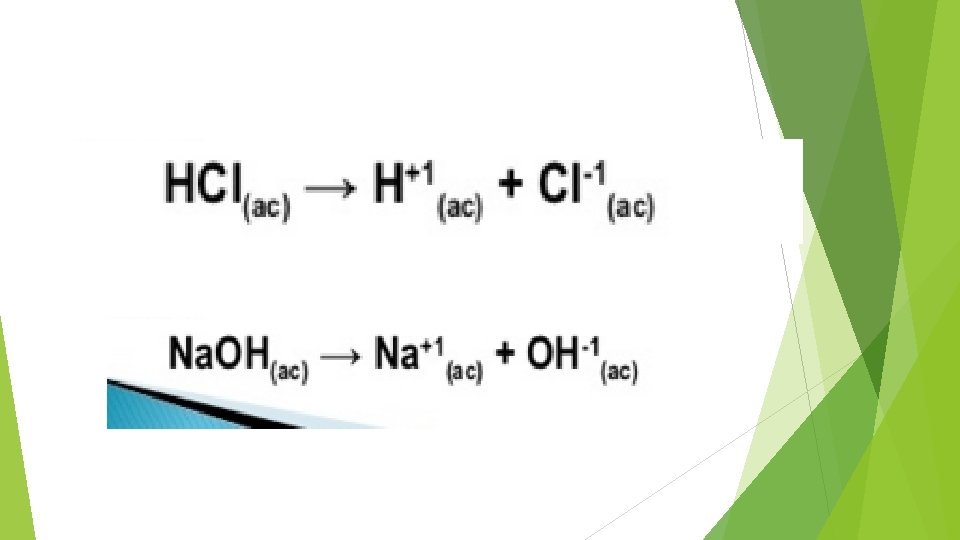
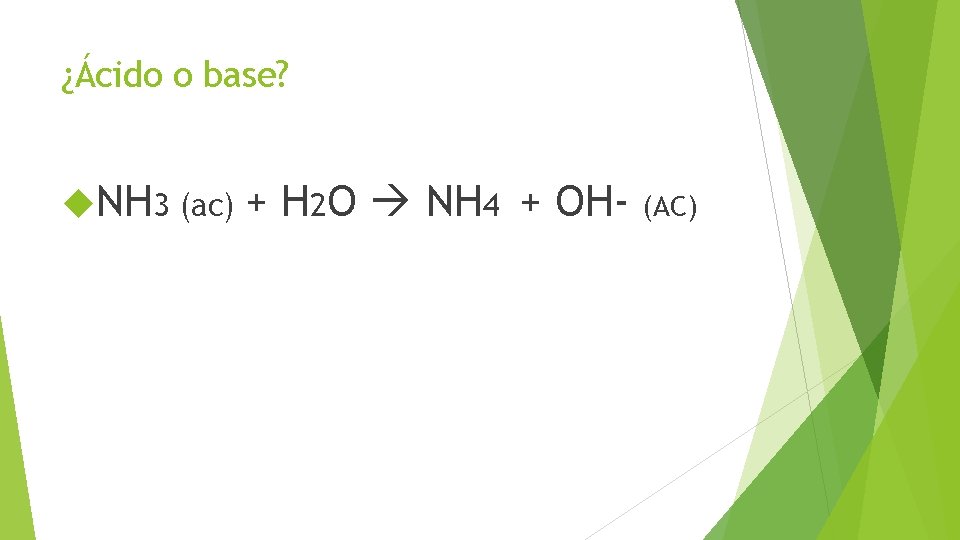
¿Ácido o base? NH 3 (ac) + H 2 O NH 4 + OH- (AC)

Definición de ácido y de base según teoría de Brönsted-Lowry “Las reacciones acido-base implican transferencia de iones hidrogeno de una sustancia a otra” ACIDO: BASE: sustancia que dona ion H+ sustancia que capta ion H+

HCl (g) + H 2 O (l) → H 3 O+(ac) + Cl– (ac)

Cuando un ácido pierde H+ se convierte en su “base conjugada” y cuando una base captura H+ se convierte en su “ácido conjugado”

Teoría de Lewis ÁCIDOS: “Sustancia que contiene al menos un átomo capaz de aceptar un par de electrones y formar un enlace covalente coordinado” BASES: “Sustancia que contiene al menos un átomo capaz de aportar un par de electrones para formar un enlace covalente coordinado”
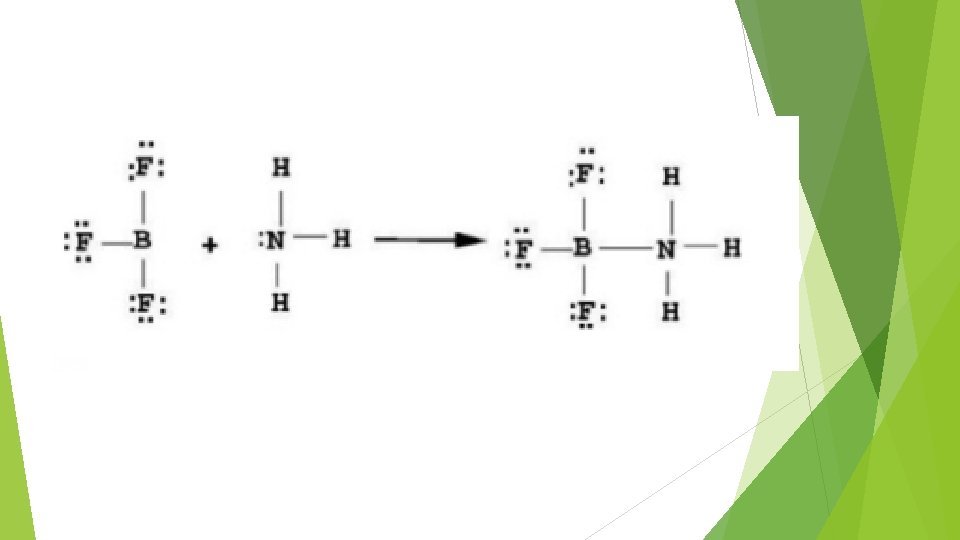

Ejercicios HI (ac) H+ (ac) + I- (ac) KOH(ac) K+ (ac) + OH – (ac) CH 3 COOH (ac) + H 2 O (l) CH 3 COO- (ac) + H 3 O+ (ac) BF 3 (ac) + : NH 3 (ac) H 3 N: BF 3 (ac)

Obj: p. OH compreder y aplicar la relación entre p. H y
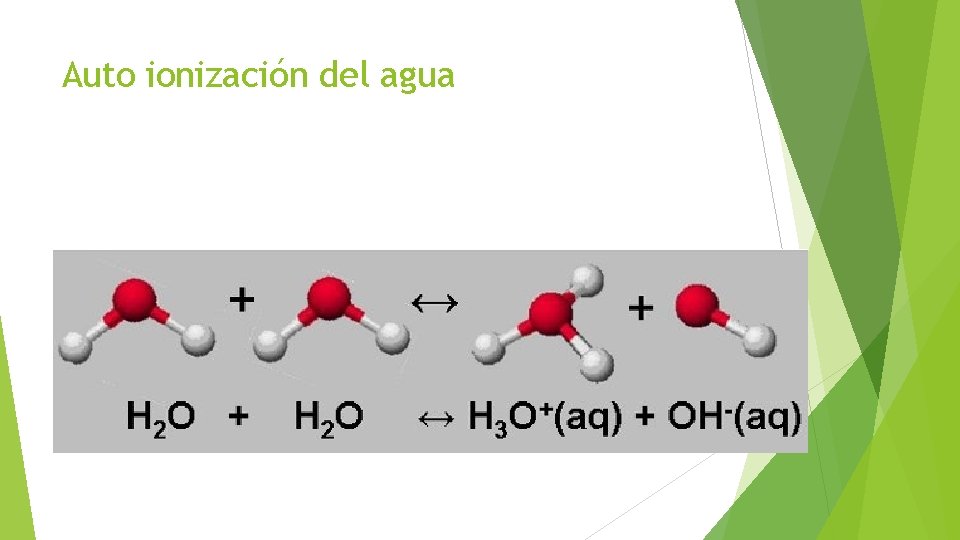
Auto ionización del agua

La auto ionización del agua, dura muy poco tiempo, las reacciones son sumamente rápidas (en ambos sentidos), por lo que es un proceso de equilibrio , por tanto existe una CONSTANTE DE EQUILIBRIO:
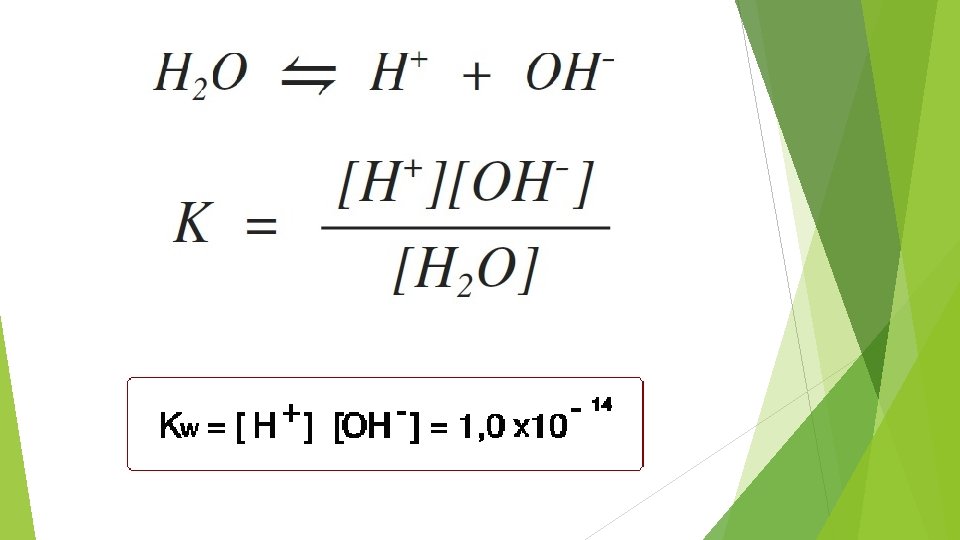

Kw útil para cualquier disolución acuosa Se calcula para obtener el valor de H+ teniendo [OH-] Se calcula para obtener el valor de OH- teniendo [H+] EJEMPLO Si [H+] tiene un valor de 1 x 10 -3, cual es el valor de [OH-]
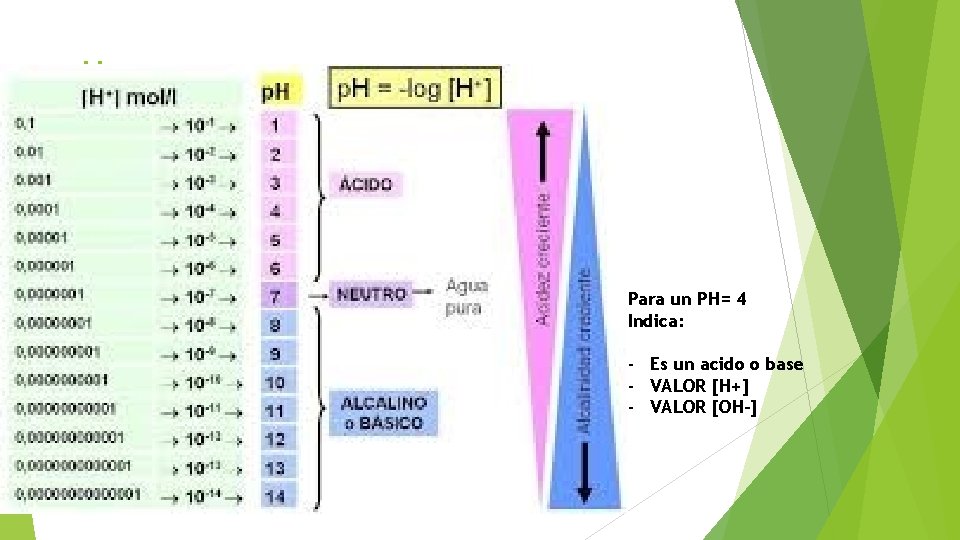
p. H Para un PH= 4 Indica: - Es un acido o base - VALOR [H+] - VALOR [OH-]

p. Kw= p. H + p. OH = 14 Ejemplo: que valor de p. OH posee una sustancia de p. H = 8
![Sustancia ácida neutra base [H+] p. H Sustancia ácida neutra base [H+] p. H](http://slidetodoc.com/presentation_image_h2/4106141ea6b0cb3b9e6cd00915dc3143/image-27.jpg)
Sustancia ácida neutra base [H+] p. H


Ejercicio El acido clorhídrico es uno de los principales componentes del acido gástrico, en una mezcla su concentración alcanza a ser 0, 03 M, y este se disocia completamente. ¿Cual es su p. H? Reacción Inicialmente Cambio equilibrio

El hidróxido de sodio (Na. OH) es la soda caustica, generalmente se recomienda disolver 10 gr del producto en 1 litro de agua, por lo que se genera una concentración de 0, 25 M Establezca cual es el p. H de la disolución formada, sabiendo que se disocia completamente Reacción Inicialmente Cambio Equilibro

FUERZA BASES RELATIVA DE ACIDOS Y

OBJ: comprender y aplicar la fuerza de los ácidos y bases

Acido o base fuerte: se disocia completamente Acido o base débil, se disocia solo una parte

Calculo de p. H en ácidos y bases fuertes Para una disolución de 0, 1 M de HBr ¿Cuál es su p. H? Sabiendo que es una ácido fuerte

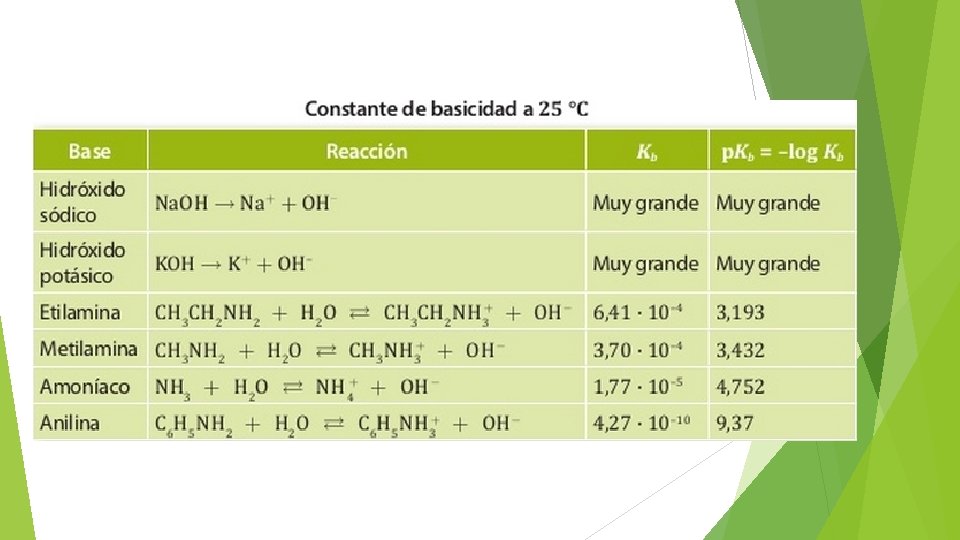
Equilibrio iónico de ácidos y bases El criterio teórico para distinguir la fuerza de un acido es su constante de acidez Ka Ka= [productos]/[reactantes] Ka > 1 acido es fuerte Ka < 1 el acido es débil La mayoría de los ácidos y bases son electrolitos débiles
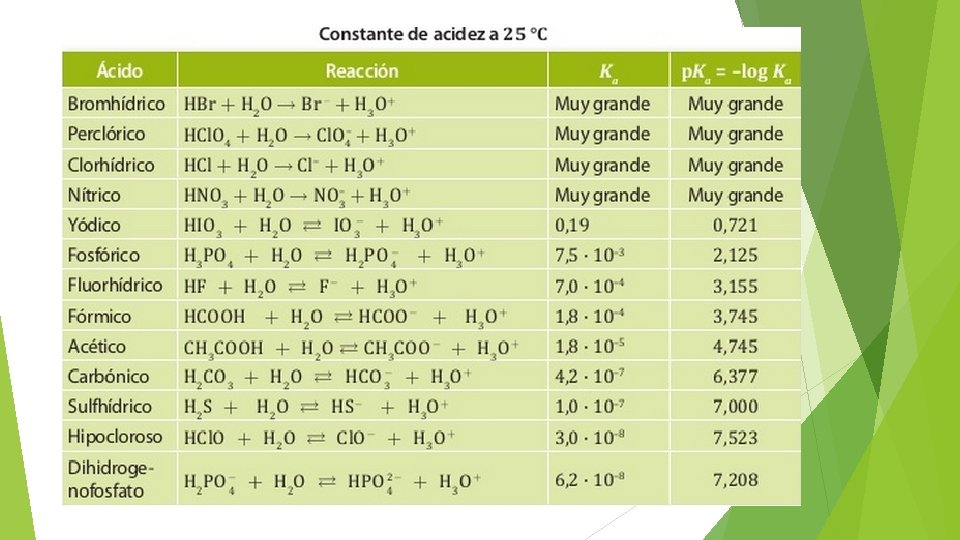
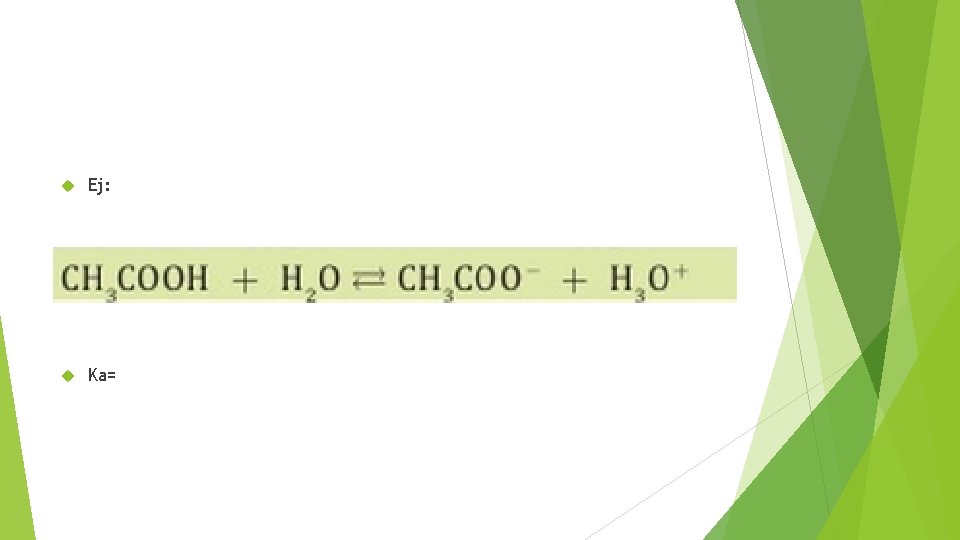
Ej: Ka=

En las bases, se denomina constante de basicidad Kb Ka y Kb, se relacionan en la expresión de la constante del agua Kw Kw= Ka x Kb Con logaritmo tenemos que: p. Kw= p. Ka + p. Kb =14

Porcentaje de ionización Otra forma de medir la fuerza de un acido es por su porcentaje de ionización %= [H+]/ [HA] x 100 [H+] =concentración de H [HA]= concentración en mol Cuando mas fuerte es un acido, mayor es su porcentaje de ionización
![Si p. H = -log [H+], al despejar [H+] se tiene: p. OH Si p. H = -log [H+], al despejar [H+] se tiene: p. OH](http://slidetodoc.com/presentation_image_h2/4106141ea6b0cb3b9e6cd00915dc3143/image-41.jpg)
Si p. H = -log [H+], al despejar [H+] se tiene: p. OH = - log [OH-] , al despejar [OH-] se tiene:

Si el acido fluorhídrico tiene un p. H de 2, 3 ¿ cual es su concentración de [H+] en una disolución?

Ej: si el HF de concentración 0, 05 M tiene un p. H =2, 2 ¿ es un acido fuerte o débil?
- Slides: 43