Acidi e Basi Definizione di Arrhenius 1887 acidi



Acidi e Basi Definizione di Arrhenius (1887): acidi e basi sono composti che in acqua danno luogo a dissociazione elettrolitica: Svante August Arrhenius Wijk (Svezia), 1859 – Stoccolma, 1927 Acido H+(aq) +. . . Base OH-(aq) +. . .

Insufficienza della definizione di Arrhenius: Molte basi, come per esempio NH 3, non possono formare OH-(aq) per semplice dissociazione elettrolitica. La reazione acido-base deve essere di tipo diverso.




Definizione di Brønsted e Lowry (per acidi e basi in soluzioni acquose) Acido = donatore di protoni Base = accettore di protoni

Carenze della teoria di Brønsted e Lowry : Vi sono alcune sostanze che portano ad una variazione del p. H di una soluzione senza accettare o donare protoni. Serve un modello più generale di cui gli altri modelli sono dei casi speciali.

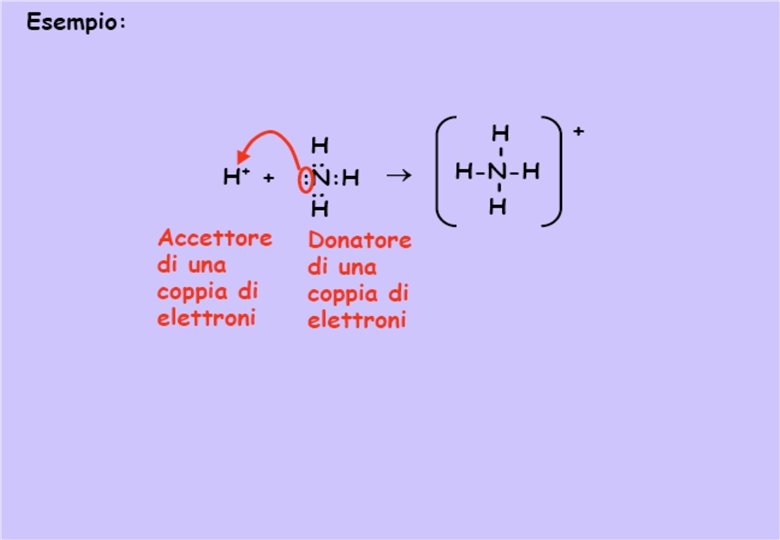
Definizione di Lewis Acido = accettore di una coppia di elettroni Base = donatore di una coppia di elettroni




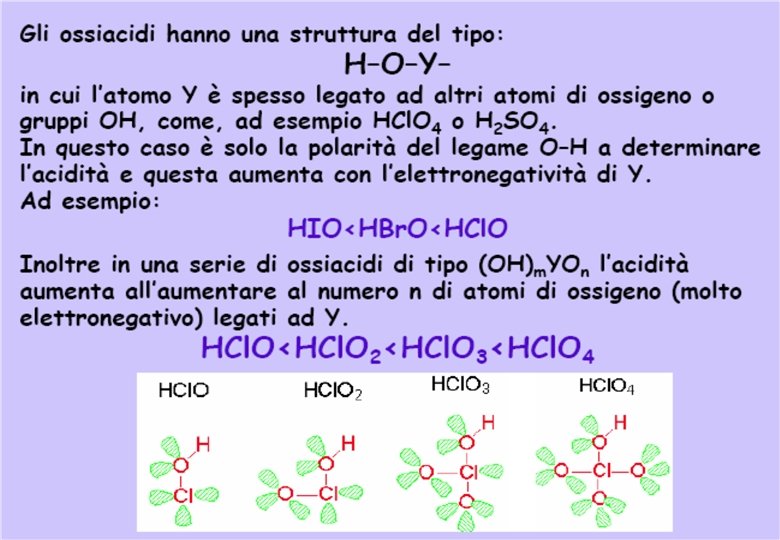
diminuisce






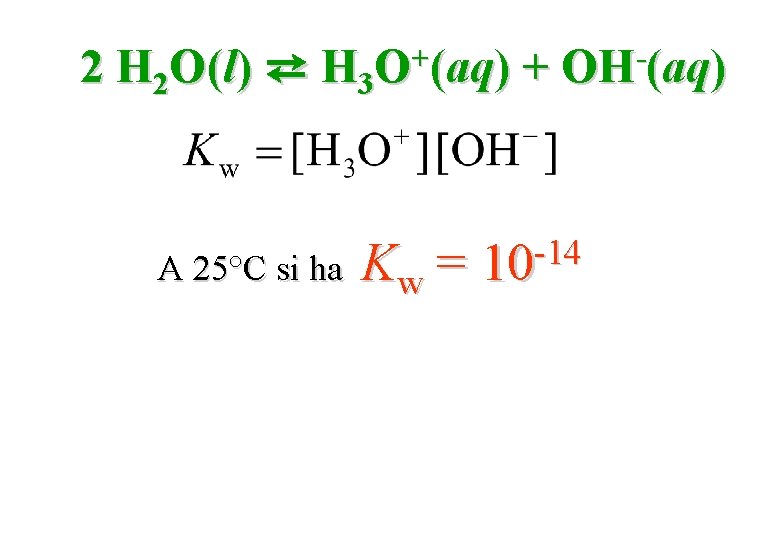
2 H 2 O(l) + ⇄ H 3 O (aq) A 25°C si ha Kw = + OH (aq) -14 10


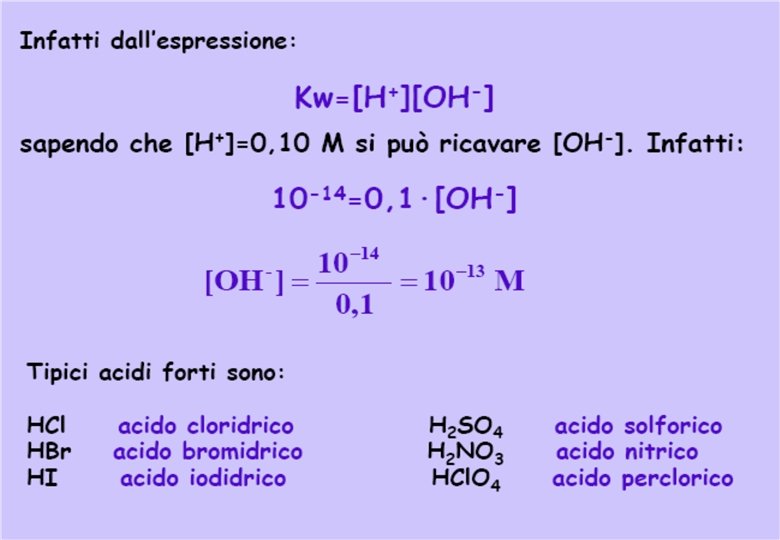





![a 25°C [H 3 O+] > [OH-] [H 3 O+] 10 0 [H 3 a 25°C [H 3 O+] > [OH-] [H 3 O+] 10 0 [H 3](http://slidetodoc.com/presentation_image_h/142672a7eeed35fb6def79b2e5f1f7e9/image-32.jpg)
a 25°C [H 3 O+] > [OH-] [H 3 O+] 10 0 [H 3 O+] < [OH-] 10 -1 10 -2 10 -3 10 -4 10 -5 10 -6 10 -7 10 -8 10 -9 10 -10 10 -11 10 -12 10 -13 10 -14 soluzione acida soluzione basica [H 3 O+] > 10 -7 M [OH-] < 10 -7 M soluzione neutra [H 3 O+] = [OH-] = 10 -7 M [H 3 O+] < 10 -7 M [OH-] > 10 -7 M
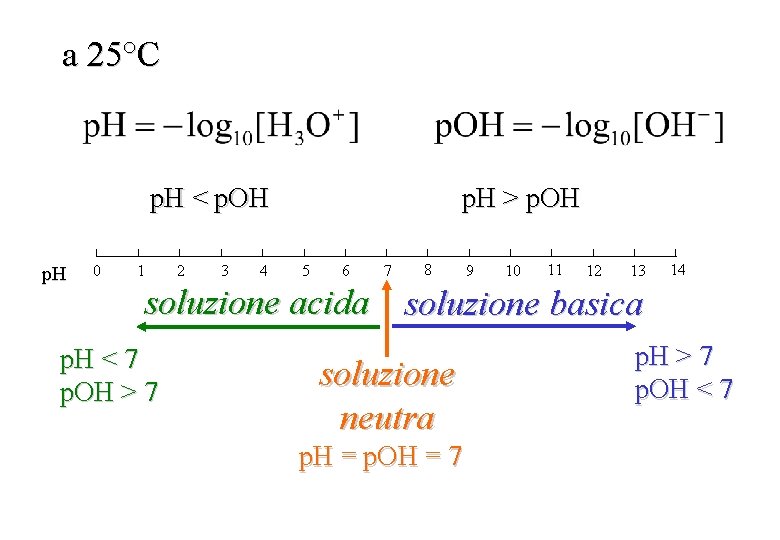
a 25°C p. H > p. OH p. H < p. OH p. H 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 soluzione acida soluzione basica p. H < 7 p. OH > 7 soluzione neutra p. H = p. OH = 7 p. H > 7 p. OH < 7
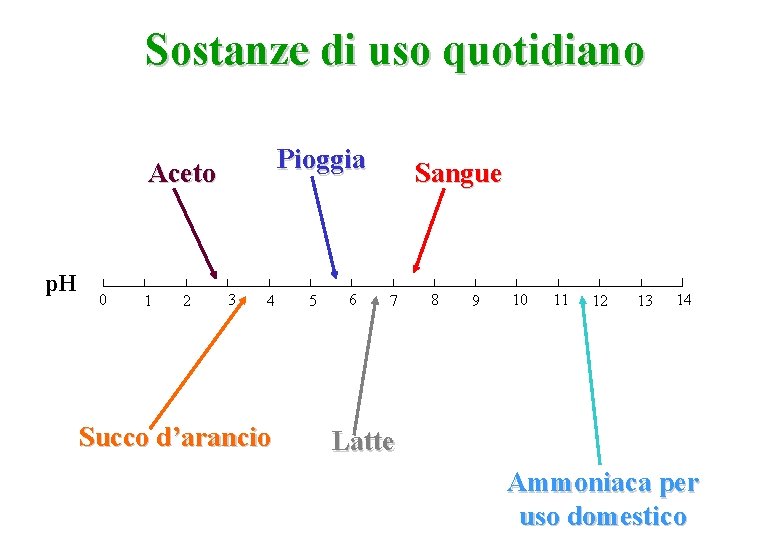
Sostanze di uso quotidiano Pioggia Aceto p. H 0 1 2 3 4 Succo d’arancio 5 6 Sangue 7 8 9 10 11 12 13 14 Latte Ammoniaca per uso domestico








o di dissociazione

Grado di dissociazione • È la frazione di acido HA ( o di base) che si dissociqa e si indica con a • Per acidi forti a = 1 • Per acidi deboli 0< a <1 In generale , dato un acido debole HA, il grado di dissociazione è dato da a = [H+] [ concentrazione dell’acido]

Si calcoli il grado di dissociazione dell’ammoniaca in una soluzione 0. 55 M (Kb= 1. 85· 10 -5) Kb= [NH 4+] [OH-] [NH 3] a = 5. 8· 10 -3 = (0. 55 a)2 0. 55 (1 -a ) = 1. 85· 10 -5
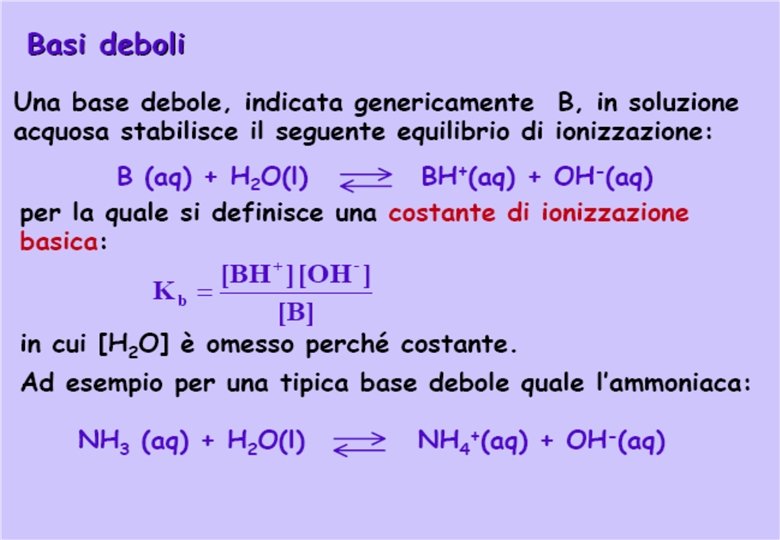












In tutti i casi, per una coppia acido-base coniugati si ha: Ka Kb = K w Per esempio, per NH 4+-NH 3:



- Slides: 60