Acidi e Basi Acido una parola che deriva

Acidi e Basi Acido è una parola che deriva dal latino “acetum” (aceto). Col tempo la parola si è estesa a tutte le sostanze che hanno un analogo sapore “acidulo”. Basi o alcali (dall’arabo al kali = la cenere delle piante) sono le sostanze in grado di neutralizzare gli acidi.

Lavoisier pensava che un acido fosse caratterizzato da molecole contenenti ossigeno (oxys genes = generatore d’acido). Antoine Lavoisier 1743 -1794 Nel 1810 Humphry Davy dimostrò che l’acido cloridrico (detto allora muriatico) era formato solo da cloro e idrogeno. Da allora fu accettata l’idea che gli acidi fossero caratterizzati dalla presenza d’idrogeno nella molecola. Humpry Davy 1778 -1829

Definizione di Arrhenius (1887) acidi e basi sono composti che in acqua danno luogo a dissociazione elettrolitica liberando rispettivamente ioni H+ e OH-: Acido H+(aq) +. . . Base OH-(aq) +. . . Svante August Arrhenius Wijk (Svezia), 1859 – Stoccolma, 1927 Premio Nobel per la Chimica 1903 Neutralizzazione acido-base: H+(aq) + OH-(aq) H 2 O(l)

Un acido ed una base si dicono forti quando sono completamente dissociati. Le reazioni di neutralizzazione sono reazioni tra acidi e basi: HCl + KOH KCl + H 2 O che in forma ionica si può esprimere: H+(aq) + Cl-(aq) + K+(aq) + OH-(aq) K+(aq) + Cl-(aq) + H 2 O che semplificata equivale a H+(aq) + OH-(aq) H 2 O (equazione ionica netta) Il concetto di Arrhenius non si può applicare in solventi diversi dall’acqua.

Insufficienza della definizione di Arrhenius: Molte basi, come per esempio l’ammoniaca, NH 3, non possono formare OH-(aq) per dissociazione elettrolitica. La reazione acido-base deve essere quindi di tipo diverso.

Definizione di Brønsted e Lowry (1923) (per acidi e basi in soluzione acquosa) Johannes Nicolaus Brønsted 1879 -1947 Thomas Martin Lowry 1874 -1936 Acido = donatore di protoni, H+ Base = accettore di protoni, H+
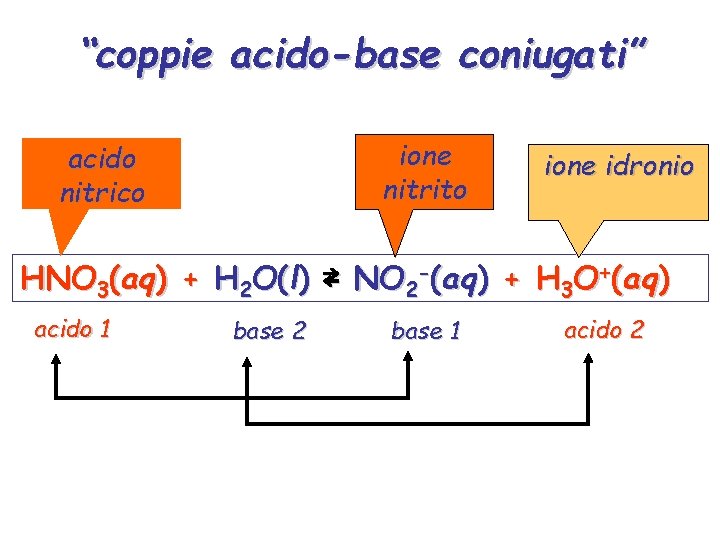
“coppie acido-base coniugati” ione nitrito acido nitrico ione idronio HNO 3(aq) + H 2 O(l) ⇄ NO 2 -(aq) + H 3 O+(aq) acido 1 base 2 base 1 acido 2
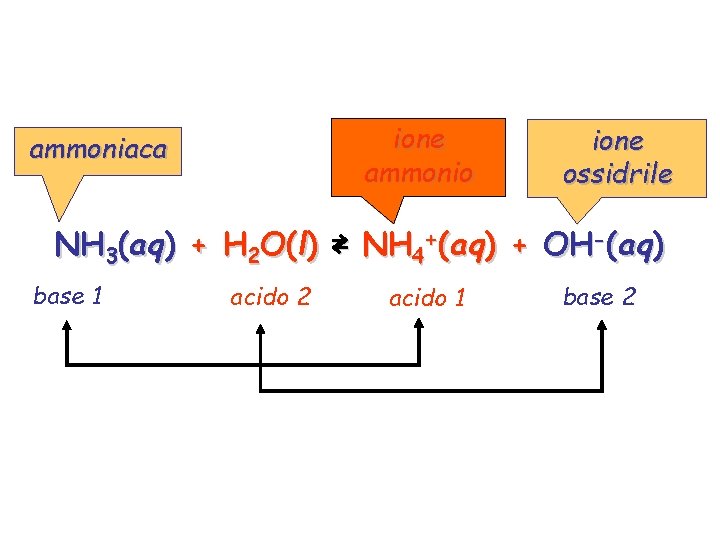
ione ammonio ammoniaca ione ossidrile NH 3(aq) + H 2 O(l) ⇄ NH 4+(aq) + OH-(aq) base 1 acido 2 acido 1 base 2
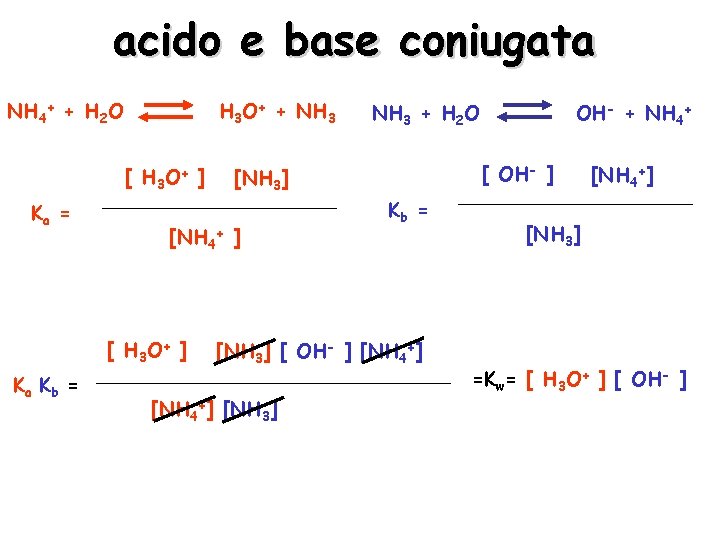
acido e base coniugata NH 4+ + H 2 O H 3 O+ + NH 3 [ H 3 O+ ] Ka = Ka Kb = [NH 3] [ OH- ] [NH 4+] [NH 3] OH- + NH 4+ [ OH- ] [NH 3] [NH 4+ ] [ H 3 O+ ] NH 3 + H 2 O [NH 4+] [NH 3] =Kw= [ H 3 O+ ] [ OH- ]

La forza di acidi e basi Sono considerati forti gli acidi e le basi che in acqua sono completamente dissociati, ovvero con equilibrio fortemente spostato verso destra. Ad esempio: HCl(aq) + H 2 O(l) ⇄ Cl-(aq) + H 3 O+(aq) Na. OH(aq) + H 2 O(l) ⇄ Na+(aq) + OH-(aq) In entrambi gli esempi l’equilibrio è fortemente spostato verso destra: tutte le molecole di acido cloridrico e idrossido di sodio risultano in pratica dissociate. Di conseguenza, una mole di HCl forma 1 mole di H+ e 1 mole di Na. OH forma una mole di OH-.

La forza di acidi e basi Sono considerati deboli gli acidi e le basi che in acqua sono parzialmente dissociati, ovvero con equilibrio spostato verso sinistra. Ad esempio: H 2 S(aq) + H 2 O(l) ⇄ HS-(aq) + H 3 O+(aq) NH 3(aq) + H 2 O(l) ⇄ NH 4+(aq) + OH-(aq) In entrambi gli esempi l’equilibrio è spostato verso sinistra: solo una parte delle molecole di acido solfidrico e ammoniaca risultano dissociate. Di conseguenza, una mole di H 2 S NON forma 1 mole di H+ e 1 mole di NH 4 NON forma una mole di OH-.
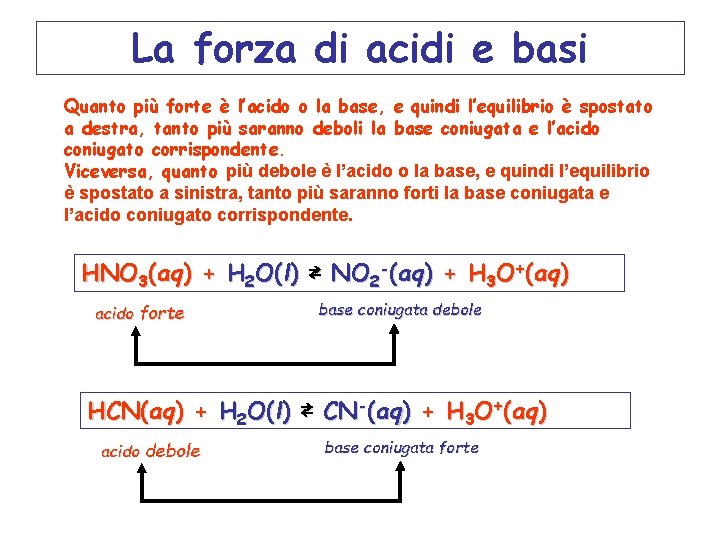
La forza di acidi e basi Quanto più forte è l’acido o la base, e quindi l’equilibrio è spostato a destra, tanto più saranno deboli la base coniugata e l’acido coniugato corrispondente. Viceversa, quanto più debole è l’acido o la base, e quindi l’equilibrio è spostato a sinistra, tanto più saranno forti la base coniugata e l’acido coniugato corrispondente. HNO 3(aq) + H 2 O(l) ⇄ NO 2 -(aq) + H 3 O+(aq) acido forte base coniugata debole HCN(aq) + H 2 O(l) ⇄ CN-(aq) + H 3 O+(aq) acido debole base coniugata forte
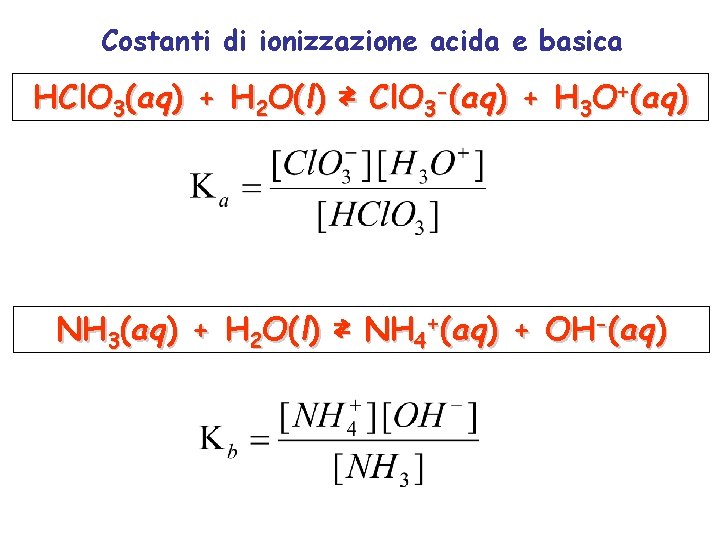
Costanti di ionizzazione acida e basica HCl. O 3(aq) + H 2 O(l) ⇄ Cl. O 3 -(aq) + H 3 O+(aq) NH 3(aq) + H 2 O(l) ⇄ NH 4+(aq) + OH-(aq)

La forza di un acido è determinata dalla costante di dissociazione acida Ka = [H 3 O+]x [A-] [HA] Tanto maggiore sarà il valore della costante e tanto piu’ l’acido sarà propenso a dissociarsi in soluzione, liberando ioni H + HA + H 2 O H 3 O + + A -

Acido e base coniugata Tanto piu’ un acido è forte, tanto piu’ sarà debole la sua base coniugata HCl Cl- CH 3 COOH CH 3 COO- H 2 CO 3 HCO 3 - HCN CNNH 3 NH 4+ H 2 O OH- = idrossidi ionici, es: Na. OH, Ca(OH)2, KOH
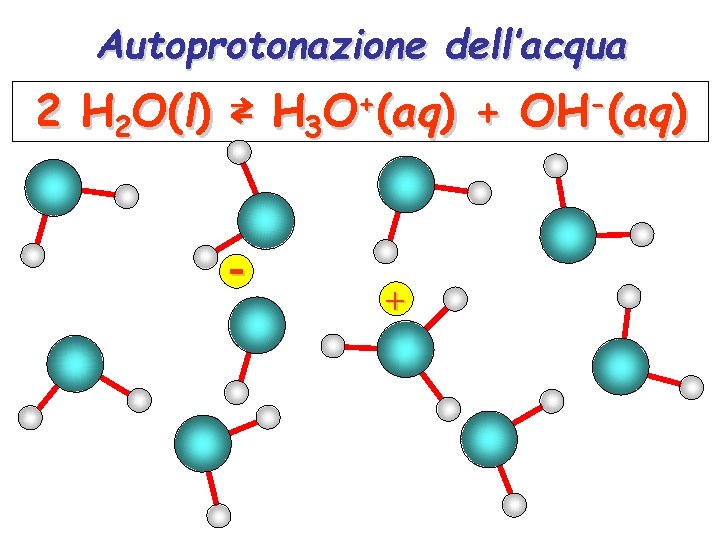
Autoprotonazione dell’acqua 2 H 2 O(l) ⇄ H 3 O+(aq) + OH-(aq) - +
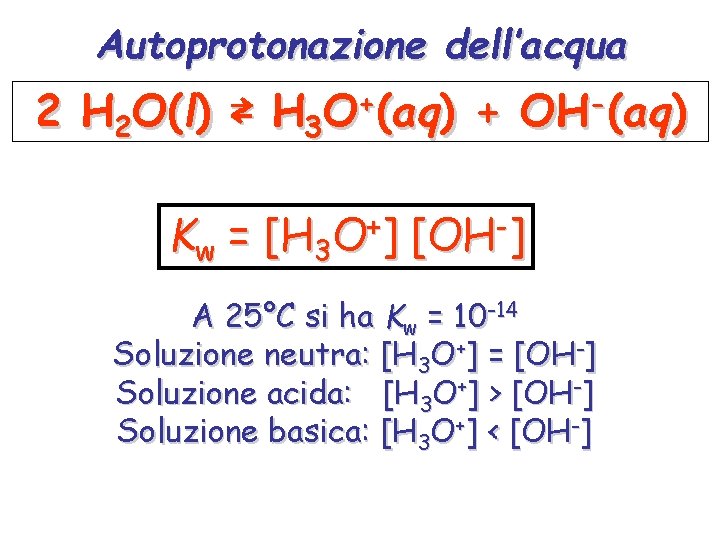
Autoprotonazione dell’acqua 2 H 2 O(l) ⇄ H 3 O+(aq) + OH-(aq) Kw = [H 3 O+] [OH-] A 25°C si ha Kw = 10 -14 Soluzione neutra: [H 3 O+] = [OH-] Soluzione acida: [H 3 O+] > [OH-] Soluzione basica: [H 3 O+] < [OH-]
![Kw = + [H 3 O ] Soluzione neutra: Soluzione acida: Soluzione basica: [OH Kw = + [H 3 O ] Soluzione neutra: Soluzione acida: Soluzione basica: [OH](http://slidetodoc.com/presentation_image_h/c92c24580d525a71d553ff8a14478b22/image-18.jpg)
Kw = + [H 3 O ] Soluzione neutra: Soluzione acida: Soluzione basica: [OH ]
![a 25°C [H 3 O+] < [OH-] [H 3 O+] > [OH-] [H 3 a 25°C [H 3 O+] < [OH-] [H 3 O+] > [OH-] [H 3](http://slidetodoc.com/presentation_image_h/c92c24580d525a71d553ff8a14478b22/image-19.jpg)
a 25°C [H 3 O+] < [OH-] [H 3 O+] > [OH-] [H 3 O+] 100 10 -1 10 -2 10 -3 10 -4 10 -5 10 -6 soluzione acida [H 3 O+] > 10 -7 [OH-] < 10 -7 10 -8 10 -9 10 -10 10 -11 10 -12 10 -13 10 -14 soluzione basica soluzione neutra [H 3 O+] = [OH-] = 10 -7 [H 3 O+] < 10 -7 [OH-] > 10 -7

I logaritmi, questi sconosciuti log A= B log 107= 7 log 1= 0 10 B= A log 10 -3= -3 1= 100 log Ax. B= log. A + log. B log 1/A= - log. A log 3, 2 x 10 -3= log 3, 2 - 3 log 1/10 -7 =-(log 10 -7)= -(-7)=7
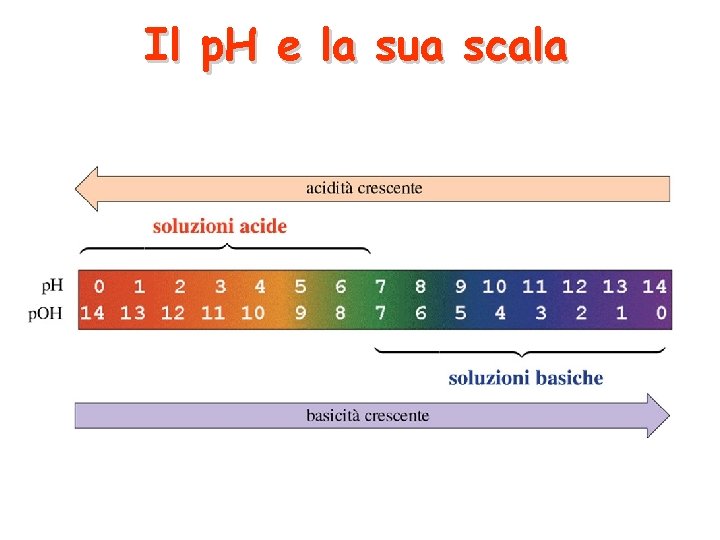
Il p. H e la sua scala
![a 25°C p. H = -log 10[H 3 O+] 100 10 -1 10 -2 a 25°C p. H = -log 10[H 3 O+] 100 10 -1 10 -2](http://slidetodoc.com/presentation_image_h/c92c24580d525a71d553ff8a14478b22/image-22.jpg)
a 25°C p. H = -log 10[H 3 O+] 100 10 -1 10 -2 10 -3 10 -4 10 -5 p. OH = -log 10[OH-] 10 -6 soluzione acida p. H < 7 p. OH > 7 10 -8 10 -9 10 -10 10 -11 10 -12 10 -13 10 -14 soluzione basica soluzione neutra p. H = p. OH = 7 p. H > 7 p. OH < 7
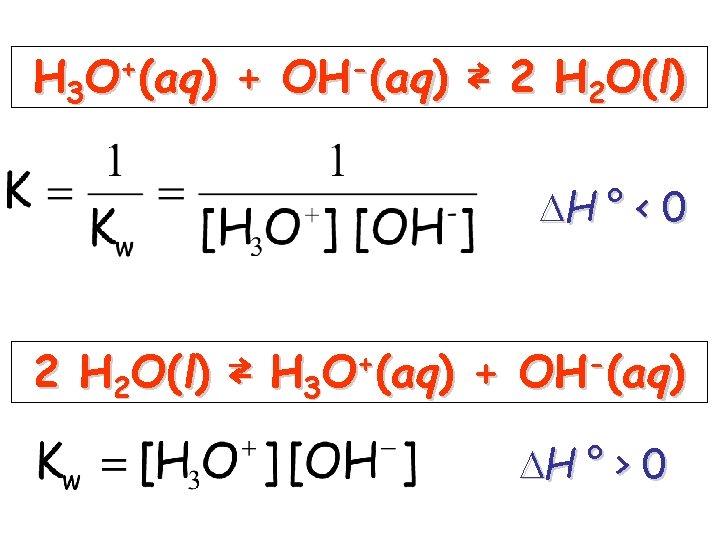
H 3 O+(aq) + OH-(aq) ⇄ 2 H 2 O(l) H ° < 0 2 H 2 O(l) ⇄ H 3 O+(aq) + OH-(aq) H ° > 0
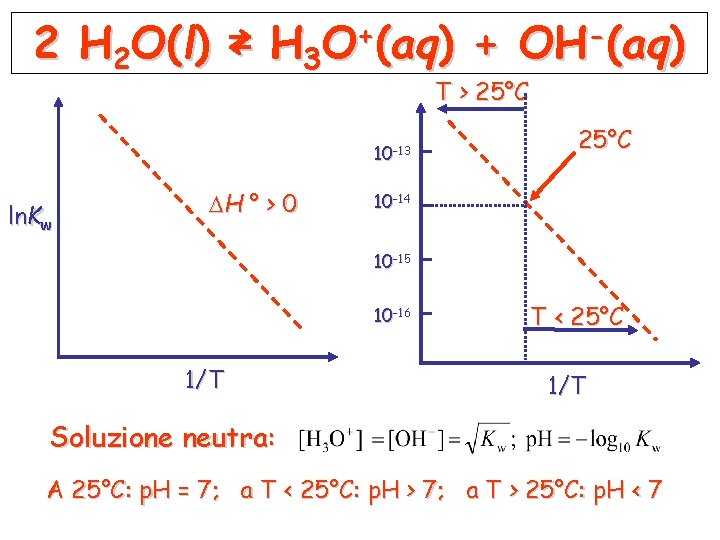
2 H 2 O(l) ⇄ H 3 O+(aq) + OH-(aq) T > 25°C 10 -13 ln. Kw H ° > 0 25°C 10 -14 10 -15 10 -16 1/T T < 25°C 1/T Soluzione neutra: A 25°C: p. H = 7; a T < 25°C: p. H > 7; a T > 25°C: p. H < 7
![Il p. H [H 3 O+] p. H = - Log [H 3 O+] Il p. H [H 3 O+] p. H = - Log [H 3 O+]](http://slidetodoc.com/presentation_image_h/c92c24580d525a71d553ff8a14478b22/image-25.jpg)
Il p. H [H 3 O+] p. H = - Log [H 3 O+] ACQUA PURA, T=25 °C [H 3 O+] = 1 x 10 -7 p. H = 7 [OH-] p. OH = - Log [OH-] ACQUA PURA, T=25 °C [OH-] = 1 x 10 -7 p. OH = 7 p. Kw = - Log (Kw) Kw = [H 3 O+][OH-] = 10 -7· 10 -7 = 1 x 10 -14 -Log (Kw) = -Log {[H 3 O+][OH-]} = -Log [H 3 O+] - Log [OH-] p. Kw = p. H + p. OH = 14

Acido debole (Ka < 1) in concentrazione ca HA(aq) + H 2 O(l) ⇄ A-(aq) + H 3 O+(aq) (ca – x) x x Se l’acido è così debole che x << ca, allora:

Base debole (Kb < 1) in concentrazione cb B(aq) (cb – + H 2 O(l) ⇄ BH+(aq) + OH-(aq) x) x x Se la base è così debole che x << cb, allora:

L’Altalena Coniugata HA(aq) + H 2 O(l) ⇄ A-(aq) + H 3 O+(aq) A-(aq) + H 2 O(l) ⇄ HA(aq) + OH-(aq)

L’Altalena Coniugata BOH(aq) ⇄ B+(aq) + OH-(aq) B+(aq) + H 2 O(l) ⇄ BOH(aq) + H+(aq)

L’Altalena Coniugata

Gli Acidi e le Basi Poliprotiche Definiamo ACIDO POLIPROTICO, secondo Brønsted. Lowry, un acido in grado di cedere più di un protone, H+. Definiamo BASE POLIPROTICA, secondo Brønsted. Lowry, una base in grado di accettare più di un protone. H 2 CO 3(aq) + H 2 O(l) ⇄ HCO 3 -(aq) + H 3 O+(aq) HCO 3 -(aq) + H 2 O(l) ⇄ CO 32 -(aq) + H 3 O+(aq) H 2 CO 3(aq) + 2 H 2 O(l) ⇄ CO 32 -(aq) + 2 H 3 O+(aq)

Si calcolino il p. H ed il p. OH di una soluzione acquosa 1. 00 x 10 -4 M di HCl. O 4 è un acido forte con Ka > 1 quindi in H 2 O si dissocia completamente: [H 3 O+] derivante dall’acido = CHCl. O 4= 1. 00 p. H = -log 1. 00 poiché [H 3 O+] [OH-] = 1. 0 x x 10 -4 M 10 -4 = 4 10 -14 M risulta che: 10 -14/1. 0 x 10 -4 = 1. 0 p. OH = 10. 0 Si noti che p. H + p. OH = p. Kw= 14 x 10 -10 M

Nel problema non si è tenuto conto del contributo degli ioni H 3 O+ derivanti dalla dissociazione dell’H 2 O Si verifica a posteriori che l’approssimazione fatta sia lecita: dato che la [OH-] = 10 -10 M deriva dalla dissociazione delle molecole di H 2 O, la [H 3 O+] derivante dalla medesima dissociazione sarà uguale, cioè pari a 10 -10 M Questa concentrazione è trascurabile rispetto alla concentrazione di [H 3 O+] derivante dall’acido (10 -4 M)

Si calcoli il p. H di una soluzione 1. 00 di HCl. O 4 x 10 -7 M HCl. O 4 è un acido forte con Ka > 1 quindi in H 2 O si dissocia completamente: CH 3 O+ derivante dall’acido = CHCl. O 4= 1. 00 x 10 -7 M tale concentrazione è paragonabile alla dissociazione delle molecole di H 2 O che quindi contribuirà al p. H della soluzione: [H 3 O+] = 1. 00 x 10 -7 + x dove x è la concentrazione di H 3 O+ , e quindi anche di OH-, derivante dalla dissociazione del solvente

quindi: Kw = (1. 00 x 10 -7 + x) x = 1. 0 x = 0. 62 x x 10 -14 10 -7 M la concentrazione totale di [H 3 O+] = 1. 62 x 10 -7 M p. H = 6. 79 Si noti che il p. H è acido come atteso Solo quando gli ioni H 3 O+ derivanti da un acido sono in concentrazione < 10 -6 M occorre tenere conto del contributo della dissociazione dell’acqua al p. H
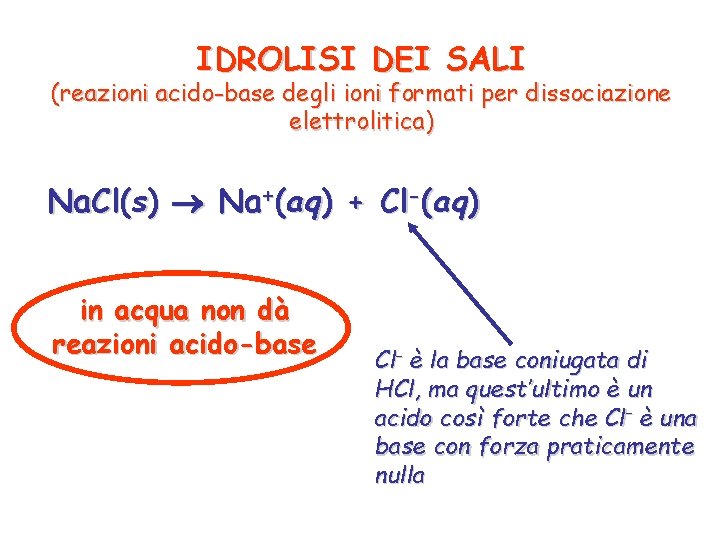
IDROLISI DEI SALI (reazioni acido-base degli ioni formati per dissociazione elettrolitica) Na. Cl(s) Na+(aq) + Cl-(aq) in acqua non dà reazioni acido-base Cl- è la base coniugata di HCl, ma quest’ultimo è un acido così forte che Cl- è una base con forza praticamente nulla
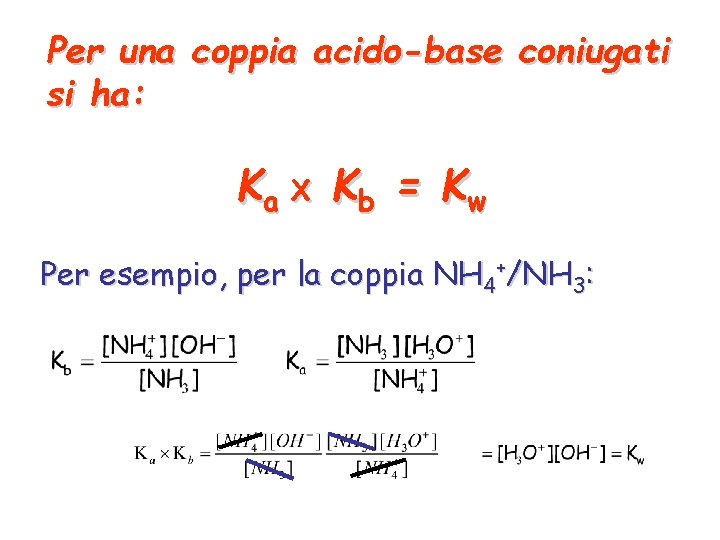
Per una coppia acido-base coniugati si ha: Ka X Kb = Kw Per esempio, per la coppia NH 4+/NH 3:
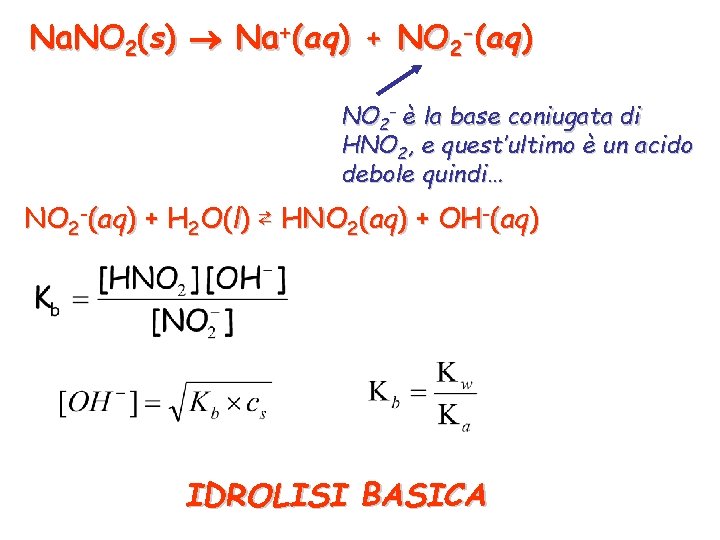
Na. NO 2(s) Na+(aq) + NO 2 -(aq) NO 2 - è la base coniugata di HNO 2, e quest’ultimo è un acido debole quindi… NO 2 -(aq) + H 2 O(l) ⇄ HNO 2(aq) + OH-(aq) IDROLISI BASICA
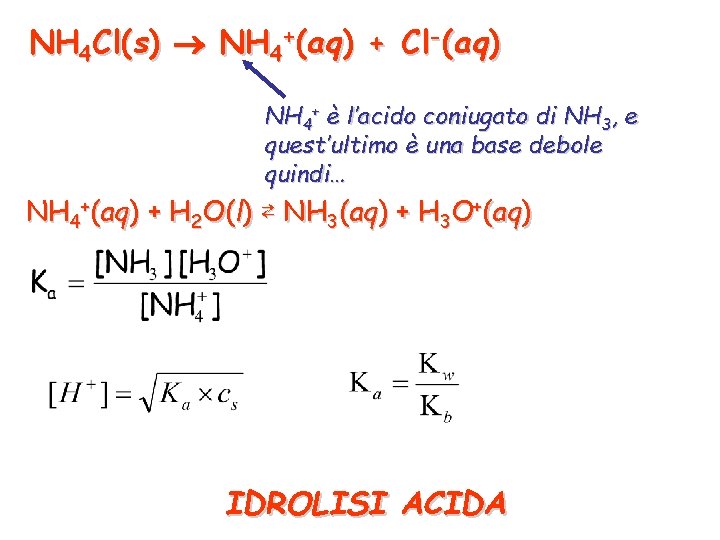
NH 4 Cl(s) NH 4+(aq) + Cl-(aq) NH 4+ è l’acido coniugato di NH 3, e quest’ultimo è una base debole quindi… NH 4+(aq) + H 2 O(l) ⇄ NH 3(aq) + H 3 O+(aq) IDROLISI ACIDA

Quando in una soluzione sono presenti sia un acido debole che la sua base coniugata… Ad esempio, una soluzione di acido Ipocloroso (HCl. O, concentrazione ca) e Ipoclorito di sodio (Na. Cl. O, concentrazione cb), formerà il seguente equilibrio: HCl. O(aq) + H 2 O(l) ⇄ Cl. O-(aq) + H 3 O+(aq) cb+x ca -x x con ca e cb in quantità paragonabili se x << ca e x << cb

Un soluzione con un acido debole e la sua base coniugata, con ca e cb in quantità paragonabili, è un tampone. Per esempio: NH 3(aq) + H 2 O(l) ⇄ NH 4+(aq) + OH-(aq) cb ca L’aggiunta di una piccola quantità di acido sposta la reazione a destra L’aggiunta di una piccola quantità di base sposta la reazione a sinistra Il p. H non cambia molto in ambedue i casi

Riepilogo: Acido debole: Base debole: Idrolisi acida: Idrolisi basica:

Riepilogo: Tampone formato da un acido debole e la sua base coniugata: Tampone formato da una base debole e il suo acido coniugato:
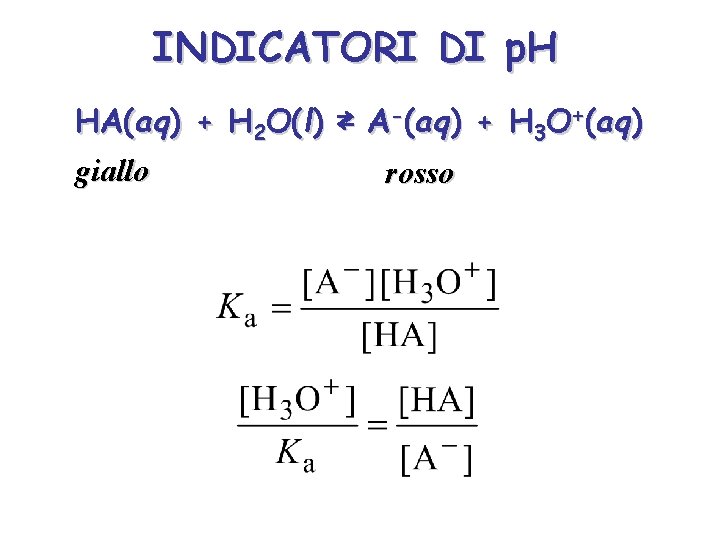
INDICATORI DI p. H HA(aq) + H 2 O(l) ⇄ A-(aq) + H 3 O+(aq) giallo rosso
![giallo rosso Quando [H 3 O+] >> Ka la soluzione appare gialla Quando [H giallo rosso Quando [H 3 O+] >> Ka la soluzione appare gialla Quando [H](http://slidetodoc.com/presentation_image_h/c92c24580d525a71d553ff8a14478b22/image-45.jpg)
giallo rosso Quando [H 3 O+] >> Ka la soluzione appare gialla Quando [H 3 O+] << Ka la soluzione appare rossa Quando [H 3 O+] Ka la soluzione appare arancione p. Ka = - log 10 Ka p. H 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
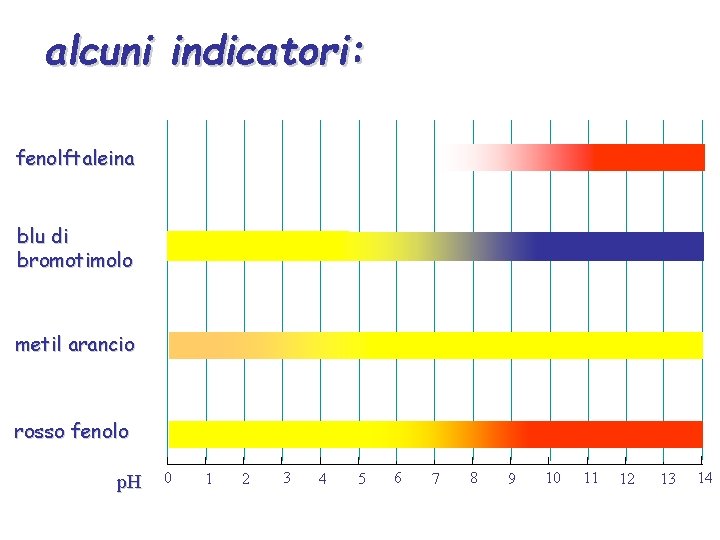
alcuni indicatori: fenolftaleina blu di bromotimolo metil arancio rosso fenolo p. H 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
- Slides: 46