Acidi e basi Acidi LOssigeno ad esempio contenuto

Acidi e basi
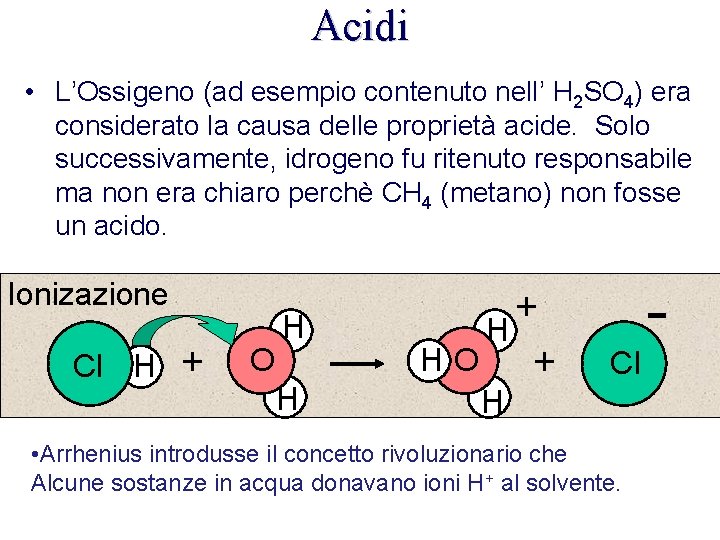
Acidi • L’Ossigeno (ad esempio contenuto nell’ H 2 SO 4) era considerato la causa delle proprietà acide. Solo successivamente, idrogeno fu ritenuto responsabile ma non era chiaro perchè CH 4 (metano) non fosse un acido. Ionizazione Cl H + O H H + H HO + Cl H • Arrhenius introdusse il concetto rivoluzionario che Alcune sostanze in acqua donavano ioni H+ al solvente.

Teoria di Arrhenius: Acidi: un composto di formula generale HA che in acqua libera ioni H+ Basi: un composto di formula generale BOH che in acqua libera ioni OH- (ioni ossidrili) HCl H 2 O H+ + Cl- Na. OH H 2 O Na+ + OH-
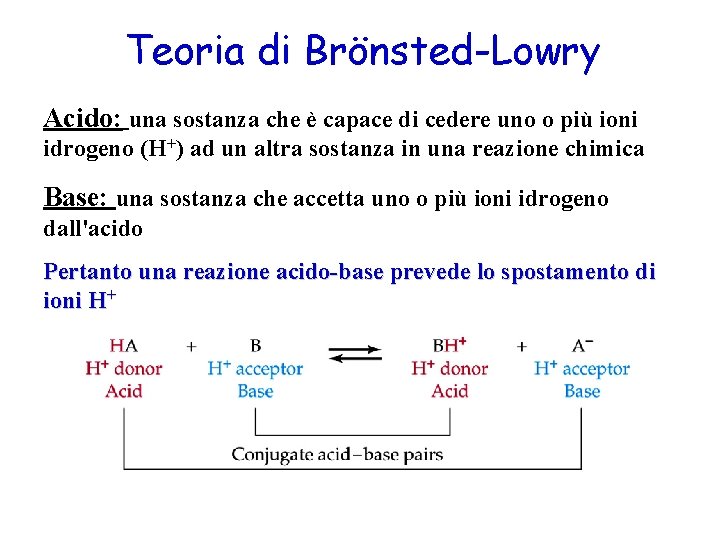
Teoria di Brönsted-Lowry Acido: una sostanza che è capace di cedere uno o più ioni idrogeno (H+) ad un altra sostanza in una reazione chimica Base: una sostanza che accetta uno o più ioni idrogeno dall'acido Pertanto una reazione acido-base prevede lo spostamento di ioni H+
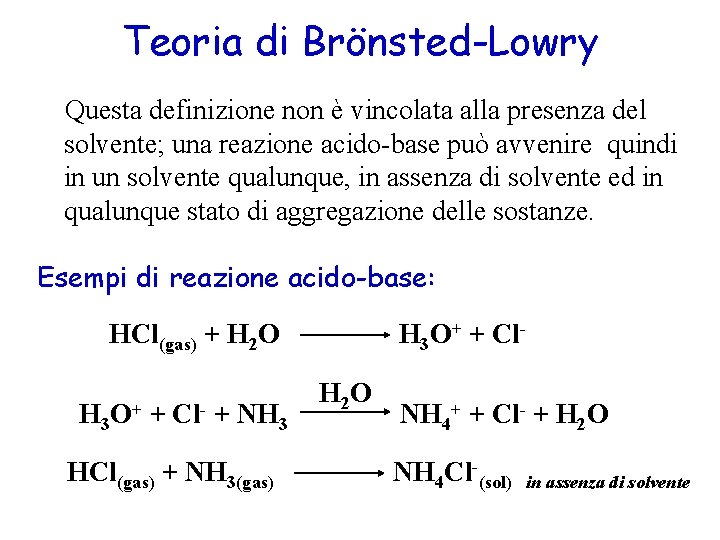
Teoria di Brönsted-Lowry Questa definizione non è vincolata alla presenza del solvente; una reazione acido-base può avvenire quindi in un solvente qualunque, in assenza di solvente ed in qualunque stato di aggregazione delle sostanze. Esempi di reazione acido-base: HCl(gas) + H 2 O H 3 O+ + Cl- + NH 3 HCl(gas) + NH 3(gas) H 3 O+ + Cl. H 2 O NH 4+ + Cl- + H 2 O NH 4 Cl-(sol) in assenza di solvente
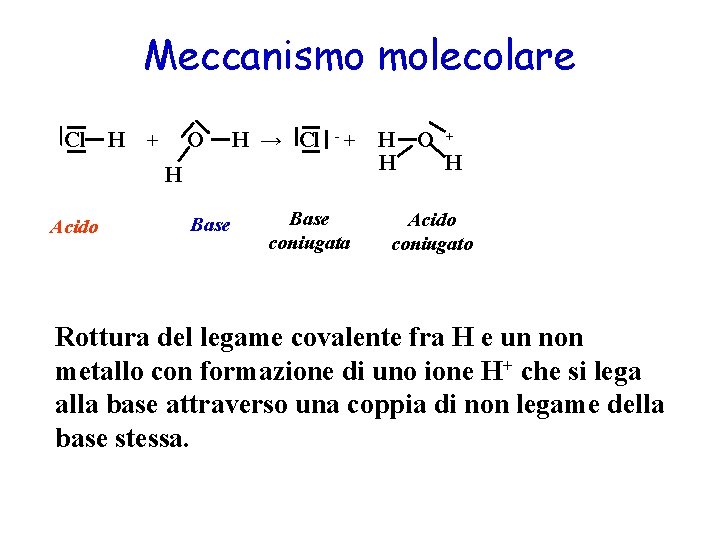
Meccanismo molecolare Cl H + O H → Cl -+ H Acido Base coniugata H O + H H Acido coniugato Rottura del legame covalente fra H e un non metallo con formazione di uno ione H+ che si lega alla base attraverso una coppia di non legame della base stessa.

Teoria di Lewis Definizione che si basa sulle caratteristiche elettroniche delle specie che interagiscono tra di loro • Acido: specie chimica in grado di accettare uno o più coppie di elettroni (elettrofilo) • Base: specie chimica in grado di fornire uno o più coppie di elettroni (nucleofilo) La teoria di Lewis estende il concetto di acido e base a reazioni che non coinvolgono il trasferimento di protoni
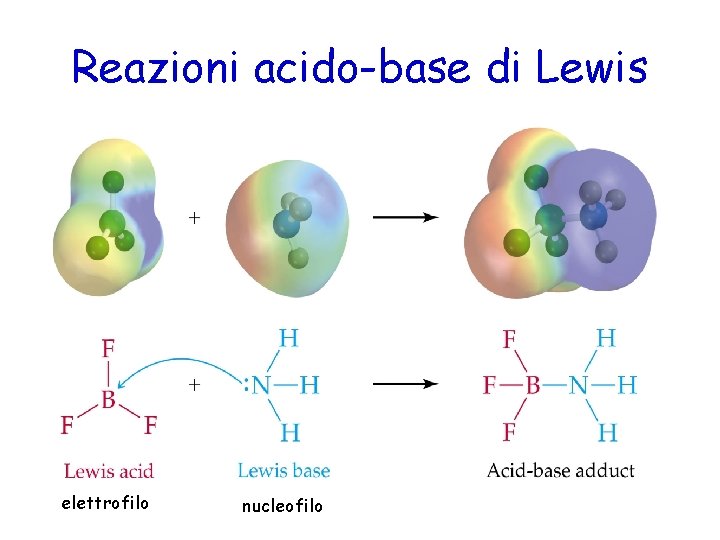
Reazioni acido-base di Lewis elettrofilo nucleofilo

Forza di un acido
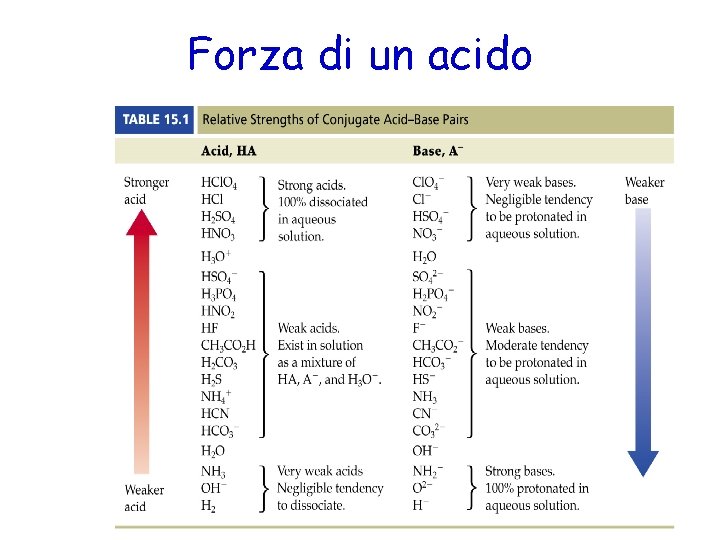
Forza di un acido
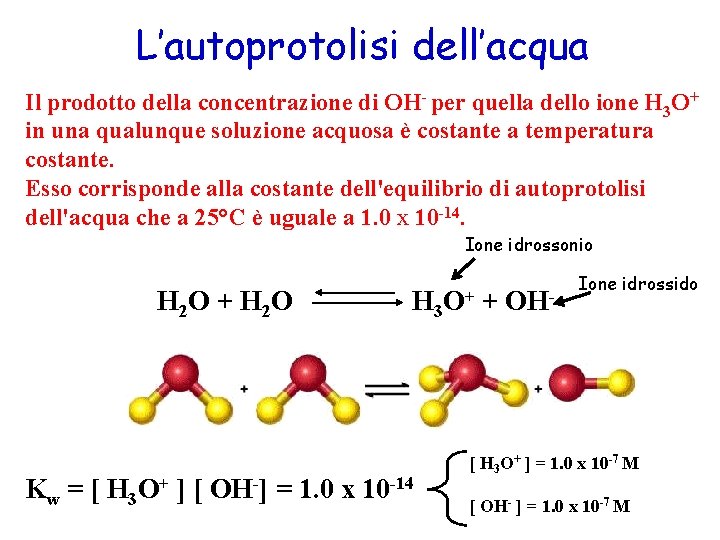
L’autoprotolisi dell’acqua Il prodotto della concentrazione di OH- per quella dello ione H 3 O+ in una qualunque soluzione acquosa è costante a temperatura costante. Esso corrisponde alla costante dell'equilibrio di autoprotolisi dell'acqua che a 25°C è uguale a 1. 0 x 10 -14. Ione idrossonio H 2 O + H 2 O H 3 O+ Kw = [ H 3 O+ ] [ OH-] = 1. 0 x 10 -14 + OH- Ione idrossido [ H 3 O+ ] = 1. 0 x 10 -7 M [ OH- ] = 1. 0 x 10 -7 M

Gli equilibri acido-base: Ka, Kb HA + H 2 O A- + H 2 O Ka*Kb = H 3 O + + A - OH- + HA [ H 3 O+ ] [A- ] [ HA ] * Ka = Kb = [ H 3 O+ ] [A- ] [ HA ] [ OH- ] [ HA ] [A-] Ka*Kb = [ H 3 O+ ][ OH-] = Kw = 1. 0 x 10 -14

Equilibrio delle basi deboli B + H 2 O HB+ + H 2 O OH- + HB+ H 3 O + + B Kb = Ka = [ OH- ] [ HB+ ] [B] [H 3 O+ ] [ B ] [ HB+ ] Ka x Kb = [ H 3 O+ ] [ OH-] = Kw = 1. 0 x 10 -14
![Il p. H Poichè le [H 3 O+] e [OH-] sono legate matematicamente dalla Il p. H Poichè le [H 3 O+] e [OH-] sono legate matematicamente dalla](http://slidetodoc.com/presentation_image_h/1c9f5390e2bc1231dbe85f79e3b4d7dd/image-14.jpg)
Il p. H Poichè le [H 3 O+] e [OH-] sono legate matematicamente dalla Kw per caratterizzare le proprietà acido/base di una soluzione è sufficiente indicare una sola delle due concentrazioni ([H 3 O+]) ü Soluzioni Neutre: [H 3 O+]= [OH-] = 1. 0 x 10– 7 M, p. H = 7. 00 ü Soluzioni Acide: [H 3 O+]> 1. 0 x 10– 7 M, p. H < 7. 00 ü Soluzioni Basiche: [H 3 O+]< 1. 0 x 10– 7 M, p. H > 7. 00 • Il p. H di una soluzione è il logaritmo negativo della concentrazione dello ione idrogeno (in mol/L). p. H = –log [H+]
![Il p. H e la sua scala p. H = -log [H 3 O+] Il p. H e la sua scala p. H = -log [H 3 O+]](http://slidetodoc.com/presentation_image_h/1c9f5390e2bc1231dbe85f79e3b4d7dd/image-15.jpg)
Il p. H e la sua scala p. H = -log [H 3 O+] p. OH = -log [OH-] p. H + p. OH = p. Kw = 14 Soluzioni basiche p. H 0 1 2 3 basicità crescente 4 5 6 7 8 9 10 11 12 13 14 14 13 12 11 10 9 8 7 6 5 4 acidità crescente Soluzioni acide 3 2 1 0 p. OH

Il calcolo del p. H Acidi forti Si calcoli il p. H di una soluzione di 0. 100 M di HNO 3 è un acido forte in H 2 O con Ka > 1, quindi la reazione è spostata verso i prodotti per cui cede il protone all’acqua: [H 3 O+] derivante dall’acido HNO 3= 0. 100 M p. H = -log 0. 100 = 1 Il p. H risultante è acido

Si calcoli il p. H ed il p. OH di una soluzione acquosa di 1. 00 x 10 -4 M di HCl. O 4 è un acido forte con Ka > 1 quindi : [H 3 O+] derivante dall’acido = CHCl. O 4= 1. 00 x 10 -4 M p. H = -log 1. 00 x 10 -4 = 4 poiché [H 3 O+] [OH-] = 1. 0 x 10 -14 M risulta che: [OH-] = 1. 0 x 10 -14/1. 0 x 10 -4 = 1. 0 x 10 -10 M p. OH = 10. 0 Si noti che p. H + p. OH = p. Kw= 14

Nel problema non si è tenuto conto del contributo degli ioni H 3 O+ derivanti dalla dissociazione dell’H 2 O Si verifica a posteriori che l’approssimazione fatta sia lecita: dato che la [OH-] = 10 -10 M deriva dalla dissociazione delle molecole di H 2 O, la [H 3 O+] derivante dalla medesima dissociazione sarà uguale, cioè pari a 10 -10 M Questa concentrazione è trascurabile rispetto alla concentrazione di [H 3 O+] derivante dall’acido (10 -4 M)

Si calcoli il p. H di una soluzione 1. 00 x 10 -7 M di HCl. O 4 è un acido forte con Ka > 1 quindi : [H 3 O+] derivante dall’acido HCl. O 4= 1. 00 x 10 -7 M tale concentrazione è paragonabile alla dissociazione delle molecole di H 2 O che quindi contribuirà al p. H della soluzione: [H 3 O+] = 1. 00 x 10 -7 + x dove x è la concentrazione di H 3 O+ , e quindi anche di OH-, derivante dalla dissociazione del solvente

quindi: Kw = (1. 00 x 10 -7 + x) x = 1. 0 x 10 -14 x = 0. 62 x 10 -7 M la concentrazione totale di [H 3 O+] = 1. 62 x 10 -7 M p. H = 6. 79 Si noti che il p. H è acido come atteso.

Solo quando gli ioni H 3 O+ derivanti da un acido sono in concentrazione < 10 -6 M occorre tenere conto del contributo della dissociazione dell’acqua al p. H

Il calcolo del p. H Acidi deboli Si calcoli il p. H di una soluzione 0. 100 M di CH 3 COOH è un acido debole con Ka = 1. 8 x 10 -5, quindi in H 2 O non si dissocia completamente: La concentrazione di H 3 O+ derivante dalla sua dissociazione si può ricavare dalla Ka. + ][ CH COO- ] [ H O -5 3 3 Ka = __________ = 1. 8 x 10 [ CH 3 COOH ]
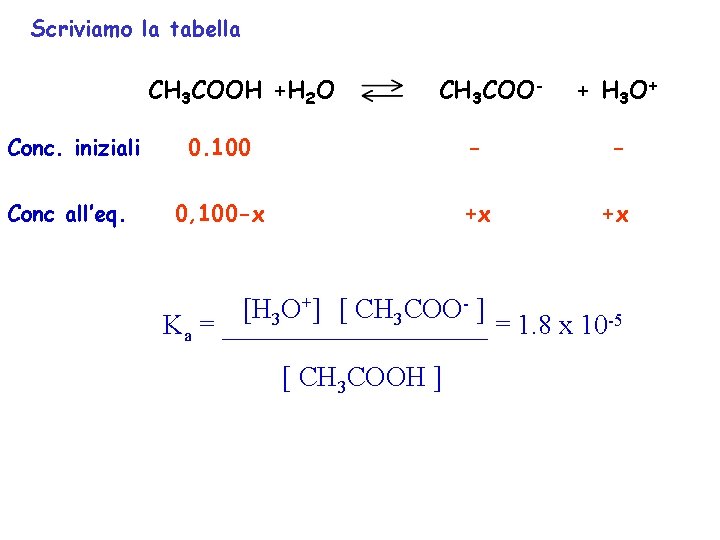
Scriviamo la tabella CH 3 COOH +H 2 O Conc. iniziali Conc all’eq. CH 3 COO- + H 3 O + 0. 100 - - 0, 100 -x +x +x [H 3 O+] [ CH 3 COO- ] Ka = __________ = 1. 8 x 10 -5 [ CH 3 COOH ]

2 x Ka = _______ = 1. 8 x 10 -5 0. 100 -x 0. 100 x 2 x = 1. 34 x 10 -3 p. H = 2. 9 molto meno acido di quello di un acido forte nella stessa concentrazione Si controlla che l’approssimazione fatta sia corretta: 1. 34 x 10 -3 è trascurabile rispetto a 1 x 10 -1 In generale per un acido debole l’approssimazione x<<[HA]0 che permette di evitare di risolvere l’equazione di secondo grado con il termine di 1° grado vale se si ha: Ka<<[HA]0 almeno di un fattore 102 -103

Il calcolo del p. H basi deboli Calcolare le concentrazioni di tutte le specie e il p. H di una soluzione 0, 10 M di metilamina (Kb=4, 3 10 -4) Conc. iniziali Conc all’eq CH 3 NH 2(aq) 0, 10 -x CH 3 NH 3+ (aq) + OH-(aq) -x Dall’equazione della costante di equilibrio si ha: -- x

Questa è un’equazione di secondo grado da risolvere rispetto ad x e può ancora essere semplificata poichè Kb è molto piccola e quindi x sarà molto piccolo e trascurabile rispetto alla concentrazione iniziale 0, 10: x<<0, 10 -x 0, 10 Si ha quindi: x 2 = 4, 3 10 -4 0, 10 = 4, 3 10 -5 L’approssimazione fatta è ancora valida: x = 0, 0066 << 0, 10 -x = 0, 10 - 0, 0066 = 0, 0934 0, 10
![Le concentrazioni all’equilibrio sono quindi: [OH-] = x = 6, 6 10 -3 [CH Le concentrazioni all’equilibrio sono quindi: [OH-] = x = 6, 6 10 -3 [CH](http://slidetodoc.com/presentation_image_h/1c9f5390e2bc1231dbe85f79e3b4d7dd/image-27.jpg)
Le concentrazioni all’equilibrio sono quindi: [OH-] = x = 6, 6 10 -3 [CH 3 NH 3+] = x = 6, 6 10 -3 [CH 3 NH 2] = 0, 10 - x = 0, 10 - 6, 6 10 -3 = 0, 0934 0, 10 Il calcolo non dà direttamente [H+] e per calcolare il p. H conviene prima calcolare il p. OH e poi sottrarre a 14 p. OH = -log(6, 6 10 -3 )=2, 2 p. H = 14 -p. OH=14 -2, 2 = 11, 8
![In generale per una base debole l’approssimazione x<<[B]0 che permette di evitare di risolvere In generale per una base debole l’approssimazione x<<[B]0 che permette di evitare di risolvere](http://slidetodoc.com/presentation_image_h/1c9f5390e2bc1231dbe85f79e3b4d7dd/image-28.jpg)
In generale per una base debole l’approssimazione x<<[B]0 che permette di evitare di risolvere l’equazione di secondo grado con il termine di 1° grado vale se si ha: Kb<<[B]0 almeno di un fattore 102 -103
- Slides: 28